【章末题型强化训练】浙教版9年级上册 第1章 物质及其变化 选择题(含答案)
文档属性
| 名称 | 【章末题型强化训练】浙教版9年级上册 第1章 物质及其变化 选择题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-11-24 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
浙教版9年级上册 第一章 选择题
一、物质及其变化
1.(2021九上·西湖月考)下列叙述中,前者是物理变化,后者是利用物质化学性质的是( )
A. 石蜡熔化,干冰用于人工降雨 B. 煤干馏,稀有气体用作焊接金属的保护气
C. 钢铁生锈,氦气用于填充探空气球 D. 活性炭去除冰箱异味,熟石灰用来改良酸性土壤
2.(2021九上·杭州开学考)下列推理不正确的是 ( )
①燃烧过程中伴随着发光放热,所以有发光放热现象的变化一定是燃烧
②分子可以构成物质,所以物质一定由分子构成的
③单质只含一种元素,所以含一种元素的物质一定是单质
④物理变化没有新物质生成,所以没有新物质生成的变化一定是物理变化
⑤同种元素质子数相同,所以质子数相同的粒子一定是同种元素
A.③ ⑤ B.① ② ⑤ C.① ③ ④ D.① ② ③ ⑤
3.(2021·金华)金华酒传统酿造技艺、浦江剪纸、永康锡雕、东阳竹编等,是金华拥有的众多国家级非物质文化遗产的典型代表。下列非物质文化遗产制作过程,主要利用化学变化的是( )
A. 酿酒 B. 剪纸 C. 锡雕 D. 竹编
4.(2021·龙港模拟)在治疗新冠肺炎中,中药发挥了重要作用。下列中药煎制步骤中涉及化学变化的是( )
A. 冷水浸泡 B. 加热煎制
C. 取液弃渣 D. 装袋保存
5.(2020九上·西湖月考)下列用微观图示表示的物质变化中,属于化学变化的是( )
A. ①② B. ②③ C. ①③ D. ①②③
二、物质的酸碱性
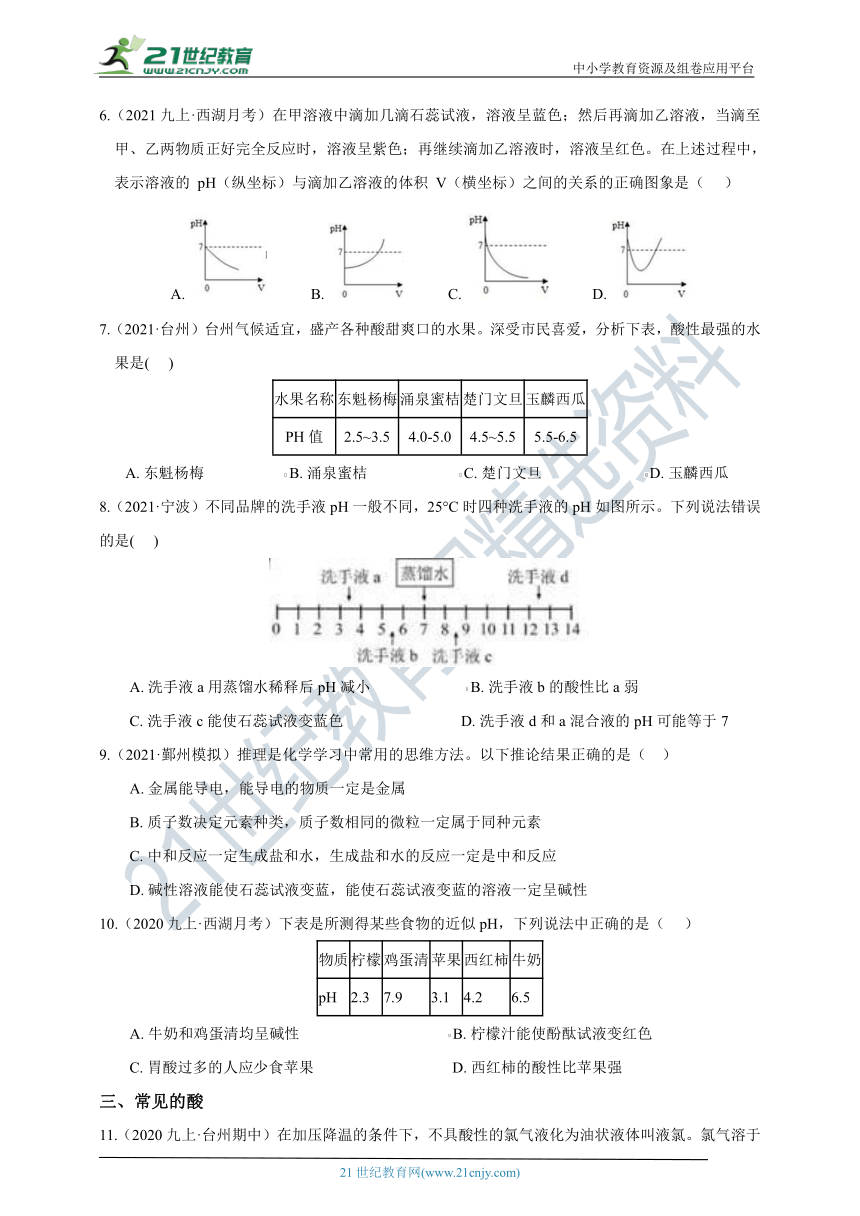
6.(2021九上·西湖月考)在甲溶液中滴加几滴石蕊试液,溶液呈蓝色;然后再滴加乙溶液,当滴至甲、乙两物质正好完全反应时,溶液呈紫色;再继续滴加乙溶液时,溶液呈红色。在上述过程中,表示溶液的 pH(纵坐标)与滴加乙溶液的体积 V(横坐标)之间的关系的正确图象是( )
A. B. C. D.
7.(2021·台州)台州气候适宜,盛产各种酸甜爽口的水果。深受市民喜爱,分析下表,酸性最强的水果是( )
水果名称 东魁杨梅 涌泉蜜桔 楚门文旦 玉麟西瓜
PH值 2.5~3.5 4.0-5.0 4.5~5.5 5.5-6.5
A. 东魁杨梅 B. 涌泉蜜桔 C. 楚门文旦 D. 玉麟西瓜
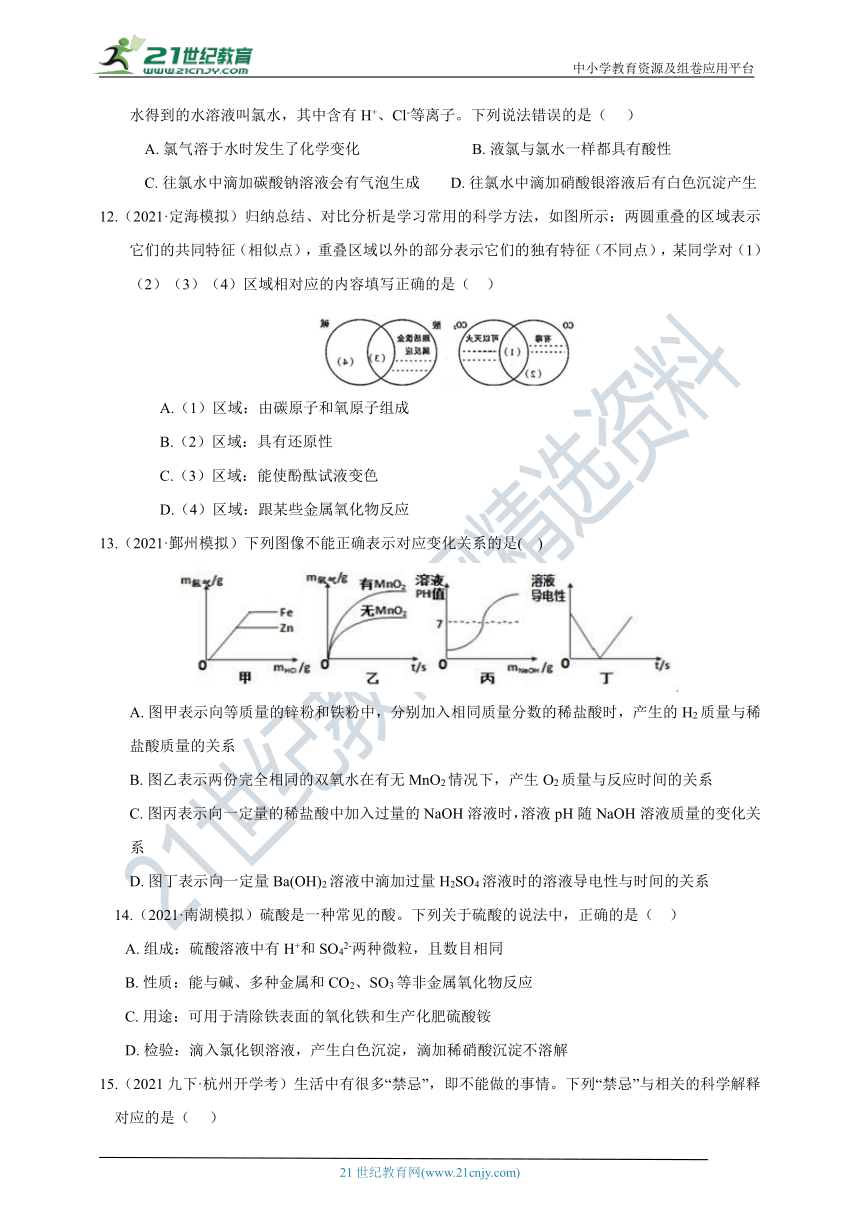
8.(2021·宁波)不同品牌的洗手液pH一般不同,25°C时四种洗手液的pH如图所示。下列说法错误的是( )
A. 洗手液a用蒸馏水稀释后pH减小 B. 洗手液b的酸性比a弱
C. 洗手液c能使石蕊试液变蓝色 D. 洗手液d和a混合液的pH可能等于7
9.(2021·鄞州模拟)推理是化学学习中常用的思维方法。以下推论结果正确的是( )
A. 金属能导电,能导电的物质一定是金属
B. 质子数决定元素种类,质子数相同的微粒一定属于同种元素
C. 中和反应一定生成盐和水,生成盐和水的反应一定是中和反应
D. 碱性溶液能使石蕊试液变蓝,能使石蕊试液变蓝的溶液一定呈碱性
10.(2020九上·西湖月考)下表是所测得某些食物的近似pH,下列说法中正确的是( )
物质 柠檬 鸡蛋清 苹果 西红柿 牛奶
pH 2.3 7.9 3.1 4.2 6.5
A. 牛奶和鸡蛋清均呈碱性 B. 柠檬汁能使酚酞试液变红色
C. 胃酸过多的人应少食苹果 D. 西红柿的酸性比苹果强
三、常见的酸
11.(2020九上·台州期中)在加压降温的条件下,不具酸性的氯气液化为油状液体叫液氯。氯气溶于水得到的水溶液叫氯水,其中含有H+、Cl-等离子。下列说法错误的是( )
A. 氯气溶于水时发生了化学变化 B. 液氯与氯水一样都具有酸性
C. 往氯水中滴加碳酸钠溶液会有气泡生成 D. 往氯水中滴加硝酸银溶液后有白色沉淀产生
12.(2021·定海模拟)归纳总结、对比分析是学习常用的科学方法,如图所示:两圆重叠的区域表示它们的共同特征(相似点),重叠区域以外的部分表示它们的独有特征(不同点),某同学对(1)(2)(3)(4)区域相对应的内容填写正确的是( )
A.(1)区域:由碳原子和氧原子组成
B.(2)区域:具有还原性
C.(3)区域:能使酚酞试液变色
D.(4)区域:跟某些金属氧化物反应
13.(2021·鄞州模拟)下列图像不能正确表示对应变化关系的是( )
A. 图甲表示向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸时,产生的H2质量与稀盐酸质量的关系
B. 图乙表示两份完全相同的双氧水在有无MnO2情况下,产生O2质量与反应时间的关系
C. 图丙表示向一定量的稀盐酸中加入过量的NaOH溶液时,溶液pH随NaOH溶液质量的变化关系
D. 图丁表示向一定量Ba(OH)2溶液中滴加过量H2SO4溶液时的溶液导电性与时间的关系
14.(2021·南湖模拟)硫酸是一种常见的酸。下列关于硫酸的说法中,正确的是( )
A. 组成:硫酸溶液中有H+和SO42-两种微粒,且数目相同
B. 性质:能与碱、多种金属和CO2、SO3等非金属氧化物反应
C. 用途:可用于清除铁表面的氧化铁和生产化肥硫酸铵
D. 检验:滴入氯化钡溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解
15.(2021九下·杭州开学考)生活中有很多“禁忌”,即不能做的事情。下列“禁忌”与相关的科学解释对应的是( )
选项 禁忌 原理解释
A 用锡壶装醋酸 活动性顺序:SnB 煤气泄漏时,开灯检查 电火花会点燃混合气体,气体爆炸
C 用稀HCl除铁锈时,浸泡太久 6HCl+2Fe=2FeCl3+3H2↑
D 浓硫酸洒在手上,直接用水冲洗 浓硫酸具有吸水性
A. A B. B C. C D. D
16.(2021九上·台州开学考)现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如右图所示.下列说法正确的是( )
A. 滴至a克时,溶液中反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B. 滴至b克时,溶液中含HCl、NaCl两种溶质
C. 滴至c克时,溶液中溶质质量比原混合溶液中溶质质量大
D. 滴至d克时,溶液呈中性
17.(2020九上·绍兴月考)在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入100g溶质质量分数为19.6%的稀硫酸,将天平调节至平衡,然后向左盘的烧杯中投入一定质量的铁,向右盘的烧杯中投入一定质量的镁,均恰好完全反应。下列说法正确的是( )
A. 实验结束后,指针偏向右盘
B. 由于消耗的硫酸质量相等,实验结束后,指针不偏转
C. 实验结束后,欲使天平重新平衡,则可向左盘的烧杯中加入6.4g的铁
D. 实验结束后,欲使天平重新平衡,则可向右盘的烧杯中加入6.4g的镁
18.(2020九上·瑞安月考)天平两边各放质量相等的烧杯,分别盛有等质量、等质量分数的足量稀硫酸,此时天平平衡。然后在两边的烧杯中各加入下列物质,充分反应后天平仍保持平衡的是( )
①10克铁和10克氧化铁
②10克铜和10克氧化铜
③5.6克铁和6.5克锌
④6.5克锌和6.3克氧化锌
A. ①②③ B. ①②④ C. ②④ D. ③④
四、常见的碱
19.(2021·金华模拟)向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
A.a点溶液中滴入紫色石蕊试液变蓝
B.d点溶液中的溶质是NaCl和NaOH
C.ab段(不含b点)反应的化学方程式为HCl+NaOH=NaCl+H2O
D.整个变化过程溶液中镁离子数目没有改变
20.(2021·鄞州模拟)一定温度下,向ag FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述错误的是( )
A. P点对应的溶液中NaOH达到饱和状态
B. 加入 ngNaOH时,NaOH固体和FeCl3溶液恰好完全反应
C. m>c-a
D. 生成Fe(OH)3的质量为(b-a)g
21.(2020九上·吴兴月考)某化学小组在课外活动时做了一个实验:在甲试管中装入固体物质,乙试管中装入液体试剂,按如图所示组装好仪器(图中铁架台等仪器已略去)。通过分液漏斗加入足量的稀硫酸,同时打开止水夹,看到乙试管液体中有气泡冒出,一段时间后,关闭止水夹,发现乙中液面上升,溶液变浑浊。符合以上实验现象的一组试剂是( )
A. KNO3 BaCl2 B. Na2CO3 NaOH C. Zn Ba(NO3)2 D. MgCO3 NaNO3
22.归纳和演绎是重要的科学方法。下列归纳或演绎合理的是( )
A. 有机物是一类含碳化合物,所以CH4、CO2都是有机物
B. 稀有气体可做保护气,可做保护气的一定是稀有气体
C. 金属Fe、Zn能与酸反应生成氢气,所以金属都能与酸反应生成氢气
D. 单质是由一种元素组成,由一种元素组成的纯净物一定是单质
23.(2020九上·萧山期中)将a%的氢氧化钠溶液b克和b%的硫酸溶液a克混合,充分反应后,下列物质不能与这种混合液发生反应的是( )
A. 铁粉 B. 氯化铁溶液 C. 盐酸 D. 氯化钡溶液
24.(2021九上·金华月考)取200g一定质量分数的CuSO4溶液,先逐滴滴加100gBa(OH)2溶液至b点,后再逐滴滴加稀HCl溶液至过量,整个过程中加入溶液的质量与沉淀质量关系如图所示。下列说法不正确的是( )
A.oa段溶液的导电性将逐渐减弱
B.至d点时溶液中所含的溶质有BaCl2、CuCl2、HCl
C.bc段发生反应的化学方程式2HCl+Ba(OH)2=BaCl2+2H2O
D.m的值是3.35g
25.(2020·宁波)某锥形瓶内盛有盐酸和氯化铜的混合溶液100g,向其中加入溶质质量分数为10%的V氢氧化钠溶液,锥形瓶内溶液质量m1与加入的氢氧化钠溶液质量m2的变化关系如图所示。下列说法错误的是( )
A. 反应至A点时,所加NaOH溶液的质量为40g
B. 反应至A点时,溶液中的溶质有CuCl2和NaCl
C. 反应至B点时,锥形瓶内溶液的质量为280.4g
D. 反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
26.(2019·宁波模拟)烧杯中盛有MgSO4和HCl的混合溶液100.0g,向其中逐滴滴加Ba(OH)2溶液,产生沉淀的质量与滴加的溶液质量关系如图所示。下列说法正确的是()
A. a点对应溶液中溶质是MgCl2 B. Ba(OH)2溶液的溶质质量分数为17.1%
C. b-c段是MgSO4与Ba(OH)2反应 D. 0-a段产生的沉淀是BaSO4与Mg(OH)2
27.小科为研究“碱与盐反应”的规律,设计了如图所示的五组实验,每支试管盛有3毫升溶液,分别向试管中只滴加3滴溶液。除氢氧化钙溶液是饱和外,其余溶液的质量分数都为5%。下列叙述正确的是( )
A. 甲组和乙组实验能观察到相同现象 B. 乙组和丙组实验均能观察到蓝色沉淀
C. 乙组实验产生的沉淀质量比丁组多 D. 戊组实验产生的沉淀质量比丙组少
五、酸碱之间的反应
28.如图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。下列说法正确的是( )
A. 在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B. 在a曲线所示的实验中,若用酚酞做指示剂,酚酞试液由红色变为无色
C. 在a、b、c三种曲线所示的实验中,反应速率相同
D. 在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
29.(2018·温州模拟)将a%的氢氧化钾溶液b克和b%的硫酸溶液a克混合,下列物质不能与这种混合液发生反应的是( )
A. 氧化铜粉末 B. 盐酸 C. 氢氧化钠固体 D. 氯化钡溶液
30.完全中和一定量的某盐酸溶液,需要100克8%的KOH溶液,若改用100克8%的NaOH溶液,则反应后溶液的pH为( )
A. 大于7 B. 小于7 C. 等于7 D. 无法确定
31.如图是物质间发生化学反应的颜色变化,其中X是( )
A. 稀盐酸 B. 稀硫酸 C. 硫酸钠溶液 D. 澄清石灰水
32.将10g质量分数为20%的氢氧化钠溶液与20g质量分数为10%的硫酸溶液混合后,下列物质中不能与该溶液发生反应的是( )
A. Na2CO3 B. CuCl2 C. CO2 D. Ba(NO3)2
3.右图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是( )
A. 反应结束时溶液的pH=7 B. 反应前后元素的种类没有变化
C. 反应后溶液中存在的粒子只有Na+和Cl- D. 该反应的实质是H+和OH-结合生成H2O分子
34. 下列4个图形能正确反映对应变化关系的是( )
A. 向一定量稀硫酸中加入NaOH溶液
B. 向一定量CuSO4溶液中加入Zn粉
C. 加热KClO3与MnO2固体混合物
D. 向一定量NaOH和Ca(OH)2的混合溶液中加入Na2CO3溶液
六、常见的盐
35.(2020·海曙模拟)向盛有HCl和CuCl2混合溶液的烧杯中逐滴加入NaOH溶液至过量。在该过程中,下列4个图像能正确反映烧杯内物质的某些科学量变化趋势的是( )
A. ①③ B. ①②④ C. ②④ D. ①②③
36.(2020九上·椒江期中)有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种。某化学兴趣小组为探究其成分做了以下实验:
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示。
Ⅱ.取少量B点时的溶液于试管中,滴加酚酞试液,溶液不变色。
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。
下列说法正确的是( )
A. BC之间能看到有气泡生成,是Na2CO3与稀硝酸反应生成
B. 原白色固体一定没有氯化钾
C. 当稀硝酸加到D点时,溶液中一定含有的溶质是NaNO3、Ba(NO3)2、HNO3 , 可能有 Na2SO4
D. 步骤Ⅰ中反生反应生成的沉淀一定是BaCO3和BaSO4
37.(2020九上·越城月考)下列各组物质的溶液,不需要外加试剂就能鉴别出来的是( )
A. NaOH,FeCl3 , NaCl,KCl B. Na2SO4 , NaCl,BaCl2 , KNO3
C. Na2SO4 , BaCl2 , Na2CO3 , HCl D. Na2CO3 , H2SO4 , HCl,KCl
38.(2020九上·余杭月考)将一定质量的Ba(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
A. N点时,所得溶液的pH=7
B. Q点时,所得溶液中的溶质只含有BaCl2
C. O至P段发生反应的化学方程式为NaOH+HCl=NaCl+H2O
D. P至Q段发生反应的化学方程式为Ba(OH)2+2HICl=BaCl2+2H2O
39.(2020九上·慈溪期中)一瓶不纯的K2CO3粉末,所含杂质可能是KNO3、Ca(NO3)2、KCl、CuCl2、Na2CO3中的一种或几种,为确定其成分,进行如下实验:
⑴取少量该粉末于烧杯中,加入适量蒸馏水,充分搅拌,得无色澄清溶液。
⑵取上述无色溶液少许于试管中,滴加AgNO3溶液有沉淀生成,再加入足量的稀HNO3溶液,沉淀部分溶解。
⑶另称取1.38g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的BaCl2溶液,充分反应后生成1.97g白色沉淀。下列说法正确的是( )
A. 杂质中可能含有KNO3、Na2CO3 B. 杂质中肯定不含有Ca(NO3)2、CuCl2、Na2CO3
C. 杂质中肯定含有KCl,可能含有Na2CO3 D. 杂质中肯定含有KCl、Na2CO3 , 可能含有KNO3
40.(2020·新昌模拟)向100克的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
A. 0-a段发生的反应属于复分解反应
B. m的值为2.33克
C. 该混合溶液中Na2CO3的质量分数是2.12%
D. 取c点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
41.(2020九上·绍兴期末)有一包不纯的碳酸钠白色粉末,可能含有硫酸钠、氢氧化钠的一种或几种,某科学兴趣小组为探究其成分做了如下实验:
Ⅰ。现取样品16g于烧杯中并加84g水搅拌,全部溶解。再向烧杯中逐渐滴加26.1%硝酸钡溶液并不断搅拌,烧杯内固体的质量随加入硝酸钡溶液的质量的变化如图甲所示;
Ⅱ。在B点开始,向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图乙所示。则下列错误的是( )
A. 原白色固体中由Na2CO3 , Na2SO4 , NaOH组成
B. E点时,溶液中一定含有的溶质是HNO3 , Ba(No3)2 , NaNO3
C. D点时,溶液中硝酸钠的溶质质量为304.94克
D. 原白色粉末中含Na2CO3质量为10.6克
42.下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是( )
①NaCl、BaCl2、CuSO4、NaOH、NH4NO3②Ba(NO3)2、NaCl、Na2SO4、H2SO4、HCl
③NaOH、FeCl3、MgSO4、BaCl2、KCl ④AgNO3、HCl、K2CO3、NaCl、BaCl2
A. ①②④ B. ①②③ C. ①③④ D. ②④
43.(2017九上·杭州月考)某同学想用实验证明 CuSO4 溶液显蓝色是由 Cu2+造成的,下列实验无意义的是( )
A. 将 CuSO4 溶液加水稀释 B. 观察 Cu( NO3)2 溶液
C. 观察 Na2SO4 D. 向 CuSO4 溶液中滴加足量 NaOH 溶液
44.(2016·宁波)现将10.6g某固体混合物样品与足量稀盐酸起反应,收集到4.4gCO2。若此混合物是由MgCO3、Na2CO3、CaCO3和K2CO3中的3种物质所组成,则该混合物组成不可能是( )
A. Na2CO3、CaCO3和K2CO3 B. Na2CO3、CaCO3和MgCO3
C. Na2CO3、K2CO3和MgCO3 D. CaCO3、K2CO3和MgCO3
45.(2016九下·镇海竞赛)一包混有杂质的Na2CO3 , 其杂质可能是Ba(NO3)2、KCl、NaHCO3一种或几种,今取10.6g样品,溶于水得澄清溶液,另取5.3克样品,加入足量的盐酸,收集到2gCO2 , 则下列判断正确的是( )
A. 样品中只含有NaHCO3 B. 样品中一定混有NaHCO3 , 可能有KCl
C. 样品中有NaHCO3 , 也有Ba(NO3)2 D. 样品中混有KCl,也可能有NaHCO3
答案解析部分
一、物质及其变化
1.【答案】 D2.【答案】 D 3.【答案】 A 4.【答案】 B 5.【答案】 C
二、物质的酸碱性
6.【答案】 C7.【答案】 A 8.【答案】 D 9.【答案】 D 10.【答案】 C
三、常见的酸
11.【答案】 B 12.【答案】 B 13.【答案】 B14.【答案】 C
15.【答案】 B 16.【答案】 C17.【答案】 D 18.【答案】 C
四、常见的碱
19.【答案】 C 20.【答案】 D 21.【答案】 C 22.【答案】 B
23.【答案】 A 24.【答案】 D 25.【答案】 D 26.【答案】 B 27.【答案】 D
五、酸碱之间的反应
28.【答案】 A 29.【答案】 B 30.【答案】 A 31.【答案】 B 32.【答案】 A
33.【答案】 C 34.【答案】 C
六、常见的盐
35.【答案】 B 36.【答案】 D 37.【答案】 C 38.【答案】 C
39.【答案】 D 40.【答案】 D 41.【答案】 C 42.【答案】 C
43.【答案】 A 44.【答案】 B 45.【答案】 D
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
浙教版9年级上册 第一章 选择题
一、物质及其变化
1.(2021九上·西湖月考)下列叙述中,前者是物理变化,后者是利用物质化学性质的是( )
A. 石蜡熔化,干冰用于人工降雨 B. 煤干馏,稀有气体用作焊接金属的保护气
C. 钢铁生锈,氦气用于填充探空气球 D. 活性炭去除冰箱异味,熟石灰用来改良酸性土壤
2.(2021九上·杭州开学考)下列推理不正确的是 ( )
①燃烧过程中伴随着发光放热,所以有发光放热现象的变化一定是燃烧
②分子可以构成物质,所以物质一定由分子构成的
③单质只含一种元素,所以含一种元素的物质一定是单质
④物理变化没有新物质生成,所以没有新物质生成的变化一定是物理变化
⑤同种元素质子数相同,所以质子数相同的粒子一定是同种元素
A.③ ⑤ B.① ② ⑤ C.① ③ ④ D.① ② ③ ⑤
3.(2021·金华)金华酒传统酿造技艺、浦江剪纸、永康锡雕、东阳竹编等,是金华拥有的众多国家级非物质文化遗产的典型代表。下列非物质文化遗产制作过程,主要利用化学变化的是( )
A. 酿酒 B. 剪纸 C. 锡雕 D. 竹编
4.(2021·龙港模拟)在治疗新冠肺炎中,中药发挥了重要作用。下列中药煎制步骤中涉及化学变化的是( )
A. 冷水浸泡 B. 加热煎制
C. 取液弃渣 D. 装袋保存
5.(2020九上·西湖月考)下列用微观图示表示的物质变化中,属于化学变化的是( )
A. ①② B. ②③ C. ①③ D. ①②③
二、物质的酸碱性
6.(2021九上·西湖月考)在甲溶液中滴加几滴石蕊试液,溶液呈蓝色;然后再滴加乙溶液,当滴至甲、乙两物质正好完全反应时,溶液呈紫色;再继续滴加乙溶液时,溶液呈红色。在上述过程中,表示溶液的 pH(纵坐标)与滴加乙溶液的体积 V(横坐标)之间的关系的正确图象是( )
A. B. C. D.
7.(2021·台州)台州气候适宜,盛产各种酸甜爽口的水果。深受市民喜爱,分析下表,酸性最强的水果是( )
水果名称 东魁杨梅 涌泉蜜桔 楚门文旦 玉麟西瓜
PH值 2.5~3.5 4.0-5.0 4.5~5.5 5.5-6.5
A. 东魁杨梅 B. 涌泉蜜桔 C. 楚门文旦 D. 玉麟西瓜
8.(2021·宁波)不同品牌的洗手液pH一般不同,25°C时四种洗手液的pH如图所示。下列说法错误的是( )
A. 洗手液a用蒸馏水稀释后pH减小 B. 洗手液b的酸性比a弱
C. 洗手液c能使石蕊试液变蓝色 D. 洗手液d和a混合液的pH可能等于7
9.(2021·鄞州模拟)推理是化学学习中常用的思维方法。以下推论结果正确的是( )
A. 金属能导电,能导电的物质一定是金属
B. 质子数决定元素种类,质子数相同的微粒一定属于同种元素
C. 中和反应一定生成盐和水,生成盐和水的反应一定是中和反应
D. 碱性溶液能使石蕊试液变蓝,能使石蕊试液变蓝的溶液一定呈碱性
10.(2020九上·西湖月考)下表是所测得某些食物的近似pH,下列说法中正确的是( )
物质 柠檬 鸡蛋清 苹果 西红柿 牛奶
pH 2.3 7.9 3.1 4.2 6.5
A. 牛奶和鸡蛋清均呈碱性 B. 柠檬汁能使酚酞试液变红色
C. 胃酸过多的人应少食苹果 D. 西红柿的酸性比苹果强
三、常见的酸
11.(2020九上·台州期中)在加压降温的条件下,不具酸性的氯气液化为油状液体叫液氯。氯气溶于水得到的水溶液叫氯水,其中含有H+、Cl-等离子。下列说法错误的是( )
A. 氯气溶于水时发生了化学变化 B. 液氯与氯水一样都具有酸性
C. 往氯水中滴加碳酸钠溶液会有气泡生成 D. 往氯水中滴加硝酸银溶液后有白色沉淀产生
12.(2021·定海模拟)归纳总结、对比分析是学习常用的科学方法,如图所示:两圆重叠的区域表示它们的共同特征(相似点),重叠区域以外的部分表示它们的独有特征(不同点),某同学对(1)(2)(3)(4)区域相对应的内容填写正确的是( )
A.(1)区域:由碳原子和氧原子组成
B.(2)区域:具有还原性
C.(3)区域:能使酚酞试液变色
D.(4)区域:跟某些金属氧化物反应
13.(2021·鄞州模拟)下列图像不能正确表示对应变化关系的是( )
A. 图甲表示向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸时,产生的H2质量与稀盐酸质量的关系
B. 图乙表示两份完全相同的双氧水在有无MnO2情况下,产生O2质量与反应时间的关系
C. 图丙表示向一定量的稀盐酸中加入过量的NaOH溶液时,溶液pH随NaOH溶液质量的变化关系
D. 图丁表示向一定量Ba(OH)2溶液中滴加过量H2SO4溶液时的溶液导电性与时间的关系
14.(2021·南湖模拟)硫酸是一种常见的酸。下列关于硫酸的说法中,正确的是( )
A. 组成:硫酸溶液中有H+和SO42-两种微粒,且数目相同
B. 性质:能与碱、多种金属和CO2、SO3等非金属氧化物反应
C. 用途:可用于清除铁表面的氧化铁和生产化肥硫酸铵
D. 检验:滴入氯化钡溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解
15.(2021九下·杭州开学考)生活中有很多“禁忌”,即不能做的事情。下列“禁忌”与相关的科学解释对应的是( )
选项 禁忌 原理解释
A 用锡壶装醋酸 活动性顺序:Sn
C 用稀HCl除铁锈时,浸泡太久 6HCl+2Fe=2FeCl3+3H2↑
D 浓硫酸洒在手上,直接用水冲洗 浓硫酸具有吸水性
A. A B. B C. C D. D
16.(2021九上·台州开学考)现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如右图所示.下列说法正确的是( )
A. 滴至a克时,溶液中反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B. 滴至b克时,溶液中含HCl、NaCl两种溶质
C. 滴至c克时,溶液中溶质质量比原混合溶液中溶质质量大
D. 滴至d克时,溶液呈中性
17.(2020九上·绍兴月考)在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入100g溶质质量分数为19.6%的稀硫酸,将天平调节至平衡,然后向左盘的烧杯中投入一定质量的铁,向右盘的烧杯中投入一定质量的镁,均恰好完全反应。下列说法正确的是( )
A. 实验结束后,指针偏向右盘
B. 由于消耗的硫酸质量相等,实验结束后,指针不偏转
C. 实验结束后,欲使天平重新平衡,则可向左盘的烧杯中加入6.4g的铁
D. 实验结束后,欲使天平重新平衡,则可向右盘的烧杯中加入6.4g的镁
18.(2020九上·瑞安月考)天平两边各放质量相等的烧杯,分别盛有等质量、等质量分数的足量稀硫酸,此时天平平衡。然后在两边的烧杯中各加入下列物质,充分反应后天平仍保持平衡的是( )
①10克铁和10克氧化铁
②10克铜和10克氧化铜
③5.6克铁和6.5克锌
④6.5克锌和6.3克氧化锌
A. ①②③ B. ①②④ C. ②④ D. ③④
四、常见的碱
19.(2021·金华模拟)向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
A.a点溶液中滴入紫色石蕊试液变蓝
B.d点溶液中的溶质是NaCl和NaOH
C.ab段(不含b点)反应的化学方程式为HCl+NaOH=NaCl+H2O
D.整个变化过程溶液中镁离子数目没有改变
20.(2021·鄞州模拟)一定温度下,向ag FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述错误的是( )
A. P点对应的溶液中NaOH达到饱和状态
B. 加入 ngNaOH时,NaOH固体和FeCl3溶液恰好完全反应
C. m>c-a
D. 生成Fe(OH)3的质量为(b-a)g
21.(2020九上·吴兴月考)某化学小组在课外活动时做了一个实验:在甲试管中装入固体物质,乙试管中装入液体试剂,按如图所示组装好仪器(图中铁架台等仪器已略去)。通过分液漏斗加入足量的稀硫酸,同时打开止水夹,看到乙试管液体中有气泡冒出,一段时间后,关闭止水夹,发现乙中液面上升,溶液变浑浊。符合以上实验现象的一组试剂是( )
A. KNO3 BaCl2 B. Na2CO3 NaOH C. Zn Ba(NO3)2 D. MgCO3 NaNO3
22.归纳和演绎是重要的科学方法。下列归纳或演绎合理的是( )
A. 有机物是一类含碳化合物,所以CH4、CO2都是有机物
B. 稀有气体可做保护气,可做保护气的一定是稀有气体
C. 金属Fe、Zn能与酸反应生成氢气,所以金属都能与酸反应生成氢气
D. 单质是由一种元素组成,由一种元素组成的纯净物一定是单质
23.(2020九上·萧山期中)将a%的氢氧化钠溶液b克和b%的硫酸溶液a克混合,充分反应后,下列物质不能与这种混合液发生反应的是( )
A. 铁粉 B. 氯化铁溶液 C. 盐酸 D. 氯化钡溶液
24.(2021九上·金华月考)取200g一定质量分数的CuSO4溶液,先逐滴滴加100gBa(OH)2溶液至b点,后再逐滴滴加稀HCl溶液至过量,整个过程中加入溶液的质量与沉淀质量关系如图所示。下列说法不正确的是( )
A.oa段溶液的导电性将逐渐减弱
B.至d点时溶液中所含的溶质有BaCl2、CuCl2、HCl
C.bc段发生反应的化学方程式2HCl+Ba(OH)2=BaCl2+2H2O
D.m的值是3.35g
25.(2020·宁波)某锥形瓶内盛有盐酸和氯化铜的混合溶液100g,向其中加入溶质质量分数为10%的V氢氧化钠溶液,锥形瓶内溶液质量m1与加入的氢氧化钠溶液质量m2的变化关系如图所示。下列说法错误的是( )
A. 反应至A点时,所加NaOH溶液的质量为40g
B. 反应至A点时,溶液中的溶质有CuCl2和NaCl
C. 反应至B点时,锥形瓶内溶液的质量为280.4g
D. 反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
26.(2019·宁波模拟)烧杯中盛有MgSO4和HCl的混合溶液100.0g,向其中逐滴滴加Ba(OH)2溶液,产生沉淀的质量与滴加的溶液质量关系如图所示。下列说法正确的是()
A. a点对应溶液中溶质是MgCl2 B. Ba(OH)2溶液的溶质质量分数为17.1%
C. b-c段是MgSO4与Ba(OH)2反应 D. 0-a段产生的沉淀是BaSO4与Mg(OH)2
27.小科为研究“碱与盐反应”的规律,设计了如图所示的五组实验,每支试管盛有3毫升溶液,分别向试管中只滴加3滴溶液。除氢氧化钙溶液是饱和外,其余溶液的质量分数都为5%。下列叙述正确的是( )
A. 甲组和乙组实验能观察到相同现象 B. 乙组和丙组实验均能观察到蓝色沉淀
C. 乙组实验产生的沉淀质量比丁组多 D. 戊组实验产生的沉淀质量比丙组少
五、酸碱之间的反应
28.如图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。下列说法正确的是( )
A. 在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B. 在a曲线所示的实验中,若用酚酞做指示剂,酚酞试液由红色变为无色
C. 在a、b、c三种曲线所示的实验中,反应速率相同
D. 在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
29.(2018·温州模拟)将a%的氢氧化钾溶液b克和b%的硫酸溶液a克混合,下列物质不能与这种混合液发生反应的是( )
A. 氧化铜粉末 B. 盐酸 C. 氢氧化钠固体 D. 氯化钡溶液
30.完全中和一定量的某盐酸溶液,需要100克8%的KOH溶液,若改用100克8%的NaOH溶液,则反应后溶液的pH为( )
A. 大于7 B. 小于7 C. 等于7 D. 无法确定
31.如图是物质间发生化学反应的颜色变化,其中X是( )
A. 稀盐酸 B. 稀硫酸 C. 硫酸钠溶液 D. 澄清石灰水
32.将10g质量分数为20%的氢氧化钠溶液与20g质量分数为10%的硫酸溶液混合后,下列物质中不能与该溶液发生反应的是( )
A. Na2CO3 B. CuCl2 C. CO2 D. Ba(NO3)2
3.右图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是( )
A. 反应结束时溶液的pH=7 B. 反应前后元素的种类没有变化
C. 反应后溶液中存在的粒子只有Na+和Cl- D. 该反应的实质是H+和OH-结合生成H2O分子
34. 下列4个图形能正确反映对应变化关系的是( )
A. 向一定量稀硫酸中加入NaOH溶液
B. 向一定量CuSO4溶液中加入Zn粉
C. 加热KClO3与MnO2固体混合物
D. 向一定量NaOH和Ca(OH)2的混合溶液中加入Na2CO3溶液
六、常见的盐
35.(2020·海曙模拟)向盛有HCl和CuCl2混合溶液的烧杯中逐滴加入NaOH溶液至过量。在该过程中,下列4个图像能正确反映烧杯内物质的某些科学量变化趋势的是( )
A. ①③ B. ①②④ C. ②④ D. ①②③
36.(2020九上·椒江期中)有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种。某化学兴趣小组为探究其成分做了以下实验:
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示。
Ⅱ.取少量B点时的溶液于试管中,滴加酚酞试液,溶液不变色。
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。
下列说法正确的是( )
A. BC之间能看到有气泡生成,是Na2CO3与稀硝酸反应生成
B. 原白色固体一定没有氯化钾
C. 当稀硝酸加到D点时,溶液中一定含有的溶质是NaNO3、Ba(NO3)2、HNO3 , 可能有 Na2SO4
D. 步骤Ⅰ中反生反应生成的沉淀一定是BaCO3和BaSO4
37.(2020九上·越城月考)下列各组物质的溶液,不需要外加试剂就能鉴别出来的是( )
A. NaOH,FeCl3 , NaCl,KCl B. Na2SO4 , NaCl,BaCl2 , KNO3
C. Na2SO4 , BaCl2 , Na2CO3 , HCl D. Na2CO3 , H2SO4 , HCl,KCl
38.(2020九上·余杭月考)将一定质量的Ba(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
A. N点时,所得溶液的pH=7
B. Q点时,所得溶液中的溶质只含有BaCl2
C. O至P段发生反应的化学方程式为NaOH+HCl=NaCl+H2O
D. P至Q段发生反应的化学方程式为Ba(OH)2+2HICl=BaCl2+2H2O
39.(2020九上·慈溪期中)一瓶不纯的K2CO3粉末,所含杂质可能是KNO3、Ca(NO3)2、KCl、CuCl2、Na2CO3中的一种或几种,为确定其成分,进行如下实验:
⑴取少量该粉末于烧杯中,加入适量蒸馏水,充分搅拌,得无色澄清溶液。
⑵取上述无色溶液少许于试管中,滴加AgNO3溶液有沉淀生成,再加入足量的稀HNO3溶液,沉淀部分溶解。
⑶另称取1.38g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的BaCl2溶液,充分反应后生成1.97g白色沉淀。下列说法正确的是( )
A. 杂质中可能含有KNO3、Na2CO3 B. 杂质中肯定不含有Ca(NO3)2、CuCl2、Na2CO3
C. 杂质中肯定含有KCl,可能含有Na2CO3 D. 杂质中肯定含有KCl、Na2CO3 , 可能含有KNO3
40.(2020·新昌模拟)向100克的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
A. 0-a段发生的反应属于复分解反应
B. m的值为2.33克
C. 该混合溶液中Na2CO3的质量分数是2.12%
D. 取c点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
41.(2020九上·绍兴期末)有一包不纯的碳酸钠白色粉末,可能含有硫酸钠、氢氧化钠的一种或几种,某科学兴趣小组为探究其成分做了如下实验:
Ⅰ。现取样品16g于烧杯中并加84g水搅拌,全部溶解。再向烧杯中逐渐滴加26.1%硝酸钡溶液并不断搅拌,烧杯内固体的质量随加入硝酸钡溶液的质量的变化如图甲所示;
Ⅱ。在B点开始,向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图乙所示。则下列错误的是( )
A. 原白色固体中由Na2CO3 , Na2SO4 , NaOH组成
B. E点时,溶液中一定含有的溶质是HNO3 , Ba(No3)2 , NaNO3
C. D点时,溶液中硝酸钠的溶质质量为304.94克
D. 原白色粉末中含Na2CO3质量为10.6克
42.下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是( )
①NaCl、BaCl2、CuSO4、NaOH、NH4NO3②Ba(NO3)2、NaCl、Na2SO4、H2SO4、HCl
③NaOH、FeCl3、MgSO4、BaCl2、KCl ④AgNO3、HCl、K2CO3、NaCl、BaCl2
A. ①②④ B. ①②③ C. ①③④ D. ②④
43.(2017九上·杭州月考)某同学想用实验证明 CuSO4 溶液显蓝色是由 Cu2+造成的,下列实验无意义的是( )
A. 将 CuSO4 溶液加水稀释 B. 观察 Cu( NO3)2 溶液
C. 观察 Na2SO4 D. 向 CuSO4 溶液中滴加足量 NaOH 溶液
44.(2016·宁波)现将10.6g某固体混合物样品与足量稀盐酸起反应,收集到4.4gCO2。若此混合物是由MgCO3、Na2CO3、CaCO3和K2CO3中的3种物质所组成,则该混合物组成不可能是( )
A. Na2CO3、CaCO3和K2CO3 B. Na2CO3、CaCO3和MgCO3
C. Na2CO3、K2CO3和MgCO3 D. CaCO3、K2CO3和MgCO3
45.(2016九下·镇海竞赛)一包混有杂质的Na2CO3 , 其杂质可能是Ba(NO3)2、KCl、NaHCO3一种或几种,今取10.6g样品,溶于水得澄清溶液,另取5.3克样品,加入足量的盐酸,收集到2gCO2 , 则下列判断正确的是( )
A. 样品中只含有NaHCO3 B. 样品中一定混有NaHCO3 , 可能有KCl
C. 样品中有NaHCO3 , 也有Ba(NO3)2 D. 样品中混有KCl,也可能有NaHCO3
答案解析部分
一、物质及其变化
1.【答案】 D2.【答案】 D 3.【答案】 A 4.【答案】 B 5.【答案】 C
二、物质的酸碱性
6.【答案】 C7.【答案】 A 8.【答案】 D 9.【答案】 D 10.【答案】 C
三、常见的酸
11.【答案】 B 12.【答案】 B 13.【答案】 B14.【答案】 C
15.【答案】 B 16.【答案】 C17.【答案】 D 18.【答案】 C
四、常见的碱
19.【答案】 C 20.【答案】 D 21.【答案】 C 22.【答案】 B
23.【答案】 A 24.【答案】 D 25.【答案】 D 26.【答案】 B 27.【答案】 D
五、酸碱之间的反应
28.【答案】 A 29.【答案】 B 30.【答案】 A 31.【答案】 B 32.【答案】 A
33.【答案】 C 34.【答案】 C
六、常见的盐
35.【答案】 B 36.【答案】 D 37.【答案】 C 38.【答案】 C
39.【答案】 D 40.【答案】 D 41.【答案】 C 42.【答案】 C
43.【答案】 A 44.【答案】 B 45.【答案】 D
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
