5.1 金属的性质和利用 同步训练— 2021-2022学年九年级沪教版(全国)上册(有答案)
文档属性
| 名称 | 5.1 金属的性质和利用 同步训练— 2021-2022学年九年级沪教版(全国)上册(有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 354.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-24 00:00:00 | ||
图片预览



文档简介
5.1 金属的性质和利用
一、单选题
1.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。有关判断正确的是( )
A.滤渣中一定有银,没有铜和锌
B.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤渣中一定有银和锌,可能有铜
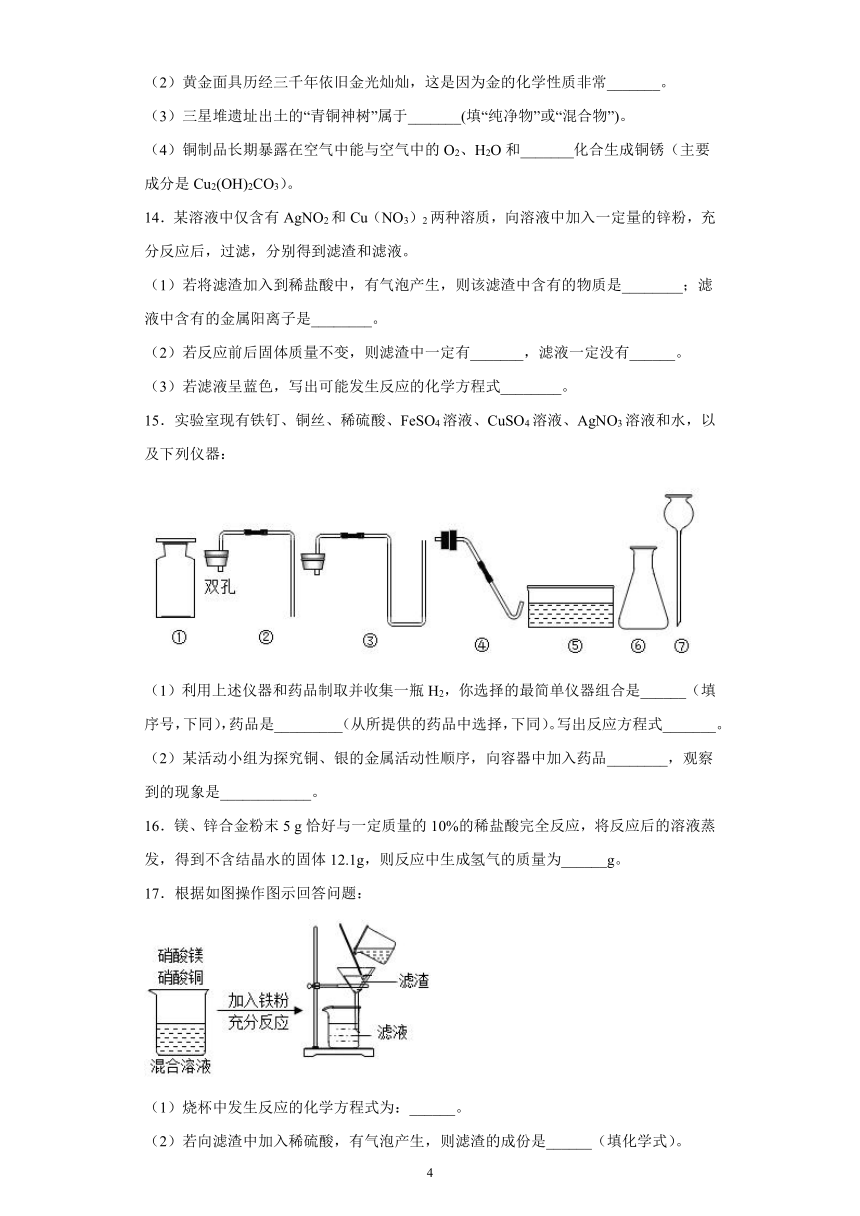
2.等质量的铁粉和锌粉与足量的同浓度的稀硫酸反应,下列图象正确的是( )
A. B. C. D.
3.将30g某合金粉末与足量的稀硫酸发生反应,生成1g氢气,这种合金的成分可能组成是( )
A.镁和铁 B.铁和锌 C.铝和镁 D.锌和铜
4.四川广汉三星堆出土的“青铜神树”让世人惊艳,史前文明或许存在。青铜属于( )
A.合金 B.盐 C.单质 D.化合物
5.下列物质与颜色对应错误的是( )
A.高锰酸钾—— 白色 B.二氧化锰—— 黑色
C.铜——红色 D.硫酸铜溶液—— 蓝色
6.下列有关物质的应用不正确的是( )
A.氧气炼钢
B.东汉晚期的青铜奔马
C.钛制人造骨
D.用锡制灯丝
7.有许多日常用品应用了物质的性质,下列说法不正确的是( )
A.冰箱门吸应用了磁铁的磁性 B.撑竽跳高应用了撑竿的弹性
C.导线用铜制造是应用了铜的导热性 D.不锈钢制作餐具利用了它的抗腐蚀性
8.下列关于“物质一用途一性质”的说法不正确的是( )
A.氧气一火箭发射一可燃性 B.铜一做导线一导电性好
C.氮气一食品防腐一常温下化学性质稳定 D.氦气一填充飞艇一密度小
9.下下列物质中,可用金属跟盐酸直接反应而制得的是( )
A.FeCl3 B.CuCl2 C.AlCl3 D.AgCl
10.下列图像中不能正确反映其对应实验操作的是( )
A. 等质量的铝片、镁片分别与足量且质量分数相同的稀盐酸反应
B. 等质量的铝片、铁片分别与足量且质量分数相同的稀硫酸反应
C. 金属镁与稀硫酸反应时的温度变化
D. 向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉
11.合金和金属在生活中广泛应用,下列说法不正确的是( )
A.硬币镀镍或镀铜能提高耐腐蚀性
B.铝常常用于户外输电线,是因为铝的化学性质不活泼
C.不锈钢是通过改变金属内部结构来提高抗腐蚀和抗氧化能力
D.钛合金与人体有良好的“相容性”在医疗上可用于制造人骨替代品
12.以铁、氧化铜、稀硫酸三种物质为原料制取铜,有两条途径:①;②,若需制得相同质量的铜,在实际实验过程中这两条途径所消耗的有关物质质量相同的是( )
A.消耗相同质量的氧化铜 B.消耗相同质量的铁
C.消耗相同质量的硫酸 D.生成硫酸亚铁的质量相同
二、填空题
13.2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有(填序号);
A.象牙 B.黄金 C.丝织品 D.青铜
(2)黄金面具历经三千年依旧金光灿灿,这是因为金的化学性质非常_______。
(3)三星堆遗址出土的“青铜神树”属于_______(填“纯净物”或“混合物”)。
(4)铜制品长期暴露在空气中能与空气中的O2、H2O和_______化合生成铜锈(主要成分是Cu2(OH)2CO3)。
14.某溶液中仅含有AgNO2和Cu(NO3)2两种溶质,向溶液中加入一定量的锌粉,充分反应后,过滤,分别得到滤渣和滤液。
(1)若将滤渣加入到稀盐酸中,有气泡产生,则该滤渣中含有的物质是________;滤液中含有的金属阳离子是________。
(2)若反应前后固体质量不变,则滤渣中一定有_______,滤液一定没有______。
(3)若滤液呈蓝色,写出可能发生反应的化学方程式________。
15.实验室现有铁钉、铜丝、稀硫酸、FeSO4溶液、CuSO4溶液、AgNO3溶液和水,以及下列仪器:
(1)利用上述仪器和药品制取并收集一瓶H2,你选择的最简单仪器组合是______(填序号,下同),药品是_________(从所提供的药品中选择,下同)。写出反应方程式_______。
(2)某活动小组为探究铜、银的金属活动性顺序,向容器中加入药品________,观察到的现象是____________。
16.镁、锌合金粉末5 g恰好与一定质量的10%的稀盐酸完全反应,将反应后的溶液蒸发,得到不含结晶水的固体12.1g,则反应中生成氢气的质量为______g。
17.根据如图操作图示回答问题:
(1)烧杯中发生反应的化学方程式为:______。
(2)若向滤渣中加入稀硫酸,有气泡产生,则滤渣的成份是______(填化学式)。
(3)反应后的滤液中溶质的化学式为______。
三、实验题
18.某化学小组的同学探究银、铜、铁三种金属的有关性质,设计了A、B、C三个方案。
方案A 方案B 方案C
(1)能验证三种金属活动性顺序的方案是______(填“A”或“B”或“C”)。
(2)方案B中,证明铁的活动性比铜强的现象是______。
(3)方案B有一只试管中的物质能与稀盐酸反应,原因是______。
(4)方案C试管内物质反应结束后,将①②试管内的物质倒入烧杯中(如图),一段时间后,溶液中一定有的阳离子______。如果看到______现象时,能证明银、铜、铁三种金属的活动性顺序。
19.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一支试管,取一次盐酸的探究方案。请你和他们一起完善下表的探究方案并回答有关问题:
(1)填表:
实验步骤 观察到的现象
①在试管中取少量盐酸,插入铁丝,充分反应 ___________
②在①所得的溶液中,插入___________,充分反应 无明显现象
③在②所得的溶液中插入___________,充分反应 ___________
结论:金属活动性:A1>Fe>Cu
(2)写出铁与盐酸反应的化学方程式___________;将铝丝插入前应进行的操作是___________。
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论。小华要补充的实验是___________。
(4)小强同学认为要得到A1>Fe>H>Cu的结论,不必做补充实验,需将小刚同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是___________。
20.按要求写出下列仪器的名称。
(1)量取8mL水选用_________(选填“50mL”或“10mL”)量筒、胶头滴管;
(2)收集和储存气体的是__________。
(3)用如图装置进行实验(夹持仪器略去)。加热一段时间后,蜡烛熔化、掉落,之后火柴燃烧,并且铜片变黑。
①请你写出铜片变黑的化学反应方程式__________。
②能体现物质化学性质的现象或变化有__________(填序号)。
A.酒精燃烧B.蜡烛熔化C.火柴燃烧D.铜片变黑
(4)1859年,镁燃烧产生的强光被用于拍摄高速运动的物体,被称为镁光灯。请你写出镁燃烧的现象________,镁燃烧的化学反应方程式_________。
参考答案
1.B
2.B
3.B
4.A
5.A
6.D
7.C
8.A
9.C
10.B
11.B
12.A
13.
(1)BD
(2)稳定
(3)混合物
(4)CO2
14.
(1) 锌、铜、银 锌离子2+
(2) Cu、Ag AgNO3
(3)
15.
(1) ①③⑥ 铁钉、稀硫酸 Fe+H2SO4=FeSO4+H2↑
(2) 铜丝和AgNO3溶液 铜丝表面附着白色固体,溶液由无色变为蓝色
16.0.2
17.
(1)
(2)Fe、Cu
(3)Mg(NO3)2、Fe(NO3)2
18.
(1)A
(2)试管②中无明显现象,试管③中有气泡产生
(3)在金属活动性顺序表中,铁的活动性排在氢之前 (其他合理叙述均可)
(4) 亚铁离子2+ 红色固体表面出现银白色物质
19.
(1) 产生气泡,溶液由无色变为浅绿色 铜丝 铝丝 溶液由浅绿色变为无色
(2) 用砂纸打磨,除去其表面的氧化膜
(3)把铜丝插入稀盐酸中
(4)Cu、Fe、Al
20.
(1)10ml
(2)集气瓶
(3) A、C、D
(4) 剧烈燃烧,发出耀眼的白光,生成白色固体
一、单选题
1.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。有关判断正确的是( )
A.滤渣中一定有银,没有铜和锌
B.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤渣中一定有银和锌,可能有铜
2.等质量的铁粉和锌粉与足量的同浓度的稀硫酸反应,下列图象正确的是( )
A. B. C. D.
3.将30g某合金粉末与足量的稀硫酸发生反应,生成1g氢气,这种合金的成分可能组成是( )
A.镁和铁 B.铁和锌 C.铝和镁 D.锌和铜
4.四川广汉三星堆出土的“青铜神树”让世人惊艳,史前文明或许存在。青铜属于( )
A.合金 B.盐 C.单质 D.化合物
5.下列物质与颜色对应错误的是( )
A.高锰酸钾—— 白色 B.二氧化锰—— 黑色
C.铜——红色 D.硫酸铜溶液—— 蓝色
6.下列有关物质的应用不正确的是( )
A.氧气炼钢
B.东汉晚期的青铜奔马
C.钛制人造骨
D.用锡制灯丝
7.有许多日常用品应用了物质的性质,下列说法不正确的是( )
A.冰箱门吸应用了磁铁的磁性 B.撑竽跳高应用了撑竿的弹性
C.导线用铜制造是应用了铜的导热性 D.不锈钢制作餐具利用了它的抗腐蚀性
8.下列关于“物质一用途一性质”的说法不正确的是( )
A.氧气一火箭发射一可燃性 B.铜一做导线一导电性好
C.氮气一食品防腐一常温下化学性质稳定 D.氦气一填充飞艇一密度小
9.下下列物质中,可用金属跟盐酸直接反应而制得的是( )
A.FeCl3 B.CuCl2 C.AlCl3 D.AgCl
10.下列图像中不能正确反映其对应实验操作的是( )
A. 等质量的铝片、镁片分别与足量且质量分数相同的稀盐酸反应
B. 等质量的铝片、铁片分别与足量且质量分数相同的稀硫酸反应
C. 金属镁与稀硫酸反应时的温度变化
D. 向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉
11.合金和金属在生活中广泛应用,下列说法不正确的是( )
A.硬币镀镍或镀铜能提高耐腐蚀性
B.铝常常用于户外输电线,是因为铝的化学性质不活泼
C.不锈钢是通过改变金属内部结构来提高抗腐蚀和抗氧化能力
D.钛合金与人体有良好的“相容性”在医疗上可用于制造人骨替代品
12.以铁、氧化铜、稀硫酸三种物质为原料制取铜,有两条途径:①;②,若需制得相同质量的铜,在实际实验过程中这两条途径所消耗的有关物质质量相同的是( )
A.消耗相同质量的氧化铜 B.消耗相同质量的铁
C.消耗相同质量的硫酸 D.生成硫酸亚铁的质量相同
二、填空题
13.2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有(填序号);
A.象牙 B.黄金 C.丝织品 D.青铜
(2)黄金面具历经三千年依旧金光灿灿,这是因为金的化学性质非常_______。
(3)三星堆遗址出土的“青铜神树”属于_______(填“纯净物”或“混合物”)。
(4)铜制品长期暴露在空气中能与空气中的O2、H2O和_______化合生成铜锈(主要成分是Cu2(OH)2CO3)。
14.某溶液中仅含有AgNO2和Cu(NO3)2两种溶质,向溶液中加入一定量的锌粉,充分反应后,过滤,分别得到滤渣和滤液。
(1)若将滤渣加入到稀盐酸中,有气泡产生,则该滤渣中含有的物质是________;滤液中含有的金属阳离子是________。
(2)若反应前后固体质量不变,则滤渣中一定有_______,滤液一定没有______。
(3)若滤液呈蓝色,写出可能发生反应的化学方程式________。
15.实验室现有铁钉、铜丝、稀硫酸、FeSO4溶液、CuSO4溶液、AgNO3溶液和水,以及下列仪器:
(1)利用上述仪器和药品制取并收集一瓶H2,你选择的最简单仪器组合是______(填序号,下同),药品是_________(从所提供的药品中选择,下同)。写出反应方程式_______。
(2)某活动小组为探究铜、银的金属活动性顺序,向容器中加入药品________,观察到的现象是____________。
16.镁、锌合金粉末5 g恰好与一定质量的10%的稀盐酸完全反应,将反应后的溶液蒸发,得到不含结晶水的固体12.1g,则反应中生成氢气的质量为______g。
17.根据如图操作图示回答问题:
(1)烧杯中发生反应的化学方程式为:______。
(2)若向滤渣中加入稀硫酸,有气泡产生,则滤渣的成份是______(填化学式)。
(3)反应后的滤液中溶质的化学式为______。
三、实验题
18.某化学小组的同学探究银、铜、铁三种金属的有关性质,设计了A、B、C三个方案。
方案A 方案B 方案C
(1)能验证三种金属活动性顺序的方案是______(填“A”或“B”或“C”)。
(2)方案B中,证明铁的活动性比铜强的现象是______。
(3)方案B有一只试管中的物质能与稀盐酸反应,原因是______。
(4)方案C试管内物质反应结束后,将①②试管内的物质倒入烧杯中(如图),一段时间后,溶液中一定有的阳离子______。如果看到______现象时,能证明银、铜、铁三种金属的活动性顺序。
19.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一支试管,取一次盐酸的探究方案。请你和他们一起完善下表的探究方案并回答有关问题:
(1)填表:
实验步骤 观察到的现象
①在试管中取少量盐酸,插入铁丝,充分反应 ___________
②在①所得的溶液中,插入___________,充分反应 无明显现象
③在②所得的溶液中插入___________,充分反应 ___________
结论:金属活动性:A1>Fe>Cu
(2)写出铁与盐酸反应的化学方程式___________;将铝丝插入前应进行的操作是___________。
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论。小华要补充的实验是___________。
(4)小强同学认为要得到A1>Fe>H>Cu的结论,不必做补充实验,需将小刚同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是___________。
20.按要求写出下列仪器的名称。
(1)量取8mL水选用_________(选填“50mL”或“10mL”)量筒、胶头滴管;
(2)收集和储存气体的是__________。
(3)用如图装置进行实验(夹持仪器略去)。加热一段时间后,蜡烛熔化、掉落,之后火柴燃烧,并且铜片变黑。
①请你写出铜片变黑的化学反应方程式__________。
②能体现物质化学性质的现象或变化有__________(填序号)。
A.酒精燃烧B.蜡烛熔化C.火柴燃烧D.铜片变黑
(4)1859年,镁燃烧产生的强光被用于拍摄高速运动的物体,被称为镁光灯。请你写出镁燃烧的现象________,镁燃烧的化学反应方程式_________。
参考答案
1.B
2.B
3.B
4.A
5.A
6.D
7.C
8.A
9.C
10.B
11.B
12.A
13.
(1)BD
(2)稳定
(3)混合物
(4)CO2
14.
(1) 锌、铜、银 锌离子2+
(2) Cu、Ag AgNO3
(3)
15.
(1) ①③⑥ 铁钉、稀硫酸 Fe+H2SO4=FeSO4+H2↑
(2) 铜丝和AgNO3溶液 铜丝表面附着白色固体,溶液由无色变为蓝色
16.0.2
17.
(1)
(2)Fe、Cu
(3)Mg(NO3)2、Fe(NO3)2
18.
(1)A
(2)试管②中无明显现象,试管③中有气泡产生
(3)在金属活动性顺序表中,铁的活动性排在氢之前 (其他合理叙述均可)
(4) 亚铁离子2+ 红色固体表面出现银白色物质
19.
(1) 产生气泡,溶液由无色变为浅绿色 铜丝 铝丝 溶液由浅绿色变为无色
(2) 用砂纸打磨,除去其表面的氧化膜
(3)把铜丝插入稀盐酸中
(4)Cu、Fe、Al
20.
(1)10ml
(2)集气瓶
(3) A、C、D
(4) 剧烈燃烧,发出耀眼的白光,生成白色固体
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
