3.3.1 物质的组成(课件 34页)
图片预览








文档简介
(共34张PPT)
课题1 物质的变化和性质
沪教版 化学(初中)
第3节 物质的组成
(第1课时)
同步课堂
学习目标:
重点难点:
1.知道化学式的涵义
2.会写出单质及简单化合物的化学式
3.归纳书写化学式的方法
1.化学式的涵义
2.化学式的书写
内 容 导 航
◆ 化学式反映物质的组成
◆ 化学式的书写
我们已经知道,水可以用H2O表示,氧气可以用O2表示,二氧化碳可以用CO,表示等。这些用元素符号和数字的组合表示纯净物组成的式子,称为该物质的化学式(chemical formula)。
【新课引入】
想一想,以上的“钙”、“铁”、“锌”、“碘”指的是什么?
请回忆,水、双氧水、二氧化锰、五氧化磷、高锰酸钾等化合物该用什么符号来表示呢?
H2O H2O2 MnO2 P2O5 KMnO4
学习过程:
一、化学式反映物质的组成
化学式是国际通用的表示物质组成的化学符号。它源于一个基本的事实:任何纯净物都有固定的组成,不同的物质组成不同。因此,化学式反映了物质的组成情况。
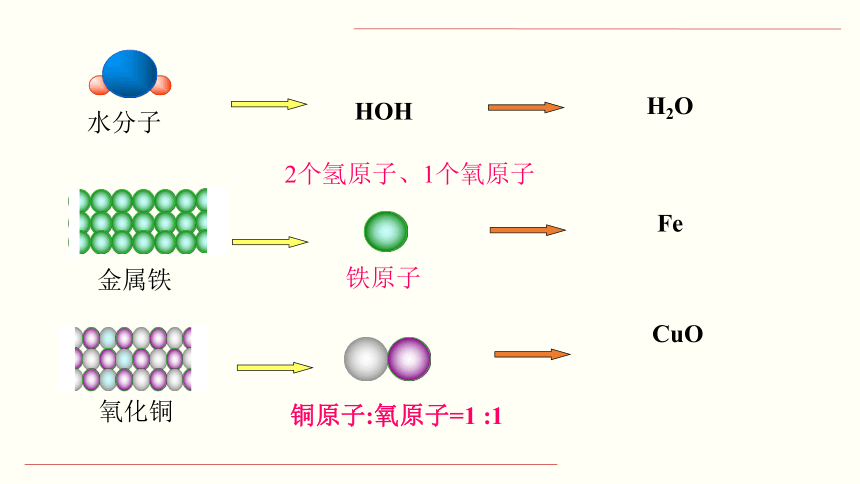
现在我们从微观角度来考察几种物质的组成与化学式的关系
水分子
金属铁
氧化铜
HOH
H2O
Fe
CuO
铜原子:氧原子=1 :1
铁原子
2个氢原子、1个氧原子
归纳与总结
用元素符号和数字的组合来表示物质组成的式子叫化学式。
(元素符号+数字)
注意:每种纯净物质的组成是固定的,所以只有纯净物才有化学式,且每一种物质只有一个化学式。
化学式定义:
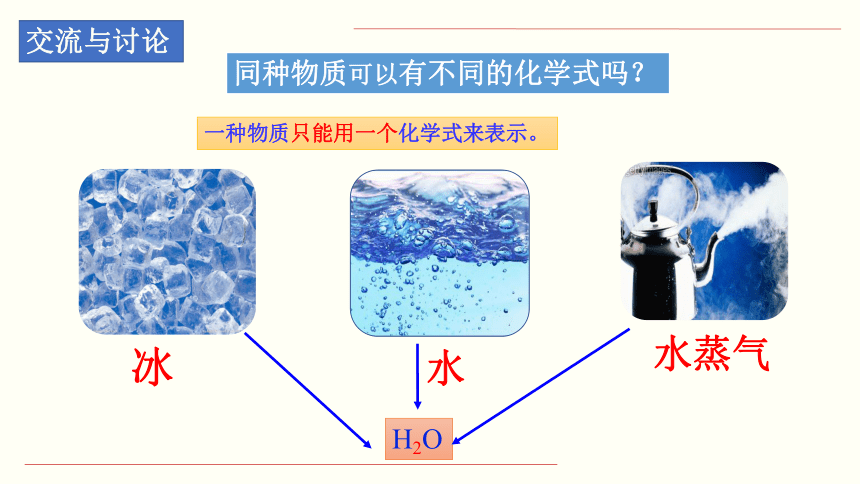
一种物质只能用一个化学式来表示。
同种物质可以有不同的化学式吗?
H2O
冰
水蒸气
水
交流与讨论
水由大量水分子聚集而成,水的组成元素是H和O,每个水分子由2个氢原子和1个氧原子构成。表示水组成的化学式H2O ,实际上表示了水分子的构成,也可称为水的分子式。
金属铁由许许多多铁原子构成,用铁的元素符号Fe来表示金属铁。其他金属和稀有气体也用元素符号来表示它们的构成,如Cu表示金属铜,表示这些物质构成的元素符号也就是它们的化学式。
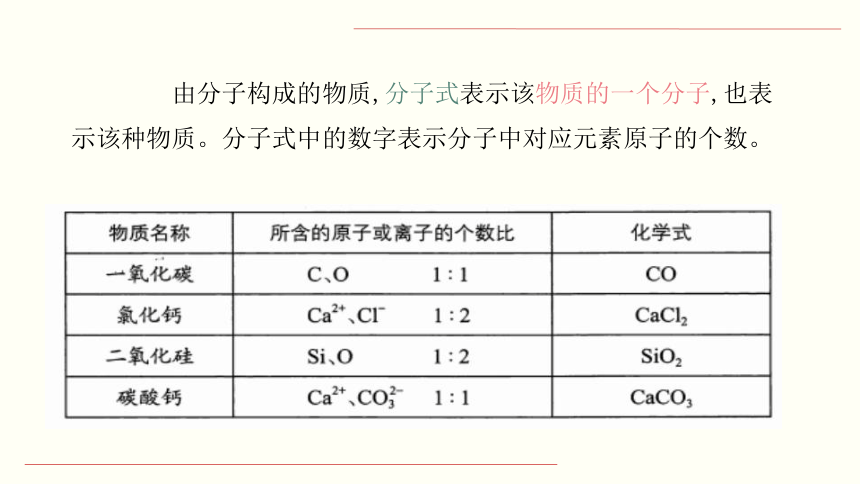
由分子构成的物质,分子式表示该物质的一个分子,也表示该种物质。分子式中的数字表示分子中对应元素原子的个数。
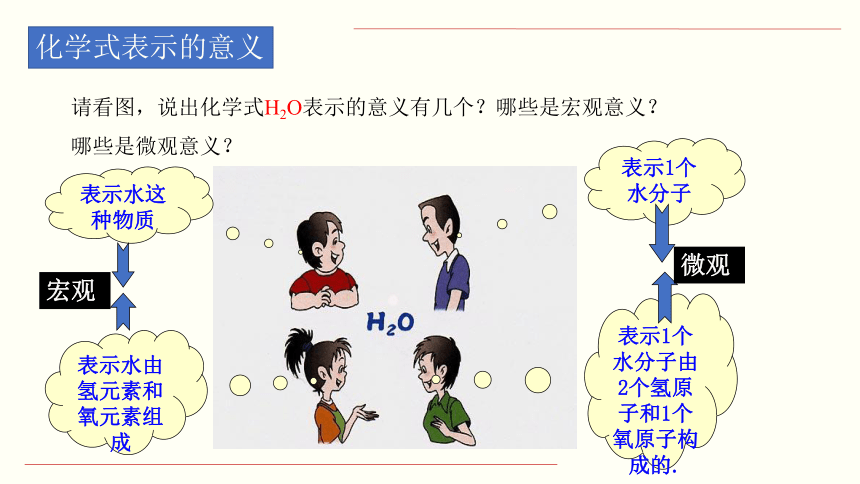
化学式表示的意义
表示1个水分子由2个氢原子和1个氧原子构成的.
表示1个水分子
表示水这种物质
表示水由氢元素和氧元素组成
请看图,说出化学式H2O表示的意义有几个?哪些是宏观意义?
哪些是微观意义?
宏观
微观
③表示一个分子
④表示一个分子由几个原子构成
①表示一种物质
②表示物质由什么元素组成
宏观
微观
归纳与小结
化学式的意义
交流与讨论
3.化学式前加数字就只具有微观意义。
只表示2个水分子。
一个水分子中含有2个氢原子
2H2O:
化学式周围数字的意义?
2.化学式中元素符号右下角的数字表示每个分子中的原子个数。
1.化学式前面的数字表示分子个数。
单质是由同种元素组成的纯净物。有些单质的化学式直接用组成元素的元素符号表示,那你们知道化合物的化学式该怎么表示?
二、化学式的书写
单质
( 1 )金属和某些固态非金属单质(结构较复杂,直接用元素符号表示)如:Fe、Cu、Al,C、S、P等
( 2 )双原子或多原子分子构成的单质,如:O2、N2、H2、Br2、O3等
( 3 )稀有气体由原子构成,用元素符号表示,如:He、Ne、Ar等
化学式的书写
①原则:必须依据实验测定的结果书写,不能凭空臆造。
②书写规则:
单质
物质类别
化合物
书写规则
化学式实例
金属单质
稀有气体单质
固态非金属单质
气态非金属单质
用元素符号表示
铁 Fe 铝 Al
碳 C 红磷 P
氦气 He 氖气 Ne
元素符号右下角写一个分子所含原子个数
氢气 H2 氧气 O2
氧化物
氧在后,另一元素在前,原子个数
分别写在右下角
二氧化碳 CO2
五氧化二磷 P2O5
其它化合物
金属元素在前,非金属元素在后,
原子个数分别写在右下角
氯化钠 NaCl
氯化镁 MgCl2
化合价
化合物都有固定的组成,元素的原子之间有固定的个数比,如:
HCl H2O NaCl Na2S Fe2O3
1:1 2:1 1:1 2:1 2:3
1、化合价概念:
化学上用“化合价”来表示不同原子之间相互化合的数目。
注意:但是化合价≠原子个数比
结论:元素的化合价是元素的原子之间形成化合物时表现出来的一种性质,用来表示原子间化合的数目。化合价有正价和负价。
原子团(根)
注意:
NaOH、 Ca(OH)2 、Cu(NO3)2、NH4NO3、BaSO4、CaCO3、 H3PO4
根:
离子:
OH-:
NH4+:
NO3-:
CO32-:
SO42-:
PO43-:
氢氧根离子
铵根离子
硝酸根离子
碳酸根离子
硫酸根离子
磷酸根离子
作为一个整体参加反应的原子集团(就好像一个原子一样),原子团也叫作根。
①原子团不能单独存在;
②带电荷的原子团也是离子。
归纳与小结
离子符号和化合价的表示方法不同:
离子:数字在前,“+”“-”号在后;写在右上角。
化合价:数字在后,“+”“-”号在前;写在正上方。
化合价与离子所带电荷的联系:数字相同,正负号相同。
离子符号与化合价的比较:
离子符号 Na+ Mg2+ Al3+ F- O2-
化合价 Na Mg Al F O
+1
+2
+3
-1
-2
交流与讨论
归纳与小结
化合价歌谣
一价钾钠氯氢银,二价氧钙钡镁锌,
三铝四硅五氮磷,二三铁、二四碳,
二四六硫均齐全,铜汞二价最常见,
化合价,要记清,莫忘单质价为零!
归纳与小结
化合价的有关规律:
①在任何化合物里,正负化合价的代数和为零。
②在化合物里氢通常显+1价,氧通常显-2价。
③金属元素通常显正价,非金属元素通常显负价。
④单质里元素的化合价为零。
⑤许多元素具有可变化合价,同种元素在不同的化合物里可显不
同的化合价,如:FeO,Fe2O3中铁元素的化合价分别为+2和+3。
根据化合价书写化合物的化学式
步骤如下:
一排序:元素符号按正价前,负价后顺序排列。
二标价:标出各元素的化合价,若有原子团只标出原子团的化合价。
三交叉:将元素化合价的绝对值交叉写在另一元素符号的右下角。
四约简:将各元素的原子个数约成最简整数比。
五检查:查化合价代数和是否为零。
一排顺序二标价
价数交叉写右下
约简价数作角码
总价为零去检查
口诀
“排 标 叉 查”
排列素
正价前
负价在后
标出元素
的化合价
交叉价数
检查代数和是否为零
已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式。
【思路】
(1)先写元素符号(正前负后)
(2)标出各元素的化合价(正上)
(3)把化合价数值化为最简
(4)把化简后的数字交叉写在
相应元素符号的右下角(1省略不写)
P O
+5 -2
P O
P2 O 5
+ 5 -2
+ 5 -2
P O
2 5
+ 5 -2
即化学式为:P2 O 5
写出下列化合物的化学式。
氧化钾
氧化钙
氧化铁
氯化钾
氯化镁
氯化亚铁
氢氧化钾
氢氧化钙
氢氧化铁
硫酸钾
硫酸钙
硫酸铁
Fe2O3
FeCl2
Fe(OH)3
Fe 2 (SO4) 3
K2O
MgCl2
KCl
KOH
K2SO4
CaO
Ca(OH)2
Ca SO4
课堂练习
【典例精讲】
A
例1.(2021河南省郑州市金水区二模)下列化学符号能表示2个氢原子的是( )
A.2H B.H2
C.2H2 D.2H+
【解析】表示原子个数时只需要在元素符号前面加数字即可,A正确;B表示一个氢分子或氢气,不符题意;C表示两个氢分子,不符题意;D表示两个氢离子,不符题意。故选A。
【答案】D
【解析】A、在室温下,1L水中能溶解约30mL氧气,而氢气难溶于水,室温下,溶解的比氧气少,
故得到氧气和氢气的体积比小于1:2,不符合题意;
B、碳能与氧气在一定条件下反应生成二氧化碳,故可能是部分氧气与碳棒发生了反应,不符合题意;
C、碳棒具有疏松多孔的结构,可能会吸附一部分氧气,不符合题意;
D、在电解水实验中,“正氧负氢”,氧气在正极生成,氢气在负极生成,故氧气与氢气不可能重新生成水,符合题意。故选D。
例2.(2021黑龙江齐齐哈尔阿城区二模)下列化学用语表述正确的是( )
A.硫酸钾的化学式:K2SO4 B.1 个氯分子:Cl
C.2 个硝酸根:2NO2 D.铜离子:Cu
【解析】硫酸钾的化学式为K2SO4 ,A正确; 1 个氯分子为 Cl2,B错误;2 个硝酸根为2NO3﹣,C错误;铜离子为Cu2+,D错误。故选A。
A
【典例精讲】
例3.(2021·广西中考真题)钛和钛合金是制造飞机的重要材料,钛
酸亚铁(FeTiO3)中钛元素的化合价为( )
A.+2 B.+3
C.+4 D.+5
【解析】钛酸亚铁中铁元素化合价为正二价、氧元素化合价为负二价,设钛元素化合价为x,化合物中正负化合价代数和为零;则(+2)+ x +(-2)×3=0,x=+4。故选C。
C
【典例精讲】
A
【达标测评】
1.下列化学式中,书写错误的是 ( )
A.氧化钙(OCa)
B.氧化镁(MgO)
C.三氯化铁 (FeCl3)
D.三氧化硫(SO3)
2.(2021·湖北襄阳市·中考真题)化学用语是学习和研究化学的工具。
下列化学用语表示正确的是( )
A.汞元素:HG B.镁离子:Mg2+
C.高锰酸钾:K2MnO4 D.2个氮原子:N2
B
【达标测评】
【归纳小结】
化学式
意义
写方法
宏观意义
微观意义
1.完成配套练习册;
2.预习物质的组成。
【作业布置】
谢 谢!
课题1 物质的变化和性质
沪教版 化学(初中)
第3节 物质的组成
(第1课时)
同步课堂
学习目标:
重点难点:
1.知道化学式的涵义
2.会写出单质及简单化合物的化学式
3.归纳书写化学式的方法
1.化学式的涵义
2.化学式的书写
内 容 导 航
◆ 化学式反映物质的组成
◆ 化学式的书写
我们已经知道,水可以用H2O表示,氧气可以用O2表示,二氧化碳可以用CO,表示等。这些用元素符号和数字的组合表示纯净物组成的式子,称为该物质的化学式(chemical formula)。
【新课引入】
想一想,以上的“钙”、“铁”、“锌”、“碘”指的是什么?
请回忆,水、双氧水、二氧化锰、五氧化磷、高锰酸钾等化合物该用什么符号来表示呢?
H2O H2O2 MnO2 P2O5 KMnO4
学习过程:
一、化学式反映物质的组成
化学式是国际通用的表示物质组成的化学符号。它源于一个基本的事实:任何纯净物都有固定的组成,不同的物质组成不同。因此,化学式反映了物质的组成情况。
现在我们从微观角度来考察几种物质的组成与化学式的关系
水分子
金属铁
氧化铜
HOH
H2O
Fe
CuO
铜原子:氧原子=1 :1
铁原子
2个氢原子、1个氧原子
归纳与总结
用元素符号和数字的组合来表示物质组成的式子叫化学式。
(元素符号+数字)
注意:每种纯净物质的组成是固定的,所以只有纯净物才有化学式,且每一种物质只有一个化学式。
化学式定义:
一种物质只能用一个化学式来表示。
同种物质可以有不同的化学式吗?
H2O
冰
水蒸气
水
交流与讨论
水由大量水分子聚集而成,水的组成元素是H和O,每个水分子由2个氢原子和1个氧原子构成。表示水组成的化学式H2O ,实际上表示了水分子的构成,也可称为水的分子式。
金属铁由许许多多铁原子构成,用铁的元素符号Fe来表示金属铁。其他金属和稀有气体也用元素符号来表示它们的构成,如Cu表示金属铜,表示这些物质构成的元素符号也就是它们的化学式。
由分子构成的物质,分子式表示该物质的一个分子,也表示该种物质。分子式中的数字表示分子中对应元素原子的个数。
化学式表示的意义
表示1个水分子由2个氢原子和1个氧原子构成的.
表示1个水分子
表示水这种物质
表示水由氢元素和氧元素组成
请看图,说出化学式H2O表示的意义有几个?哪些是宏观意义?
哪些是微观意义?
宏观
微观
③表示一个分子
④表示一个分子由几个原子构成
①表示一种物质
②表示物质由什么元素组成
宏观
微观
归纳与小结
化学式的意义
交流与讨论
3.化学式前加数字就只具有微观意义。
只表示2个水分子。
一个水分子中含有2个氢原子
2H2O:
化学式周围数字的意义?
2.化学式中元素符号右下角的数字表示每个分子中的原子个数。
1.化学式前面的数字表示分子个数。
单质是由同种元素组成的纯净物。有些单质的化学式直接用组成元素的元素符号表示,那你们知道化合物的化学式该怎么表示?
二、化学式的书写
单质
( 1 )金属和某些固态非金属单质(结构较复杂,直接用元素符号表示)如:Fe、Cu、Al,C、S、P等
( 2 )双原子或多原子分子构成的单质,如:O2、N2、H2、Br2、O3等
( 3 )稀有气体由原子构成,用元素符号表示,如:He、Ne、Ar等
化学式的书写
①原则:必须依据实验测定的结果书写,不能凭空臆造。
②书写规则:
单质
物质类别
化合物
书写规则
化学式实例
金属单质
稀有气体单质
固态非金属单质
气态非金属单质
用元素符号表示
铁 Fe 铝 Al
碳 C 红磷 P
氦气 He 氖气 Ne
元素符号右下角写一个分子所含原子个数
氢气 H2 氧气 O2
氧化物
氧在后,另一元素在前,原子个数
分别写在右下角
二氧化碳 CO2
五氧化二磷 P2O5
其它化合物
金属元素在前,非金属元素在后,
原子个数分别写在右下角
氯化钠 NaCl
氯化镁 MgCl2
化合价
化合物都有固定的组成,元素的原子之间有固定的个数比,如:
HCl H2O NaCl Na2S Fe2O3
1:1 2:1 1:1 2:1 2:3
1、化合价概念:
化学上用“化合价”来表示不同原子之间相互化合的数目。
注意:但是化合价≠原子个数比
结论:元素的化合价是元素的原子之间形成化合物时表现出来的一种性质,用来表示原子间化合的数目。化合价有正价和负价。
原子团(根)
注意:
NaOH、 Ca(OH)2 、Cu(NO3)2、NH4NO3、BaSO4、CaCO3、 H3PO4
根:
离子:
OH-:
NH4+:
NO3-:
CO32-:
SO42-:
PO43-:
氢氧根离子
铵根离子
硝酸根离子
碳酸根离子
硫酸根离子
磷酸根离子
作为一个整体参加反应的原子集团(就好像一个原子一样),原子团也叫作根。
①原子团不能单独存在;
②带电荷的原子团也是离子。
归纳与小结
离子符号和化合价的表示方法不同:
离子:数字在前,“+”“-”号在后;写在右上角。
化合价:数字在后,“+”“-”号在前;写在正上方。
化合价与离子所带电荷的联系:数字相同,正负号相同。
离子符号与化合价的比较:
离子符号 Na+ Mg2+ Al3+ F- O2-
化合价 Na Mg Al F O
+1
+2
+3
-1
-2
交流与讨论
归纳与小结
化合价歌谣
一价钾钠氯氢银,二价氧钙钡镁锌,
三铝四硅五氮磷,二三铁、二四碳,
二四六硫均齐全,铜汞二价最常见,
化合价,要记清,莫忘单质价为零!
归纳与小结
化合价的有关规律:
①在任何化合物里,正负化合价的代数和为零。
②在化合物里氢通常显+1价,氧通常显-2价。
③金属元素通常显正价,非金属元素通常显负价。
④单质里元素的化合价为零。
⑤许多元素具有可变化合价,同种元素在不同的化合物里可显不
同的化合价,如:FeO,Fe2O3中铁元素的化合价分别为+2和+3。
根据化合价书写化合物的化学式
步骤如下:
一排序:元素符号按正价前,负价后顺序排列。
二标价:标出各元素的化合价,若有原子团只标出原子团的化合价。
三交叉:将元素化合价的绝对值交叉写在另一元素符号的右下角。
四约简:将各元素的原子个数约成最简整数比。
五检查:查化合价代数和是否为零。
一排顺序二标价
价数交叉写右下
约简价数作角码
总价为零去检查
口诀
“排 标 叉 查”
排列素
正价前
负价在后
标出元素
的化合价
交叉价数
检查代数和是否为零
已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式。
【思路】
(1)先写元素符号(正前负后)
(2)标出各元素的化合价(正上)
(3)把化合价数值化为最简
(4)把化简后的数字交叉写在
相应元素符号的右下角(1省略不写)
P O
+5 -2
P O
P2 O 5
+ 5 -2
+ 5 -2
P O
2 5
+ 5 -2
即化学式为:P2 O 5
写出下列化合物的化学式。
氧化钾
氧化钙
氧化铁
氯化钾
氯化镁
氯化亚铁
氢氧化钾
氢氧化钙
氢氧化铁
硫酸钾
硫酸钙
硫酸铁
Fe2O3
FeCl2
Fe(OH)3
Fe 2 (SO4) 3
K2O
MgCl2
KCl
KOH
K2SO4
CaO
Ca(OH)2
Ca SO4
课堂练习
【典例精讲】
A
例1.(2021河南省郑州市金水区二模)下列化学符号能表示2个氢原子的是( )
A.2H B.H2
C.2H2 D.2H+
【解析】表示原子个数时只需要在元素符号前面加数字即可,A正确;B表示一个氢分子或氢气,不符题意;C表示两个氢分子,不符题意;D表示两个氢离子,不符题意。故选A。
【答案】D
【解析】A、在室温下,1L水中能溶解约30mL氧气,而氢气难溶于水,室温下,溶解的比氧气少,
故得到氧气和氢气的体积比小于1:2,不符合题意;
B、碳能与氧气在一定条件下反应生成二氧化碳,故可能是部分氧气与碳棒发生了反应,不符合题意;
C、碳棒具有疏松多孔的结构,可能会吸附一部分氧气,不符合题意;
D、在电解水实验中,“正氧负氢”,氧气在正极生成,氢气在负极生成,故氧气与氢气不可能重新生成水,符合题意。故选D。
例2.(2021黑龙江齐齐哈尔阿城区二模)下列化学用语表述正确的是( )
A.硫酸钾的化学式:K2SO4 B.1 个氯分子:Cl
C.2 个硝酸根:2NO2 D.铜离子:Cu
【解析】硫酸钾的化学式为K2SO4 ,A正确; 1 个氯分子为 Cl2,B错误;2 个硝酸根为2NO3﹣,C错误;铜离子为Cu2+,D错误。故选A。
A
【典例精讲】
例3.(2021·广西中考真题)钛和钛合金是制造飞机的重要材料,钛
酸亚铁(FeTiO3)中钛元素的化合价为( )
A.+2 B.+3
C.+4 D.+5
【解析】钛酸亚铁中铁元素化合价为正二价、氧元素化合价为负二价,设钛元素化合价为x,化合物中正负化合价代数和为零;则(+2)+ x +(-2)×3=0,x=+4。故选C。
C
【典例精讲】
A
【达标测评】
1.下列化学式中,书写错误的是 ( )
A.氧化钙(OCa)
B.氧化镁(MgO)
C.三氯化铁 (FeCl3)
D.三氧化硫(SO3)
2.(2021·湖北襄阳市·中考真题)化学用语是学习和研究化学的工具。
下列化学用语表示正确的是( )
A.汞元素:HG B.镁离子:Mg2+
C.高锰酸钾:K2MnO4 D.2个氮原子:N2
B
【达标测评】
【归纳小结】
化学式
意义
写方法
宏观意义
微观意义
1.完成配套练习册;
2.预习物质的组成。
【作业布置】
谢 谢!
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
