3.4 物质组成的表示式课件--2021-2022学年九年级化学科粤版(2012)上册(19张PPT)
文档属性
| 名称 | 3.4 物质组成的表示式课件--2021-2022学年九年级化学科粤版(2012)上册(19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-25 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第三章第4节
物质组成的表示式
一、怎样用式子表示物质的组成
用元素符号和数字的组合来表示物质组成的式子,叫做化学式。
化学式定义
只有纯净物才能用化学式表示其组成;
一种物质只能用一个化学式来表示;
化学式的书写必须依据实验的结果或化合价来推求。
注意
微观意义
③表示物质的一个分子
④表示物质一个分子的构成情况
①表示一种物质
②表示一种物质的元素组成
宏观意义
CO2
宏观意义
二氧化碳
二氧化碳由碳元素和氧元素组成
微观意义
一个二氧化碳分子
一个二氧化碳分子由一个碳原子和两个氧原子构成
化学式
的意义
一、怎样用式子表示物质的组成
例如:
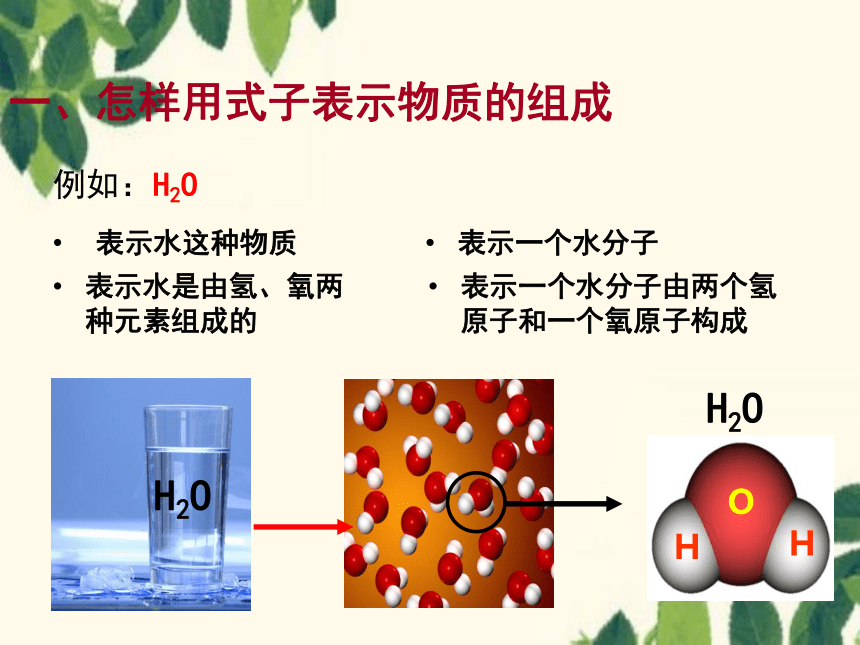
例如:H2O
H2O
H2O
O
H
H
表示一个水分子
表示一个水分子由两个氢原子和一个氧原子构成
表示水这种物质
表示水是由氢、氧两种元素组成的
一、怎样用式子表示物质的组成
稀有气体单质:
He Ne Ar
金属单质:
Cu Fe Hg Mg
非金属固态单质:
C P S Si
非金属气体:
H2 O2 N2 Cl2
直接用元素符号表示化学式;读元素符号的名称。
用元素符号及其右下角的数字表示;读“某气”。
单
质
元素符号右下角数字是表示分子中所含这种原子的个数。
化学式的写法与读法
一、怎样用式子表示物质的组成
直接用元素符号表示化学式;读“某气”。
化合物
氧化物的化学式:
如:CO2 SO2 P2O5 Fe3O4 MnO2
写法:氧元素在后,另一种元素在前
读法:氧化某或几氧化几某(几代表数字)
金属元素和非金属元素组成的化合物:
如:NaCl KCl HgO MgO
写法:金属元素在前,非金属元素在后
读法:某(非金属)化某(金属)或几某化几某
化合物化学式小结
原则:顺写反读 读作:某化某
注:原子个数为1省略不写
一、怎样用式子表示物质的组成
一些物质组成元素的原子个数比
物质 HCl H2O NaCl Fe2O3
原子个数比 1∶1 2∶1 1∶1 2∶3
二、元素的化合价
化学上用“化合价”来确定化合物中原子或离子之间相互结合的数目。
化合价的定义
Mg
+2
化合价为+2价的镁元素
Mg2+
带2个单位正电荷的镁离子
HCl
-1
氯化氢中的氯元素为-1价
化合价的表示方法
在元素符号的正上方写+或-号,后面加数值,注意1不能省略;
元素的化合价由该元素原子的最外层电子数决定。
二、元素的化合价
例如:
化合价 离子符号
表示方法
符号
联系
标在元素符号的正上方,先符号后数目(1不省略)
标在元素符号的右上角, 先数目后符号(1省略)
Al、O、Mg
+3
-2
+2
Al3+、O2-、Mg2+
同种元素的化合价与离子的电荷,通常数值相等,正负相同,位置不同,写法相反
化合价与离子符号的比较
二、元素的化合价
概念:作为一个整体参加反应的原子集团,又叫根。
根的名称 根的符号 常见化合价
氢氧根 OH -1
硝酸根 NO3 -1
硫酸根 SO4 -2
碳酸根 CO3 -2
铵根 NH4 +1
原子团
二、元素的化合价
NaOH、Ca(OH)2、Cu(OH)2、Fe(OH)3
读氢氧化某
H2CO3、H2SO4、HNO3
读某酸(中间元素的名称)
读某(酸根)酸某
CaCO3、CuSO4、NaNO3
举例:
原子团
二、元素的化合价
化合价有正价和负价。
氧元素通常显-2价。
氢元素通常显+1价。
金属元素跟非金属元素化合时,
金属元素显正价,非金属元素显负价。
一些元素在不同物质中可显不同的化合价。
在化合物里正负化合价的代数和为0。
元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此在单质分子里,元素的化合价为0。
化合价的一般规律
二、元素的化合价
一价氢氯钾钠银 二价氧钙钡镁锌
三铝四硅五价磷 二三铁,二四碳
二四六硫都齐全 铜汞二价最常见
条件不同价不同 单质为零永不变
负一硝酸氢氧根 负二硫酸碳酸根
负三记住磷酸根 正一价的是铵根
一些常见元素化合价口诀
一些常见原子团的化合价
二、元素的化合价
例题:已知磷为+5价,氧为-2价,写出磷的这种化合物的化学式。
解:
1.写出组成的元素:正价在前,负价在后
2.求正负化合价绝对值的最小公倍数
3.求各元素的原子数:最小公倍数/正价数
(或负价数)=原子个数
4.原子个数写在元素符号右下角
5.检查正误:正负化合价代数和等于0
P O
5×2=10
P:10/5=2 O:10/2=5
P2O5
+5×2+(-2)×5=0
根据化合价推写化学式
+5 -2
二、元素的化合价
原子个数比
元素符号右下角数字比(相同的元素的原子个数要合并),如H2O中氢原子与氧原子个数比为2:1。
KMnO4
K:Mn:O=1:1:4
NH4NO3 Cu2(OH)2CO3
K2MnO4
三、有关化学式的计算
N:H:O=2:4:3
K:Mn:O=2:1:4
Cu:C:H:O=2:1:2:5
举例:
相对分子质量
化学式中各原子的相对原子质量总和。
例如:O2的相对分子质量=16×2=32
相对分子质量 = 某元素的相对原子质量×原子个数+另一种元素
的相对原子质量×原子个数+……
KMnO4
K2MnO4
NH4NO3
Cu2(OH)2CO3
39+55+16×4=158
39×2+55+16×4=197
14+1×4+14+16×3=80
64×2+(16+1)×2+12+16×3=222
三、有关化学式的计算
物质组成元素的质量比 = 某元素的相对原子质量×原子个数∶另一种元素的相对原子质量×原子个数∶ ……
例如:二氧化碳(CO2)中碳元素和氧元素的质量比等于
12 ∶ (16×2)= 3 ∶ 8
H2O
KMnO4
NH4NO3
Cu2(OH)2CO3
1 ∶ 8
39 ∶ 55 ∶ 64
7 ∶ 1 ∶ 12
64 ∶ 40 ∶ 1 ∶ 6
计算物质组成元素的质量比
三、有关化学式的计算
物质中某元素的质量分数,就是该元素的质量与组成物质的元素总质量之比。
例:求硝酸铵(NH4NO3)中氮元素的质量分数。
解:NH4NO3的相对分子质量 =14+1×4+14+16×3=80
氮元素的质量分数= ×100% =35%
计算物质中某元素的质量分数
三、有关化学式的计算
14×2
80
答:硝酸铵(NH4NO3)中氮元素的质量分数为35%。
“达菲”是治疗人类感染甲型流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H10O5)存在于我国盛产的八角茴香中。下列说法不正确的是( D )
A.莽草酸中碳、氢、氧三种元素的质量比为42:5:40
B.莽草酸的相对分子质量为174
C.每个莽草酸分子中含有22个原子
D.莽草酸中碳元素的质量分数约为21%
练习
三、有关化学式的计算
第三章第4节
物质组成的表示式
一、怎样用式子表示物质的组成
用元素符号和数字的组合来表示物质组成的式子,叫做化学式。
化学式定义
只有纯净物才能用化学式表示其组成;
一种物质只能用一个化学式来表示;
化学式的书写必须依据实验的结果或化合价来推求。
注意
微观意义
③表示物质的一个分子
④表示物质一个分子的构成情况
①表示一种物质
②表示一种物质的元素组成
宏观意义
CO2
宏观意义
二氧化碳
二氧化碳由碳元素和氧元素组成
微观意义
一个二氧化碳分子
一个二氧化碳分子由一个碳原子和两个氧原子构成
化学式
的意义
一、怎样用式子表示物质的组成
例如:
例如:H2O
H2O
H2O
O
H
H
表示一个水分子
表示一个水分子由两个氢原子和一个氧原子构成
表示水这种物质
表示水是由氢、氧两种元素组成的
一、怎样用式子表示物质的组成
稀有气体单质:
He Ne Ar
金属单质:
Cu Fe Hg Mg
非金属固态单质:
C P S Si
非金属气体:
H2 O2 N2 Cl2
直接用元素符号表示化学式;读元素符号的名称。
用元素符号及其右下角的数字表示;读“某气”。
单
质
元素符号右下角数字是表示分子中所含这种原子的个数。
化学式的写法与读法
一、怎样用式子表示物质的组成
直接用元素符号表示化学式;读“某气”。
化合物
氧化物的化学式:
如:CO2 SO2 P2O5 Fe3O4 MnO2
写法:氧元素在后,另一种元素在前
读法:氧化某或几氧化几某(几代表数字)
金属元素和非金属元素组成的化合物:
如:NaCl KCl HgO MgO
写法:金属元素在前,非金属元素在后
读法:某(非金属)化某(金属)或几某化几某
化合物化学式小结
原则:顺写反读 读作:某化某
注:原子个数为1省略不写
一、怎样用式子表示物质的组成
一些物质组成元素的原子个数比
物质 HCl H2O NaCl Fe2O3
原子个数比 1∶1 2∶1 1∶1 2∶3
二、元素的化合价
化学上用“化合价”来确定化合物中原子或离子之间相互结合的数目。
化合价的定义
Mg
+2
化合价为+2价的镁元素
Mg2+
带2个单位正电荷的镁离子
HCl
-1
氯化氢中的氯元素为-1价
化合价的表示方法
在元素符号的正上方写+或-号,后面加数值,注意1不能省略;
元素的化合价由该元素原子的最外层电子数决定。
二、元素的化合价
例如:
化合价 离子符号
表示方法
符号
联系
标在元素符号的正上方,先符号后数目(1不省略)
标在元素符号的右上角, 先数目后符号(1省略)
Al、O、Mg
+3
-2
+2
Al3+、O2-、Mg2+
同种元素的化合价与离子的电荷,通常数值相等,正负相同,位置不同,写法相反
化合价与离子符号的比较
二、元素的化合价
概念:作为一个整体参加反应的原子集团,又叫根。
根的名称 根的符号 常见化合价
氢氧根 OH -1
硝酸根 NO3 -1
硫酸根 SO4 -2
碳酸根 CO3 -2
铵根 NH4 +1
原子团
二、元素的化合价
NaOH、Ca(OH)2、Cu(OH)2、Fe(OH)3
读氢氧化某
H2CO3、H2SO4、HNO3
读某酸(中间元素的名称)
读某(酸根)酸某
CaCO3、CuSO4、NaNO3
举例:
原子团
二、元素的化合价
化合价有正价和负价。
氧元素通常显-2价。
氢元素通常显+1价。
金属元素跟非金属元素化合时,
金属元素显正价,非金属元素显负价。
一些元素在不同物质中可显不同的化合价。
在化合物里正负化合价的代数和为0。
元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此在单质分子里,元素的化合价为0。
化合价的一般规律
二、元素的化合价
一价氢氯钾钠银 二价氧钙钡镁锌
三铝四硅五价磷 二三铁,二四碳
二四六硫都齐全 铜汞二价最常见
条件不同价不同 单质为零永不变
负一硝酸氢氧根 负二硫酸碳酸根
负三记住磷酸根 正一价的是铵根
一些常见元素化合价口诀
一些常见原子团的化合价
二、元素的化合价
例题:已知磷为+5价,氧为-2价,写出磷的这种化合物的化学式。
解:
1.写出组成的元素:正价在前,负价在后
2.求正负化合价绝对值的最小公倍数
3.求各元素的原子数:最小公倍数/正价数
(或负价数)=原子个数
4.原子个数写在元素符号右下角
5.检查正误:正负化合价代数和等于0
P O
5×2=10
P:10/5=2 O:10/2=5
P2O5
+5×2+(-2)×5=0
根据化合价推写化学式
+5 -2
二、元素的化合价
原子个数比
元素符号右下角数字比(相同的元素的原子个数要合并),如H2O中氢原子与氧原子个数比为2:1。
KMnO4
K:Mn:O=1:1:4
NH4NO3 Cu2(OH)2CO3
K2MnO4
三、有关化学式的计算
N:H:O=2:4:3
K:Mn:O=2:1:4
Cu:C:H:O=2:1:2:5
举例:
相对分子质量
化学式中各原子的相对原子质量总和。
例如:O2的相对分子质量=16×2=32
相对分子质量 = 某元素的相对原子质量×原子个数+另一种元素
的相对原子质量×原子个数+……
KMnO4
K2MnO4
NH4NO3
Cu2(OH)2CO3
39+55+16×4=158
39×2+55+16×4=197
14+1×4+14+16×3=80
64×2+(16+1)×2+12+16×3=222
三、有关化学式的计算
物质组成元素的质量比 = 某元素的相对原子质量×原子个数∶另一种元素的相对原子质量×原子个数∶ ……
例如:二氧化碳(CO2)中碳元素和氧元素的质量比等于
12 ∶ (16×2)= 3 ∶ 8
H2O
KMnO4
NH4NO3
Cu2(OH)2CO3
1 ∶ 8
39 ∶ 55 ∶ 64
7 ∶ 1 ∶ 12
64 ∶ 40 ∶ 1 ∶ 6
计算物质组成元素的质量比
三、有关化学式的计算
物质中某元素的质量分数,就是该元素的质量与组成物质的元素总质量之比。
例:求硝酸铵(NH4NO3)中氮元素的质量分数。
解:NH4NO3的相对分子质量 =14+1×4+14+16×3=80
氮元素的质量分数= ×100% =35%
计算物质中某元素的质量分数
三、有关化学式的计算
14×2
80
答:硝酸铵(NH4NO3)中氮元素的质量分数为35%。
“达菲”是治疗人类感染甲型流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H10O5)存在于我国盛产的八角茴香中。下列说法不正确的是( D )
A.莽草酸中碳、氢、氧三种元素的质量比为42:5:40
B.莽草酸的相对分子质量为174
C.每个莽草酸分子中含有22个原子
D.莽草酸中碳元素的质量分数约为21%
练习
三、有关化学式的计算
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
