第三单元物质构成的奥秘单元练习---2021_2022学年九年级化学人教版上册(有答案)
文档属性
| 名称 | 第三单元物质构成的奥秘单元练习---2021_2022学年九年级化学人教版上册(有答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 215.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-29 00:00:00 | ||
图片预览


文档简介
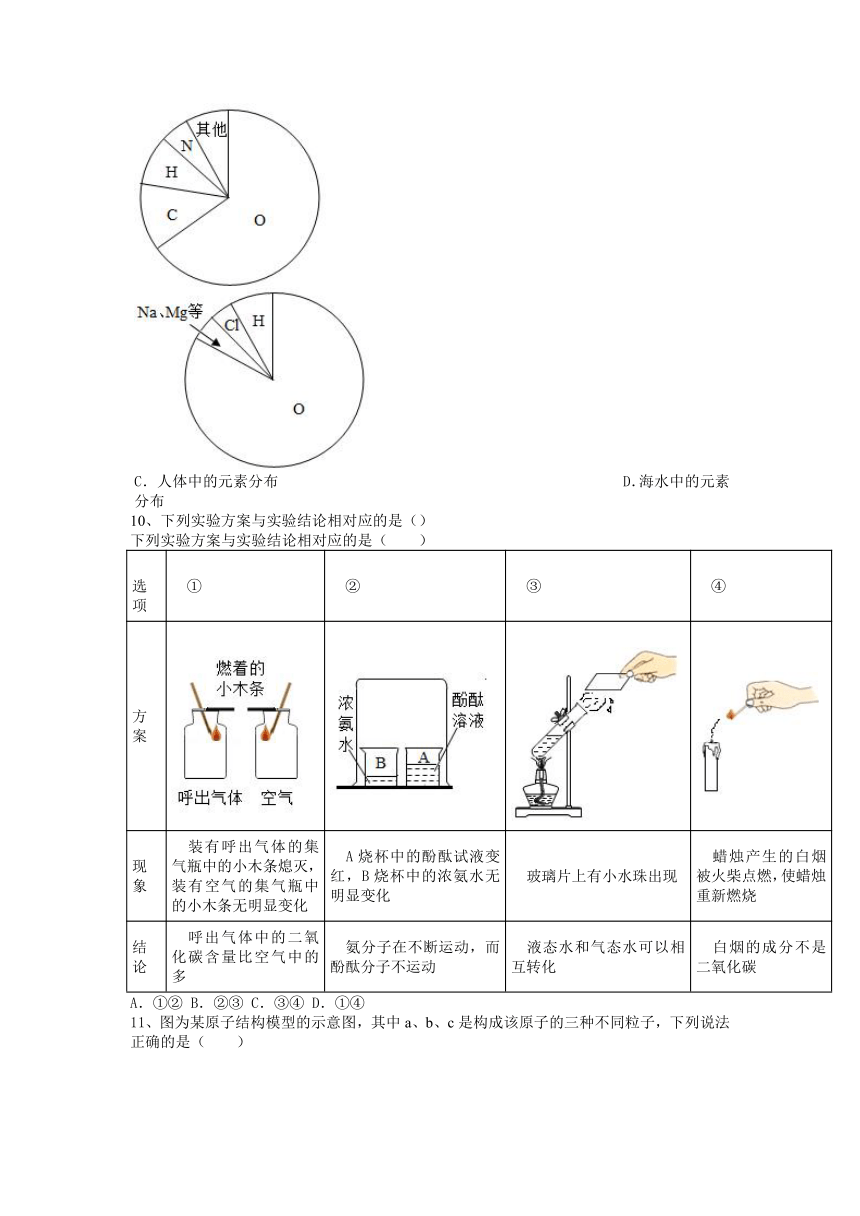
第三单元《物质构成的奥秘》单元练习
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、下列变化能证明分子可以再分的是( )
A.过氧化氢分解 B.蜡烛融化
C.水蒸发 D.碘升华
2、科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是( )
A.属于非金属元素 B.相对原子质量是6.941g
C.表示核内有3个电子 D.离子符号是Li+
3、如图是有关物质宏观组成和微观构成的思维导图,其中▲应填入的是( )
A.原子 B.中子 C.电子 D.质子
4、氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个核。如图所示,下列说法不正确的是( )
A.氘原子和氚原子的质子数相同
B.氘原子、氚原子的中子数相同
C.氘原子和氚原子的核电荷数相同
D.氦原子的原子核由2个质子和2个中子构成
5、下列对微粒的描述中,不正确的是( )
A.易失电子 B.易形成阴离子 C.阳离子 D.化学性质稳定
6、下列事实的微观解释中,不正确的是( )
A.墙内开花墙外可闻到花香--分子在不断地运动
B.蔗糖放入水中溶解--蔗糖分子分解了
C.氧气和液氧都能支持燃烧--物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起--水分子间的间隔增大
7、关于分子、原子的说法正确的是( )
A.分子、原子都可以直接构成物质
B.分子、原子都很小,但分子比原子大
C.分子可分、原子不可分
D.分子是保持物质性质的一种微粒
8、下列排序正确的是( )
A.分子间的空隙:B.原子核外电子层数:
C.地壳中元素含量:D.空气中物质的含量:
9、下列图示的各物质(或元素)相对含量错误的是( )
A.空气的组成 B.地壳中的元素分布
C.人体中的元素分布 D.海水中的元素分布
10、下列实验方案与实验结论相对应的是()
下列实验方案与实验结论相对应的是( )
选项 ① ② ③ ④
方案
现象 装有呼出气体的集气瓶中的小木条熄灭,装有空气的集气瓶中的小木条无明显变化 A烧杯中的酚酞试液变红,B烧杯中的浓氨水无明显变化 玻璃片上有小水珠出现 蜡烛产生的白烟被火柴点燃,使蜡烛重新燃烧
结论 呼出气体中的二氧化碳含量比空气中的多 氨分子在不断运动,而酚酞分子不运动 液态水和气态水可以相互转化 白烟的成分不是二氧化碳
A.①② B.②③ C.③④ D.①④
11、图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是( )
A.决定该原子种类的粒子是b
B.原子中b与c的数目一定相同且均为6
C.原子中a与c的数目一定相同
D.原子的质量集中在a和c上
12、“芯片”是电子产品的核心部件,氮化镓是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法不正确的是( )
A.镓属于金属元素,m=3
B.镓化学性质比较活泼,易形成阳离子Ga+3
C.镓元素的位置应该在Z处
D.镓的最外层电子数与Al相同
二、本大题包括5小题,共28分
13、用微粒的观点解释下列问题:
(1)50mL的水与50mL酒精混合后总体积小于100mL,说明 ;
(2)湿衣服在有阳光照射的地方比阴凉处更易晾干,说明 ;
(3)一滴水里约有十七亿亿个水的微粒,说明 ;
(4)氧气和液态氧都有助燃性,是因为 ;
(5)空气是混合物而氧气是纯净物,是因为 ;
(6)体温计能用于测体温是因为 。
14、根据下列粒子结构示意图,回答问题。
(1)图A、B、C、D四种粒子共表示 种元素。
(2)D原子的第二层电子数是 ,D原子在化学反应中易 (填“得到或“失去”)电子,D属于 元素(填“金属”“非金属”或“稀有气体”)。
(3)图中从A至F中达到相对稳定结构的是 (填序号)。
(4)E粒子带1个单位负电荷,则X= 。
(5)图中为硫原子的结构示意图是 (填序号)。
(6)A粒子所属元素位于元素周期表第 周期。
(7)若图中F粒子的相对原子质量为3,则该粒子原子核内中子数为 。
15、原子序数为1~18的原子结构示意图等信息如图所示,请认真分析并回答下列问题。
(1)在化学反应中,原子序数为13的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 ;画出该离子的结构示意图 。
(2)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子 相同,所以氟元素与氯元素的化学性质相似。
(3)同一周期,从左到右,各原子随原子序数的增加,最外层电子数 。
16、(1)、化学兴趣小组的同学进行了如图1实验请回答下列问题并填写相关空白:
①向盛有约20mL蒸馏水的小烧杯A中加入2-3滴酚酞溶液,搅拌均匀,观察A中溶液的颜色为 色。
②另取一个小烧杯B,加入约5mL浓氨水,用一个大烧杯罩住A、B两个小烧杯(如图所示),几分钟后可以观察到现象有 。产生此现象的原因是:烧杯B中的浓氨水具有挥发性,挥发出的 (从微观角度)运动到烧杯A中,溶于水形成氨水,氨水使烧杯A中的溶液出现上述现象。
③经过小组同学的讨论,同学们一致认为上述实验能得出的一般性结论是 。
(2)图2两支胶头滴管分别装有约1mL浓氨水,将B试管放置在盛有热水的烧杯中。同时挤压胶头滴管,观察几分钟。
①图2的实验现象为 ,得出关于分子的结论是 。
②请举生活实例,验证实验2得出的结论 。
17、在“宏观-微观-符号”之间建立联系,是学习化学的种重要思维方式。
(1)从宏观的角度看,氯化氢由 组成;从微粒的角度看,氯化氢由 (写微粒名称)构成。
(2)锂元素在元素周期表中的某些信息如图甲所示,锂原子与另外三种粒子的结构示意图如图乙所示。
①锂元素的相对原子质量是 ,X= ,在元素周期表中,锂元素位于第 周期。
②锂原子与图乙中 (填“A”、“B”或“C”)粒子的化学性质相似。
③图甲和图乙中,共涉及 种元素。
(3)如图是氢分子和氧分子运动的示意图。
在A、B、C中,能比较得出“温度越高,分子运动速率越快”的是 (填序号),从图中可见,影响分子运动速率的因素除温度外,还与 有关。
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、A 2、D 3、A 4、B 5、C 6、B 7、A 8、A 9、A 10、C
11、C 12、B
二、本大题包括5小题,共28分
13、答案:(1)分子之间有间隔;
(2)温度升高,分子的运动速率加快;
(3)分子的体积很小;
(4)同种的分子化学性质相同;
(5)空气中含有氮分子、氧分子、二氧化碳分子等多种分子,氧气中只含有氧分子一种分子;
(6)微粒间的间隔随着温度的改变而改变。
14、答案:(1)3;
(2)8;得到;非金属;
(3)AEF;
(4)9;
(5)C;
(6)三;
(7)1;
15、答案:(1)失去;Al3+;;
(2)最外层电子数;
(3)依次递增。
16、答案为:(1)①无;
②A烧杯中无色的酚酞溶液变红;氨分子;
③分子是不断运动的。
(2)①滴有酚酞溶液的棉花变红色,并且B比A中的先变红色;分子是不断运动的;温度越高运动的越快;
②将相同质量的蔗糖同时放入等体积的冷水和热水中,观察到热水的蔗糖首先完全溶解。
17、答案:(1)氢元素与氯元素;氯化氢分子;
(2)①6.941;3;二;
②C;
③三(或3);
(3)①BC;②分子种类。
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、下列变化能证明分子可以再分的是( )
A.过氧化氢分解 B.蜡烛融化
C.水蒸发 D.碘升华
2、科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是( )
A.属于非金属元素 B.相对原子质量是6.941g
C.表示核内有3个电子 D.离子符号是Li+
3、如图是有关物质宏观组成和微观构成的思维导图,其中▲应填入的是( )
A.原子 B.中子 C.电子 D.质子
4、氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个核。如图所示,下列说法不正确的是( )
A.氘原子和氚原子的质子数相同
B.氘原子、氚原子的中子数相同
C.氘原子和氚原子的核电荷数相同
D.氦原子的原子核由2个质子和2个中子构成
5、下列对微粒的描述中,不正确的是( )
A.易失电子 B.易形成阴离子 C.阳离子 D.化学性质稳定
6、下列事实的微观解释中,不正确的是( )
A.墙内开花墙外可闻到花香--分子在不断地运动
B.蔗糖放入水中溶解--蔗糖分子分解了
C.氧气和液氧都能支持燃烧--物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起--水分子间的间隔增大
7、关于分子、原子的说法正确的是( )
A.分子、原子都可以直接构成物质
B.分子、原子都很小,但分子比原子大
C.分子可分、原子不可分
D.分子是保持物质性质的一种微粒
8、下列排序正确的是( )
A.分子间的空隙:B.原子核外电子层数:
C.地壳中元素含量:D.空气中物质的含量:
9、下列图示的各物质(或元素)相对含量错误的是( )
A.空气的组成 B.地壳中的元素分布
C.人体中的元素分布 D.海水中的元素分布
10、下列实验方案与实验结论相对应的是()
下列实验方案与实验结论相对应的是( )
选项 ① ② ③ ④
方案
现象 装有呼出气体的集气瓶中的小木条熄灭,装有空气的集气瓶中的小木条无明显变化 A烧杯中的酚酞试液变红,B烧杯中的浓氨水无明显变化 玻璃片上有小水珠出现 蜡烛产生的白烟被火柴点燃,使蜡烛重新燃烧
结论 呼出气体中的二氧化碳含量比空气中的多 氨分子在不断运动,而酚酞分子不运动 液态水和气态水可以相互转化 白烟的成分不是二氧化碳
A.①② B.②③ C.③④ D.①④
11、图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是( )
A.决定该原子种类的粒子是b
B.原子中b与c的数目一定相同且均为6
C.原子中a与c的数目一定相同
D.原子的质量集中在a和c上
12、“芯片”是电子产品的核心部件,氮化镓是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法不正确的是( )
A.镓属于金属元素,m=3
B.镓化学性质比较活泼,易形成阳离子Ga+3
C.镓元素的位置应该在Z处
D.镓的最外层电子数与Al相同
二、本大题包括5小题,共28分
13、用微粒的观点解释下列问题:
(1)50mL的水与50mL酒精混合后总体积小于100mL,说明 ;
(2)湿衣服在有阳光照射的地方比阴凉处更易晾干,说明 ;
(3)一滴水里约有十七亿亿个水的微粒,说明 ;
(4)氧气和液态氧都有助燃性,是因为 ;
(5)空气是混合物而氧气是纯净物,是因为 ;
(6)体温计能用于测体温是因为 。
14、根据下列粒子结构示意图,回答问题。
(1)图A、B、C、D四种粒子共表示 种元素。
(2)D原子的第二层电子数是 ,D原子在化学反应中易 (填“得到或“失去”)电子,D属于 元素(填“金属”“非金属”或“稀有气体”)。
(3)图中从A至F中达到相对稳定结构的是 (填序号)。
(4)E粒子带1个单位负电荷,则X= 。
(5)图中为硫原子的结构示意图是 (填序号)。
(6)A粒子所属元素位于元素周期表第 周期。
(7)若图中F粒子的相对原子质量为3,则该粒子原子核内中子数为 。
15、原子序数为1~18的原子结构示意图等信息如图所示,请认真分析并回答下列问题。
(1)在化学反应中,原子序数为13的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 ;画出该离子的结构示意图 。
(2)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子 相同,所以氟元素与氯元素的化学性质相似。
(3)同一周期,从左到右,各原子随原子序数的增加,最外层电子数 。
16、(1)、化学兴趣小组的同学进行了如图1实验请回答下列问题并填写相关空白:
①向盛有约20mL蒸馏水的小烧杯A中加入2-3滴酚酞溶液,搅拌均匀,观察A中溶液的颜色为 色。
②另取一个小烧杯B,加入约5mL浓氨水,用一个大烧杯罩住A、B两个小烧杯(如图所示),几分钟后可以观察到现象有 。产生此现象的原因是:烧杯B中的浓氨水具有挥发性,挥发出的 (从微观角度)运动到烧杯A中,溶于水形成氨水,氨水使烧杯A中的溶液出现上述现象。
③经过小组同学的讨论,同学们一致认为上述实验能得出的一般性结论是 。
(2)图2两支胶头滴管分别装有约1mL浓氨水,将B试管放置在盛有热水的烧杯中。同时挤压胶头滴管,观察几分钟。
①图2的实验现象为 ,得出关于分子的结论是 。
②请举生活实例,验证实验2得出的结论 。
17、在“宏观-微观-符号”之间建立联系,是学习化学的种重要思维方式。
(1)从宏观的角度看,氯化氢由 组成;从微粒的角度看,氯化氢由 (写微粒名称)构成。
(2)锂元素在元素周期表中的某些信息如图甲所示,锂原子与另外三种粒子的结构示意图如图乙所示。
①锂元素的相对原子质量是 ,X= ,在元素周期表中,锂元素位于第 周期。
②锂原子与图乙中 (填“A”、“B”或“C”)粒子的化学性质相似。
③图甲和图乙中,共涉及 种元素。
(3)如图是氢分子和氧分子运动的示意图。
在A、B、C中,能比较得出“温度越高,分子运动速率越快”的是 (填序号),从图中可见,影响分子运动速率的因素除温度外,还与 有关。
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、A 2、D 3、A 4、B 5、C 6、B 7、A 8、A 9、A 10、C
11、C 12、B
二、本大题包括5小题,共28分
13、答案:(1)分子之间有间隔;
(2)温度升高,分子的运动速率加快;
(3)分子的体积很小;
(4)同种的分子化学性质相同;
(5)空气中含有氮分子、氧分子、二氧化碳分子等多种分子,氧气中只含有氧分子一种分子;
(6)微粒间的间隔随着温度的改变而改变。
14、答案:(1)3;
(2)8;得到;非金属;
(3)AEF;
(4)9;
(5)C;
(6)三;
(7)1;
15、答案:(1)失去;Al3+;;
(2)最外层电子数;
(3)依次递增。
16、答案为:(1)①无;
②A烧杯中无色的酚酞溶液变红;氨分子;
③分子是不断运动的。
(2)①滴有酚酞溶液的棉花变红色,并且B比A中的先变红色;分子是不断运动的;温度越高运动的越快;
②将相同质量的蔗糖同时放入等体积的冷水和热水中,观察到热水的蔗糖首先完全溶解。
17、答案:(1)氢元素与氯元素;氯化氢分子;
(2)①6.941;3;二;
②C;
③三(或3);
(3)①BC;②分子种类。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
