7.4结晶现象同步作业—2021-2022学年九年级化学科粤版下册(含解析)
文档属性
| 名称 | 7.4结晶现象同步作业—2021-2022学年九年级化学科粤版下册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 172.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-29 00:00:00 | ||
图片预览


文档简介
7.4 结晶现象
知识点 1 结晶法
1.大量硝酸钾固体中混有少量的氯化钠,常采用降温结晶的方式除杂,其中氯化钠不析出的原因是( )
A.在降温时氯化钠的溶解能力反而增强
B.氯化钠量少,在降温后形成的仍是不饱和溶液
C.氯化钠的溶解度随温度的降低变化较大
D.硝酸钾的溶解度比氯化钠的大
2.如图所示为氯化钠(NaCl)、碳酸钠(Na2CO3,俗称纯碱)在水中的溶解度曲线。生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”,请你解释“夏天晒盐,冬天捞碱”的原因:
。
知识点 2 过滤
3.下列有关过滤的操作中错误的是 ( )
A.取一张圆形滤纸,对折两次,打开成圆锥形,放入漏斗
B.用少量水润湿滤纸,使滤纸紧贴漏斗内壁,滤纸层与漏斗壁间不留气泡
C.用玻璃棒轻轻搅动漏斗中的液体,以加快过滤
D.如果滤纸边缘高于漏斗边缘,用剪刀剪去多余部分,使滤纸的边缘比漏斗口稍低
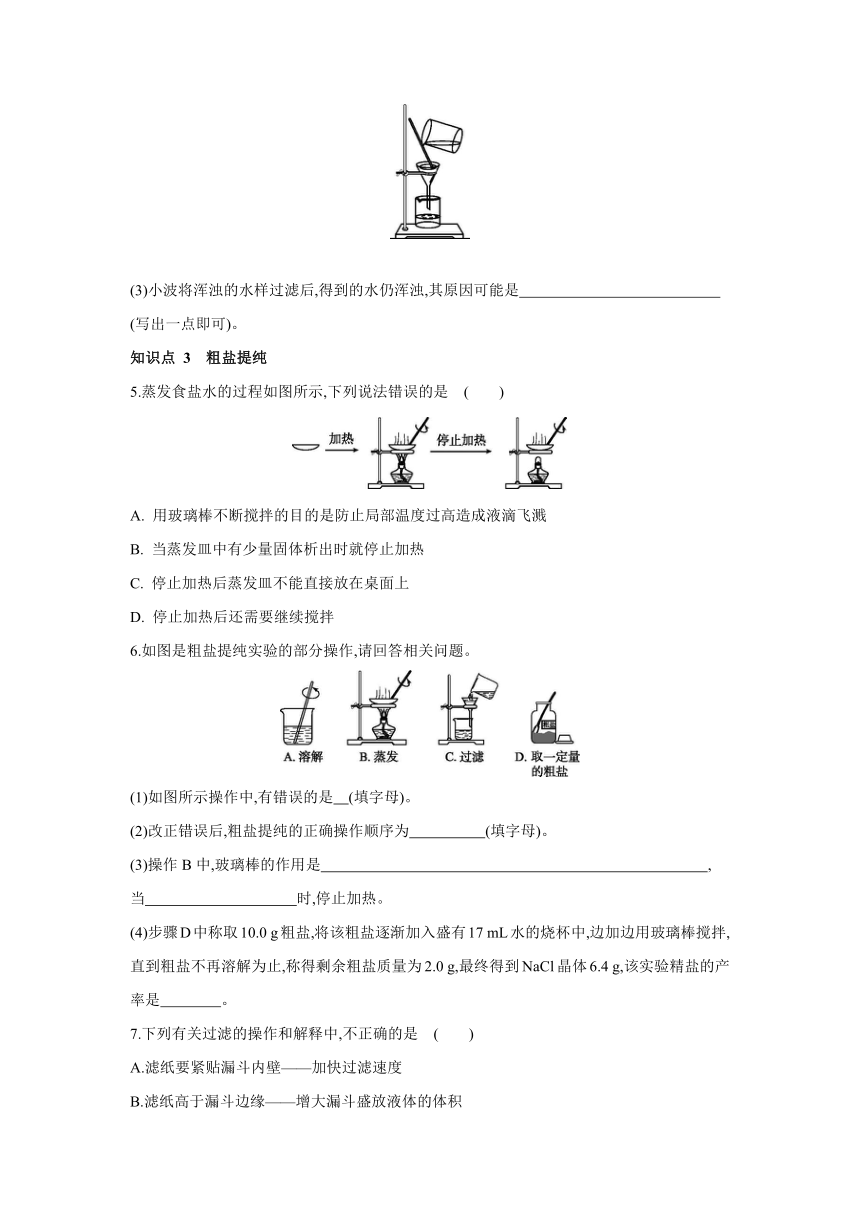
4.初中毕业化学实验操作技能考查中,小波抽到的试题是“水的净化”,请你与小波一起做实验,并回答下列问题。
(1)过滤操作中用到的玻璃仪器有漏斗、玻璃棒和 ,其中玻璃棒的作用是 。
(2)小波准备按如图所示装置进行操作时,发现装置存在一处明显错误,该错误是 。纠正错误后,接下来的过滤操作可除去水样中的 (填“可溶性”或“不溶性”)杂质。
(3)小波将浑浊的水样过滤后,得到的水仍浑浊,其原因可能是
(写出一点即可)。
知识点 3 粗盐提纯
5.蒸发食盐水的过程如图所示,下列说法错误的是 ( )
A. 用玻璃棒不断搅拌的目的是防止局部温度过高造成液滴飞溅
B. 当蒸发皿中有少量固体析出时就停止加热
C. 停止加热后蒸发皿不能直接放在桌面上
D. 停止加热后还需要继续搅拌
6.如图是粗盐提纯实验的部分操作,请回答相关问题。
(1)如图所示操作中,有错误的是 (填字母)。
(2)改正错误后,粗盐提纯的正确操作顺序为 (填字母)。
(3)操作B中,玻璃棒的作用是 ,
当 时,停止加热。
(4)步骤D中称取10.0 g粗盐,将该粗盐逐渐加入盛有17 mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐质量为2.0 g,最终得到NaCl晶体6.4 g,该实验精盐的产率是 。
7.下列有关过滤的操作和解释中,不正确的是 ( )
A.滤纸要紧贴漏斗内壁——加快过滤速度
B.滤纸高于漏斗边缘——增大漏斗盛放液体的体积
C.玻璃棒要轻靠在三层滤纸处——防止弄破滤纸
D.漏斗下端要紧靠烧杯内壁——防止滤液溅出
8.实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作流程,下列有关分析中正确的是 ( )
A.操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
9.某同学想从氯酸钾和二氧化锰制取氧气后的固体残留物中回收二氧化锰固体,设计了如图所示流程,图中序号或字母所对应的操作步骤或物质错误的是 ( )
A.操作①:加水溶解
B.操作④:洗涤
C.操作③:蒸发结晶
D.固体M为二氧化锰固体
10.分离混合物是人们改造、利用自然界中物质的重要方法。分离混合物要根据各成分不同的性质选用不同的方法,下列说法不正确的是 ( )
A.过滤法是根据混合物中各成分颗粒的大小不同
B.结晶法是利用混合物中各成分在水中的溶解度或溶解度受温度影响情况的不同
C.蒸馏法是利用混合物中各成分的熔点不同
D.化学沉淀法是根据混合物中各成分的化学性质不同
11.下表是固体A、B、C在不同温度下的溶解度。
温度/℃ 0 20 40 60 80
溶解度/g A 35.7 36.0 36.6 37.3 38.4
B 13.3 31.6 63.9 110 169
C 35.0 44.5 57.6 55.0 50.0
(1)若B的饱和溶液中混有少量的A,最好采用 的方法提纯B。
(2)将80 ℃时A、B、C三种物质的饱和溶液降温到60 ℃,其中溶质的质量分数不变的物质是 。
(3)精制A物质时,通常采用的方法是蒸发溶剂而不是降低溶液温度。据表分析其原因:
。
12.如图所示是“粗盐中难溶性杂质的去除”的实验操作示意图。
(1)仪器a的名称是 。
(2)操作A中两个托盘各放一张干净的且质量相同的纸片,其作用是
。
(3)操作B中还需要用到的玻璃仪器是 。
(4)操作C中,倒入液体时液面要低于滤纸边缘,主要是为了防止 (填字母)。
A.过滤速度慢
B.滤纸破损
C.杂质未经过滤就进入滤液
(5)图中部分操作有误,其中有的错误会导致精盐的产率明显偏低,其原因是
。
13.[2021·泰安] 如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是 ( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液中溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液中溶质质量分数由大到小的关系:a>b>c
D.在t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液质量为80 g
1.B
2.“夏天晒盐”是因为氯化钠的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,氯化钠易结晶析出;“冬天捞碱”是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱的溶解度小,易从溶液中结晶析出
3.C [解析] 不能用玻璃棒搅动漏斗中的液体,否则可能损坏滤纸。
4.(1)烧杯 引流
(2)漏斗末端的尖嘴处没有紧靠烧杯内壁 不溶性
(3)倾倒待滤液时,漏斗内液面高于滤纸的边缘(或滤纸破损,或仪器不干净等,合理即可)
5.B [解析] 蒸发过程中要用玻璃棒不断搅拌,避免因局部温度过高,造成液滴飞溅;蒸发过程中,当蒸发皿中有较多固体析出时停止加热,然后利用余热将液体蒸干,而不是有少量固体析出时就停止加热;停止加热后蒸发皿温度仍较高,直接放于桌面上会损坏桌面;停止加热后,继续搅拌可以加快水的蒸发,同时避免固体飞溅。
6.(1)C (2)DACB
(3)搅拌,防止局部温度过高造成液滴飞溅 有较多固体析出
(4)80%
[解析] (1)过滤时没有用玻璃棒引流。(2)粗盐提纯的主要步骤是溶解、过滤、蒸发结晶。(3)蒸发操作时用玻璃棒的作用是搅拌,使溶液均匀受热,防止局部温度过高造成液滴飞溅,当有较多固体析出时,停止加热,利用余热将液体蒸干。(4)精盐的产率为6.4 g÷(10.0 g-2.0 g)× 100%=80%。
7.B [解析] 滤纸的边缘应略低于漏斗的边缘。
8.D [解析] 提纯含少量氯化钠杂质的硝酸钾固体,结合流程可知,操作Ⅰ为溶解,操作Ⅱ为蒸发浓缩、冷却结晶,操作Ⅲ是过滤、洗涤。
9.D [解析] 氯化钾易溶于水,二氧化锰难溶于水,分离氯化钾和二氧化锰的固体混合物,可加水溶解、过滤,滤液蒸发结晶得到氯化钾;滤渣洗涤、干燥,得到二氧化锰。
10.C [解析] 蒸馏法是利用混合物中各成分的沸点不同将混合物分离;化学沉淀法是根据混合物中各成分的化学性质不同,将某些物质转化为沉淀分离。
11.(1)降温结晶(或冷却结晶) (2)C
(3)A物质的溶解度受温度变化的影响不大
12.(1)铁架台
(2)防止粗盐腐蚀托盘,同时能使称量更准确
(3)胶头滴管 (4)C
(5)蒸发时没有用玻璃棒搅拌,会导致液滴飞溅,造成部分氯化钠损失
13.C [解析] a的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,采用降温结晶的方法,a的饱和溶液能够析出晶体,c的饱和溶液不能析出晶体;未指明溶液是否饱和,t1 ℃时,a、c两种物质的溶液中溶质质量分数不一定相等;t2 ℃时,a、b、c三种物质的溶解度大小关系是a>b>c,所以饱和溶液中溶质质量分数的大小关系是a>b>c;在t2 ℃时,a的溶解度是50 g,将30 g a物质加入50 g水中,充分溶解,所得溶液质量为25 g+50 g=75 g。
知识点 1 结晶法
1.大量硝酸钾固体中混有少量的氯化钠,常采用降温结晶的方式除杂,其中氯化钠不析出的原因是( )
A.在降温时氯化钠的溶解能力反而增强
B.氯化钠量少,在降温后形成的仍是不饱和溶液
C.氯化钠的溶解度随温度的降低变化较大
D.硝酸钾的溶解度比氯化钠的大
2.如图所示为氯化钠(NaCl)、碳酸钠(Na2CO3,俗称纯碱)在水中的溶解度曲线。生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”,请你解释“夏天晒盐,冬天捞碱”的原因:
。
知识点 2 过滤
3.下列有关过滤的操作中错误的是 ( )
A.取一张圆形滤纸,对折两次,打开成圆锥形,放入漏斗
B.用少量水润湿滤纸,使滤纸紧贴漏斗内壁,滤纸层与漏斗壁间不留气泡
C.用玻璃棒轻轻搅动漏斗中的液体,以加快过滤
D.如果滤纸边缘高于漏斗边缘,用剪刀剪去多余部分,使滤纸的边缘比漏斗口稍低
4.初中毕业化学实验操作技能考查中,小波抽到的试题是“水的净化”,请你与小波一起做实验,并回答下列问题。
(1)过滤操作中用到的玻璃仪器有漏斗、玻璃棒和 ,其中玻璃棒的作用是 。
(2)小波准备按如图所示装置进行操作时,发现装置存在一处明显错误,该错误是 。纠正错误后,接下来的过滤操作可除去水样中的 (填“可溶性”或“不溶性”)杂质。
(3)小波将浑浊的水样过滤后,得到的水仍浑浊,其原因可能是
(写出一点即可)。
知识点 3 粗盐提纯
5.蒸发食盐水的过程如图所示,下列说法错误的是 ( )
A. 用玻璃棒不断搅拌的目的是防止局部温度过高造成液滴飞溅
B. 当蒸发皿中有少量固体析出时就停止加热
C. 停止加热后蒸发皿不能直接放在桌面上
D. 停止加热后还需要继续搅拌
6.如图是粗盐提纯实验的部分操作,请回答相关问题。
(1)如图所示操作中,有错误的是 (填字母)。
(2)改正错误后,粗盐提纯的正确操作顺序为 (填字母)。
(3)操作B中,玻璃棒的作用是 ,
当 时,停止加热。
(4)步骤D中称取10.0 g粗盐,将该粗盐逐渐加入盛有17 mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐质量为2.0 g,最终得到NaCl晶体6.4 g,该实验精盐的产率是 。
7.下列有关过滤的操作和解释中,不正确的是 ( )
A.滤纸要紧贴漏斗内壁——加快过滤速度
B.滤纸高于漏斗边缘——增大漏斗盛放液体的体积
C.玻璃棒要轻靠在三层滤纸处——防止弄破滤纸
D.漏斗下端要紧靠烧杯内壁——防止滤液溅出
8.实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作流程,下列有关分析中正确的是 ( )
A.操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
9.某同学想从氯酸钾和二氧化锰制取氧气后的固体残留物中回收二氧化锰固体,设计了如图所示流程,图中序号或字母所对应的操作步骤或物质错误的是 ( )
A.操作①:加水溶解
B.操作④:洗涤
C.操作③:蒸发结晶
D.固体M为二氧化锰固体
10.分离混合物是人们改造、利用自然界中物质的重要方法。分离混合物要根据各成分不同的性质选用不同的方法,下列说法不正确的是 ( )
A.过滤法是根据混合物中各成分颗粒的大小不同
B.结晶法是利用混合物中各成分在水中的溶解度或溶解度受温度影响情况的不同
C.蒸馏法是利用混合物中各成分的熔点不同
D.化学沉淀法是根据混合物中各成分的化学性质不同
11.下表是固体A、B、C在不同温度下的溶解度。
温度/℃ 0 20 40 60 80
溶解度/g A 35.7 36.0 36.6 37.3 38.4
B 13.3 31.6 63.9 110 169
C 35.0 44.5 57.6 55.0 50.0
(1)若B的饱和溶液中混有少量的A,最好采用 的方法提纯B。
(2)将80 ℃时A、B、C三种物质的饱和溶液降温到60 ℃,其中溶质的质量分数不变的物质是 。
(3)精制A物质时,通常采用的方法是蒸发溶剂而不是降低溶液温度。据表分析其原因:
。
12.如图所示是“粗盐中难溶性杂质的去除”的实验操作示意图。
(1)仪器a的名称是 。
(2)操作A中两个托盘各放一张干净的且质量相同的纸片,其作用是
。
(3)操作B中还需要用到的玻璃仪器是 。
(4)操作C中,倒入液体时液面要低于滤纸边缘,主要是为了防止 (填字母)。
A.过滤速度慢
B.滤纸破损
C.杂质未经过滤就进入滤液
(5)图中部分操作有误,其中有的错误会导致精盐的产率明显偏低,其原因是
。
13.[2021·泰安] 如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是 ( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液中溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液中溶质质量分数由大到小的关系:a>b>c
D.在t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液质量为80 g
1.B
2.“夏天晒盐”是因为氯化钠的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,氯化钠易结晶析出;“冬天捞碱”是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱的溶解度小,易从溶液中结晶析出
3.C [解析] 不能用玻璃棒搅动漏斗中的液体,否则可能损坏滤纸。
4.(1)烧杯 引流
(2)漏斗末端的尖嘴处没有紧靠烧杯内壁 不溶性
(3)倾倒待滤液时,漏斗内液面高于滤纸的边缘(或滤纸破损,或仪器不干净等,合理即可)
5.B [解析] 蒸发过程中要用玻璃棒不断搅拌,避免因局部温度过高,造成液滴飞溅;蒸发过程中,当蒸发皿中有较多固体析出时停止加热,然后利用余热将液体蒸干,而不是有少量固体析出时就停止加热;停止加热后蒸发皿温度仍较高,直接放于桌面上会损坏桌面;停止加热后,继续搅拌可以加快水的蒸发,同时避免固体飞溅。
6.(1)C (2)DACB
(3)搅拌,防止局部温度过高造成液滴飞溅 有较多固体析出
(4)80%
[解析] (1)过滤时没有用玻璃棒引流。(2)粗盐提纯的主要步骤是溶解、过滤、蒸发结晶。(3)蒸发操作时用玻璃棒的作用是搅拌,使溶液均匀受热,防止局部温度过高造成液滴飞溅,当有较多固体析出时,停止加热,利用余热将液体蒸干。(4)精盐的产率为6.4 g÷(10.0 g-2.0 g)× 100%=80%。
7.B [解析] 滤纸的边缘应略低于漏斗的边缘。
8.D [解析] 提纯含少量氯化钠杂质的硝酸钾固体,结合流程可知,操作Ⅰ为溶解,操作Ⅱ为蒸发浓缩、冷却结晶,操作Ⅲ是过滤、洗涤。
9.D [解析] 氯化钾易溶于水,二氧化锰难溶于水,分离氯化钾和二氧化锰的固体混合物,可加水溶解、过滤,滤液蒸发结晶得到氯化钾;滤渣洗涤、干燥,得到二氧化锰。
10.C [解析] 蒸馏法是利用混合物中各成分的沸点不同将混合物分离;化学沉淀法是根据混合物中各成分的化学性质不同,将某些物质转化为沉淀分离。
11.(1)降温结晶(或冷却结晶) (2)C
(3)A物质的溶解度受温度变化的影响不大
12.(1)铁架台
(2)防止粗盐腐蚀托盘,同时能使称量更准确
(3)胶头滴管 (4)C
(5)蒸发时没有用玻璃棒搅拌,会导致液滴飞溅,造成部分氯化钠损失
13.C [解析] a的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,采用降温结晶的方法,a的饱和溶液能够析出晶体,c的饱和溶液不能析出晶体;未指明溶液是否饱和,t1 ℃时,a、c两种物质的溶液中溶质质量分数不一定相等;t2 ℃时,a、b、c三种物质的溶解度大小关系是a>b>c,所以饱和溶液中溶质质量分数的大小关系是a>b>c;在t2 ℃时,a的溶解度是50 g,将30 g a物质加入50 g水中,充分溶解,所得溶液质量为25 g+50 g=75 g。
