第4章 认识化学变化测试题—2021-2022学年沪教版(全国)化学九年级上册(有答案)
文档属性
| 名称 | 第4章 认识化学变化测试题—2021-2022学年沪教版(全国)化学九年级上册(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 179.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-29 00:00:00 | ||
图片预览

文档简介
第4章《认识化学变化》测试题
一、单选题
1.2019年9月29日,宁波一家日用品加工企业的香水灌装车间起火,车间员工的一系列错误行为让原本很容易扑灭的小火扩散,酿成19人死亡、3人受伤的悲剧,如果掌握一些灭火措施和安全知识,可以减少悲剧的发生。下列说法你认为错误的是
A.酒精灯不慎打翻起火,立即用湿抹布扑灭
B.香水、酒精、油等燃料着火时最好用水扑灭
C.炒菜时油锅中的油不慎着火,可用锅盖盖灭
D.发现厨房内天然气管道漏气,应立即关闭气阀并轻轻开窗通风
2.某化学反应的微观示意图如下,下列说法正确的是
A.反应前后分子总数不变 B.甲发生了氧化反应
C.甲、乙两物质反应的质量比为17:32 D.氮元素的化合价在反应前后没有变化
3.2020年11月24日4时30分,长征五号遥五运载火箭在中国文昌航天发射场点火升空,将运送嫦娥五号探测器至地月转移轨道。长征五号遥五运载火箭采用液氧与液氢组合推进剂,下列有关说法错误的是
A.液氢与液氧反应会释放出大量的能量
B.液氢汽化过程中,氢分子之间的间隔增大
C.液氢与液氧反应的本质是氢、氧原子的重新组合
D.液氢与液氧化合生成水,元素种类和化合价都不变
4.如图是某化学反应的微观示意图,“”“”表示两种不同的原子,据图分析下列说法正确的是
A.在化学变化中分子不可以再分
B.化学反应前后原子的种类和数目都不改变
C.该反应中,各物质的元素化合价不一定发生改变
D.该反应中,反应物参加反应的各物质的微粒个数比为4:1或1:4
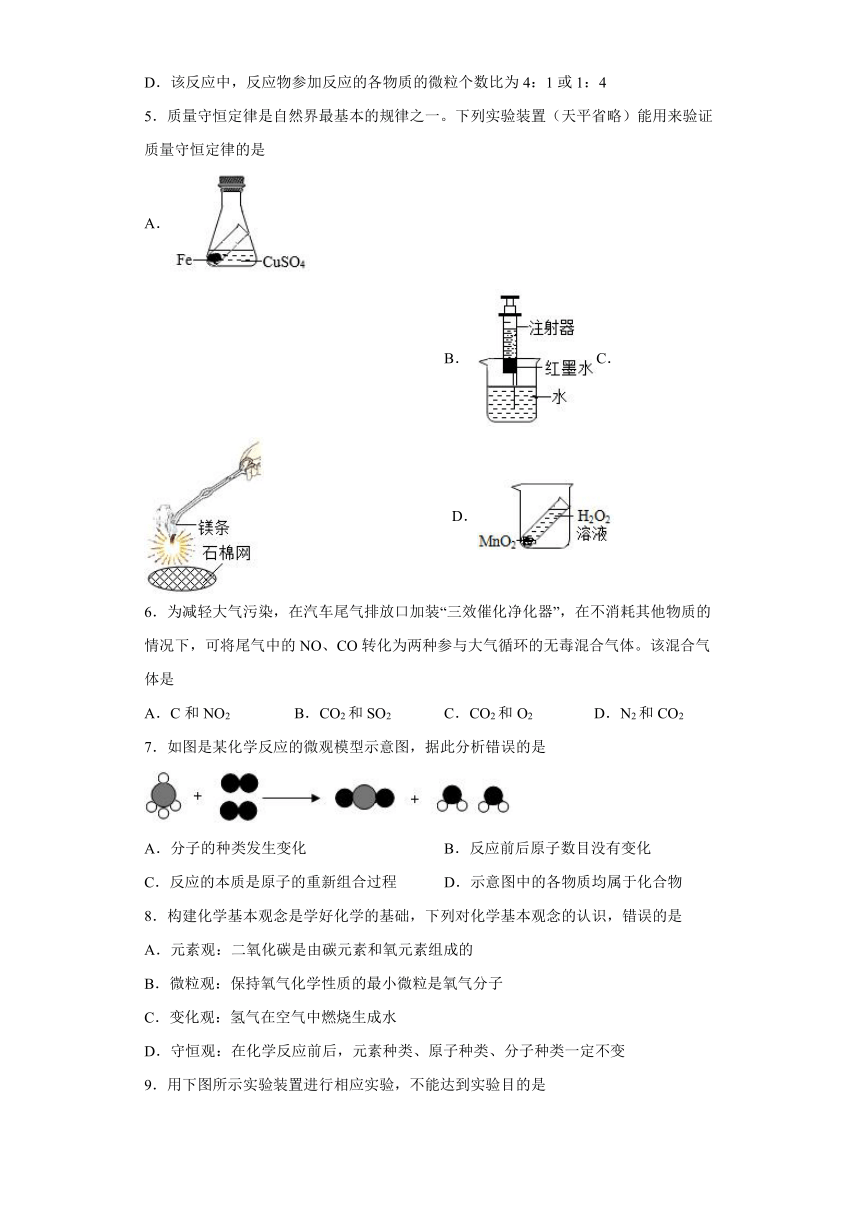
5.质量守恒定律是自然界最基本的规律之一。下列实验装置(天平省略)能用来验证质量守恒定律的是
A. B.C. D.
6.为减轻大气污染,在汽车尾气排放口加装“三效催化净化器”,在不消耗其他物质的情况下,可将尾气中的NO、CO转化为两种参与大气循环的无毒混合气体。该混合气体是
A.C和NO2 B.CO2和SO2 C.CO2和O2 D.N2和CO2
7.如图是某化学反应的微观模型示意图,据此分析错误的是
A.分子的种类发生变化 B.反应前后原子数目没有变化
C.反应的本质是原子的重新组合过程 D.示意图中的各物质均属于化合物
8.构建化学基本观念是学好化学的基础,下列对化学基本观念的认识,错误的是
A.元素观:二氧化碳是由碳元素和氧元素组成的
B.微粒观:保持氧气化学性质的最小微粒是氧气分子
C.变化观:氢气在空气中燃烧生成水
D.守恒观:在化学反应前后,元素种类、原子种类、分子种类一定不变
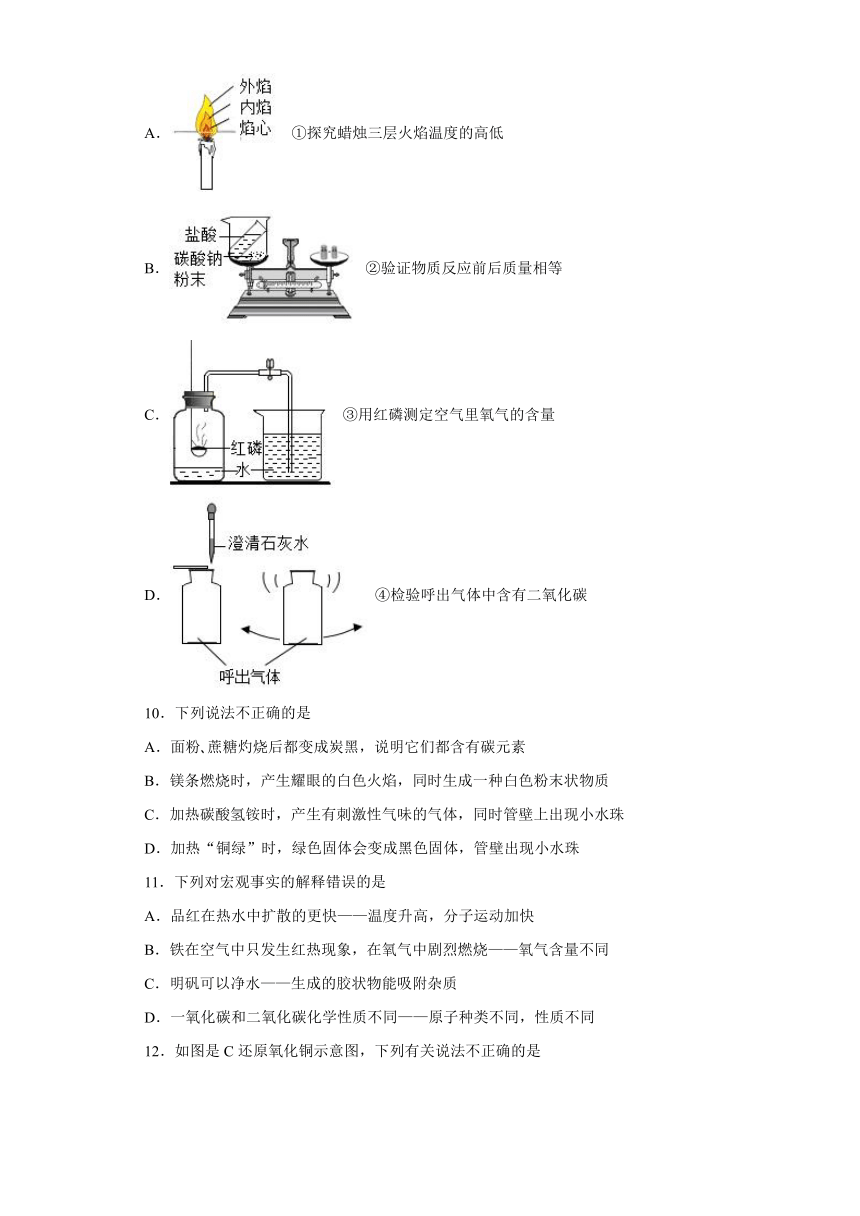
9.用下图所示实验装置进行相应实验,不能达到实验目的是
A. ①探究蜡烛三层火焰温度的高低
B. ②验证物质反应前后质量相等
C. ③用红磷测定空气里氧气的含量
D. ④检验呼出气体中含有二氧化碳
10.下列说法不正确的是
A.面粉 蔗糖灼烧后都变成炭黑,说明它们都含有碳元素
B.镁条燃烧时,产生耀眼的白色火焰,同时生成一种白色粉末状物质
C.加热碳酸氢铵时,产生有刺激性气味的气体,同时管壁上出现小水珠
D.加热“铜绿”时,绿色固体会变成黑色固体,管壁出现小水珠
11.下列对宏观事实的解释错误的是
A.品红在热水中扩散的更快——温度升高,分子运动加快
B.铁在空气中只发生红热现象,在氧气中剧烈燃烧——氧气含量不同
C.明矾可以净水——生成的胶状物能吸附杂质
D.一氧化碳和二氧化碳化学性质不同——原子种类不同,性质不同
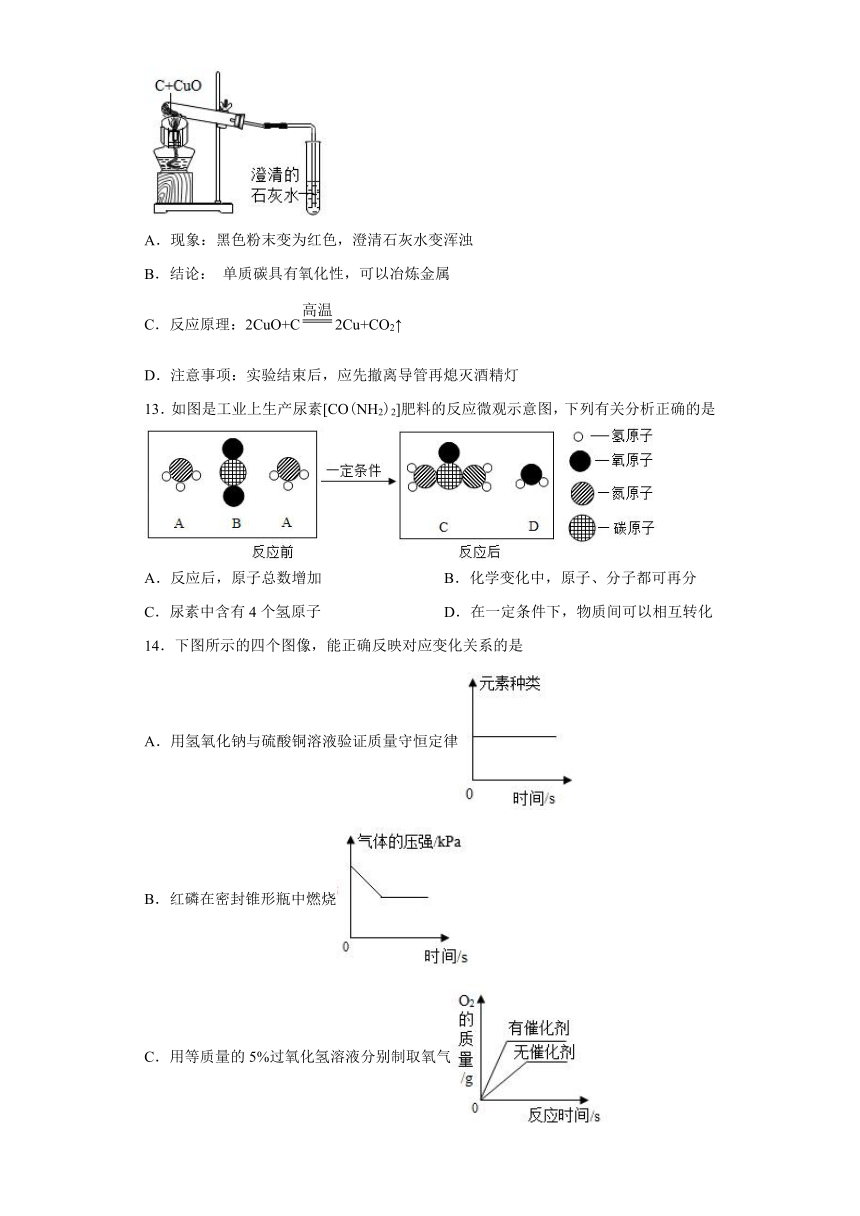
12.如图是C还原氧化铜示意图,下列有关说法不正确的是
A.现象:黑色粉末变为红色,澄清石灰水变浑浊
B.结论: 单质碳具有氧化性,可以冶炼金属
C.反应原理:2CuO+C2Cu+CO2↑
D.注意事项:实验结束后,应先撤离导管再熄灭酒精灯
13.如图是工业上生产尿素[CO(NH2)2]肥料的反应微观示意图,下列有关分析正确的是
A.反应后,原子总数增加 B.化学变化中,原子、分子都可再分
C.尿素中含有4个氢原子 D.在一定条件下,物质间可以相互转化
14.下图所示的四个图像,能正确反映对应变化关系的是
A.用氢氧化钠与硫酸铜溶液验证质量守恒定律
B.红磷在密封锥形瓶中燃烧
C.用等质量的5%过氧化氢溶液分别制取氧气
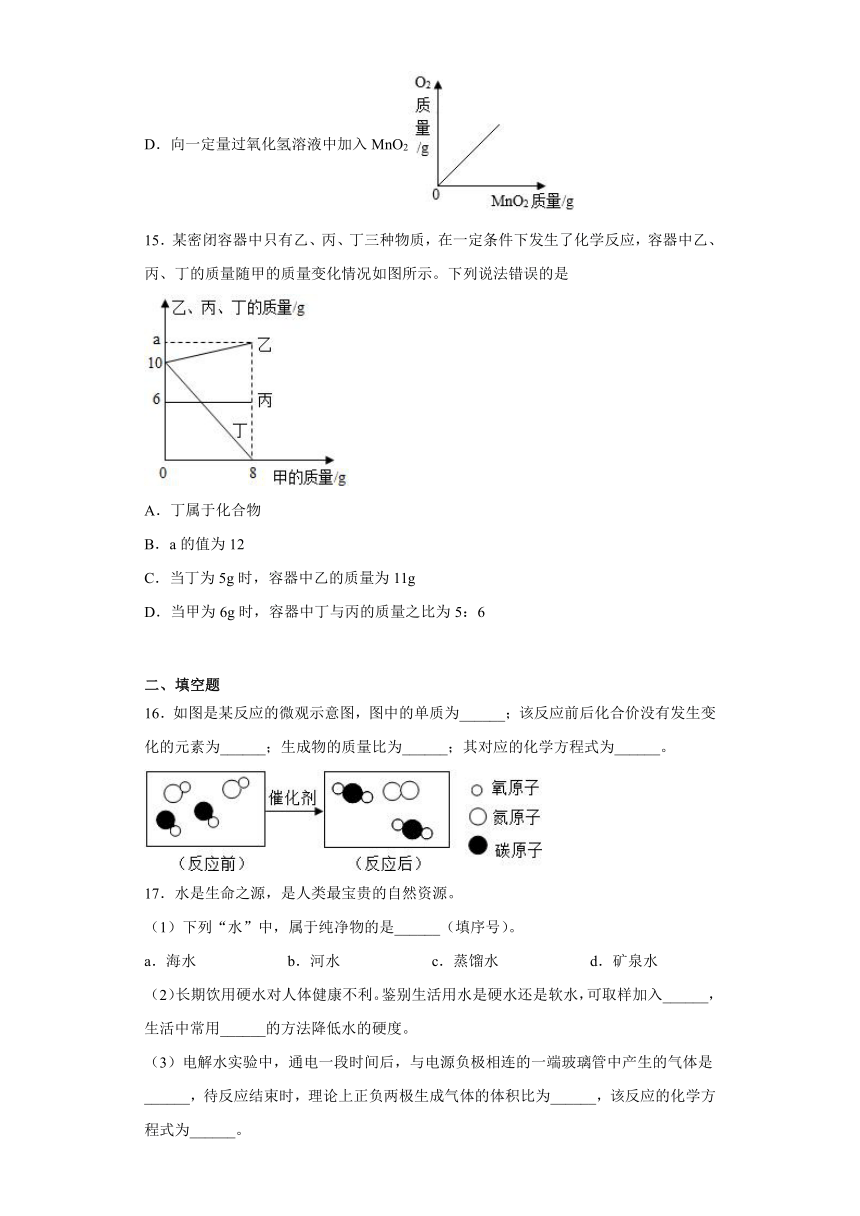
D.向一定量过氧化氢溶液中加入MnO2
15.某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了化学反应,容器中乙、丙、丁的质量随甲的质量变化情况如图所示。下列说法错误的是
A.丁属于化合物
B.a的值为12
C.当丁为5g时,容器中乙的质量为11g
D.当甲为6g时,容器中丁与丙的质量之比为5:6
二、填空题
16.如图是某反应的微观示意图,图中的单质为______;该反应前后化合价没有发生变化的元素为______;生成物的质量比为______;其对应的化学方程式为______。
17.水是生命之源,是人类最宝贵的自然资源。
(1)下列“水”中,属于纯净物的是______(填序号)。
a.海水 b.河水 c.蒸馏水 d.矿泉水
(2)长期饮用硬水对人体健康不利。鉴别生活用水是硬水还是软水,可取样加入______,生活中常用______的方法降低水的硬度。
(3)电解水实验中,通电一段时间后,与电源负极相连的一端玻璃管中产生的气体是______,待反应结束时,理论上正负两极生成气体的体积比为______,该反应的化学方程式为______。
(4)做好自我防护,养成良好的卫生习惯。如合理佩戴口罩、不到人群聚集的地方等。口罩的防护原理与化学中的______(填实验操作名称)相似。
18.宏观和微观相结合是认识物质结构的有效方法之一。
(一)已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表。
X Y Z W
对应元素名称 氧 镁 铝 氯
核电荷数 8 12 13 17
电子层 第一层 2 2 2 2
第二层 a 8 8 8
第三层 3 8
请回答下列问题:
①若X表示离子,a=______。单质X2与单质Z的反应中,Z原子______(填“得到”或“失去”)电子,Y位于元素周期表的第______周期。
②Y、W形成的化合物由______构成(用粒子符号表示)。
(二)写出实验室用两种固体混合物制取X单质的化学方程式:______。
(三)用“”和“”分别代表两种不同元素的原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如图:
(1)从物质的分类看,图A中的物质属于______(纯净物或混合物),判断的理由_____。
(2)该反应的基本反应类型是______。
(3)从图中你可以得出的正确结论有______(填序号)。
①分子是由原子构成的
②化学反应中,分子可以分成原子,原子不能再分
③反应前后分子种类不变
(四)实验测得某氯元素的氧化物中,氯元素与氧元素的质量比为71:64,该氧化物中氯元素的化合价______。
19.2019年是俄国化学家门捷列夫发明元素周期表150周年,元素周期表揭示了化学元素间的内在联系,使其构成一个完整体系。
(1)中国科学院院士张青莲对铟、铱、锗等的相对原子质量的测定做出了杰出贡献。锗元素在元素周期表中的部分信息如图所示,锗的相对原子质量为___________,该元素属于___________(填“金属”或“非金属”)元素。
(2)中国科学家姜雪峰当选为“全球青年化学家元素周期表硫元素大使”。
①如图是硫离子结构示意图,则硫原子的最外层电子数是___________。
②火药是中国古代四大发明之一,已知黑火药爆炸反应的化学方程式为:,则X的化学式为___________。
20.质量相等的四种物质①KMnO4 ②KClO3 ③H2O2 ④H2O,完全分解后所制得氧气的质量由大到小的顺序为_______________(填序号)。相同质量的一氧化碳和二氧化碳所含分子个数之比_____________。
三、推断题
21.图中甲、乙、丙、丁为初中化学常见的纯净物。甲是一种黑色固体单质,乙、丙、丁通常情况下都是气体,且乙、丙组成元素相同,它们之间的转化关系(“→”表示一种物质可生成另一种物质,图中部分反应物、生成物及反应条件已略去)如右图所示。请回答下列问题:
(1)甲的化学式为____________,丁的化学式为_____________。
(2)乙、丙化学性质不同的原因是_____________。
(3)乙→丙的化学方程式为_____________,该反应的现象为_____________。
22.A、B、C、D、E是初中化学常见物质,A、B两物质的组成元素相同,C、D、E为相同类别的物质,它们之间的关系如图所示,“一”表示物质间相互反应,“→”表示一种物质生成另一种物质。
(1)写出D物质的一种用途___________。
(2)保持A物质化学性质的最小微粒是___________。
(3)描述D与E反应的现象___________。
(4)C→B反应的化学方程式___________,其基本反应类型是___________。
(5)C与D反应的微观实质___________。
四、实验题
23.某些兴趣小组对“四氧化三铁能否作过氧化氢分解的催化剂”进行了探究实验。
试验编号 操作 现象 分析
① 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 有少量气泡产生,木条不复燃 过氧化氢分解,但反应速率太慢
② ______ 有大量气泡产生,木条复燃 四氧化三铁能加快过氧化氢分解
(1)请帮该小组填写表中未填完的表格______。
(2)实验结论:四氧化三铁是过氧化氢分解的催化剂,该反应的化学方程式为:______。
(3)小明同学认为仅由上述实验还不能得出上述结论,还需要补充实验验证四氧化三铁的______和______在反应前后是否改变。
(4)小明在实验时发现试管内有许多水雾,由此推断过氧化氢分解是______(填“放热”或“吸热”)。
(5)实验过程中发现将过氧化氢加入盛有四氧化三铁的试管后,反应速率逐渐加快,然后又逐渐变慢(如图2)从影响化学反应速率的因素(温度、反应物的浓度等)来分析,过氧化氢分解速率发生变化原因。
反应速率先变快原因:______。反应速率后变慢原因:______。
24.根据所学知识并结合如图所示装置回答下列问题:
(1)图中标有①、②的仪器名称:①________;②________。
(2)若选择A和C装置制取并收集氧气,则要对A装置进行的改进是_____,检验C中氧气收集满的方法是______;该实验选择高锰酸钾制取氧气时,还需要在试管口加一小团棉花,原因是_______,用B装置制取氧气的化学方程式是________。
(3)还可以选择E装置收集氧气,是因为______(填写氧气的性质);需等______时开始收集氧气;正确的操作顺序为______(按顺序填编号)。
a.将导管伸入集气瓶口,让气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面
(4)某同学想制取氧气做F实验,他最好采用______装置收集氧气。
五、计算题
25.某兴趣小组用氯酸钾和二氧化锰的混合物制取氧气,实验过程中固体的质量随时间变化的数据见下表。
加热时间/min 0 t1 t2 t3
固体质量/g 56 46.4 36.8 36.8
(1)共制得氧气_______g。
(2)计算原固体混合物中氯酸钾的质量______。
26.84消毒液是一种含氯消毒剂,其有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是Cl2+2NaOH=NaCIO+NaCl+H2O。某同学将Cl2通入185.8g NaOH 溶液中(NaOH过量),充分反应后得到混合溶液200g。
(1)“含氯消毒剂”中的“氯”是指______(填字母)。
A.氯原子 B.氯元素 C.氯分子 D.氯离子
(2)次氯酸钠中,钠元素、氧元素的质量比是______。
(3)参加反应的氯气质量为______g。
(4)已知次氯酸钠与混合溶液质量的百分比,是混合溶液中次氧酸钠的质量分数,求该质量分数。
参考答案
1.B 2.B 3.D 4.B 5.A 6.D 7.D 8.D 9.B 10.B 11.D 12.B 13.D 14.A 15.D
16.氮气
17.(1)c
(2) 肥皂水 煮沸
(3) 氢气2 1:2 2H2O2H2↑+O2↑
(4)过滤
18.8 失去 三 Mg2+、Cl-
混合物 该物质中含有两种分子(合理即可) 分解反应 ①② +4
19.(1) 72.63 金属
(2) 6 K2S
20.④③②① 11:7
21.(1) C O2
(2)二者分子构成不同
(3) 或 产生蓝色火焰,放热(或黑色固体变成红色等合理即可)
22.(1)炼钢、用于医疗急救等
(2)过氧化氢分子2O2
(3)剧烈燃烧、火星四射、生成黑色固体,放出热量
(4) 化合反应
(5)氢分子分为氢原子,氧分子分为氧原子,每2个氢原子和1个氧原子结合成1个水分子
23.(1)取5mL5%的过氧化氢溶液于试管中,加入四氧化三铁,然后伸入带火星的木条
(2)
(3) 质量 化学性质
(4)放热
(5) 反应放热能加快反应速率 随着反应的进行,过氧化氢浓度降低,化学反应速度随之减慢
24.(1) 酒精灯 集气瓶
(2) 试管口向下倾斜 用带火星的木条放到集气瓶口,若木条复燃证明氧气已收集 防止加热时,高锰酸钾粉末随气流进入导管
(3) 氧气不易溶于水,且与水不反应 气泡连续、均匀放出 bac
(4)E
25.(1)19.2
(2)解:设原固体混合物中氯酸钾的质量为x
答:氯酸钾质量为49g。
26.(1)B
(2)23:16
(3)14.2
(4)设混合溶液中次氧酸钠的质量为
混合溶液中次氧酸钠的质量分数=
答:混合溶液中次氧酸钠的质量分数是7.45%
一、单选题
1.2019年9月29日,宁波一家日用品加工企业的香水灌装车间起火,车间员工的一系列错误行为让原本很容易扑灭的小火扩散,酿成19人死亡、3人受伤的悲剧,如果掌握一些灭火措施和安全知识,可以减少悲剧的发生。下列说法你认为错误的是
A.酒精灯不慎打翻起火,立即用湿抹布扑灭
B.香水、酒精、油等燃料着火时最好用水扑灭
C.炒菜时油锅中的油不慎着火,可用锅盖盖灭
D.发现厨房内天然气管道漏气,应立即关闭气阀并轻轻开窗通风
2.某化学反应的微观示意图如下,下列说法正确的是
A.反应前后分子总数不变 B.甲发生了氧化反应
C.甲、乙两物质反应的质量比为17:32 D.氮元素的化合价在反应前后没有变化
3.2020年11月24日4时30分,长征五号遥五运载火箭在中国文昌航天发射场点火升空,将运送嫦娥五号探测器至地月转移轨道。长征五号遥五运载火箭采用液氧与液氢组合推进剂,下列有关说法错误的是
A.液氢与液氧反应会释放出大量的能量
B.液氢汽化过程中,氢分子之间的间隔增大
C.液氢与液氧反应的本质是氢、氧原子的重新组合
D.液氢与液氧化合生成水,元素种类和化合价都不变
4.如图是某化学反应的微观示意图,“”“”表示两种不同的原子,据图分析下列说法正确的是
A.在化学变化中分子不可以再分
B.化学反应前后原子的种类和数目都不改变
C.该反应中,各物质的元素化合价不一定发生改变
D.该反应中,反应物参加反应的各物质的微粒个数比为4:1或1:4
5.质量守恒定律是自然界最基本的规律之一。下列实验装置(天平省略)能用来验证质量守恒定律的是
A. B.C. D.
6.为减轻大气污染,在汽车尾气排放口加装“三效催化净化器”,在不消耗其他物质的情况下,可将尾气中的NO、CO转化为两种参与大气循环的无毒混合气体。该混合气体是
A.C和NO2 B.CO2和SO2 C.CO2和O2 D.N2和CO2
7.如图是某化学反应的微观模型示意图,据此分析错误的是
A.分子的种类发生变化 B.反应前后原子数目没有变化
C.反应的本质是原子的重新组合过程 D.示意图中的各物质均属于化合物
8.构建化学基本观念是学好化学的基础,下列对化学基本观念的认识,错误的是
A.元素观:二氧化碳是由碳元素和氧元素组成的
B.微粒观:保持氧气化学性质的最小微粒是氧气分子
C.变化观:氢气在空气中燃烧生成水
D.守恒观:在化学反应前后,元素种类、原子种类、分子种类一定不变
9.用下图所示实验装置进行相应实验,不能达到实验目的是
A. ①探究蜡烛三层火焰温度的高低
B. ②验证物质反应前后质量相等
C. ③用红磷测定空气里氧气的含量
D. ④检验呼出气体中含有二氧化碳
10.下列说法不正确的是
A.面粉 蔗糖灼烧后都变成炭黑,说明它们都含有碳元素
B.镁条燃烧时,产生耀眼的白色火焰,同时生成一种白色粉末状物质
C.加热碳酸氢铵时,产生有刺激性气味的气体,同时管壁上出现小水珠
D.加热“铜绿”时,绿色固体会变成黑色固体,管壁出现小水珠
11.下列对宏观事实的解释错误的是
A.品红在热水中扩散的更快——温度升高,分子运动加快
B.铁在空气中只发生红热现象,在氧气中剧烈燃烧——氧气含量不同
C.明矾可以净水——生成的胶状物能吸附杂质
D.一氧化碳和二氧化碳化学性质不同——原子种类不同,性质不同
12.如图是C还原氧化铜示意图,下列有关说法不正确的是
A.现象:黑色粉末变为红色,澄清石灰水变浑浊
B.结论: 单质碳具有氧化性,可以冶炼金属
C.反应原理:2CuO+C2Cu+CO2↑
D.注意事项:实验结束后,应先撤离导管再熄灭酒精灯
13.如图是工业上生产尿素[CO(NH2)2]肥料的反应微观示意图,下列有关分析正确的是
A.反应后,原子总数增加 B.化学变化中,原子、分子都可再分
C.尿素中含有4个氢原子 D.在一定条件下,物质间可以相互转化
14.下图所示的四个图像,能正确反映对应变化关系的是
A.用氢氧化钠与硫酸铜溶液验证质量守恒定律
B.红磷在密封锥形瓶中燃烧
C.用等质量的5%过氧化氢溶液分别制取氧气
D.向一定量过氧化氢溶液中加入MnO2
15.某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了化学反应,容器中乙、丙、丁的质量随甲的质量变化情况如图所示。下列说法错误的是
A.丁属于化合物
B.a的值为12
C.当丁为5g时,容器中乙的质量为11g
D.当甲为6g时,容器中丁与丙的质量之比为5:6
二、填空题
16.如图是某反应的微观示意图,图中的单质为______;该反应前后化合价没有发生变化的元素为______;生成物的质量比为______;其对应的化学方程式为______。
17.水是生命之源,是人类最宝贵的自然资源。
(1)下列“水”中,属于纯净物的是______(填序号)。
a.海水 b.河水 c.蒸馏水 d.矿泉水
(2)长期饮用硬水对人体健康不利。鉴别生活用水是硬水还是软水,可取样加入______,生活中常用______的方法降低水的硬度。
(3)电解水实验中,通电一段时间后,与电源负极相连的一端玻璃管中产生的气体是______,待反应结束时,理论上正负两极生成气体的体积比为______,该反应的化学方程式为______。
(4)做好自我防护,养成良好的卫生习惯。如合理佩戴口罩、不到人群聚集的地方等。口罩的防护原理与化学中的______(填实验操作名称)相似。
18.宏观和微观相结合是认识物质结构的有效方法之一。
(一)已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表。
X Y Z W
对应元素名称 氧 镁 铝 氯
核电荷数 8 12 13 17
电子层 第一层 2 2 2 2
第二层 a 8 8 8
第三层 3 8
请回答下列问题:
①若X表示离子,a=______。单质X2与单质Z的反应中,Z原子______(填“得到”或“失去”)电子,Y位于元素周期表的第______周期。
②Y、W形成的化合物由______构成(用粒子符号表示)。
(二)写出实验室用两种固体混合物制取X单质的化学方程式:______。
(三)用“”和“”分别代表两种不同元素的原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如图:
(1)从物质的分类看,图A中的物质属于______(纯净物或混合物),判断的理由_____。
(2)该反应的基本反应类型是______。
(3)从图中你可以得出的正确结论有______(填序号)。
①分子是由原子构成的
②化学反应中,分子可以分成原子,原子不能再分
③反应前后分子种类不变
(四)实验测得某氯元素的氧化物中,氯元素与氧元素的质量比为71:64,该氧化物中氯元素的化合价______。
19.2019年是俄国化学家门捷列夫发明元素周期表150周年,元素周期表揭示了化学元素间的内在联系,使其构成一个完整体系。
(1)中国科学院院士张青莲对铟、铱、锗等的相对原子质量的测定做出了杰出贡献。锗元素在元素周期表中的部分信息如图所示,锗的相对原子质量为___________,该元素属于___________(填“金属”或“非金属”)元素。
(2)中国科学家姜雪峰当选为“全球青年化学家元素周期表硫元素大使”。
①如图是硫离子结构示意图,则硫原子的最外层电子数是___________。
②火药是中国古代四大发明之一,已知黑火药爆炸反应的化学方程式为:,则X的化学式为___________。
20.质量相等的四种物质①KMnO4 ②KClO3 ③H2O2 ④H2O,完全分解后所制得氧气的质量由大到小的顺序为_______________(填序号)。相同质量的一氧化碳和二氧化碳所含分子个数之比_____________。
三、推断题
21.图中甲、乙、丙、丁为初中化学常见的纯净物。甲是一种黑色固体单质,乙、丙、丁通常情况下都是气体,且乙、丙组成元素相同,它们之间的转化关系(“→”表示一种物质可生成另一种物质,图中部分反应物、生成物及反应条件已略去)如右图所示。请回答下列问题:
(1)甲的化学式为____________,丁的化学式为_____________。
(2)乙、丙化学性质不同的原因是_____________。
(3)乙→丙的化学方程式为_____________,该反应的现象为_____________。
22.A、B、C、D、E是初中化学常见物质,A、B两物质的组成元素相同,C、D、E为相同类别的物质,它们之间的关系如图所示,“一”表示物质间相互反应,“→”表示一种物质生成另一种物质。
(1)写出D物质的一种用途___________。
(2)保持A物质化学性质的最小微粒是___________。
(3)描述D与E反应的现象___________。
(4)C→B反应的化学方程式___________,其基本反应类型是___________。
(5)C与D反应的微观实质___________。
四、实验题
23.某些兴趣小组对“四氧化三铁能否作过氧化氢分解的催化剂”进行了探究实验。
试验编号 操作 现象 分析
① 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 有少量气泡产生,木条不复燃 过氧化氢分解,但反应速率太慢
② ______ 有大量气泡产生,木条复燃 四氧化三铁能加快过氧化氢分解
(1)请帮该小组填写表中未填完的表格______。
(2)实验结论:四氧化三铁是过氧化氢分解的催化剂,该反应的化学方程式为:______。
(3)小明同学认为仅由上述实验还不能得出上述结论,还需要补充实验验证四氧化三铁的______和______在反应前后是否改变。
(4)小明在实验时发现试管内有许多水雾,由此推断过氧化氢分解是______(填“放热”或“吸热”)。
(5)实验过程中发现将过氧化氢加入盛有四氧化三铁的试管后,反应速率逐渐加快,然后又逐渐变慢(如图2)从影响化学反应速率的因素(温度、反应物的浓度等)来分析,过氧化氢分解速率发生变化原因。
反应速率先变快原因:______。反应速率后变慢原因:______。
24.根据所学知识并结合如图所示装置回答下列问题:
(1)图中标有①、②的仪器名称:①________;②________。
(2)若选择A和C装置制取并收集氧气,则要对A装置进行的改进是_____,检验C中氧气收集满的方法是______;该实验选择高锰酸钾制取氧气时,还需要在试管口加一小团棉花,原因是_______,用B装置制取氧气的化学方程式是________。
(3)还可以选择E装置收集氧气,是因为______(填写氧气的性质);需等______时开始收集氧气;正确的操作顺序为______(按顺序填编号)。
a.将导管伸入集气瓶口,让气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面
(4)某同学想制取氧气做F实验,他最好采用______装置收集氧气。
五、计算题
25.某兴趣小组用氯酸钾和二氧化锰的混合物制取氧气,实验过程中固体的质量随时间变化的数据见下表。
加热时间/min 0 t1 t2 t3
固体质量/g 56 46.4 36.8 36.8
(1)共制得氧气_______g。
(2)计算原固体混合物中氯酸钾的质量______。
26.84消毒液是一种含氯消毒剂,其有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是Cl2+2NaOH=NaCIO+NaCl+H2O。某同学将Cl2通入185.8g NaOH 溶液中(NaOH过量),充分反应后得到混合溶液200g。
(1)“含氯消毒剂”中的“氯”是指______(填字母)。
A.氯原子 B.氯元素 C.氯分子 D.氯离子
(2)次氯酸钠中,钠元素、氧元素的质量比是______。
(3)参加反应的氯气质量为______g。
(4)已知次氯酸钠与混合溶液质量的百分比,是混合溶液中次氧酸钠的质量分数,求该质量分数。
参考答案
1.B 2.B 3.D 4.B 5.A 6.D 7.D 8.D 9.B 10.B 11.D 12.B 13.D 14.A 15.D
16.氮气
17.(1)c
(2) 肥皂水 煮沸
(3) 氢气2 1:2 2H2O2H2↑+O2↑
(4)过滤
18.8 失去 三 Mg2+、Cl-
混合物 该物质中含有两种分子(合理即可) 分解反应 ①② +4
19.(1) 72.63 金属
(2) 6 K2S
20.④③②① 11:7
21.(1) C O2
(2)二者分子构成不同
(3) 或 产生蓝色火焰,放热(或黑色固体变成红色等合理即可)
22.(1)炼钢、用于医疗急救等
(2)过氧化氢分子2O2
(3)剧烈燃烧、火星四射、生成黑色固体,放出热量
(4) 化合反应
(5)氢分子分为氢原子,氧分子分为氧原子,每2个氢原子和1个氧原子结合成1个水分子
23.(1)取5mL5%的过氧化氢溶液于试管中,加入四氧化三铁,然后伸入带火星的木条
(2)
(3) 质量 化学性质
(4)放热
(5) 反应放热能加快反应速率 随着反应的进行,过氧化氢浓度降低,化学反应速度随之减慢
24.(1) 酒精灯 集气瓶
(2) 试管口向下倾斜 用带火星的木条放到集气瓶口,若木条复燃证明氧气已收集 防止加热时,高锰酸钾粉末随气流进入导管
(3) 氧气不易溶于水,且与水不反应 气泡连续、均匀放出 bac
(4)E
25.(1)19.2
(2)解:设原固体混合物中氯酸钾的质量为x
答:氯酸钾质量为49g。
26.(1)B
(2)23:16
(3)14.2
(4)设混合溶液中次氧酸钠的质量为
混合溶液中次氧酸钠的质量分数=
答:混合溶液中次氧酸钠的质量分数是7.45%
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
