第5章金属的冶炼与利用测试题—2021-2022学年九年级化学沪教版(全国)上册(有答案)
文档属性
| 名称 | 第5章金属的冶炼与利用测试题—2021-2022学年九年级化学沪教版(全国)上册(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 97.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-29 00:00:00 | ||
图片预览



文档简介
第5章《金属的冶炼与利用》测试题
一、单选题
1.物质性质决定用途。下列说法不正确的是
A.氧气能支持燃烧,用于做火箭的燃料 B.金刚石硬度大,用于切割玻璃
C.铜具有良好的导电性,用于做导线 D.氢气有可燃性,用于高能燃料
2.下列关于资源、能源的叙述错误的是
A.废旧金属的回收利用,不但可以节约金属资源,还可以减少对环境的污染
B.空气是人类生产活动的重要资源
C.海洋是地球上巨大的资源宝库,海水中含有80多种化学物质
D.地球表面约71%被水覆盖,其中绝大多数是海洋水
3.下列物质的用途主要由其化学性质决定的是
A.铜丝作导线 B.液氮作增雨剂
C.氮气作保护气 D.稀有气体作霓虹灯
4.推理是一种重要的研究和学习方法,下列推理正确的是
A.铁丝能在氧气中燃烧,空气中含有氧气,所以铁丝也能在空气中燃烧
B.化合物由不同种元素组成,但不同种元素组成的物质不一定是化合物
C.单质是由同种元素组成的,则由同种元素组成的物质都是单质
D.铁、铝、铜等金属都是固体,则所有的金属都是固态物质
5.下列物质中,不能由金属单质和盐酸直接反应生成的是
A.ZnCl2 B.AlCl3 C.FeCl3 D.MgCl2
6.氧气的化学性质活泼,下列物质与氧气反应的现象描述不正确的是
A.镁条在空气中燃烧:发出耀眼的白光,生成白色固体粉末
B.细铁丝在氧气中燃烧:火星四射,生成黑色固体
C.木炭在氧气中燃烧:发出耀眼的白光,放出大量的热,生成二氧化碳气体
D.在空气中加热铜粉:红色固体粉末逐渐变成黑色
7.下列实验现象描述不正确的是
A.红磷在空气中燃烧,产生大量白烟
B.黄铜和纯铜相互刻划,黄铜表面留有划痕
C.细铁丝在氧气中燃烧,火星四射,生成黑色固体
D.镁在空气中燃烧,发出耀眼的白光,生成一种白色固体
8.下列说法错误的是
A.空气中的氧气与水中溶解的氧气化学性质同样活泼
B.工业上可以利用分离液态空气法制取氧气
C.氧气可以支持燃烧,说明氧气具有助燃性
D.生铁、紫铜、氧化镁都属于金属材料
9.鉴别下列各物质的方法,正确的是
需鉴别的物质 方法
A 吸入的气体和呼出的气体 观察颜色
B 氧气和空气 闻气味
C 铁粉和炭粉 用磁铁
D 氮气与二氧化碳 燃着的木条
A.A B.B C.C D.D
10.下列关于“物质一用途一性质”的说法不正确的是
A.氧气一火箭发射一可燃性 B.铜一做导线一导电性好
C.氮气一食品防腐一常温下化学性质稳定 D.氦气一填充飞艇一密度小
11.下列生活中的变化属于物理变化的是
A.花生霉变 B.木材燃烧 C.钢铁生锈 D.水果榨汁
12.为验证甲、乙、丙三种金属的活动性顺序,把三种金属分别放入稀盐酸中,只有乙表面无明显变化,把甲放入丙的硝酸盐溶液中,甲的表面有丙析出,则甲、乙、丙三种金属的活动性顺序由强到弱的是
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.丙>乙>甲
13.在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图,有关说法正确的是
A.该反应属于置换反应
B.该反应的生成物都是化合物
C.反应前后各元素的化合价都发生了改变
D.参加反应的A与B的分子个数比为1︰1
14.如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是
A.图中有两种氧化物 B.生成单质与化合物的质量比为7:22
C.生成物的分子个数比为1:1 D.该反应为置换反应
15.在装有下列固体的烧杯中,加入足量的稀盐酸,烧杯中最后只得到无色溶液的是
A.Fe2O3 B.Fe C.Mg D.AgNO3
二、填空题
16.“家”是一个化学小世界,蕴含丰富的化学知识,请回答下列问题。
(1)小红的妈妈做她最爱吃的“红烧肉”时加入了“加铁酱油”,其中“加铁酱油”中的“铁”指_____(填“元素”或“原子”),身体一旦缺铁可能患有的疾病是_______。
(2)做饭时油锅突然起火,妈妈采用了立即盖上锅盖的方法灭火,灭火的原理是_______。
(3)烧菜时用到了不锈钢锅,不锈钢属于_______。(填“合成材料”或“合金”)
(4)碳酸饮料中常加入防腐剂——苯甲酸(C6H5COOH),其碳、氢元素的质量比为_______,该防腐剂属于_______(填“有机物”或“无机物”)。
17.请用化学用语回答下列问题。
(1)生活中常用氢气或氦气填充气球,但氢气球容易爆炸, 氦气球则相对安全,应用较广。氦气的化学式为______。
(2)“喝酒不开车,开车不喝酒”。交警使用的酒精检测器里盛放经过酸化处理的含强氧化剂三氧化铬(CrO3)的硅胶。如果司机喝过酒,呼出气体中含有的乙醇蒸气将CrO3还原成硫酸铬[Cr2(SO4)3],检测器就会由暗红色变成蓝绿色。硫酸铬中铬元素的化合价为______。
(3)铝的化学性质很活泼,但在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为______。
18.化学物质及其变化同日常生活密切相关,请据所学知识回答下列问题。
(1)人体缺_______(填元素符号)元素能导致佝偻病或骨质疏松。
(2)空气中主要气体之一,化学性质不活泼,可充入食品包装防腐是_______。
(3)铁锅常用作炊具,是因为铁具有良好的_______性。(填一种物理性质)
(4)某品牌加碘盐中添加的是碘酸钾(KIO3),KIO3中碘元素的化合价是_______。
(5)建筑工地上盛有石灰水的水池中,常会看到一层白膜覆盖在石灰水的水面上,形成白膜的反应符号(或文字)表达式是:_______。
19.依据所学知识回答问题
(1)请用化学符号填空:
①4个氦原子:_______;
②标出KClO3中氯元素的化合价:_______;
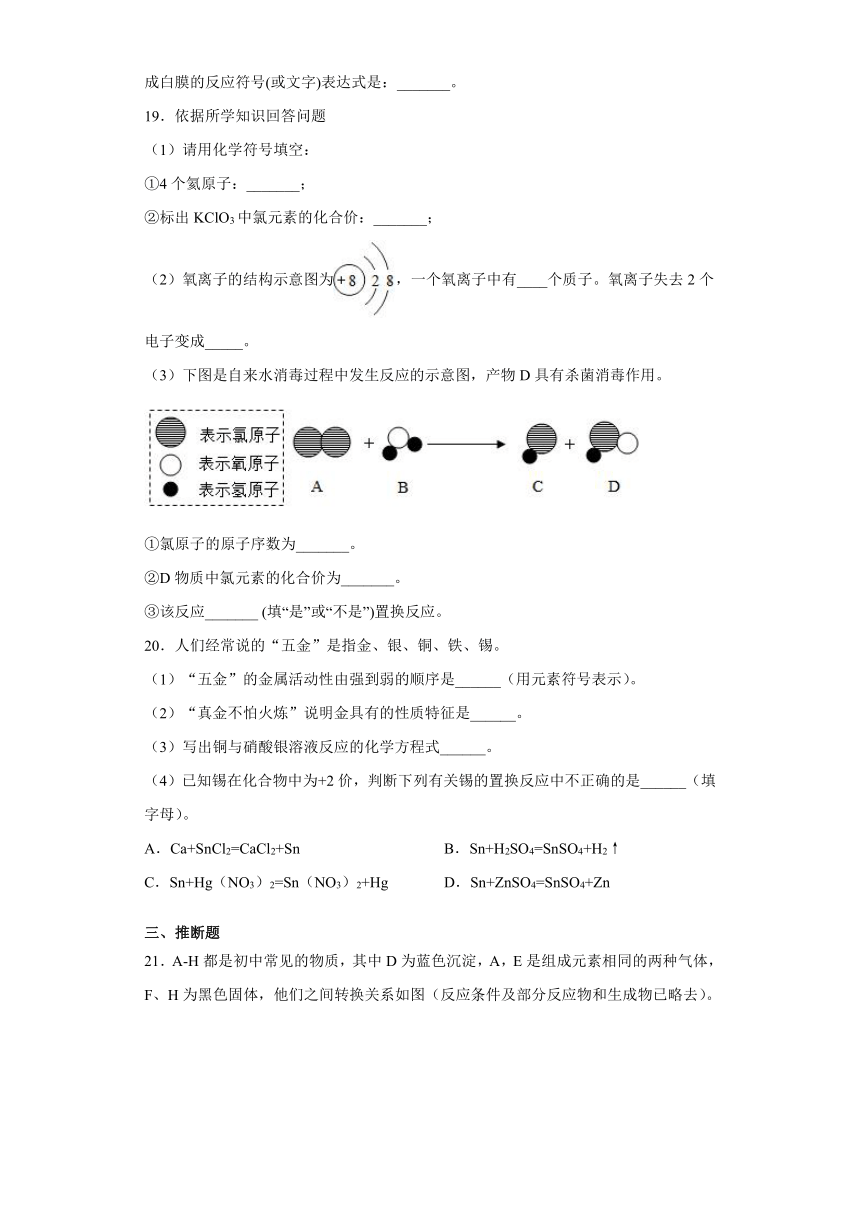
(2)氧离子的结构示意图为,一个氧离子中有____个质子。氧离子失去2个电子变成_____。
(3)下图是自来水消毒过程中发生反应的示意图,产物D具有杀菌消毒作用。
①氯原子的原子序数为_______。
②D物质中氯元素的化合价为_______。
③该反应_______ (填“是”或“不是”)置换反应。
20.人们经常说的“五金”是指金、银、铜、铁、锡。
(1)“五金”的金属活动性由强到弱的顺序是______(用元素符号表示)。
(2)“真金不怕火炼”说明金具有的性质特征是______。
(3)写出铜与硝酸银溶液反应的化学方程式______。
(4)已知锡在化合物中为+2价,判断下列有关锡的置换反应中不正确的是______(填字母)。
A.Ca+SnCl2=CaCl2+Sn B.Sn+H2SO4=SnSO4+H2↑
C.Sn+Hg(NO3)2=Sn(NO3)2+Hg D.Sn+ZnSO4=SnSO4+Zn
三、推断题
21.A-H都是初中常见的物质,其中D为蓝色沉淀,A,E是组成元素相同的两种气体,F、H为黑色固体,他们之间转换关系如图(反应条件及部分反应物和生成物已略去)。
(1)反应FB属于______(填基本反应类型)
(2)D的化学式是______,X属于______类物质.
(3)写出反应AB的化学方程式______.
(4)答出G的一种用途______.
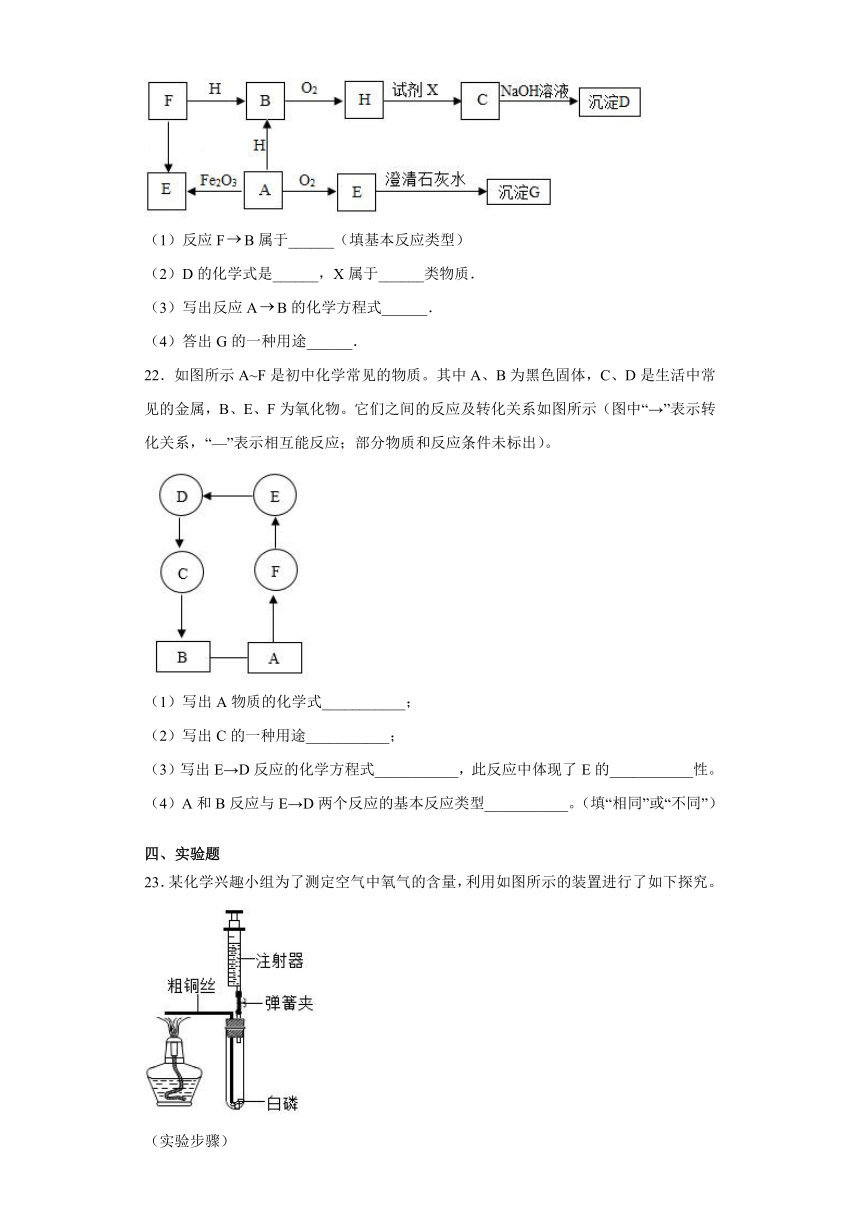
22.如图所示A~F是初中化学常见的物质。其中A、B为黑色固体,C、D是生活中常见的金属,B、E、F为氧化物。它们之间的反应及转化关系如图所示(图中“→”表示转化关系,“—”表示相互能反应;部分物质和反应条件未标出)。
(1)写出A物质的化学式___________;
(2)写出C的一种用途___________;
(3)写出E→D反应的化学方程式___________,此反应中体现了E的___________性。
(4)A和B反应与E→D两个反应的基本反应类型___________。(填“相同”或“不同”)
四、实验题
23.某化学兴趣小组为了测定空气中氧气的含量,利用如图所示的装置进行了如下探究。
(实验步骤)
①测量试管的容积为50mL;②检查装置的气密性良好;③装药品,将注射器活塞调整到合适位置,连接好仪器;④用弹簧夹夹紧胶皮管,加热粗铜丝,观察现象;⑤燃烧结束,试管冷却到室温后打开弹簧夹,观察注射器活塞的移动情况。
(反思与交流)
(1)实验中利用了铜丝的___________性。
(2)试管中发生反应的文字表达式(或符号表达式或化学方程式)是___________;
(3)步骤③中注射器活塞至少应调到___________mL处(填整数)。
(4)该实验装置的优点是:___________。
(5)该实验中能否使用硫粉燃烧来测定氧气含量?请写出你的看法及理由___________ 。
24.根据下图所示的实验回答问题
A.木炭在氧气中燃烧
B.证明蜡烛中含有氢元素
C.探究铁生锈的条件
(1)实验A中为了使木炭与氧气充分接触发生反应,木炭插入瓶内的具体操作是______;
(2)实验B中证明蜡烛中含有氢元素的理论依据是______;
(3)探究铁生锈条件的实验中,所用蒸馏水要预先煮沸,其目的是______。
五、计算题
25.实验室用20g含氧化铁80%的赤铁矿石进行炼铁,理论上可炼出纯铁的质量是多少?
26..现在用200吨含氧化铁80%的赤铁矿石进行炼铁,能炼出含杂质为4%的生铁多少吨?(保留一位小数)
参考答案
1.A 2.C 3.C 4.B 5.C 6.C 7.B 8.D 9.C 10.A 11.D 12.C 13.A 14.B 15.C
16.(1) 元素 贫血症
(2)隔绝空气(氧气)
(3)合金
(4) 12:1 有机物
17.(1)He
(2)+3
(3)
18.(1)Ca
(2)略
(3)略
(4)+5
(5)或
19.(1) 4He
(2) 8 氧原子
(3) 17 +1 不是
20.(1)Fe>Sn>Cu>Ag>Au
(2)化学性质稳定
(3)
(4)AD
21.(1)置换反应
(2) Cu(OH)2 酸
(3)
(4)做建筑材料
22.C 电线、电缆、电器、子弹、炮弹等(合理即可) 还原 不同
23.(1)导热
(2)
(3)10
(4)实验误差小,减少空气污染
(5)不能,因为硫燃烧会产生二氧化硫气体,影响实验结果
24.(1)自上而下缓慢插入
(2)质量守恒定律,反应前后的元素种类不变
(3)除去水中溶有的氧气
25.解:样品为20g,赤铁矿含80%氧化铁,则其中铁元素质量=
所以理论上20g赤铁矿可提炼出11.2g铁。
答:理论上可炼出纯铁的质量是11.2g。
26.解:赤铁矿石中铁元素的质量=200吨×80%× ×100%=112吨
炼出含杂质为4%的生铁的质量=112吨÷(1 4%)≈116.7吨
答:能炼出含杂质为4%的生铁的质量为116.7吨。
一、单选题
1.物质性质决定用途。下列说法不正确的是
A.氧气能支持燃烧,用于做火箭的燃料 B.金刚石硬度大,用于切割玻璃
C.铜具有良好的导电性,用于做导线 D.氢气有可燃性,用于高能燃料
2.下列关于资源、能源的叙述错误的是
A.废旧金属的回收利用,不但可以节约金属资源,还可以减少对环境的污染
B.空气是人类生产活动的重要资源
C.海洋是地球上巨大的资源宝库,海水中含有80多种化学物质
D.地球表面约71%被水覆盖,其中绝大多数是海洋水
3.下列物质的用途主要由其化学性质决定的是
A.铜丝作导线 B.液氮作增雨剂
C.氮气作保护气 D.稀有气体作霓虹灯
4.推理是一种重要的研究和学习方法,下列推理正确的是
A.铁丝能在氧气中燃烧,空气中含有氧气,所以铁丝也能在空气中燃烧
B.化合物由不同种元素组成,但不同种元素组成的物质不一定是化合物
C.单质是由同种元素组成的,则由同种元素组成的物质都是单质
D.铁、铝、铜等金属都是固体,则所有的金属都是固态物质
5.下列物质中,不能由金属单质和盐酸直接反应生成的是
A.ZnCl2 B.AlCl3 C.FeCl3 D.MgCl2
6.氧气的化学性质活泼,下列物质与氧气反应的现象描述不正确的是
A.镁条在空气中燃烧:发出耀眼的白光,生成白色固体粉末
B.细铁丝在氧气中燃烧:火星四射,生成黑色固体
C.木炭在氧气中燃烧:发出耀眼的白光,放出大量的热,生成二氧化碳气体
D.在空气中加热铜粉:红色固体粉末逐渐变成黑色
7.下列实验现象描述不正确的是
A.红磷在空气中燃烧,产生大量白烟
B.黄铜和纯铜相互刻划,黄铜表面留有划痕
C.细铁丝在氧气中燃烧,火星四射,生成黑色固体
D.镁在空气中燃烧,发出耀眼的白光,生成一种白色固体
8.下列说法错误的是
A.空气中的氧气与水中溶解的氧气化学性质同样活泼
B.工业上可以利用分离液态空气法制取氧气
C.氧气可以支持燃烧,说明氧气具有助燃性
D.生铁、紫铜、氧化镁都属于金属材料
9.鉴别下列各物质的方法,正确的是
需鉴别的物质 方法
A 吸入的气体和呼出的气体 观察颜色
B 氧气和空气 闻气味
C 铁粉和炭粉 用磁铁
D 氮气与二氧化碳 燃着的木条
A.A B.B C.C D.D
10.下列关于“物质一用途一性质”的说法不正确的是
A.氧气一火箭发射一可燃性 B.铜一做导线一导电性好
C.氮气一食品防腐一常温下化学性质稳定 D.氦气一填充飞艇一密度小
11.下列生活中的变化属于物理变化的是
A.花生霉变 B.木材燃烧 C.钢铁生锈 D.水果榨汁
12.为验证甲、乙、丙三种金属的活动性顺序,把三种金属分别放入稀盐酸中,只有乙表面无明显变化,把甲放入丙的硝酸盐溶液中,甲的表面有丙析出,则甲、乙、丙三种金属的活动性顺序由强到弱的是
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.丙>乙>甲
13.在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图,有关说法正确的是
A.该反应属于置换反应
B.该反应的生成物都是化合物
C.反应前后各元素的化合价都发生了改变
D.参加反应的A与B的分子个数比为1︰1
14.如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是
A.图中有两种氧化物 B.生成单质与化合物的质量比为7:22
C.生成物的分子个数比为1:1 D.该反应为置换反应
15.在装有下列固体的烧杯中,加入足量的稀盐酸,烧杯中最后只得到无色溶液的是
A.Fe2O3 B.Fe C.Mg D.AgNO3
二、填空题
16.“家”是一个化学小世界,蕴含丰富的化学知识,请回答下列问题。
(1)小红的妈妈做她最爱吃的“红烧肉”时加入了“加铁酱油”,其中“加铁酱油”中的“铁”指_____(填“元素”或“原子”),身体一旦缺铁可能患有的疾病是_______。
(2)做饭时油锅突然起火,妈妈采用了立即盖上锅盖的方法灭火,灭火的原理是_______。
(3)烧菜时用到了不锈钢锅,不锈钢属于_______。(填“合成材料”或“合金”)
(4)碳酸饮料中常加入防腐剂——苯甲酸(C6H5COOH),其碳、氢元素的质量比为_______,该防腐剂属于_______(填“有机物”或“无机物”)。
17.请用化学用语回答下列问题。
(1)生活中常用氢气或氦气填充气球,但氢气球容易爆炸, 氦气球则相对安全,应用较广。氦气的化学式为______。
(2)“喝酒不开车,开车不喝酒”。交警使用的酒精检测器里盛放经过酸化处理的含强氧化剂三氧化铬(CrO3)的硅胶。如果司机喝过酒,呼出气体中含有的乙醇蒸气将CrO3还原成硫酸铬[Cr2(SO4)3],检测器就会由暗红色变成蓝绿色。硫酸铬中铬元素的化合价为______。
(3)铝的化学性质很活泼,但在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为______。
18.化学物质及其变化同日常生活密切相关,请据所学知识回答下列问题。
(1)人体缺_______(填元素符号)元素能导致佝偻病或骨质疏松。
(2)空气中主要气体之一,化学性质不活泼,可充入食品包装防腐是_______。
(3)铁锅常用作炊具,是因为铁具有良好的_______性。(填一种物理性质)
(4)某品牌加碘盐中添加的是碘酸钾(KIO3),KIO3中碘元素的化合价是_______。
(5)建筑工地上盛有石灰水的水池中,常会看到一层白膜覆盖在石灰水的水面上,形成白膜的反应符号(或文字)表达式是:_______。
19.依据所学知识回答问题
(1)请用化学符号填空:
①4个氦原子:_______;
②标出KClO3中氯元素的化合价:_______;
(2)氧离子的结构示意图为,一个氧离子中有____个质子。氧离子失去2个电子变成_____。
(3)下图是自来水消毒过程中发生反应的示意图,产物D具有杀菌消毒作用。
①氯原子的原子序数为_______。
②D物质中氯元素的化合价为_______。
③该反应_______ (填“是”或“不是”)置换反应。
20.人们经常说的“五金”是指金、银、铜、铁、锡。
(1)“五金”的金属活动性由强到弱的顺序是______(用元素符号表示)。
(2)“真金不怕火炼”说明金具有的性质特征是______。
(3)写出铜与硝酸银溶液反应的化学方程式______。
(4)已知锡在化合物中为+2价,判断下列有关锡的置换反应中不正确的是______(填字母)。
A.Ca+SnCl2=CaCl2+Sn B.Sn+H2SO4=SnSO4+H2↑
C.Sn+Hg(NO3)2=Sn(NO3)2+Hg D.Sn+ZnSO4=SnSO4+Zn
三、推断题
21.A-H都是初中常见的物质,其中D为蓝色沉淀,A,E是组成元素相同的两种气体,F、H为黑色固体,他们之间转换关系如图(反应条件及部分反应物和生成物已略去)。
(1)反应FB属于______(填基本反应类型)
(2)D的化学式是______,X属于______类物质.
(3)写出反应AB的化学方程式______.
(4)答出G的一种用途______.
22.如图所示A~F是初中化学常见的物质。其中A、B为黑色固体,C、D是生活中常见的金属,B、E、F为氧化物。它们之间的反应及转化关系如图所示(图中“→”表示转化关系,“—”表示相互能反应;部分物质和反应条件未标出)。
(1)写出A物质的化学式___________;
(2)写出C的一种用途___________;
(3)写出E→D反应的化学方程式___________,此反应中体现了E的___________性。
(4)A和B反应与E→D两个反应的基本反应类型___________。(填“相同”或“不同”)
四、实验题
23.某化学兴趣小组为了测定空气中氧气的含量,利用如图所示的装置进行了如下探究。
(实验步骤)
①测量试管的容积为50mL;②检查装置的气密性良好;③装药品,将注射器活塞调整到合适位置,连接好仪器;④用弹簧夹夹紧胶皮管,加热粗铜丝,观察现象;⑤燃烧结束,试管冷却到室温后打开弹簧夹,观察注射器活塞的移动情况。
(反思与交流)
(1)实验中利用了铜丝的___________性。
(2)试管中发生反应的文字表达式(或符号表达式或化学方程式)是___________;
(3)步骤③中注射器活塞至少应调到___________mL处(填整数)。
(4)该实验装置的优点是:___________。
(5)该实验中能否使用硫粉燃烧来测定氧气含量?请写出你的看法及理由___________ 。
24.根据下图所示的实验回答问题
A.木炭在氧气中燃烧
B.证明蜡烛中含有氢元素
C.探究铁生锈的条件
(1)实验A中为了使木炭与氧气充分接触发生反应,木炭插入瓶内的具体操作是______;
(2)实验B中证明蜡烛中含有氢元素的理论依据是______;
(3)探究铁生锈条件的实验中,所用蒸馏水要预先煮沸,其目的是______。
五、计算题
25.实验室用20g含氧化铁80%的赤铁矿石进行炼铁,理论上可炼出纯铁的质量是多少?
26..现在用200吨含氧化铁80%的赤铁矿石进行炼铁,能炼出含杂质为4%的生铁多少吨?(保留一位小数)
参考答案
1.A 2.C 3.C 4.B 5.C 6.C 7.B 8.D 9.C 10.A 11.D 12.C 13.A 14.B 15.C
16.(1) 元素 贫血症
(2)隔绝空气(氧气)
(3)合金
(4) 12:1 有机物
17.(1)He
(2)+3
(3)
18.(1)Ca
(2)略
(3)略
(4)+5
(5)或
19.(1) 4He
(2) 8 氧原子
(3) 17 +1 不是
20.(1)Fe>Sn>Cu>Ag>Au
(2)化学性质稳定
(3)
(4)AD
21.(1)置换反应
(2) Cu(OH)2 酸
(3)
(4)做建筑材料
22.C 电线、电缆、电器、子弹、炮弹等(合理即可) 还原 不同
23.(1)导热
(2)
(3)10
(4)实验误差小,减少空气污染
(5)不能,因为硫燃烧会产生二氧化硫气体,影响实验结果
24.(1)自上而下缓慢插入
(2)质量守恒定律,反应前后的元素种类不变
(3)除去水中溶有的氧气
25.解:样品为20g,赤铁矿含80%氧化铁,则其中铁元素质量=
所以理论上20g赤铁矿可提炼出11.2g铁。
答:理论上可炼出纯铁的质量是11.2g。
26.解:赤铁矿石中铁元素的质量=200吨×80%× ×100%=112吨
炼出含杂质为4%的生铁的质量=112吨÷(1 4%)≈116.7吨
答:能炼出含杂质为4%的生铁的质量为116.7吨。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
