第八单元课题2第1课时金属与氧气、盐酸、稀硫酸的反应同步作业 —2020-2021学年九年级化学人教版下册(含解析)
文档属性
| 名称 | 第八单元课题2第1课时金属与氧气、盐酸、稀硫酸的反应同步作业 —2020-2021学年九年级化学人教版下册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 199.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-29 00:00:00 | ||
图片预览


文档简介
课题2 金属的化学性质
第1课时 金属与氧气、盐酸、稀硫酸的反应
知识点 1 金属与氧气的反应
1.生活中常见的铝制器皿不易被腐蚀,原因是 ( )
A.铝的硬度大
B.铝的密度小
C.铝的化学性质稳定,不易与其他物质发生反应
D.铝在常温下易与氧气反应生成致密的氧化膜
2.下列关于金属与氧气反应的说法中正确的是( )
A.金属都能与氧气反应
B.红热的细铁丝能在空气中剧烈燃烧
C.金属与氧气反应的难易和剧烈程度不同,说明金属的活泼性不同
D.真金不怕火炼,说明金的熔点高
3.写出下列反应的化学方程式。
(1)镁带在氧气中燃烧: 。
(2)铝在常温下与氧气反应: 。
(3)铁丝在氧气中燃烧: 。
(4)铜片在空气中灼烧: 。
知识点 2 金属与盐酸、稀硫酸的反应
4.如图所示,在装有镁条的试管中加入足量的稀盐酸,下列现象不正确的是 ( )
A.有气泡产生
B.镁条逐渐溶解
C.试管发热
D.液体变为浅绿色
5.在盛有少量镁、锌、铁、铜的试管中分别加入5 mL稀盐酸。下列说法不正确的是 ( )
A.镁、锌、铁都能与稀盐酸反应
B.与稀盐酸反应的剧烈程度为镁>铁>锌
C.铜的表面无现象,说明铜与稀盐酸不反应
D.将稀盐酸换为稀硫酸,现象相同
6.下列有关金属与酸反应的说法不正确的是 ( )
A.Mg、Zn、Fe能与酸反应产生氢气,Cu不能
B.Mg、Zn、Fe属于活泼金属,Cu属于不活泼金属
C.Mg、Zn、Fe的金属活动性比Cu强
D.不能通过金属能否与酸反应产生氢气比较金属的活动性
知识点 3 置换反应
7.下列反应不属于置换反应的是 ( )
A.H2+CuOCu+H2O
B.CO+CuOCu+CO2
C.C+2CuO2Cu+CO2↑
D.Fe+CuSO4FeSO4+Cu
8.海带中富含碘元素,可利用反应2NaI+Cl22NaCl+I2从海带中提取碘单质。此反应属于( )
A.化合反应 B.置换反应
C.分解反应 D.以上都不是
9.欲鉴别金光闪闪的假金元宝(含铜和锌的合金),你认为下列方法不可行的是 ( )
A.用火烧 B.加入稀硫酸
C.测密度 D. 看颜色
10.下列物质中,不能由金属和盐酸直接反应得到的是 ( )
A.FeCl2 B.CuCl2
C.MgCl2 D.ZnCl2
11.将少量的生铁粉末加入足量稀硫酸中,下列叙述正确的是 ( )
①有气泡冒出 ②液体变为浅绿色 ③粉末全部消失 ④液体质量减少 ⑤留有少量黑色残渣
A.①②③ B.①②④
C.①②⑤ D.①④⑤
12.下列金属各30 g分别与足量的稀盐酸反应,生成氢气质量最多的是 ( )
A.Al B.Fe
C.Zn D.Mg
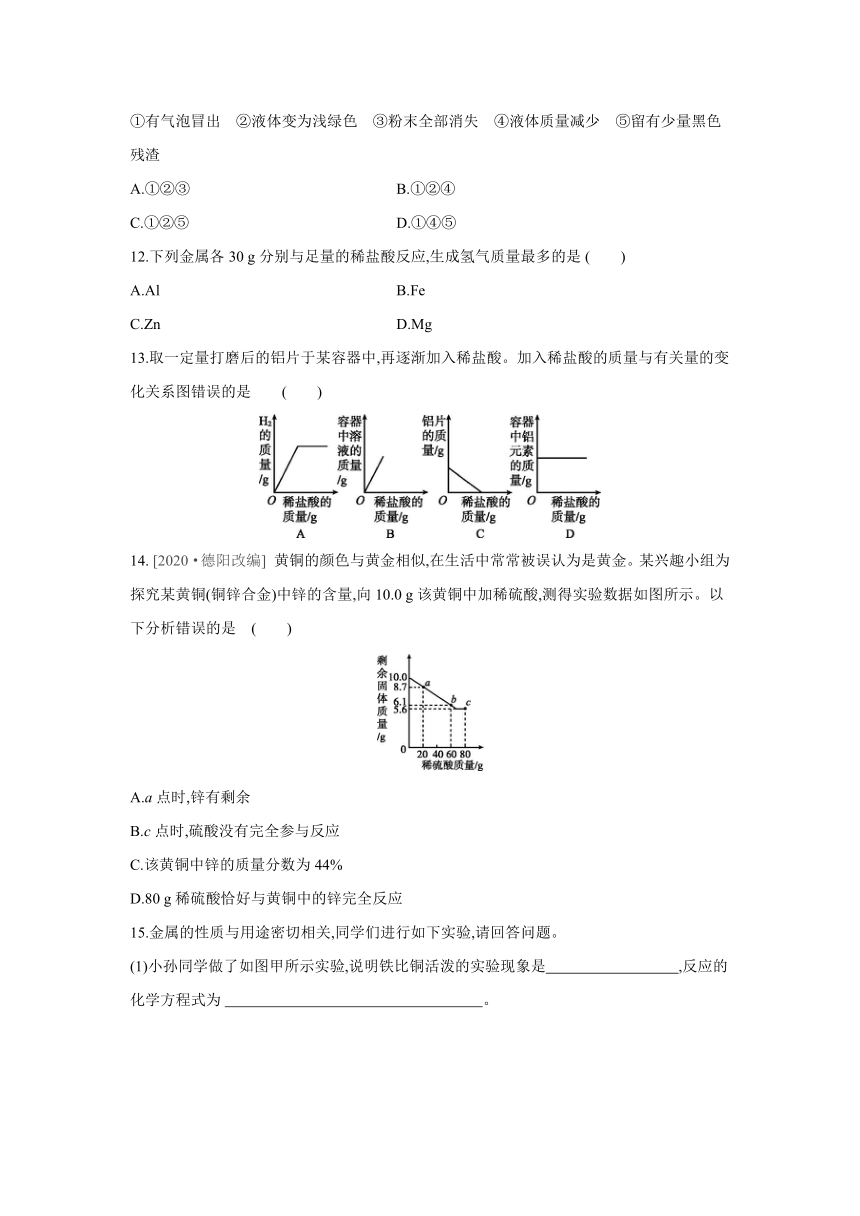
13.取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。加入稀盐酸的质量与有关量的变化关系图错误的是 ( )
14. [2020·德阳改编] 黄铜的颜色与黄金相似,在生活中常常被误认为是黄金。某兴趣小组为探究某黄铜(铜锌合金)中锌的含量,向10.0 g该黄铜中加稀硫酸,测得实验数据如图所示。以下分析错误的是 ( )
A.a点时,锌有剩余
B.c点时,硫酸没有完全参与反应
C.该黄铜中锌的质量分数为44%
D.80 g稀硫酸恰好与黄铜中的锌完全反应
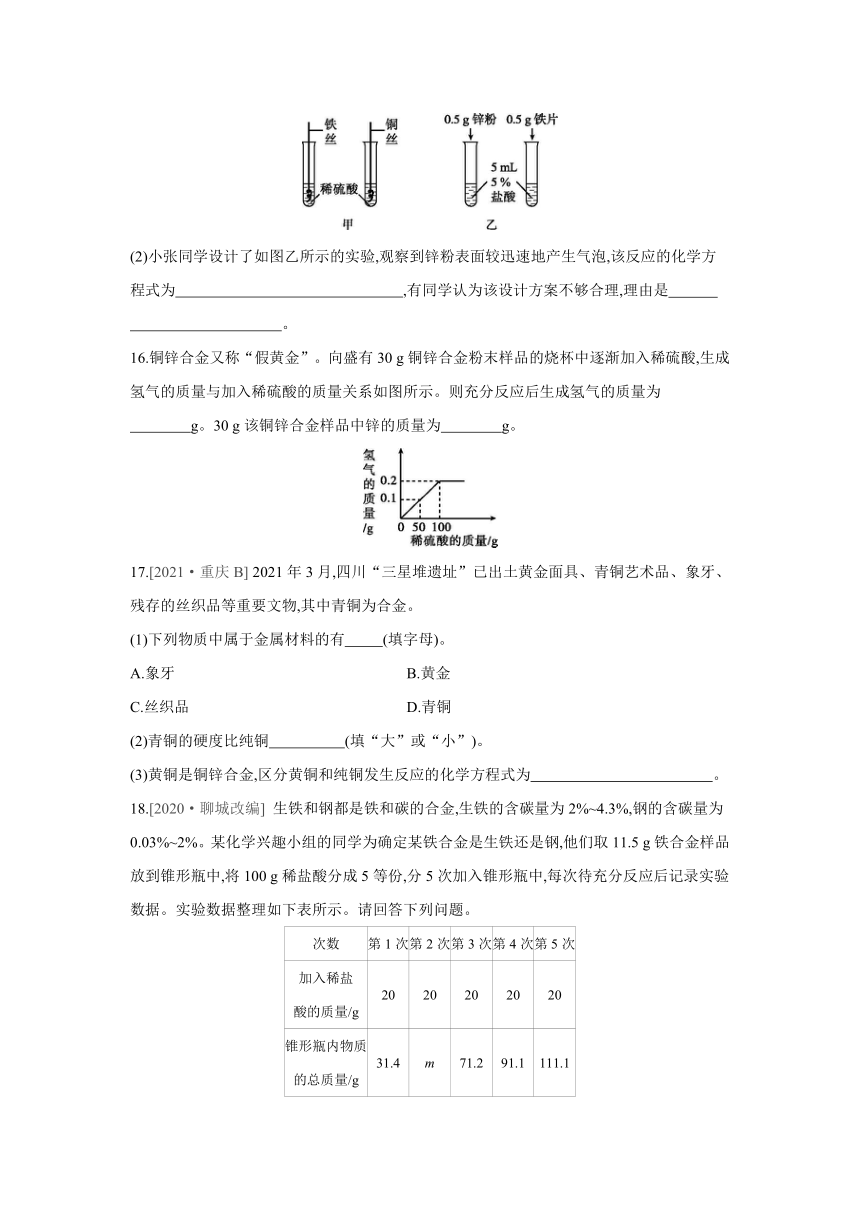
15.金属的性质与用途密切相关,同学们进行如下实验,请回答问题。
(1)小孙同学做了如图甲所示实验,说明铁比铜活泼的实验现象是 ,反应的化学方程式为 。
(2)小张同学设计了如图乙所示的实验,观察到锌粉表面较迅速地产生气泡,该反应的化学方程式为 ,有同学认为该设计方案不够合理,理由是
。
16.铜锌合金又称“假黄金”。向盛有30 g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示。则充分反应后生成氢气的质量为
g。30 g该铜锌合金样品中锌的质量为 g。
17.[2021·重庆B] 2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有 (填字母)。
A.象牙 B.黄金
C.丝织品 D.青铜
(2)青铜的硬度比纯铜 (填“大”或“小”)。
(3)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为 。
18.[2020·聊城改编] 生铁和钢都是铁和碳的合金,生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。某化学兴趣小组的同学为确定某铁合金是生铁还是钢,他们取11.5 g铁合金样品放到锥形瓶中,将100 g稀盐酸分成5等份,分5次加入锥形瓶中,每次待充分反应后记录实验数据。实验数据整理如下表所示。请回答下列问题。
次数 第1次 第2次 第3次 第4次 第5次
加入稀盐 酸的质量/g 20 20 20 20 20
锥形瓶内物质 的总质量/g 31.4 m 71.2 91.1 111.1
[查阅资料] 碳不与稀盐酸反应。
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果精确到0.1%)。
1.D 2.C
3.(1)2Mg+O22MgO
(2)4Al+3O22Al2O3
(3)3Fe+2O2Fe3O4
(4)2Cu+O22CuO
4.D
5.B [解析] 镁、锌、铁与稀盐酸反应的剧烈程度为镁>锌>铁。
6.D
7.B [解析] 置换反应是指由一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。B选项的两种反应物都为化合物,不属于置换反应。
8.B 9.D 10.B
11.C [解析] 生铁是含少量碳的铁合金,将其加入足量稀硫酸中,铁与稀硫酸反应,碳不与稀硫酸反应,所以有气泡冒出,粉末大部分消失,液体变为浅绿色,液体质量增加,有部分黑色粉末残留。
12.A 13.B
14.D [解析] 铜不与稀硫酸反应,锌与稀硫酸反应生成硫酸锌和氢气,向黄铜中加入稀硫酸,固体质量不断减少,直至锌完全反应,固体质量不再改变。a点时,只有部分锌与硫酸反应,样品中还有锌;c点时加入的硫酸过量,即硫酸没有完全参与反应;由图可知,10.0 g样品中铜的质量为5.6 g,所以样品中锌的质量为10.0 g-5.6 g=4.4 g,因此样品中锌的质量分数为× 100%= 44%;根据图可知,黄铜中的锌并不能完全消耗80 g稀硫酸。
15.(1)铁丝表面有气泡产生,铜丝表面无明显现象
Fe+H2SO4FeSO4+H2↑
(2)Zn+2HClZnCl2+H2↑ 金属与酸的接触面积不同
16.0.2 6.5
[解析] 由图像可知,反应生成氢气的质量为0.2 g,设30 g 该铜锌合金样品中锌的质量为x。
Zn+H2SO4ZnSO4+H2↑
65 2
x 0.2 g
=
x=6.5 g
17.(1)BD
(2)大
(3)Zn+H2SO4ZnSO4+H2↑(合理即可)
[解析] (3)黄铜是铜锌合金,锌能够与酸反应,铜不能与酸反应,区分黄铜和纯铜发生反应的化学方程式为Zn+H2SO4ZnSO4+H2↑或Zn+2HClZnCl2+H2↑。
18.(1)0.4 g
(2)51.3
(3)解:设11.5 g铁合金中铁的质量为x。
Fe+2HClFeCl2+H2↑
56 2
x 0.4 g
= x=11.2 g
该铁合金中含碳量为×100%=2.6%。
2%<2.6%<4.3%,所以该铁合金是生铁。
答:该铁合金是生铁。
第1课时 金属与氧气、盐酸、稀硫酸的反应
知识点 1 金属与氧气的反应
1.生活中常见的铝制器皿不易被腐蚀,原因是 ( )
A.铝的硬度大
B.铝的密度小
C.铝的化学性质稳定,不易与其他物质发生反应
D.铝在常温下易与氧气反应生成致密的氧化膜
2.下列关于金属与氧气反应的说法中正确的是( )
A.金属都能与氧气反应
B.红热的细铁丝能在空气中剧烈燃烧
C.金属与氧气反应的难易和剧烈程度不同,说明金属的活泼性不同
D.真金不怕火炼,说明金的熔点高
3.写出下列反应的化学方程式。
(1)镁带在氧气中燃烧: 。
(2)铝在常温下与氧气反应: 。
(3)铁丝在氧气中燃烧: 。
(4)铜片在空气中灼烧: 。
知识点 2 金属与盐酸、稀硫酸的反应
4.如图所示,在装有镁条的试管中加入足量的稀盐酸,下列现象不正确的是 ( )
A.有气泡产生
B.镁条逐渐溶解
C.试管发热
D.液体变为浅绿色
5.在盛有少量镁、锌、铁、铜的试管中分别加入5 mL稀盐酸。下列说法不正确的是 ( )
A.镁、锌、铁都能与稀盐酸反应
B.与稀盐酸反应的剧烈程度为镁>铁>锌
C.铜的表面无现象,说明铜与稀盐酸不反应
D.将稀盐酸换为稀硫酸,现象相同
6.下列有关金属与酸反应的说法不正确的是 ( )
A.Mg、Zn、Fe能与酸反应产生氢气,Cu不能
B.Mg、Zn、Fe属于活泼金属,Cu属于不活泼金属
C.Mg、Zn、Fe的金属活动性比Cu强
D.不能通过金属能否与酸反应产生氢气比较金属的活动性
知识点 3 置换反应
7.下列反应不属于置换反应的是 ( )
A.H2+CuOCu+H2O
B.CO+CuOCu+CO2
C.C+2CuO2Cu+CO2↑
D.Fe+CuSO4FeSO4+Cu
8.海带中富含碘元素,可利用反应2NaI+Cl22NaCl+I2从海带中提取碘单质。此反应属于( )
A.化合反应 B.置换反应
C.分解反应 D.以上都不是
9.欲鉴别金光闪闪的假金元宝(含铜和锌的合金),你认为下列方法不可行的是 ( )
A.用火烧 B.加入稀硫酸
C.测密度 D. 看颜色
10.下列物质中,不能由金属和盐酸直接反应得到的是 ( )
A.FeCl2 B.CuCl2
C.MgCl2 D.ZnCl2
11.将少量的生铁粉末加入足量稀硫酸中,下列叙述正确的是 ( )
①有气泡冒出 ②液体变为浅绿色 ③粉末全部消失 ④液体质量减少 ⑤留有少量黑色残渣
A.①②③ B.①②④
C.①②⑤ D.①④⑤
12.下列金属各30 g分别与足量的稀盐酸反应,生成氢气质量最多的是 ( )
A.Al B.Fe
C.Zn D.Mg
13.取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。加入稀盐酸的质量与有关量的变化关系图错误的是 ( )
14. [2020·德阳改编] 黄铜的颜色与黄金相似,在生活中常常被误认为是黄金。某兴趣小组为探究某黄铜(铜锌合金)中锌的含量,向10.0 g该黄铜中加稀硫酸,测得实验数据如图所示。以下分析错误的是 ( )
A.a点时,锌有剩余
B.c点时,硫酸没有完全参与反应
C.该黄铜中锌的质量分数为44%
D.80 g稀硫酸恰好与黄铜中的锌完全反应
15.金属的性质与用途密切相关,同学们进行如下实验,请回答问题。
(1)小孙同学做了如图甲所示实验,说明铁比铜活泼的实验现象是 ,反应的化学方程式为 。
(2)小张同学设计了如图乙所示的实验,观察到锌粉表面较迅速地产生气泡,该反应的化学方程式为 ,有同学认为该设计方案不够合理,理由是
。
16.铜锌合金又称“假黄金”。向盛有30 g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示。则充分反应后生成氢气的质量为
g。30 g该铜锌合金样品中锌的质量为 g。
17.[2021·重庆B] 2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有 (填字母)。
A.象牙 B.黄金
C.丝织品 D.青铜
(2)青铜的硬度比纯铜 (填“大”或“小”)。
(3)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为 。
18.[2020·聊城改编] 生铁和钢都是铁和碳的合金,生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。某化学兴趣小组的同学为确定某铁合金是生铁还是钢,他们取11.5 g铁合金样品放到锥形瓶中,将100 g稀盐酸分成5等份,分5次加入锥形瓶中,每次待充分反应后记录实验数据。实验数据整理如下表所示。请回答下列问题。
次数 第1次 第2次 第3次 第4次 第5次
加入稀盐 酸的质量/g 20 20 20 20 20
锥形瓶内物质 的总质量/g 31.4 m 71.2 91.1 111.1
[查阅资料] 碳不与稀盐酸反应。
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果精确到0.1%)。
1.D 2.C
3.(1)2Mg+O22MgO
(2)4Al+3O22Al2O3
(3)3Fe+2O2Fe3O4
(4)2Cu+O22CuO
4.D
5.B [解析] 镁、锌、铁与稀盐酸反应的剧烈程度为镁>锌>铁。
6.D
7.B [解析] 置换反应是指由一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。B选项的两种反应物都为化合物,不属于置换反应。
8.B 9.D 10.B
11.C [解析] 生铁是含少量碳的铁合金,将其加入足量稀硫酸中,铁与稀硫酸反应,碳不与稀硫酸反应,所以有气泡冒出,粉末大部分消失,液体变为浅绿色,液体质量增加,有部分黑色粉末残留。
12.A 13.B
14.D [解析] 铜不与稀硫酸反应,锌与稀硫酸反应生成硫酸锌和氢气,向黄铜中加入稀硫酸,固体质量不断减少,直至锌完全反应,固体质量不再改变。a点时,只有部分锌与硫酸反应,样品中还有锌;c点时加入的硫酸过量,即硫酸没有完全参与反应;由图可知,10.0 g样品中铜的质量为5.6 g,所以样品中锌的质量为10.0 g-5.6 g=4.4 g,因此样品中锌的质量分数为× 100%= 44%;根据图可知,黄铜中的锌并不能完全消耗80 g稀硫酸。
15.(1)铁丝表面有气泡产生,铜丝表面无明显现象
Fe+H2SO4FeSO4+H2↑
(2)Zn+2HClZnCl2+H2↑ 金属与酸的接触面积不同
16.0.2 6.5
[解析] 由图像可知,反应生成氢气的质量为0.2 g,设30 g 该铜锌合金样品中锌的质量为x。
Zn+H2SO4ZnSO4+H2↑
65 2
x 0.2 g
=
x=6.5 g
17.(1)BD
(2)大
(3)Zn+H2SO4ZnSO4+H2↑(合理即可)
[解析] (3)黄铜是铜锌合金,锌能够与酸反应,铜不能与酸反应,区分黄铜和纯铜发生反应的化学方程式为Zn+H2SO4ZnSO4+H2↑或Zn+2HClZnCl2+H2↑。
18.(1)0.4 g
(2)51.3
(3)解:设11.5 g铁合金中铁的质量为x。
Fe+2HClFeCl2+H2↑
56 2
x 0.4 g
= x=11.2 g
该铁合金中含碳量为×100%=2.6%。
2%<2.6%<4.3%,所以该铁合金是生铁。
答:该铁合金是生铁。
同课章节目录
