中考化学实验专题复习
图片预览




文档简介
(共31张PPT)
中考化学实验专题复习
一、常见仪器的使用
二、化学实验基本操作
三、气体的制取、净化和检验
四、综合实验
第一课时
药匙
石棉网
蒸发皿
坩埚钳
锥形瓶
长颈漏斗
干燥管
漏斗
量筒
烧杯
胶头滴管
铁架台
试管
酒精灯
水槽
集气瓶
一、常见仪器的使用
三脚架
1、常用作少量物质的反应容器,或给少量液体或固体加热的仪器是 。
2、搅拌、过滤、蘸取液体时常用 。
3、向NaOH溶液中逐滴滴入盐酸 。
4、收集或贮存少量气体 。
5、取粉末状药品 。
6、溶液蒸发、浓缩和结晶 。
7、量取80mL的盐酸 。
选择合适的仪器填空:
试管
玻璃棒
胶头滴管
集气瓶
药匙或纸槽
蒸发皿
量筒
8、将锌粒加入试管 。
9、取18克NaCl固体 。
10、往酒精灯里添加酒精 。
11、盛硫磺在集气瓶中燃烧 。
12、拿到热的蒸发皿 。
13、使烧杯、烧瓶均匀受热 。
14、用于装配气体发生器,便于往装置中添加液体 。
15、给较大量加热,较大量物质反应容器,过滤中用于承接滤液 。
镊子
天平
漏斗
燃烧匙
坩埚钳
石棉网
长颈漏斗
烧杯
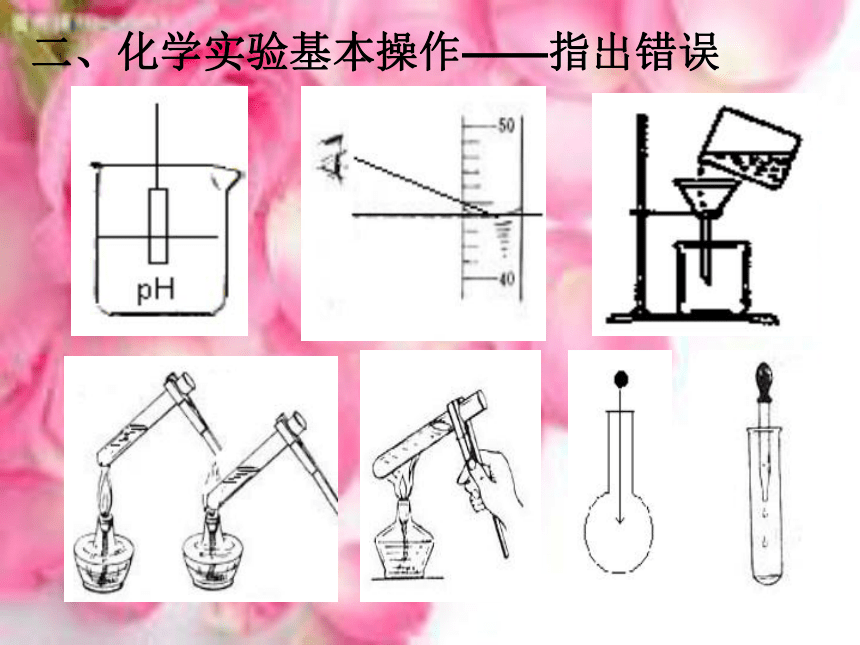
二、化学实验基本操作——指出错误
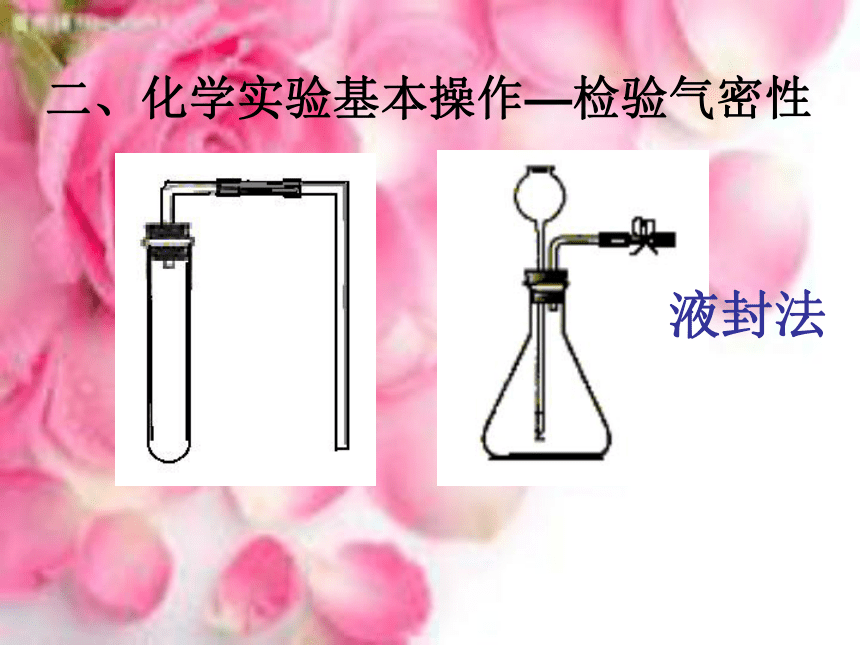
二、化学实验基本操作—检验气密性
液封法
1、气体的制取— ①发生装置
三、气体的制取、净化和检验
固体加热装置
固液不加热装置
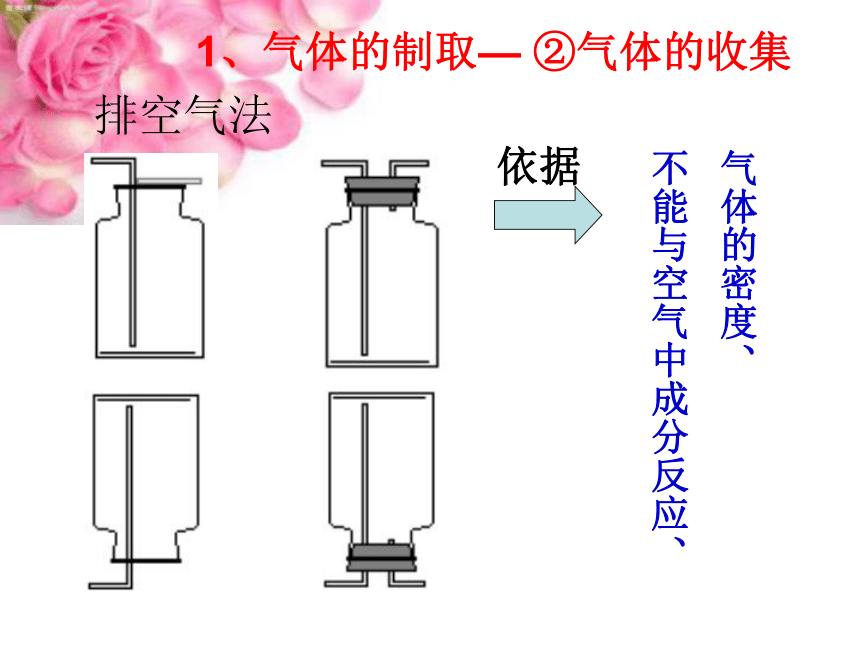
1、气体的制取— ②气体的收集
气体的密度、
不能与空气中成分反应、
依据
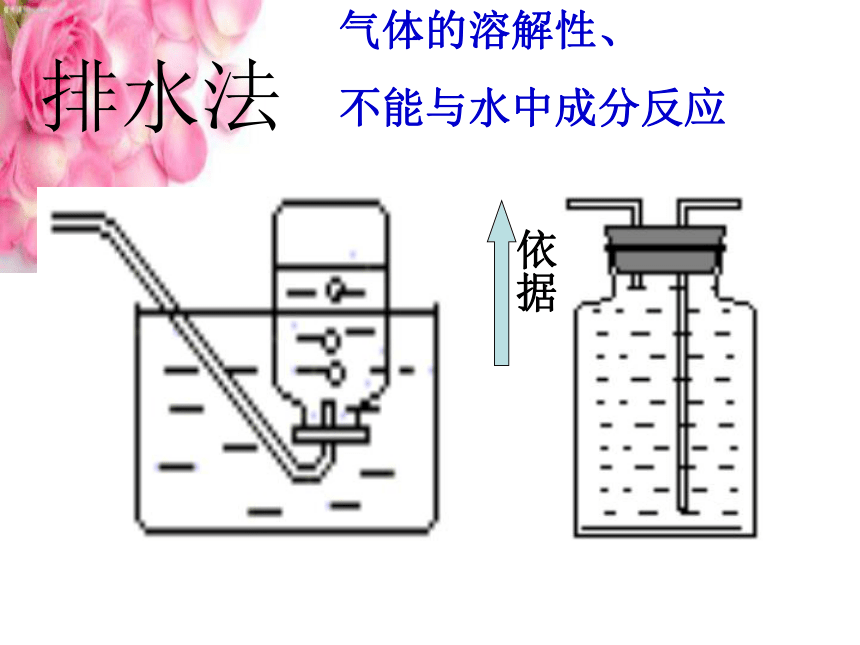
气体的溶解性、
不能与水中成分反应
依据
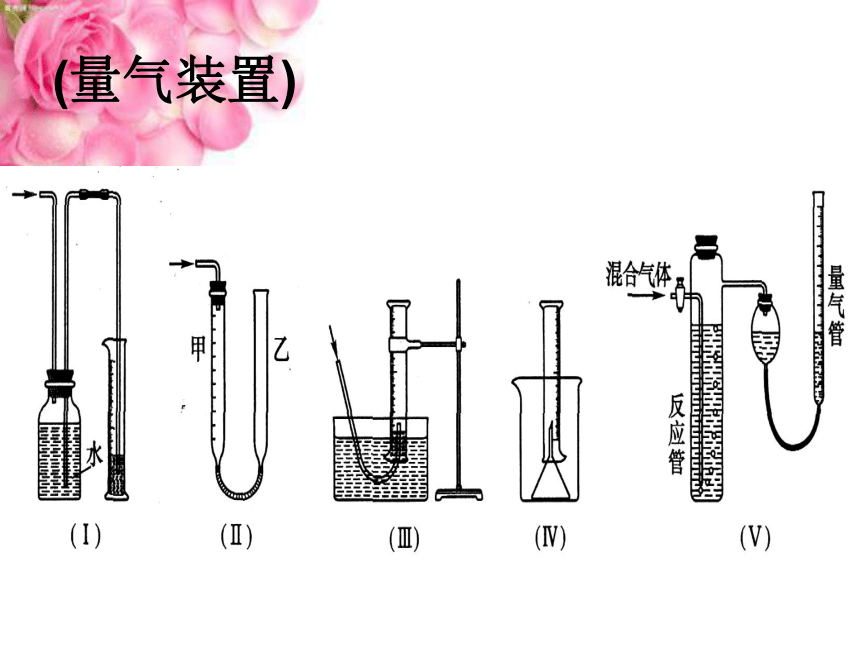
(量气装置)
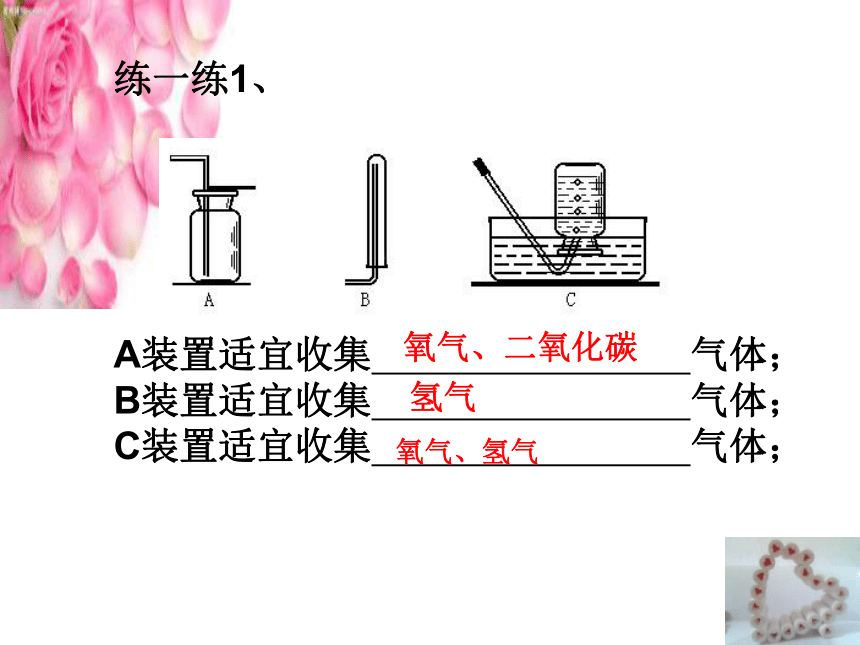
练一练1、
A装置适宜收集 气体;
B装置适宜收集 气体;
C装置适宜收集 气体;
氧气、二氧化碳
氢气
氧气、氢气
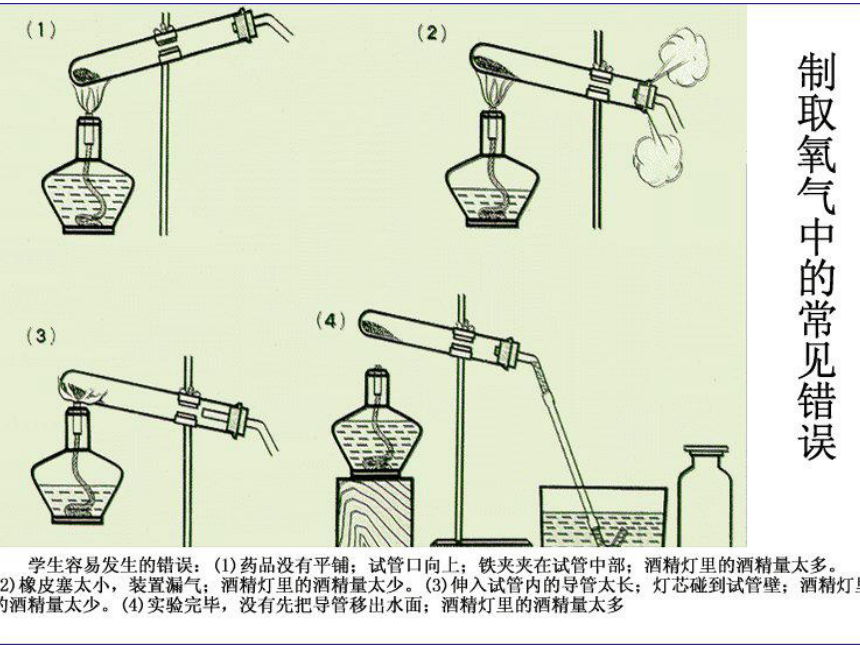
练一练2、指出图中存在的错误之处:
气体净化装置的设计原则:
根据净化药品的状态和净化条件
2、气体的净化及检验
选择原则
①气体在被干燥的过程中要不能被减少
②不要引入新的杂质。
(1)、常见干燥剂
可干燥气体 不可干燥气体
浓硫酸
碱石灰
无水氯化钙
H2、O2、CO、CO2、HCl
NH3
H2、O2、CO、NH3
CO2、HCl
H2、O2、CO、CO2
NH3
(2)、常用装置
球型干燥管
洗气瓶
燃烧管
U型干燥管
(3)、气体的检验
气体 方法或所加试剂 现象
O2
CO2
H2O
H2
CH4
带火星的木条
木条复燃
澄清石灰水
澄清石灰水变浑浊
无水CuSO4
无水CuSO4由白变蓝
点燃用干燥的烧杯罩在火焰上
有无色液滴生成
点燃用干燥的烧杯罩在火焰上
有无色液滴生成,并滴加澄清石灰水,变浑浊
气体的净化、转化与检验
实验目的 装置 所用药品
检验水蒸气
检验CO2气体
检验HCl气体
A
A
B
除去N2中的O2
将CO转化为CO2
将CO2转化为CO
B
无水硫酸铜
澄清石灰水
硝酸银溶液
NaOH溶液
饱和NaHCO3
碱石灰
C
C
C
木炭
A
A
除去CO2气体
除去氯化氢气体
铜丝
氧化铜
除去水、CO2
1)、 燃烧法
如CH4、H2、CO等。
2)、碱液吸收法
如Cl2、H2S、CO2、SO2、NO2等。
3)、水溶解法
如HCl、NH3等。
3、除尾气装置
4)、袋装储存法
NO等
练一练1、为了除去N2中混有的少量的CO2和水蒸气,两位同学将混合气体分别通过下面两个装置,最后得到的气体分别是什么?
N2和水蒸气
N2
用稀盐酸和锌粒反应制取氢气时,常常混有氯化氢、水蒸气等杂质。设计实验证明并除去杂质,取得纯净干燥的氢气。
无水硫酸铜
a
b
c
d
e
f
g
h
A
B
C
D
E
1、要制备纯净干燥的氢气,各仪器的连接顺序是(按接口字母)___________________
2、C装置中发生的现象是__________作用是__________
3、D装置中发生的现象是__________作用是____________
a→f →g →e →d →b →c →h
产生白色沉淀
检验并除去氯化氢气体
白色固体变蓝色
证明水蒸气存在并吸收水蒸气
练一练2:
为了验证某混合气体由H2、CO和HCl三种气体组成,请从下图中选择适当的装置设计一实验,并回答问题(假设每步均完全反应):
1、首先你想证明哪种气体是否存在?
2、装置连接的顺序是 。
3、 A装置在实验过程中玻璃管中现象
C-B-A-E-D
管壁有水珠产生,黑色变红色
练一练3
HCl气体
思考:
分析右图装置有哪些作用?
1、净化气体
2、收集气体(密度比空气大)
4、排水集气法收集气体
3、收集气体(密度比空气小)
四、综合实验
综合实验的主要内容:
①气体的制取、净化、性质的组合;
②混合气体成分的验证;
③定性实验和定量实验的结合;
例1、草酸(H2C2O4)是一种无色晶体,实验室用其加热制取CO气体:
H2C2O4 =CO↑+CO2 ↑ + H2O
①加热草酸制取CO的发生装置应选用与实验室制 (O2、H2、CO2)相同的装置
②要得到干燥纯净的CO,并用CO还原氧化铁,写出各装置正确连接顺序 。
③装置丙中NaOH的作用是 。
④尾气应如何处理 。
例2、为了验证某混合气体由H2、CO和HCl三种气体组成,请从下图中选择适当的装置设计一实验,并回答问题(假设每步均完全反应):
①装置连接的顺序是 。
②你所选 择的第一装置的作用 。
③最后一个装置中反应化学方程式 。
④A装置在实验过程中玻璃管中现象 。
⑤若省略第二个装置,不能验证的气体 。
例3、甲、乙两同学利用下面装置测定铜和氧化铜的混合物中铜元素的质量分数。回答问题:
①A中可观察到的现象 ,化学方程式 。
②B装置作用 ;C装置作用 。
③D装置中铜和氧化铜总质量为10克,充分反应后,E装置的质量增加1.8克,则原混合物中铜元素的质量分数为 。
④F装置的作用是吸收空气中的水,如果没有F装置,会使实验结果 (偏大、偏小)。
例4、现只有稀盐酸、浓硫酸和NaOH溶液。要用如图所示装置对H2和CO2的混合气体进行分离和干燥,则:
①甲中应盛 ,乙中应盛 ;
②首先打开活塞a,可分离出 ,反应化学方程式为 。
③再关闭活塞a,向b中加入稀盐酸,又可分离出 ,反应化学方程式 。
④b仪器为何要伸入液面下 。
5、双氧水常用于消毒,漂白,它是过氧化氢(H2O2)的水溶液。含H2O230%的水溶液以MnO2作催化剂,可迅速分解出O2和H2O,按下图装置可制取干燥纯净的氧气。
⑴ 写出用这种方法制取氧气的化学反应方程式。
⑵ 为了干燥生成的气体,B瓶中应装何种物质?
⑶ C装置中出现什么现象,表示气体已经干燥。
30%的H2O2
MnO2
无水CuSO4
A
B
C
6、有一不纯的氮气,其中混有氢气和水蒸气,现有下图所示A、B、C三种装置,要求证明氮气中混有这两种气体,并除去这两种气体,还能收集到纯净的干燥的氮气。
无水硫酸铜
C
氧化铜
B
浓H2SO4
A
中考化学实验专题复习
一、常见仪器的使用
二、化学实验基本操作
三、气体的制取、净化和检验
四、综合实验
第一课时
药匙
石棉网
蒸发皿
坩埚钳
锥形瓶
长颈漏斗
干燥管
漏斗
量筒
烧杯
胶头滴管
铁架台
试管
酒精灯
水槽
集气瓶
一、常见仪器的使用
三脚架
1、常用作少量物质的反应容器,或给少量液体或固体加热的仪器是 。
2、搅拌、过滤、蘸取液体时常用 。
3、向NaOH溶液中逐滴滴入盐酸 。
4、收集或贮存少量气体 。
5、取粉末状药品 。
6、溶液蒸发、浓缩和结晶 。
7、量取80mL的盐酸 。
选择合适的仪器填空:
试管
玻璃棒
胶头滴管
集气瓶
药匙或纸槽
蒸发皿
量筒
8、将锌粒加入试管 。
9、取18克NaCl固体 。
10、往酒精灯里添加酒精 。
11、盛硫磺在集气瓶中燃烧 。
12、拿到热的蒸发皿 。
13、使烧杯、烧瓶均匀受热 。
14、用于装配气体发生器,便于往装置中添加液体 。
15、给较大量加热,较大量物质反应容器,过滤中用于承接滤液 。
镊子
天平
漏斗
燃烧匙
坩埚钳
石棉网
长颈漏斗
烧杯
二、化学实验基本操作——指出错误
二、化学实验基本操作—检验气密性
液封法
1、气体的制取— ①发生装置
三、气体的制取、净化和检验
固体加热装置
固液不加热装置
1、气体的制取— ②气体的收集
气体的密度、
不能与空气中成分反应、
依据
气体的溶解性、
不能与水中成分反应
依据
(量气装置)
练一练1、
A装置适宜收集 气体;
B装置适宜收集 气体;
C装置适宜收集 气体;
氧气、二氧化碳
氢气
氧气、氢气
练一练2、指出图中存在的错误之处:
气体净化装置的设计原则:
根据净化药品的状态和净化条件
2、气体的净化及检验
选择原则
①气体在被干燥的过程中要不能被减少
②不要引入新的杂质。
(1)、常见干燥剂
可干燥气体 不可干燥气体
浓硫酸
碱石灰
无水氯化钙
H2、O2、CO、CO2、HCl
NH3
H2、O2、CO、NH3
CO2、HCl
H2、O2、CO、CO2
NH3
(2)、常用装置
球型干燥管
洗气瓶
燃烧管
U型干燥管
(3)、气体的检验
气体 方法或所加试剂 现象
O2
CO2
H2O
H2
CH4
带火星的木条
木条复燃
澄清石灰水
澄清石灰水变浑浊
无水CuSO4
无水CuSO4由白变蓝
点燃用干燥的烧杯罩在火焰上
有无色液滴生成
点燃用干燥的烧杯罩在火焰上
有无色液滴生成,并滴加澄清石灰水,变浑浊
气体的净化、转化与检验
实验目的 装置 所用药品
检验水蒸气
检验CO2气体
检验HCl气体
A
A
B
除去N2中的O2
将CO转化为CO2
将CO2转化为CO
B
无水硫酸铜
澄清石灰水
硝酸银溶液
NaOH溶液
饱和NaHCO3
碱石灰
C
C
C
木炭
A
A
除去CO2气体
除去氯化氢气体
铜丝
氧化铜
除去水、CO2
1)、 燃烧法
如CH4、H2、CO等。
2)、碱液吸收法
如Cl2、H2S、CO2、SO2、NO2等。
3)、水溶解法
如HCl、NH3等。
3、除尾气装置
4)、袋装储存法
NO等
练一练1、为了除去N2中混有的少量的CO2和水蒸气,两位同学将混合气体分别通过下面两个装置,最后得到的气体分别是什么?
N2和水蒸气
N2
用稀盐酸和锌粒反应制取氢气时,常常混有氯化氢、水蒸气等杂质。设计实验证明并除去杂质,取得纯净干燥的氢气。
无水硫酸铜
a
b
c
d
e
f
g
h
A
B
C
D
E
1、要制备纯净干燥的氢气,各仪器的连接顺序是(按接口字母)___________________
2、C装置中发生的现象是__________作用是__________
3、D装置中发生的现象是__________作用是____________
a→f →g →e →d →b →c →h
产生白色沉淀
检验并除去氯化氢气体
白色固体变蓝色
证明水蒸气存在并吸收水蒸气
练一练2:
为了验证某混合气体由H2、CO和HCl三种气体组成,请从下图中选择适当的装置设计一实验,并回答问题(假设每步均完全反应):
1、首先你想证明哪种气体是否存在?
2、装置连接的顺序是 。
3、 A装置在实验过程中玻璃管中现象
C-B-A-E-D
管壁有水珠产生,黑色变红色
练一练3
HCl气体
思考:
分析右图装置有哪些作用?
1、净化气体
2、收集气体(密度比空气大)
4、排水集气法收集气体
3、收集气体(密度比空气小)
四、综合实验
综合实验的主要内容:
①气体的制取、净化、性质的组合;
②混合气体成分的验证;
③定性实验和定量实验的结合;
例1、草酸(H2C2O4)是一种无色晶体,实验室用其加热制取CO气体:
H2C2O4 =CO↑+CO2 ↑ + H2O
①加热草酸制取CO的发生装置应选用与实验室制 (O2、H2、CO2)相同的装置
②要得到干燥纯净的CO,并用CO还原氧化铁,写出各装置正确连接顺序 。
③装置丙中NaOH的作用是 。
④尾气应如何处理 。
例2、为了验证某混合气体由H2、CO和HCl三种气体组成,请从下图中选择适当的装置设计一实验,并回答问题(假设每步均完全反应):
①装置连接的顺序是 。
②你所选 择的第一装置的作用 。
③最后一个装置中反应化学方程式 。
④A装置在实验过程中玻璃管中现象 。
⑤若省略第二个装置,不能验证的气体 。
例3、甲、乙两同学利用下面装置测定铜和氧化铜的混合物中铜元素的质量分数。回答问题:
①A中可观察到的现象 ,化学方程式 。
②B装置作用 ;C装置作用 。
③D装置中铜和氧化铜总质量为10克,充分反应后,E装置的质量增加1.8克,则原混合物中铜元素的质量分数为 。
④F装置的作用是吸收空气中的水,如果没有F装置,会使实验结果 (偏大、偏小)。
例4、现只有稀盐酸、浓硫酸和NaOH溶液。要用如图所示装置对H2和CO2的混合气体进行分离和干燥,则:
①甲中应盛 ,乙中应盛 ;
②首先打开活塞a,可分离出 ,反应化学方程式为 。
③再关闭活塞a,向b中加入稀盐酸,又可分离出 ,反应化学方程式 。
④b仪器为何要伸入液面下 。
5、双氧水常用于消毒,漂白,它是过氧化氢(H2O2)的水溶液。含H2O230%的水溶液以MnO2作催化剂,可迅速分解出O2和H2O,按下图装置可制取干燥纯净的氧气。
⑴ 写出用这种方法制取氧气的化学反应方程式。
⑵ 为了干燥生成的气体,B瓶中应装何种物质?
⑶ C装置中出现什么现象,表示气体已经干燥。
30%的H2O2
MnO2
无水CuSO4
A
B
C
6、有一不纯的氮气,其中混有氢气和水蒸气,现有下图所示A、B、C三种装置,要求证明氮气中混有这两种气体,并除去这两种气体,还能收集到纯净的干燥的氮气。
无水硫酸铜
C
氧化铜
B
浓H2SO4
A
