人教版(2019)选择性必修第三册《第2章+气体、固体和液体》2021年单元测试卷(6word版含答案)
文档属性
| 名称 | 人教版(2019)选择性必修第三册《第2章+气体、固体和液体》2021年单元测试卷(6word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 134.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2021-12-01 00:00:00 | ||
图片预览



文档简介
人教版(2019)选择性必修第三册《第2章 气体、固体和液体》2021年单元测试卷(6)
一.选择题(共3小题)
1.如图所示,将盛有温度为T的同种气体的两容器用水平细管相连,管中有一小段水银将A、B两部分气体隔开,若A升高到T+△TA,B升高到T+△TB,已知VA=2VB,要使水银保持不动,则( )
A.△TA=2△TB B.△TA=△TB C.△TA=△TB D.△TA=△TB
2.如图所示,左边的体积是右边的4倍,两边充以同种气体,此时连接两容器的细玻璃管的水银柱保持静止,如果容器两边的气体温度各升高10℃,则水银柱将( )
A.向左移动 B.向右移动
C.静止不动 D.条件不足,无法判断
3.如图所示,在斯特林循环的P﹣V图象中,一定质量理想气体从状态A依次经过状态B、C和D后再回到状态A,下列说法中正确的是( )
A.状态A的温度高于状态C的温度
B.B→C过程中,单位体积里气体分子数目减小
C.C→D过程中,气体分子每次与容器壁碰撞的平均冲力的平均值变小了
D.一个循环过程中,气体要从外界吸收一定的热量
二.计算题(共4小题)
4.肺活量是用标准状况下气体的体积来衡量的。设标准状况下温度为T0,大气压强为p0,且大气压强受气温影响可以忽略不计。某同学设计了一个简易测量肺活量的装置,图中A为倒扣在水中的开口圆筒,测量前排尽其中的空气,再通过B呼出空气,呼出的空气通过导管进入A内,横截面积为S,水的密度为ρ1,筒底浮出水面的高度为H。重力加速度为g。
(a)求圆筒内外水面高度差;
(b)则被测者的肺活量多大?
5.如图所示,柱形汽缸倒置在水平粗糙地面上,汽缸内部封有一定质量的理想气体,活塞质量m=25kg,其横截面积S=0.01m2,活塞与缸壁间的摩擦不计。当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力。现对汽缸加热,求缸内气体温度?(已知大气压强p0=1.0×105Pa,g=10m/s2)
6.如图,在大气中有竖直放置的固定圆筒,它由aS和S.已知B活塞下侧的空气与大气相通,活塞A的质量为2m,大气压强为P0,温度为T0.两活塞A和B用一根长为4l的不可伸长的轻线相连,把温度为T0的空气密封在两活塞之间,此时两活塞的位置如图所示.求:
(1)温度为T0时圆筒内气体的压强;
(2)现对被密封的气体加热,使其温度缓慢上升到T,活塞B恰好缓慢上升到圆筒c和b的连接处,求此时的温度.
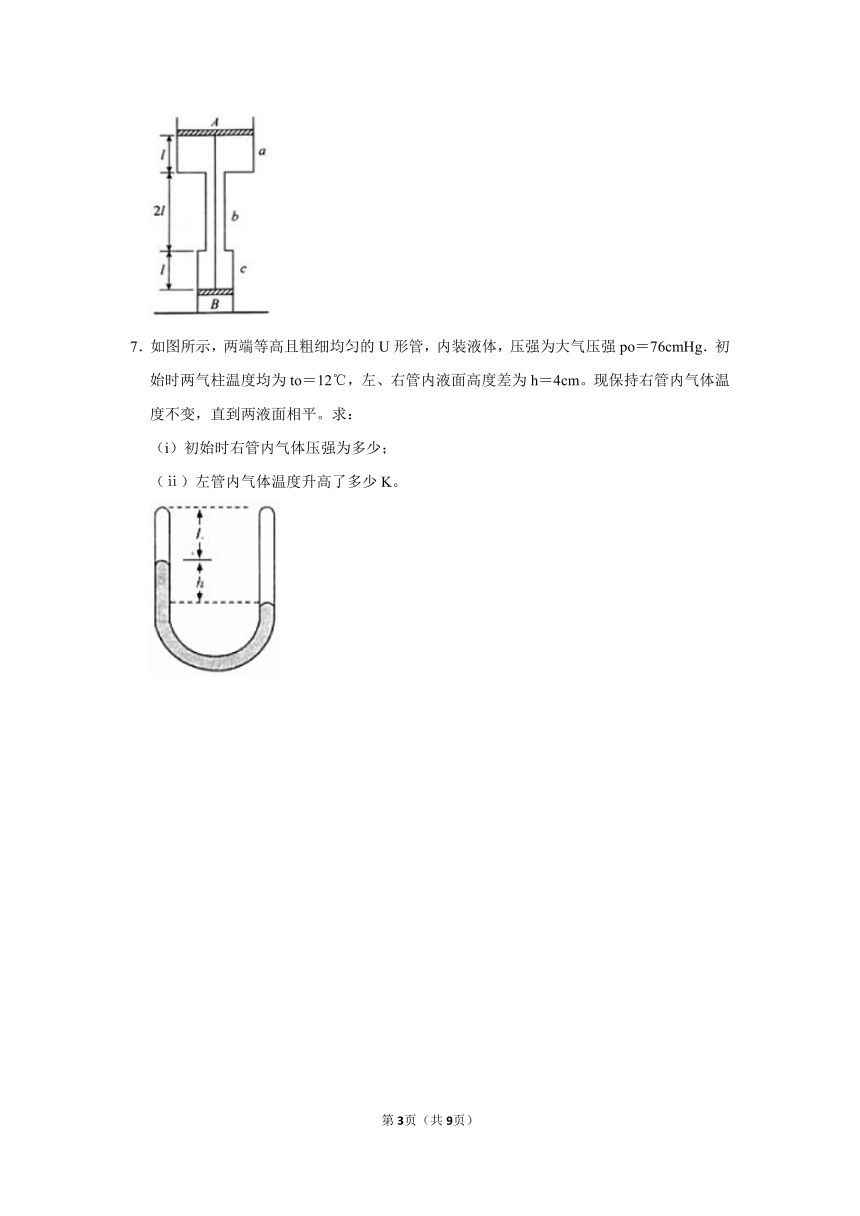
7.如图所示,两端等高且粗细均匀的U形管,内装液体,压强为大气压强po=76cmHg.初始时两气柱温度均为to=12℃,左、右管内液面高度差为h=4cm。现保持右管内气体温度不变,直到两液面相平。求:
(i)初始时右管内气体压强为多少;
(ⅱ)左管内气体温度升高了多少K。
人教版(2019)选择性必修第三册《第2章 气体、固体和液体》2021年单元测试卷(6)
参考答案与试题解析
一.选择题(共3小题)
1.如图所示,将盛有温度为T的同种气体的两容器用水平细管相连,管中有一小段水银将A、B两部分气体隔开,若A升高到T+△TA,B升高到T+△TB,已知VA=2VB,要使水银保持不动,则( )
A.△TA=2△TB B.△TA=△TB C.△TA=△TB D.△TA=△TB
【分析】要使水银保持不动,AB两部分气体压强的增加量应相等。气体的体积不变,根据理想气体的状态方程,找出AB两部分气体的压强的变化情况,再进行分析。
【解答】解:由图分析可知原来A、B两气体的压强相等B=PA,
要使水银保持不动,A、B两部分做要发生等容变化=c
由数学知识可得:=
则△P=△T
由上知PB=PA,且初态温度相等,则要使△P相等A=△TB。
故选:B。
2.如图所示,左边的体积是右边的4倍,两边充以同种气体,此时连接两容器的细玻璃管的水银柱保持静止,如果容器两边的气体温度各升高10℃,则水银柱将( )
A.向左移动 B.向右移动
C.静止不动 D.条件不足,无法判断
【分析】这类题目只能按等容过程求解。因为水银柱的移动是由于受力不平衡而引起的,
而它的受力改变又是两段空气柱压强增量的不同造成的,所以必须从压强变化入手。
【解答】解:假定两个容器的体积不变,即V1,V2不变,所装气体温度分别为293k和283k,
当温度升高△T时,左边的压强由p3增至p'1,△p1=p'8﹣p1,右边的压强由p2增至p′2,
△p2=p′2﹣p6。
由查理定律得:
△P1=△T3=△T,
因为p2=p5,所以△p1<△p2,
即水银柱应向左移动。
故选:A。
3.如图所示,在斯特林循环的P﹣V图象中,一定质量理想气体从状态A依次经过状态B、C和D后再回到状态A,下列说法中正确的是( )
A.状态A的温度高于状态C的温度
B.B→C过程中,单位体积里气体分子数目减小
C.C→D过程中,气体分子每次与容器壁碰撞的平均冲力的平均值变小了
D.一个循环过程中,气体要从外界吸收一定的热量
【分析】气体的内能只与温度有关,根据热力学第一定律有△U=W+Q判断气体吸热还是发热;根据图象利用理想气体状态方程对每一个过程进行分析即可。
【解答】解:A、A到B是等温变化A=TB,B到C等容变化,压强增大,即TB<TC,所以状态A的温度低于状态C的温度,故A错误;
B、B→C过程中,单位体积里气体分子数不变;
C、C→D过程,分子的平均动能不变,故C错误;
D、一个循环中,气体对外界做功W<0,故D正确;
故选:D。
二.计算题(共4小题)
4.肺活量是用标准状况下气体的体积来衡量的。设标准状况下温度为T0,大气压强为p0,且大气压强受气温影响可以忽略不计。某同学设计了一个简易测量肺活量的装置,图中A为倒扣在水中的开口圆筒,测量前排尽其中的空气,再通过B呼出空气,呼出的空气通过导管进入A内,横截面积为S,水的密度为ρ1,筒底浮出水面的高度为H。重力加速度为g。
(a)求圆筒内外水面高度差;
(b)则被测者的肺活量多大?
【分析】(a)以圆筒为研究对象,结合受力分析求出圆筒内气体的压强,根据圆筒内气体的压强等于大气压加上h水水深产生的压强,求出圆筒内外水面高度差;
(b)将圆筒内气体的体积由理想气体得状态方程转化为标准状态下气体的体积,即被测者的肺活量。
【解答】解:(a)圆筒受到重力、外部大气的压力以及内部气体的压力,则:mg+p0S=pS
可得:p=
圆筒内气体的压强等于大气压加上h水水深产生的压强,即:p=p7+ρgh
可得:h=
(b)圆筒内气体的体积:V1=S(H+h),压强:p1=,温度为T1,
转化为标准状态下气体的体积为V0,压强为p2,温度为T0,
由理想气体得状态方程:
转化为标准状态下气体的体积:V0=
被测者的肺活量为
答:(a)圆筒内外水面高度差为;
(b)被测者的肺活量为。
5.如图所示,柱形汽缸倒置在水平粗糙地面上,汽缸内部封有一定质量的理想气体,活塞质量m=25kg,其横截面积S=0.01m2,活塞与缸壁间的摩擦不计。当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力。现对汽缸加热,求缸内气体温度?(已知大气压强p0=1.0×105Pa,g=10m/s2)
【分析】抓住题目中的突破口“当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力”,以活塞为研究对象,受力分析,利用平衡即可求出此时封闭气体的压强;现使缸内气体温度升高,当气缸恰对地面无压力时,以气缸为研究对象,可求出升温后封闭气体的压强,然后一封闭气体为研究对象,等容变化,利用查理定律就可求出气体温度。
【解答】解:缸内温度为T1=(27+273)K=300 K时1
活塞对地面无压力,对活塞有:p6S+mg=p0S
解得:
当温度升为T2时气缸对地面无压力,对气缸有:p2S=p6S+Mg
解得:
对缸内气体由查理定律得:
联立求解得:T2=440K
答:缸内气体温度为440K。
6.如图,在大气中有竖直放置的固定圆筒,它由aS和S.已知B活塞下侧的空气与大气相通,活塞A的质量为2m,大气压强为P0,温度为T0.两活塞A和B用一根长为4l的不可伸长的轻线相连,把温度为T0的空气密封在两活塞之间,此时两活塞的位置如图所示.求:
(1)温度为T0时圆筒内气体的压强;
(2)现对被密封的气体加热,使其温度缓慢上升到T,活塞B恰好缓慢上升到圆筒c和b的连接处,求此时的温度.
【分析】(1)对AB活塞组成的整体受力分析,根据牛顿第二定律求得被封闭气体的压强;
(2)在加热过程中,被封闭气体做等压变化,找出初末状态参量,根据盖﹣吕萨克定律求得。
【解答】解:(1)以AB活塞为整体受力分析,活塞处于平衡处于平衡状态
3mg+p0 4S+pS=p0S+p 2S,解得;
(2)当温度升高时气体压强不变,由题意
初状态:,T0
末状态:V5=2l×2S+8l×S=4lS,T
由盖﹣吕萨克定律,解得。
答:(1)温度为T0时圆筒内气体的压强为;
(2)此时的温度为.
7.如图所示,两端等高且粗细均匀的U形管,内装液体,压强为大气压强po=76cmHg.初始时两气柱温度均为to=12℃,左、右管内液面高度差为h=4cm。现保持右管内气体温度不变,直到两液面相平。求:
(i)初始时右管内气体压强为多少;
(ⅱ)左管内气体温度升高了多少K。
【分析】①先根据平衡条件求解出初始时右管内气体压强;
②左管气体发生等温变化,根据玻意耳定律列式,分析右管气体初末状态,根据理想气体状态方程列式,联立求出左管内气体升高的温度。
【解答】解:(i)右管气体压强为P=P+pgh=80 cmHg
(ⅱ)当左、右两管液面相平时,左管 L′2=L′1=7cm
对右管气体,等温变化
P=80cmhg L1=(L+h)=10cm
由玻意耳定律,P1L6=P′1L′1
右管气柱压强为P′8=100cmHg
左管气体,P2=76cmHg
P2=P′7=10cmHg
由理想气体状态方程,=
代入数据解得,T'=500K
△T=500﹣285=215K
答:(i)初始时右管内气体压强为80 cmHg;
(ⅱ)左管内气体温度升高了215K。
第1页(共1页)
一.选择题(共3小题)
1.如图所示,将盛有温度为T的同种气体的两容器用水平细管相连,管中有一小段水银将A、B两部分气体隔开,若A升高到T+△TA,B升高到T+△TB,已知VA=2VB,要使水银保持不动,则( )
A.△TA=2△TB B.△TA=△TB C.△TA=△TB D.△TA=△TB
2.如图所示,左边的体积是右边的4倍,两边充以同种气体,此时连接两容器的细玻璃管的水银柱保持静止,如果容器两边的气体温度各升高10℃,则水银柱将( )
A.向左移动 B.向右移动
C.静止不动 D.条件不足,无法判断
3.如图所示,在斯特林循环的P﹣V图象中,一定质量理想气体从状态A依次经过状态B、C和D后再回到状态A,下列说法中正确的是( )
A.状态A的温度高于状态C的温度
B.B→C过程中,单位体积里气体分子数目减小
C.C→D过程中,气体分子每次与容器壁碰撞的平均冲力的平均值变小了
D.一个循环过程中,气体要从外界吸收一定的热量
二.计算题(共4小题)
4.肺活量是用标准状况下气体的体积来衡量的。设标准状况下温度为T0,大气压强为p0,且大气压强受气温影响可以忽略不计。某同学设计了一个简易测量肺活量的装置,图中A为倒扣在水中的开口圆筒,测量前排尽其中的空气,再通过B呼出空气,呼出的空气通过导管进入A内,横截面积为S,水的密度为ρ1,筒底浮出水面的高度为H。重力加速度为g。
(a)求圆筒内外水面高度差;
(b)则被测者的肺活量多大?
5.如图所示,柱形汽缸倒置在水平粗糙地面上,汽缸内部封有一定质量的理想气体,活塞质量m=25kg,其横截面积S=0.01m2,活塞与缸壁间的摩擦不计。当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力。现对汽缸加热,求缸内气体温度?(已知大气压强p0=1.0×105Pa,g=10m/s2)
6.如图,在大气中有竖直放置的固定圆筒,它由aS和S.已知B活塞下侧的空气与大气相通,活塞A的质量为2m,大气压强为P0,温度为T0.两活塞A和B用一根长为4l的不可伸长的轻线相连,把温度为T0的空气密封在两活塞之间,此时两活塞的位置如图所示.求:
(1)温度为T0时圆筒内气体的压强;
(2)现对被密封的气体加热,使其温度缓慢上升到T,活塞B恰好缓慢上升到圆筒c和b的连接处,求此时的温度.
7.如图所示,两端等高且粗细均匀的U形管,内装液体,压强为大气压强po=76cmHg.初始时两气柱温度均为to=12℃,左、右管内液面高度差为h=4cm。现保持右管内气体温度不变,直到两液面相平。求:
(i)初始时右管内气体压强为多少;
(ⅱ)左管内气体温度升高了多少K。
人教版(2019)选择性必修第三册《第2章 气体、固体和液体》2021年单元测试卷(6)
参考答案与试题解析
一.选择题(共3小题)
1.如图所示,将盛有温度为T的同种气体的两容器用水平细管相连,管中有一小段水银将A、B两部分气体隔开,若A升高到T+△TA,B升高到T+△TB,已知VA=2VB,要使水银保持不动,则( )
A.△TA=2△TB B.△TA=△TB C.△TA=△TB D.△TA=△TB
【分析】要使水银保持不动,AB两部分气体压强的增加量应相等。气体的体积不变,根据理想气体的状态方程,找出AB两部分气体的压强的变化情况,再进行分析。
【解答】解:由图分析可知原来A、B两气体的压强相等B=PA,
要使水银保持不动,A、B两部分做要发生等容变化=c
由数学知识可得:=
则△P=△T
由上知PB=PA,且初态温度相等,则要使△P相等A=△TB。
故选:B。
2.如图所示,左边的体积是右边的4倍,两边充以同种气体,此时连接两容器的细玻璃管的水银柱保持静止,如果容器两边的气体温度各升高10℃,则水银柱将( )
A.向左移动 B.向右移动
C.静止不动 D.条件不足,无法判断
【分析】这类题目只能按等容过程求解。因为水银柱的移动是由于受力不平衡而引起的,
而它的受力改变又是两段空气柱压强增量的不同造成的,所以必须从压强变化入手。
【解答】解:假定两个容器的体积不变,即V1,V2不变,所装气体温度分别为293k和283k,
当温度升高△T时,左边的压强由p3增至p'1,△p1=p'8﹣p1,右边的压强由p2增至p′2,
△p2=p′2﹣p6。
由查理定律得:
△P1=△T3=△T,
因为p2=p5,所以△p1<△p2,
即水银柱应向左移动。
故选:A。
3.如图所示,在斯特林循环的P﹣V图象中,一定质量理想气体从状态A依次经过状态B、C和D后再回到状态A,下列说法中正确的是( )
A.状态A的温度高于状态C的温度
B.B→C过程中,单位体积里气体分子数目减小
C.C→D过程中,气体分子每次与容器壁碰撞的平均冲力的平均值变小了
D.一个循环过程中,气体要从外界吸收一定的热量
【分析】气体的内能只与温度有关,根据热力学第一定律有△U=W+Q判断气体吸热还是发热;根据图象利用理想气体状态方程对每一个过程进行分析即可。
【解答】解:A、A到B是等温变化A=TB,B到C等容变化,压强增大,即TB<TC,所以状态A的温度低于状态C的温度,故A错误;
B、B→C过程中,单位体积里气体分子数不变;
C、C→D过程,分子的平均动能不变,故C错误;
D、一个循环中,气体对外界做功W<0,故D正确;
故选:D。
二.计算题(共4小题)
4.肺活量是用标准状况下气体的体积来衡量的。设标准状况下温度为T0,大气压强为p0,且大气压强受气温影响可以忽略不计。某同学设计了一个简易测量肺活量的装置,图中A为倒扣在水中的开口圆筒,测量前排尽其中的空气,再通过B呼出空气,呼出的空气通过导管进入A内,横截面积为S,水的密度为ρ1,筒底浮出水面的高度为H。重力加速度为g。
(a)求圆筒内外水面高度差;
(b)则被测者的肺活量多大?
【分析】(a)以圆筒为研究对象,结合受力分析求出圆筒内气体的压强,根据圆筒内气体的压强等于大气压加上h水水深产生的压强,求出圆筒内外水面高度差;
(b)将圆筒内气体的体积由理想气体得状态方程转化为标准状态下气体的体积,即被测者的肺活量。
【解答】解:(a)圆筒受到重力、外部大气的压力以及内部气体的压力,则:mg+p0S=pS
可得:p=
圆筒内气体的压强等于大气压加上h水水深产生的压强,即:p=p7+ρgh
可得:h=
(b)圆筒内气体的体积:V1=S(H+h),压强:p1=,温度为T1,
转化为标准状态下气体的体积为V0,压强为p2,温度为T0,
由理想气体得状态方程:
转化为标准状态下气体的体积:V0=
被测者的肺活量为
答:(a)圆筒内外水面高度差为;
(b)被测者的肺活量为。
5.如图所示,柱形汽缸倒置在水平粗糙地面上,汽缸内部封有一定质量的理想气体,活塞质量m=25kg,其横截面积S=0.01m2,活塞与缸壁间的摩擦不计。当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力。现对汽缸加热,求缸内气体温度?(已知大气压强p0=1.0×105Pa,g=10m/s2)
【分析】抓住题目中的突破口“当缸内气体温度为27℃时,活塞刚好与地面相接触,但对地面无压力”,以活塞为研究对象,受力分析,利用平衡即可求出此时封闭气体的压强;现使缸内气体温度升高,当气缸恰对地面无压力时,以气缸为研究对象,可求出升温后封闭气体的压强,然后一封闭气体为研究对象,等容变化,利用查理定律就可求出气体温度。
【解答】解:缸内温度为T1=(27+273)K=300 K时1
活塞对地面无压力,对活塞有:p6S+mg=p0S
解得:
当温度升为T2时气缸对地面无压力,对气缸有:p2S=p6S+Mg
解得:
对缸内气体由查理定律得:
联立求解得:T2=440K
答:缸内气体温度为440K。
6.如图,在大气中有竖直放置的固定圆筒,它由aS和S.已知B活塞下侧的空气与大气相通,活塞A的质量为2m,大气压强为P0,温度为T0.两活塞A和B用一根长为4l的不可伸长的轻线相连,把温度为T0的空气密封在两活塞之间,此时两活塞的位置如图所示.求:
(1)温度为T0时圆筒内气体的压强;
(2)现对被密封的气体加热,使其温度缓慢上升到T,活塞B恰好缓慢上升到圆筒c和b的连接处,求此时的温度.
【分析】(1)对AB活塞组成的整体受力分析,根据牛顿第二定律求得被封闭气体的压强;
(2)在加热过程中,被封闭气体做等压变化,找出初末状态参量,根据盖﹣吕萨克定律求得。
【解答】解:(1)以AB活塞为整体受力分析,活塞处于平衡处于平衡状态
3mg+p0 4S+pS=p0S+p 2S,解得;
(2)当温度升高时气体压强不变,由题意
初状态:,T0
末状态:V5=2l×2S+8l×S=4lS,T
由盖﹣吕萨克定律,解得。
答:(1)温度为T0时圆筒内气体的压强为;
(2)此时的温度为.
7.如图所示,两端等高且粗细均匀的U形管,内装液体,压强为大气压强po=76cmHg.初始时两气柱温度均为to=12℃,左、右管内液面高度差为h=4cm。现保持右管内气体温度不变,直到两液面相平。求:
(i)初始时右管内气体压强为多少;
(ⅱ)左管内气体温度升高了多少K。
【分析】①先根据平衡条件求解出初始时右管内气体压强;
②左管气体发生等温变化,根据玻意耳定律列式,分析右管气体初末状态,根据理想气体状态方程列式,联立求出左管内气体升高的温度。
【解答】解:(i)右管气体压强为P=P+pgh=80 cmHg
(ⅱ)当左、右两管液面相平时,左管 L′2=L′1=7cm
对右管气体,等温变化
P=80cmhg L1=(L+h)=10cm
由玻意耳定律,P1L6=P′1L′1
右管气柱压强为P′8=100cmHg
左管气体,P2=76cmHg
P2=P′7=10cmHg
由理想气体状态方程,=
代入数据解得,T'=500K
△T=500﹣285=215K
答:(i)初始时右管内气体压强为80 cmHg;
(ⅱ)左管内气体温度升高了215K。
第1页(共1页)
