4.2水的组成同步课时练-2021-2022学年初中化学科粤版(2012)九年级上册(word版 含解析)
文档属性
| 名称 | 4.2水的组成同步课时练-2021-2022学年初中化学科粤版(2012)九年级上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 154.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-01 00:00:00 | ||
图片预览



文档简介
4.2水的组成同步课时练
一、单选题(共17题)
1.下列各组物质中是按单质、化合物排列的是 ( )
A.生铁、二氧化碳 B.铜、铁锈 C.液氧、水 D.水银、稀硫酸
2.水是生命之源。下列说法正确的是
A.液态水变成水蒸气时,水分子变大 B.用活性炭吸附的方法能使硬水转化为软水
C.蒸馏或过滤均可使海水转化为淡水 D.电解水时负极和正极生成气体的体积比为2 :1
3.下列事实与物质的化学性质无关的是
A.二氧化碳可以和水反应生成碳酸 B.氧气可以供给呼吸
C.硫能在空气中燃烧 D.氯化钠的熔点是801℃
4.水是生命之源,下列有关水的叙述正确的是
A.为了防止水体污染,禁止使用农药化肥
B.在软水中加肥皂水揽拌后会出现大量浮渣
C.在沉淀、过滤、吸附、蒸馏等对水的净化操作中,净化程度最高的是蒸馏
D.水是由2个氢原子和1个氧原子构成的
5.2021年“世界水日”的主题为Valuin Waterw。下列关于水的说法合理的是
A.水是一种常用的溶剂
B.冰水混合物不是化合物
C.水中添加活性炭可将硬水转成软水
D.水电解生成氢气和氧气,说明水中含有氢分子和氧分子
6.水是生命之源。下列有关水的说法不正确的是( )
A.可用肥皂水区别硬水和软水
B.活性炭可通过吸附将自来水变为纯净水
C.生活中常用煮沸的方法软化硬水
D.电解水得到体积较大的气体具有可燃性
7.下列对宏观事实解释不正确的是
A.酒香不怕巷子深——分子不断运动
B.压瘪的乒乓球在热水中能鼓起来——温度升高,分子变大
C.水和过氧化氢的化学性质不同——分子构成不同
D.水通电生成氢气和氧气——化学反应中分子发生了改变
8.水是生命之源,关于水的说法不正确的是
A.用肥皂水区分硬水和软水 B.水的电解实验说明水由氢气和氧气组成
C.用蒸馏的方法可以将海水淡化 D.生活中提倡使用无磷洗衣粉防止水体污染
9.水是生命之源。下面有关水的说法正确的是
A.水通电分解时产生的氢气和氧气质量比为2︰1
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成的
C.用过滤的方法可以使硬水软化
D.如果将水样蒸干后有固体析出,这种水样中一定含有可溶性杂质
10.关于水的组成的正确说法是
A.由氢、氧组成 B.由氢气和氧气两种分子组成
C.由氢气和氧气组成 D.由氢、氧两种元素组成
11.下列日常生活中常发生的一些变化,属于化学变化的是( )
A.水蒸发 B.灯泡发光 C.蔗糖溶解 D.铁生锈
12.下列关于物质的构成说法正确的是
A.电解水实验,产生了氢气和氧气,说明水是由氢气和氧气组成的
B.H2O不仅可以表示水这种物质,还可以表示水的组成
C.水是由氢元素和氧元素组成的混合物
D.冰块与水混合后得到混合物
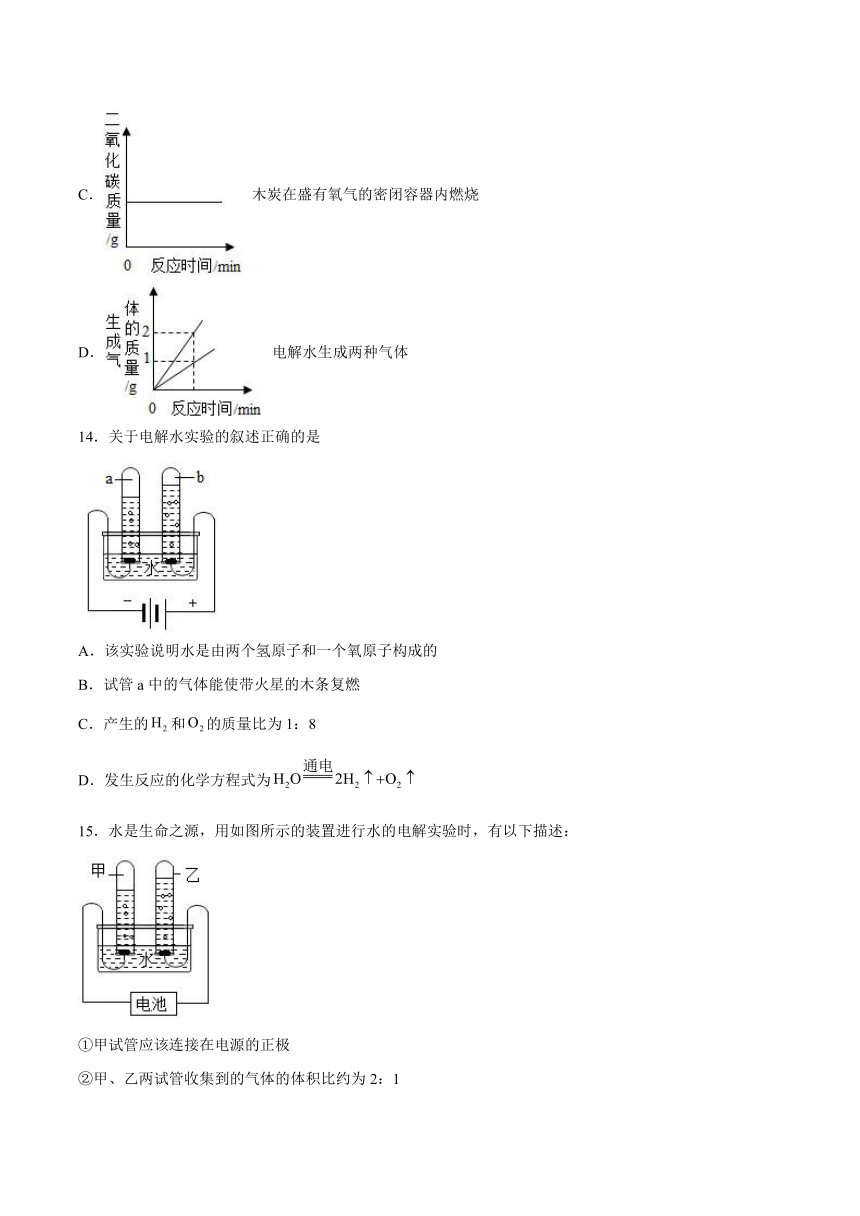
13.以下图象,能正确反映对应关系的是
A. 加热一定质量的氯酸钾固体
B. 铜丝在空气中加热
C. 木炭在盛有氧气的密闭容器内燃烧
D. 电解水生成两种气体
14.关于电解水实验的叙述正确的是
A.该实验说明水是由两个氢原子和一个氧原子构成的
B.试管a中的气体能使带火星的木条复燃
C.产生的和的质量比为1:8
D.发生反应的化学方程式为
15.水是生命之源,用如图所示的装置进行水的电解实验时,有以下描述:
①甲试管应该连接在电源的正极
②甲、乙两试管收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧,
④该实验说明水是由氢气和氧气组成的
以上描述中正确的是( )
A.
B.
C.
D.
16.中科院科研团队成功合成一种高效电解水催化剂,为未来解决氢能危机提供了可能。实验室采用如图装置电解水。下列关于电解水的叙述中错误的是
A.在水中加入一定量的稀硫酸是为了增强水的导电性
B.电解水的实验证明水是由氢、氧两种元素组成的
C.若A试管气体为10mL,则B试管气体为5mL
D.与电源正极相连的玻璃管B内得到的气体能在空气中燃烧
17.下列叙述中正确的是( )
A.水分子是保持水的性质的最小粒子
B.氧气的化学性质比较活泼,能够燃烧
C.电解水生成氢气和氧气的体积比为1:2
D.用水灭火,主要是使可燃物的温度降低到着火点以下
二、综合题(共5题)
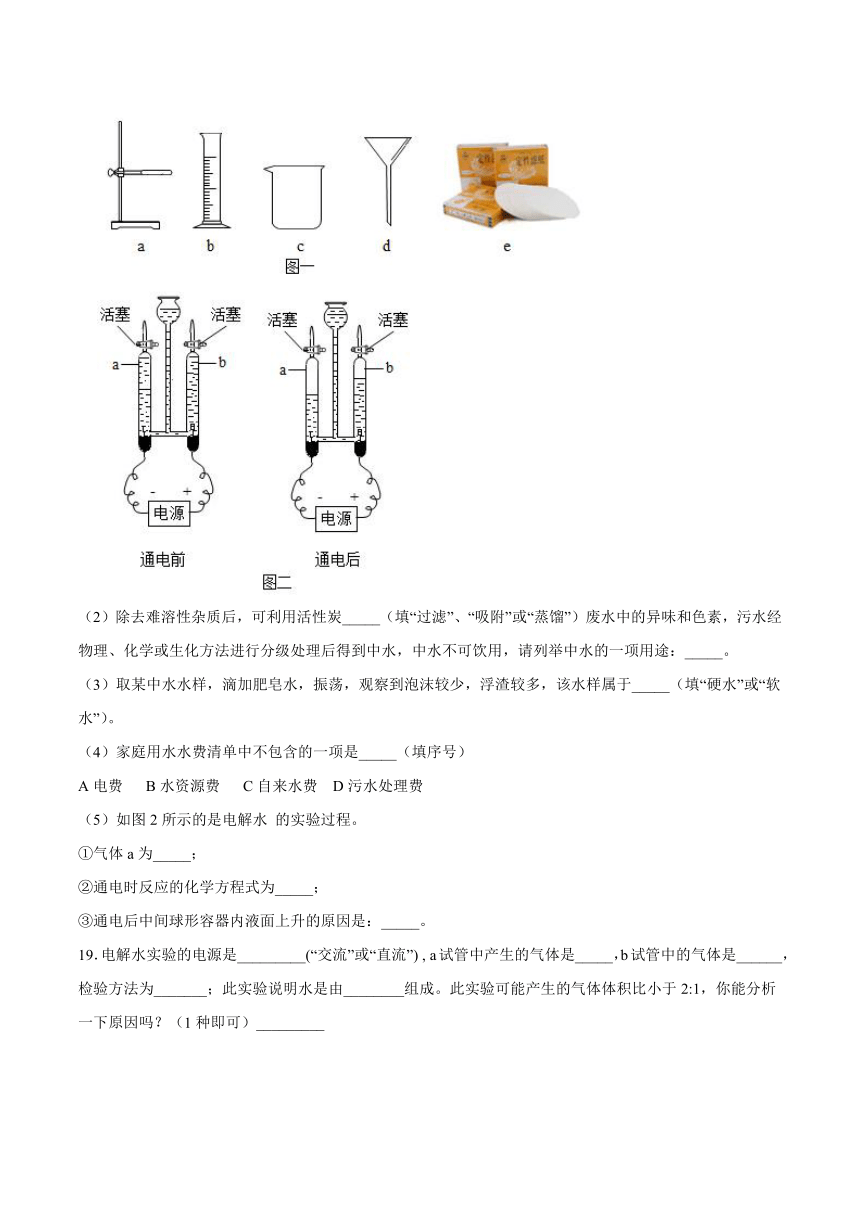
18.2017年3月22日是第25届世界水日,宣传主题是“Wastewater”(废水),请回答下列与水有关的问题:
(1)废水中常含有难溶性杂质,除去这些杂质的操作是_____(填“过滤”、“吸附”或“蒸馏”),实验完成该操作所需的玻璃仪器除玻璃棒外还有_____(填序号),其中玻璃棒的作用是_____。
(2)除去难溶性杂质后,可利用活性炭_____(填“过滤”、“吸附”或“蒸馏”)废水中的异味和色素,污水经物理、化学或生化方法进行分级处理后得到中水,中水不可饮用,请列举中水的一项用途:_____。
(3)取某中水水样,滴加肥皂水,振荡,观察到泡沫较少,浮渣较多,该水样属于_____(填“硬水”或“软水”)。
(4)家庭用水水费清单中不包含的一项是_____(填序号)
A电费 B水资源费 C自来水费 D污水处理费
(5)如图2所示的是电解水 的实验过程。
①气体a为_____;
②通电时反应的化学方程式为_____;
③通电后中间球形容器内液面上升的原因是:_____。
19.电解水实验的电源是_________(“交流”或“直流”) , a试管中产生的气体是_____,b试管中的气体是______,检验方法为_______;此实验说明水是由________组成。此实验可能产生的气体体积比小于2:1,你能分析一下原因吗?(1种即可)_________
20.多角度认识物质,能帮助我们更全面了解物质世界.以水为例,回答下列问题:
(1)认识物质的组成和构成
①从宏观上看,水由____(填“元素”、“原子”或“分子”,下同)组成.
②从微观上看,水由_____构成.
(2)认识物质的性质:水通电能发生化学变化,反应的化学方程式为_____.
(3)获得物质的方法:地球上总储水量很大,但淡水很少,海水中溶解了很多物质,又苦又咸,除了含H2O外,还含大量的Na+、Ca2+、Cl﹣、Mg2+、SO42﹣等.以海水为原料提取食盐的工艺流程如图:
①图中a是___池(填“蒸发”或“冷却”).
②根据海水晒盐的原理,下列说法中不正确的是___.
A 得到的粗盐是纯净的氯化钠
B 在a中,海水中水的质量逐渐减少
C 在a中,海水中氯化钠的质量逐渐增加
D 海水进入储水池,海水的成分基本不变
③根据上述及工艺流程图,母液中所含的离子有___.
A Ca2+、Mg2+、SO42﹣等 B Na+、Ca2+、Cl﹣、Mg2+、SO42﹣、H2O等
C Ca2+、Mg2+、SO42﹣、H2O等 D Na+、Ca2+、Cl﹣、Mg2+、SO42﹣等
21.水是生命之源,请回答下列问题。
(1)如图为电解水的装置。用 ____ 来检验b管中的气体,b管中气体与a管中气体的质量比为 ___ 。由实验得出水是由 ____ 组成的。
(2)本市某水厂生产自来水的净化步骤如下图所示:
原水→加明矾→沉淀→吸附→沙滤→加氯气→净水
向水中通入氯气,其作用是 ______ ;向水中加入 ______ (填写物质名称),吸附除去其中的异昧。
22.探究物质组成的奥秘。元素之义,人们很早就意识到,所有物质都是由几种亘古不变的基本成分-“元素”组成的。古希腊学者提出复杂的物质世界是由“水、木、火和空气”四种基本成分组成的。
I.空气是元素吗?
(1)瑞典化学家舍勒发现,将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟罩内水面大约上升_____,被消耗的气体是氧气,该反应的文字表达式为_____,舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是_____(写化学式),上述实验证明空气是一种混合物,因此,空气不是元素。
II.水是元素吗?
(实验探究)
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,写出该变化的文字表达式_____ ,该反应的基本类型是_____。法国科学家拉瓦锡发现,水通电时能分解,写出此反应的文字表达式_____。
上述两个实验说明,水不是组成物质的元素。
①图2为电解水实验,请将下表填写完整。
实验方案 实验现象 结论
_____放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体_____,(写化学式),不是水蒸气
_____放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为_____,(写化学式),不是水蒸气
②实验表明,水通电后发生了化学变化。
化学变化中不变的微粒是_____,老师指出,该微粒也是构成物质的基本粒子。小组同学通过填写物质的构成及构成物质的粒子间的关系图,理解了老师的说法。请将图3中的a、b、c三处填写完整a_____、b_____、c_____。
III.木和火是元素吗?
(3)查阅资料:“木”(木材)隔绝空气加强热可得到木煤气[主要成分为一氧化碳(CO)、氢气(H2)、甲烷(CH4)]、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”_____(填“是”或“不是”)元素。“火”不属于物质,因此,“火”不是元素。
IV.元素的概念及其应用
(4)课本上元素的概念是:“把具有……的原子归为一类,每一类原子称为一种元素。”其中“一类原子”包括_____。
A 质子数和中子数都相同的所有原子
B 质子数不同,中子数相同的所有原子
C 质子数相同,中子数不同的所有原子
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子是否都是氢元素的原子,为什么? _____。从宏观的角度看,重水是由_____(填名称)元素组成的。
(6)世界上的物质都是由元素组成的,图4为地壳中的元素分布,地壳中含量最多的金属元素与氧元素形成的化合物的化学式为_____,其相对原子质量为_____。
元素密码——元素周期表
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家_____发现化学元素的周期性,排列出第一张元素周期表。成为科学家探索未知世界的有力工具。图5是元素周期表的一部分,空白部分被墨水沾黑,图6是镁原子的结构示意图。据图回答下列问题:
②结合图6分析镁原子不显电性的原因_____。
③图5中空白处元素的原子序数为_____,位于元素周期表第_____周期,若用R表示该元素,则R与氯元素组成的化合物的化学式为_____。
参考答案
1.C
【解析】
【详解】
A.生铁是混合物,二氧化碳是化合物,故不符合题意;
B.铜是单质,铁锈是混合物,故不符合题意;
C.液氧是单质,水是化合物,故符合题意;
D.水银是单质,稀硫酸是混合物,故不符合题意。故选C。
2.D
【详解】
A、液态水变成水蒸气时,水分子不变,分子间的间隔增大,故A错误;
B、活性炭能吸附水中的色素和异味,不能除去可溶性钙、镁化合物,用活性炭吸附的方法不能使硬水转化为软水,故B错误;
C、蒸馏能够得到淡水,过滤只能除去水中的不溶性杂质,不能除去水中的氯化钠等,不能得到淡水,故C错误;
D、水通电时,正极产生氧气,负极产生氢气,体积比为1:2。电解水时负极和正极生成气体的体积比为2:1,故D正确。故选D。
3.D
【解析】
【详解】
A. 二氧化碳可以和水反应生成碳酸在化学变化中体现出来,属于化学性质,选项错误;B. 氧气可以供给呼吸需要在化学变化中体现出来,属于化学性质,选项错误;C. 硫能在空气中燃烧生成新物质,属于化学性质,选项错误;D. 氯化钠的熔点是801℃,熔点属于物质的物理性质,选项正确,故选D。
4.C
【详解】
A、防止水体污染,应合理使用化肥和农药,不能禁止,该选项说法不正确;
B、将肥皂水滴到软水中,搅拌可以看到产生少量的浮渣,该选项说法不正确;
C、对水的净化操作中,蒸馏能除去水中所有的杂质,净化程度最高的是蒸馏,该选项说法正确;
D、1个水分子是由1个氧原子和2个氢原子构成,该选项说法不正确。
故选C。
5.A
【详解】
A、水是一种常用的溶剂,正确;
B、冰水混合物只有水一种物质,水是由氢氧元素组成的化合物,错误;
C、水中添加活性炭可以除去水中色素和异味,不能除去可溶性杂质,不能将硬水转成软水,错误;
D、水电解生成氢气和氧气,说明水是由氢氧元素组成的,错误。
故选A。
6.B
【详解】
A、肥皂水遇硬水会产生较多的浮渣,遇软水会产生较多的泡沫,可以据此进行鉴别。A正确;
B、活性炭具有吸附性,可以吸附水中的色素和异味,但是不能将自来水转化为纯净水。B错误;
C、天然水煮沸过程中,水中的可溶性钙镁化合物转化为沉淀,水的硬度下降,生活中常用煮沸的方法将硬水软化。C正确;
D、电解水得到的体积较大的气体是氢气,氢气具有可燃性。D正确。
故选B。
7.B
【详解】
A、酒香不怕巷子深说明分子不断运动,A正确;
B、压瘪的乒乓球在热水中能鼓起来是由于温度升高,分子之间的间隔变大,B错误;
C、水和过氧化氢的化学性质不同是由于分子构成不同,C正确;
D、水通电生成氢气和氧气说明化学反应中分子发生了改变,D正确。
故选B。
8.B
【详解】
A、硬水和软水的区别在于所含的钙镁离子的多少,可用肥皂水来区分硬水和软水,加入肥皂水,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,故选项说法正确。
B、电解水生成氢气和氧气,氢气和氧气分别是由氢元素和氧元素组成的,说明水是由氢元素和氧元素组成的,水中不含氢气和氧气,故选项说法错误。
C、将海水蒸馏,能将水从海水中分离出来,从而实现海水淡化,故选项说法正确。
D、无磷洗衣粉可以防止水体富营养化,生活中提倡使用无磷洗衣粉防止水体污染,故选项说法正确。
故选:B。
9.D
【详解】
A、水通电分解时产生的氢气和氧气体积比为2:1,故A错误;B、电解水生成氢气和氧气,说明水是由氢和氧两种元素组成的,故B错误;C、用过滤的方法只能除去水中不溶性的杂质,不能减少钙、镁离子化合物的含量,不可以使硬水软化,故C错误;D、如果将水样蒸干后有固体析出,这种水样中一定含有杂质,故D正确;故选:D。
10.D
【分析】
通过电解水生成氢气和氧气可知,水是由氢元素和氧元素组成的物质。
【详解】
A、水是由氢元素和氧元素组成的,该选项说法不正确;
B、水不是由氢分子和氧分子组成的,该选项说法不正确;
C、水不是由氢气和氧气组成,该选项说法不正确;
D、水是由氢、氧两种元素组成的,该选项说法正确。
故选:D。
11.D
【解析】
【分析】
没有新物质生成的变化是物理变化,有新物质生成的变化是化学变化;
【详解】
A、水的蒸发是液态的水变为气态的水,没有新物质生成,故是物理变化,故错误;
B、灯泡发光的过程中没有新物质的生成,是物理变化,故错误;
C、蔗糖溶解的过程中没有新物质生成,故是物理变化,故错误;
D、铁生锈的过程中有新物质氧化铁生成,故是化学变化,故正确。故选D。
12.B
【详解】
A、电解水实验,产生了氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,反应前后元素种类不变,说明水是由氢元素和氧元素组成的,选项说法不正确;
B、H2O不仅可以表示水这种物质,还可以表示水是由氢元素和氧元素组成,选项说法正确;
C、水是纯净物,由氢元素和氧元素组成,选项说法不正确;
D、冰块与水是同一种物质,混合后属于纯净物,选项说法不正确。
故选B。
13.B
【详解】
A.氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,氧气的质量从零开始逐渐增大,然后不变,故A错误;
B.铜和氧气在加热的条件下生成氧化铜,固体的质量逐渐增大,然后不变,故B正确;
C.木炭和氧气在点燃的条件下生成二氧化碳,二氧化碳的质量从零开始逐渐增大,然后不变,故C错误;
D.水在通电的条件下生成氢气和氧气的体积比是2:1,故D错误。
故选B。
14.C
【详解】
A、该实验说明水是由氢元素和氧元祖组成的;故选项错误。
B、试管a与电源负极连接,产生氢气,不能是带火星的木条复燃;故选项错误。
C、产生的H2和O2的质量比为1:8;故选项正确;
D、发生反应的化学方程式为:2H2O2H2↑+O2↑;
故选C。
15.B
【详解】
①甲试管中产生的气体最多应该是H2,乙试管中产生的气体应该是O2,所以甲试管应该连接在电源的负极,故①错误;
②甲乙两试管中产生的气体体积比约为2:1,故②正确;
③由上述分析可知,甲试管内生成的气体是氢气,氢气可以燃烧,故③正确;
④电解水实验生成了氢气和氧气,说明水是由氢元素和氧元素组成的,故④错误。
由以上分析可知,B符合题意。
故选B。
16.D
【详解】
A、在电解水时,常加入少量的硫酸溶液,可以增强水的导电性,以加快水的电解速度,故A正确;
B、电解水用直流电,正极产生的是氧气,负极产生的是氢气,因此可以证明水是由氢氧两种元素组成的,故B正确;
C、正极产生的是氧气,负极产生的是氢气,且氢气和氧气的体积比为2:1,因此B试管内是氧气,A试管内是氢气,因此若A试管内氢气是10mL,则B试管内的氧气是5mL,故C正确;
D、与电源正极相连的玻璃管B内得到的气体是氧气,能够支持燃烧,但不能燃烧,故D错误。
故选D。
17.D
【解析】
A、水分子是保持水的化学性质的最小粒子,故A错误;
B、氧气的化学性质比较活泼,能够支持燃烧,故B错误;
C、电解水生成氢气和氧气的体积比为2:1,故C错误;
D、燃烧的条件是可燃物与氧气接触,温度达到着火点;用水灭火,主要是使可燃物的温度降低到着火点以下,故D正确。
18.过滤 c、 引流 吸附 用于冲厕 硬水 A 氢气 2H2O2H2↑+O2↑ a、b两管内汇聚气体,气压变大,将水压入中间球形容器中
【详解】
(1)过滤能将液体与固体分离。废水中常含有难溶性杂质,通常采用的实验操作是过滤,还需要用到的玻璃仪器除烧杯、漏斗,故选C;其中玻璃棒的作用是引流;
(2)除去难溶性杂质后,可利用活性炭吸附废水中的异味和色素,“中水”的水质指标低于生活饮用水的水质标准,但又高于允许排放的污水的水质标准,处于二者之间,不可饮用但可用于冲厕、灌溉、景观用水、洗车等;
(3)向水中加入肥皂水时,如果产生大量的泡沫,说明是软水;如果产生的泡沫很少或不产生泡沫,说明是硬水。
(4)家庭生活用水水费清单中包含水资源费、自来水水费、污水处理费。不包含的一项是电费。故选A;
(5)水电解时,正极产生氧气,负极产生氢气,氢气和氧气的体积比为2:1。由如图是电解水实验装置可知。实验过程中,试管a产生的气体是电源的负极产生的气体较多是氢气
②水在通电条件下生成了氢气和氧气,反应的化学方程式是:;
③通电后中间球形容器内液面上升的原因是:a、b两管内汇聚气体,气压变大,将水压入中间球形容器中。
19.直流电 氢气 氧气 将带火星的木条伸入试管口,木条复燃,证明是氧气 氢、氧元素 氧气的溶解性大于氢气的溶解性
【详解】
电解水实验的电源是直流,由电解水的装置可知,a试管中产生的气体是电源的负极产生的气体较多是氢气,b试管中的气体是电源的正极产生的气体较少是氧气,具有助燃性,检验方法为:将带火星的木条伸入试管口,木条复燃,证明是氧气;此实验说明水是由氢、氧元素组成。此实验可能产生的气体体积比小于2:1,可能的原因是:氧气的溶解性大于氢气的溶解性。
20.元素 分子 蒸发 AC D
【详解】
(1)①从宏观上看,水由氢元素和氧元素组成,故填:元素;
②从微观上看,水由水分子组成,故填:分子;
(2)水在通电的条件下分解生成氢气和氧气,该反应的化学方程式为:;
(3)①因为氯化钠的溶解度受温度影响比较小,故应采取蒸发结晶的方法,故填:蒸发;
②A、粗盐中含有泥沙等难溶性杂质和一些可溶性杂质,故不是纯净的氯化钠,属于混合物,符合题意;
B、随着蒸发的不断进行,溶剂水不断减少,不符合题意;
C、在蒸发的过程中,溶剂质量不断减少,溶质质量不变,故溶液中氯化钠的质量不变,符合题意;
D、海水属于溶液,溶液具有均一、稳定性,故海水进入储水池,海水的成分基本不变,不符合题意
故选AC;
③大部分食盐在结晶析出的同时,也会有很少的其他的晶体从溶液中结晶析出,但溶液中仍旧会有少量的氯化钠,母液中可能含有的离子是:Na+、Ca2+、Cl﹣、Mg2+、SO42﹣。
故选D。
21.带火星的木条 8:1 氢元素和氧元素 杀菌消毒 活性炭
【详解】
(1)电解水时,正极生成的是氧气,负极生成氢气,氢气是氧气体积的2倍,b管内气体为氧气,氧气有助燃性,可用带火星的木条来检验b管中的气体,b管中气体与a管中气体的质量比等于水中氧、氢两种元素的质量比,为8:1。据质量守恒定律可知,反应前后元素的种类不变,由实验得出水是由氢元素和氧元素组成的;
(2)向水中通入氯气,能与生物细胞的基础物质蛋白质反应,其作用是杀菌消毒;向水中加入活性炭,吸附除去其中的异昧,因活性炭有吸附作用。
22.1/5 磷+氧气五氧化二磷 N2 氢气+氧气水 化合反应 水氢气+氧气 将燃着的木条 H2 将带火星的木条 O2 原子 离子 原子 分子 不是 AC 是,核内质子数都是1或核内质子数相同 由氢元素和氧元素组成的 Al2O3 102 门捷列夫 原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反 20 四 RCl2
【详解】
(1)将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟置内水面大约上升五分之一,被消耗的气体是氧气,该反应的文字表达式为:磷+氧气五氧化二磷;舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是N2,上述实验证明空气是可分的,因此,空气不是元素;
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,该变化的文字表达式为:氢气+氧气水,该反应是由两种物质生成一种物质的反应,其基本类型是化合反应;水通电生成氢气和氧气,反应的文字表达式为:水氢气+氧气;
①氢气具有可燃性,在空气中能安静地燃烧,产生淡蓝色火焰,放出热量;氧气具有助燃性能使带火星的木条复燃,常用来检验氧气。
实验方案 实验现象 结论
将燃着的木条放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体H2,,不是水蒸气
将带火星的木条放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为O2,不是水蒸气
②实验表明,水通电后发生了化学变化,该化学变化过程是:构成水分子的氢原子、氧原子重新结合成氢分子、氧分子,由此可见,化学变化中不变的微粒是原子;构成物质的微粒有分子、原子和离子,原子可形成分子,原子得失电子形成离子。所以a是离子、b原子、c是分子;
(3)“木”(木材)隔绝空气加强热可得到木煤气(主要成分为CO、H2、CH4)、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”不是元素。
(4)课本上元素的概念是:把的原子归为一类,每一类原子称为一种元素。其中“一类原子”包括质子数和中子数都相同的所有原子;质子数相同,中子数不同的所有原子。故选AC;
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子都是氢元素的原子,这是因为氢原子和重氢原子核内质子数都是1或核内质子数相同;从宏观的角度看,重水是由氢元素和氧元素组成的;
(6)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,在氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,因此氧化铝的化学式是Al2O3,其相对分子质量=27×2+16×3=102;
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家门捷列夫发现化学元素的周期性,排列出第一张元素周期表;
②结合图6分析镁原子不显电子的原因是原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反;
③图5中空白处元素的原子序数为20,相对原子质量为40.08,核外电子层数是4,位于元素周期表第四周期,最外层电子数是2,在化学反应中易失去电子,若用R表示该元素,R元素在化合物中的化合价是+2,氯元素在和R总称的化合物中的化合价是-1,化合物中元素化合价代数和为零,则R与氯组成的化合物的化学式为RCl2。
一、单选题(共17题)
1.下列各组物质中是按单质、化合物排列的是 ( )
A.生铁、二氧化碳 B.铜、铁锈 C.液氧、水 D.水银、稀硫酸
2.水是生命之源。下列说法正确的是
A.液态水变成水蒸气时,水分子变大 B.用活性炭吸附的方法能使硬水转化为软水
C.蒸馏或过滤均可使海水转化为淡水 D.电解水时负极和正极生成气体的体积比为2 :1
3.下列事实与物质的化学性质无关的是
A.二氧化碳可以和水反应生成碳酸 B.氧气可以供给呼吸
C.硫能在空气中燃烧 D.氯化钠的熔点是801℃
4.水是生命之源,下列有关水的叙述正确的是
A.为了防止水体污染,禁止使用农药化肥
B.在软水中加肥皂水揽拌后会出现大量浮渣
C.在沉淀、过滤、吸附、蒸馏等对水的净化操作中,净化程度最高的是蒸馏
D.水是由2个氢原子和1个氧原子构成的
5.2021年“世界水日”的主题为Valuin Waterw。下列关于水的说法合理的是
A.水是一种常用的溶剂
B.冰水混合物不是化合物
C.水中添加活性炭可将硬水转成软水
D.水电解生成氢气和氧气,说明水中含有氢分子和氧分子
6.水是生命之源。下列有关水的说法不正确的是( )
A.可用肥皂水区别硬水和软水
B.活性炭可通过吸附将自来水变为纯净水
C.生活中常用煮沸的方法软化硬水
D.电解水得到体积较大的气体具有可燃性
7.下列对宏观事实解释不正确的是
A.酒香不怕巷子深——分子不断运动
B.压瘪的乒乓球在热水中能鼓起来——温度升高,分子变大
C.水和过氧化氢的化学性质不同——分子构成不同
D.水通电生成氢气和氧气——化学反应中分子发生了改变
8.水是生命之源,关于水的说法不正确的是
A.用肥皂水区分硬水和软水 B.水的电解实验说明水由氢气和氧气组成
C.用蒸馏的方法可以将海水淡化 D.生活中提倡使用无磷洗衣粉防止水体污染
9.水是生命之源。下面有关水的说法正确的是
A.水通电分解时产生的氢气和氧气质量比为2︰1
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成的
C.用过滤的方法可以使硬水软化
D.如果将水样蒸干后有固体析出,这种水样中一定含有可溶性杂质
10.关于水的组成的正确说法是
A.由氢、氧组成 B.由氢气和氧气两种分子组成
C.由氢气和氧气组成 D.由氢、氧两种元素组成
11.下列日常生活中常发生的一些变化,属于化学变化的是( )
A.水蒸发 B.灯泡发光 C.蔗糖溶解 D.铁生锈
12.下列关于物质的构成说法正确的是
A.电解水实验,产生了氢气和氧气,说明水是由氢气和氧气组成的
B.H2O不仅可以表示水这种物质,还可以表示水的组成
C.水是由氢元素和氧元素组成的混合物
D.冰块与水混合后得到混合物
13.以下图象,能正确反映对应关系的是
A. 加热一定质量的氯酸钾固体
B. 铜丝在空气中加热
C. 木炭在盛有氧气的密闭容器内燃烧
D. 电解水生成两种气体
14.关于电解水实验的叙述正确的是
A.该实验说明水是由两个氢原子和一个氧原子构成的
B.试管a中的气体能使带火星的木条复燃
C.产生的和的质量比为1:8
D.发生反应的化学方程式为
15.水是生命之源,用如图所示的装置进行水的电解实验时,有以下描述:
①甲试管应该连接在电源的正极
②甲、乙两试管收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧,
④该实验说明水是由氢气和氧气组成的
以上描述中正确的是( )
A.
B.
C.
D.
16.中科院科研团队成功合成一种高效电解水催化剂,为未来解决氢能危机提供了可能。实验室采用如图装置电解水。下列关于电解水的叙述中错误的是
A.在水中加入一定量的稀硫酸是为了增强水的导电性
B.电解水的实验证明水是由氢、氧两种元素组成的
C.若A试管气体为10mL,则B试管气体为5mL
D.与电源正极相连的玻璃管B内得到的气体能在空气中燃烧
17.下列叙述中正确的是( )
A.水分子是保持水的性质的最小粒子
B.氧气的化学性质比较活泼,能够燃烧
C.电解水生成氢气和氧气的体积比为1:2
D.用水灭火,主要是使可燃物的温度降低到着火点以下
二、综合题(共5题)
18.2017年3月22日是第25届世界水日,宣传主题是“Wastewater”(废水),请回答下列与水有关的问题:
(1)废水中常含有难溶性杂质,除去这些杂质的操作是_____(填“过滤”、“吸附”或“蒸馏”),实验完成该操作所需的玻璃仪器除玻璃棒外还有_____(填序号),其中玻璃棒的作用是_____。
(2)除去难溶性杂质后,可利用活性炭_____(填“过滤”、“吸附”或“蒸馏”)废水中的异味和色素,污水经物理、化学或生化方法进行分级处理后得到中水,中水不可饮用,请列举中水的一项用途:_____。
(3)取某中水水样,滴加肥皂水,振荡,观察到泡沫较少,浮渣较多,该水样属于_____(填“硬水”或“软水”)。
(4)家庭用水水费清单中不包含的一项是_____(填序号)
A电费 B水资源费 C自来水费 D污水处理费
(5)如图2所示的是电解水 的实验过程。
①气体a为_____;
②通电时反应的化学方程式为_____;
③通电后中间球形容器内液面上升的原因是:_____。
19.电解水实验的电源是_________(“交流”或“直流”) , a试管中产生的气体是_____,b试管中的气体是______,检验方法为_______;此实验说明水是由________组成。此实验可能产生的气体体积比小于2:1,你能分析一下原因吗?(1种即可)_________
20.多角度认识物质,能帮助我们更全面了解物质世界.以水为例,回答下列问题:
(1)认识物质的组成和构成
①从宏观上看,水由____(填“元素”、“原子”或“分子”,下同)组成.
②从微观上看,水由_____构成.
(2)认识物质的性质:水通电能发生化学变化,反应的化学方程式为_____.
(3)获得物质的方法:地球上总储水量很大,但淡水很少,海水中溶解了很多物质,又苦又咸,除了含H2O外,还含大量的Na+、Ca2+、Cl﹣、Mg2+、SO42﹣等.以海水为原料提取食盐的工艺流程如图:
①图中a是___池(填“蒸发”或“冷却”).
②根据海水晒盐的原理,下列说法中不正确的是___.
A 得到的粗盐是纯净的氯化钠
B 在a中,海水中水的质量逐渐减少
C 在a中,海水中氯化钠的质量逐渐增加
D 海水进入储水池,海水的成分基本不变
③根据上述及工艺流程图,母液中所含的离子有___.
A Ca2+、Mg2+、SO42﹣等 B Na+、Ca2+、Cl﹣、Mg2+、SO42﹣、H2O等
C Ca2+、Mg2+、SO42﹣、H2O等 D Na+、Ca2+、Cl﹣、Mg2+、SO42﹣等
21.水是生命之源,请回答下列问题。
(1)如图为电解水的装置。用 ____ 来检验b管中的气体,b管中气体与a管中气体的质量比为 ___ 。由实验得出水是由 ____ 组成的。
(2)本市某水厂生产自来水的净化步骤如下图所示:
原水→加明矾→沉淀→吸附→沙滤→加氯气→净水
向水中通入氯气,其作用是 ______ ;向水中加入 ______ (填写物质名称),吸附除去其中的异昧。
22.探究物质组成的奥秘。元素之义,人们很早就意识到,所有物质都是由几种亘古不变的基本成分-“元素”组成的。古希腊学者提出复杂的物质世界是由“水、木、火和空气”四种基本成分组成的。
I.空气是元素吗?
(1)瑞典化学家舍勒发现,将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟罩内水面大约上升_____,被消耗的气体是氧气,该反应的文字表达式为_____,舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是_____(写化学式),上述实验证明空气是一种混合物,因此,空气不是元素。
II.水是元素吗?
(实验探究)
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,写出该变化的文字表达式_____ ,该反应的基本类型是_____。法国科学家拉瓦锡发现,水通电时能分解,写出此反应的文字表达式_____。
上述两个实验说明,水不是组成物质的元素。
①图2为电解水实验,请将下表填写完整。
实验方案 实验现象 结论
_____放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体_____,(写化学式),不是水蒸气
_____放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为_____,(写化学式),不是水蒸气
②实验表明,水通电后发生了化学变化。
化学变化中不变的微粒是_____,老师指出,该微粒也是构成物质的基本粒子。小组同学通过填写物质的构成及构成物质的粒子间的关系图,理解了老师的说法。请将图3中的a、b、c三处填写完整a_____、b_____、c_____。
III.木和火是元素吗?
(3)查阅资料:“木”(木材)隔绝空气加强热可得到木煤气[主要成分为一氧化碳(CO)、氢气(H2)、甲烷(CH4)]、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”_____(填“是”或“不是”)元素。“火”不属于物质,因此,“火”不是元素。
IV.元素的概念及其应用
(4)课本上元素的概念是:“把具有……的原子归为一类,每一类原子称为一种元素。”其中“一类原子”包括_____。
A 质子数和中子数都相同的所有原子
B 质子数不同,中子数相同的所有原子
C 质子数相同,中子数不同的所有原子
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子是否都是氢元素的原子,为什么? _____。从宏观的角度看,重水是由_____(填名称)元素组成的。
(6)世界上的物质都是由元素组成的,图4为地壳中的元素分布,地壳中含量最多的金属元素与氧元素形成的化合物的化学式为_____,其相对原子质量为_____。
元素密码——元素周期表
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家_____发现化学元素的周期性,排列出第一张元素周期表。成为科学家探索未知世界的有力工具。图5是元素周期表的一部分,空白部分被墨水沾黑,图6是镁原子的结构示意图。据图回答下列问题:
②结合图6分析镁原子不显电性的原因_____。
③图5中空白处元素的原子序数为_____,位于元素周期表第_____周期,若用R表示该元素,则R与氯元素组成的化合物的化学式为_____。
参考答案
1.C
【解析】
【详解】
A.生铁是混合物,二氧化碳是化合物,故不符合题意;
B.铜是单质,铁锈是混合物,故不符合题意;
C.液氧是单质,水是化合物,故符合题意;
D.水银是单质,稀硫酸是混合物,故不符合题意。故选C。
2.D
【详解】
A、液态水变成水蒸气时,水分子不变,分子间的间隔增大,故A错误;
B、活性炭能吸附水中的色素和异味,不能除去可溶性钙、镁化合物,用活性炭吸附的方法不能使硬水转化为软水,故B错误;
C、蒸馏能够得到淡水,过滤只能除去水中的不溶性杂质,不能除去水中的氯化钠等,不能得到淡水,故C错误;
D、水通电时,正极产生氧气,负极产生氢气,体积比为1:2。电解水时负极和正极生成气体的体积比为2:1,故D正确。故选D。
3.D
【解析】
【详解】
A. 二氧化碳可以和水反应生成碳酸在化学变化中体现出来,属于化学性质,选项错误;B. 氧气可以供给呼吸需要在化学变化中体现出来,属于化学性质,选项错误;C. 硫能在空气中燃烧生成新物质,属于化学性质,选项错误;D. 氯化钠的熔点是801℃,熔点属于物质的物理性质,选项正确,故选D。
4.C
【详解】
A、防止水体污染,应合理使用化肥和农药,不能禁止,该选项说法不正确;
B、将肥皂水滴到软水中,搅拌可以看到产生少量的浮渣,该选项说法不正确;
C、对水的净化操作中,蒸馏能除去水中所有的杂质,净化程度最高的是蒸馏,该选项说法正确;
D、1个水分子是由1个氧原子和2个氢原子构成,该选项说法不正确。
故选C。
5.A
【详解】
A、水是一种常用的溶剂,正确;
B、冰水混合物只有水一种物质,水是由氢氧元素组成的化合物,错误;
C、水中添加活性炭可以除去水中色素和异味,不能除去可溶性杂质,不能将硬水转成软水,错误;
D、水电解生成氢气和氧气,说明水是由氢氧元素组成的,错误。
故选A。
6.B
【详解】
A、肥皂水遇硬水会产生较多的浮渣,遇软水会产生较多的泡沫,可以据此进行鉴别。A正确;
B、活性炭具有吸附性,可以吸附水中的色素和异味,但是不能将自来水转化为纯净水。B错误;
C、天然水煮沸过程中,水中的可溶性钙镁化合物转化为沉淀,水的硬度下降,生活中常用煮沸的方法将硬水软化。C正确;
D、电解水得到的体积较大的气体是氢气,氢气具有可燃性。D正确。
故选B。
7.B
【详解】
A、酒香不怕巷子深说明分子不断运动,A正确;
B、压瘪的乒乓球在热水中能鼓起来是由于温度升高,分子之间的间隔变大,B错误;
C、水和过氧化氢的化学性质不同是由于分子构成不同,C正确;
D、水通电生成氢气和氧气说明化学反应中分子发生了改变,D正确。
故选B。
8.B
【详解】
A、硬水和软水的区别在于所含的钙镁离子的多少,可用肥皂水来区分硬水和软水,加入肥皂水,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,故选项说法正确。
B、电解水生成氢气和氧气,氢气和氧气分别是由氢元素和氧元素组成的,说明水是由氢元素和氧元素组成的,水中不含氢气和氧气,故选项说法错误。
C、将海水蒸馏,能将水从海水中分离出来,从而实现海水淡化,故选项说法正确。
D、无磷洗衣粉可以防止水体富营养化,生活中提倡使用无磷洗衣粉防止水体污染,故选项说法正确。
故选:B。
9.D
【详解】
A、水通电分解时产生的氢气和氧气体积比为2:1,故A错误;B、电解水生成氢气和氧气,说明水是由氢和氧两种元素组成的,故B错误;C、用过滤的方法只能除去水中不溶性的杂质,不能减少钙、镁离子化合物的含量,不可以使硬水软化,故C错误;D、如果将水样蒸干后有固体析出,这种水样中一定含有杂质,故D正确;故选:D。
10.D
【分析】
通过电解水生成氢气和氧气可知,水是由氢元素和氧元素组成的物质。
【详解】
A、水是由氢元素和氧元素组成的,该选项说法不正确;
B、水不是由氢分子和氧分子组成的,该选项说法不正确;
C、水不是由氢气和氧气组成,该选项说法不正确;
D、水是由氢、氧两种元素组成的,该选项说法正确。
故选:D。
11.D
【解析】
【分析】
没有新物质生成的变化是物理变化,有新物质生成的变化是化学变化;
【详解】
A、水的蒸发是液态的水变为气态的水,没有新物质生成,故是物理变化,故错误;
B、灯泡发光的过程中没有新物质的生成,是物理变化,故错误;
C、蔗糖溶解的过程中没有新物质生成,故是物理变化,故错误;
D、铁生锈的过程中有新物质氧化铁生成,故是化学变化,故正确。故选D。
12.B
【详解】
A、电解水实验,产生了氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,反应前后元素种类不变,说明水是由氢元素和氧元素组成的,选项说法不正确;
B、H2O不仅可以表示水这种物质,还可以表示水是由氢元素和氧元素组成,选项说法正确;
C、水是纯净物,由氢元素和氧元素组成,选项说法不正确;
D、冰块与水是同一种物质,混合后属于纯净物,选项说法不正确。
故选B。
13.B
【详解】
A.氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,氧气的质量从零开始逐渐增大,然后不变,故A错误;
B.铜和氧气在加热的条件下生成氧化铜,固体的质量逐渐增大,然后不变,故B正确;
C.木炭和氧气在点燃的条件下生成二氧化碳,二氧化碳的质量从零开始逐渐增大,然后不变,故C错误;
D.水在通电的条件下生成氢气和氧气的体积比是2:1,故D错误。
故选B。
14.C
【详解】
A、该实验说明水是由氢元素和氧元祖组成的;故选项错误。
B、试管a与电源负极连接,产生氢气,不能是带火星的木条复燃;故选项错误。
C、产生的H2和O2的质量比为1:8;故选项正确;
D、发生反应的化学方程式为:2H2O2H2↑+O2↑;
故选C。
15.B
【详解】
①甲试管中产生的气体最多应该是H2,乙试管中产生的气体应该是O2,所以甲试管应该连接在电源的负极,故①错误;
②甲乙两试管中产生的气体体积比约为2:1,故②正确;
③由上述分析可知,甲试管内生成的气体是氢气,氢气可以燃烧,故③正确;
④电解水实验生成了氢气和氧气,说明水是由氢元素和氧元素组成的,故④错误。
由以上分析可知,B符合题意。
故选B。
16.D
【详解】
A、在电解水时,常加入少量的硫酸溶液,可以增强水的导电性,以加快水的电解速度,故A正确;
B、电解水用直流电,正极产生的是氧气,负极产生的是氢气,因此可以证明水是由氢氧两种元素组成的,故B正确;
C、正极产生的是氧气,负极产生的是氢气,且氢气和氧气的体积比为2:1,因此B试管内是氧气,A试管内是氢气,因此若A试管内氢气是10mL,则B试管内的氧气是5mL,故C正确;
D、与电源正极相连的玻璃管B内得到的气体是氧气,能够支持燃烧,但不能燃烧,故D错误。
故选D。
17.D
【解析】
A、水分子是保持水的化学性质的最小粒子,故A错误;
B、氧气的化学性质比较活泼,能够支持燃烧,故B错误;
C、电解水生成氢气和氧气的体积比为2:1,故C错误;
D、燃烧的条件是可燃物与氧气接触,温度达到着火点;用水灭火,主要是使可燃物的温度降低到着火点以下,故D正确。
18.过滤 c、 引流 吸附 用于冲厕 硬水 A 氢气 2H2O2H2↑+O2↑ a、b两管内汇聚气体,气压变大,将水压入中间球形容器中
【详解】
(1)过滤能将液体与固体分离。废水中常含有难溶性杂质,通常采用的实验操作是过滤,还需要用到的玻璃仪器除烧杯、漏斗,故选C;其中玻璃棒的作用是引流;
(2)除去难溶性杂质后,可利用活性炭吸附废水中的异味和色素,“中水”的水质指标低于生活饮用水的水质标准,但又高于允许排放的污水的水质标准,处于二者之间,不可饮用但可用于冲厕、灌溉、景观用水、洗车等;
(3)向水中加入肥皂水时,如果产生大量的泡沫,说明是软水;如果产生的泡沫很少或不产生泡沫,说明是硬水。
(4)家庭生活用水水费清单中包含水资源费、自来水水费、污水处理费。不包含的一项是电费。故选A;
(5)水电解时,正极产生氧气,负极产生氢气,氢气和氧气的体积比为2:1。由如图是电解水实验装置可知。实验过程中,试管a产生的气体是电源的负极产生的气体较多是氢气
②水在通电条件下生成了氢气和氧气,反应的化学方程式是:;
③通电后中间球形容器内液面上升的原因是:a、b两管内汇聚气体,气压变大,将水压入中间球形容器中。
19.直流电 氢气 氧气 将带火星的木条伸入试管口,木条复燃,证明是氧气 氢、氧元素 氧气的溶解性大于氢气的溶解性
【详解】
电解水实验的电源是直流,由电解水的装置可知,a试管中产生的气体是电源的负极产生的气体较多是氢气,b试管中的气体是电源的正极产生的气体较少是氧气,具有助燃性,检验方法为:将带火星的木条伸入试管口,木条复燃,证明是氧气;此实验说明水是由氢、氧元素组成。此实验可能产生的气体体积比小于2:1,可能的原因是:氧气的溶解性大于氢气的溶解性。
20.元素 分子 蒸发 AC D
【详解】
(1)①从宏观上看,水由氢元素和氧元素组成,故填:元素;
②从微观上看,水由水分子组成,故填:分子;
(2)水在通电的条件下分解生成氢气和氧气,该反应的化学方程式为:;
(3)①因为氯化钠的溶解度受温度影响比较小,故应采取蒸发结晶的方法,故填:蒸发;
②A、粗盐中含有泥沙等难溶性杂质和一些可溶性杂质,故不是纯净的氯化钠,属于混合物,符合题意;
B、随着蒸发的不断进行,溶剂水不断减少,不符合题意;
C、在蒸发的过程中,溶剂质量不断减少,溶质质量不变,故溶液中氯化钠的质量不变,符合题意;
D、海水属于溶液,溶液具有均一、稳定性,故海水进入储水池,海水的成分基本不变,不符合题意
故选AC;
③大部分食盐在结晶析出的同时,也会有很少的其他的晶体从溶液中结晶析出,但溶液中仍旧会有少量的氯化钠,母液中可能含有的离子是:Na+、Ca2+、Cl﹣、Mg2+、SO42﹣。
故选D。
21.带火星的木条 8:1 氢元素和氧元素 杀菌消毒 活性炭
【详解】
(1)电解水时,正极生成的是氧气,负极生成氢气,氢气是氧气体积的2倍,b管内气体为氧气,氧气有助燃性,可用带火星的木条来检验b管中的气体,b管中气体与a管中气体的质量比等于水中氧、氢两种元素的质量比,为8:1。据质量守恒定律可知,反应前后元素的种类不变,由实验得出水是由氢元素和氧元素组成的;
(2)向水中通入氯气,能与生物细胞的基础物质蛋白质反应,其作用是杀菌消毒;向水中加入活性炭,吸附除去其中的异昧,因活性炭有吸附作用。
22.1/5 磷+氧气五氧化二磷 N2 氢气+氧气水 化合反应 水氢气+氧气 将燃着的木条 H2 将带火星的木条 O2 原子 离子 原子 分子 不是 AC 是,核内质子数都是1或核内质子数相同 由氢元素和氧元素组成的 Al2O3 102 门捷列夫 原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反 20 四 RCl2
【详解】
(1)将磷放在密闭钟罩内的水面上方燃烧(如图1所示),产生白烟(成分为五氧化二磷),一段时间后观察到钟置内水面大约上升五分之一,被消耗的气体是氧气,该反应的文字表达式为:磷+氧气五氧化二磷;舍勒接着把一支燃着的蜡烛放进剩余的空气里,蜡烛立即熄灭了。舍勒把不能支持蜡烛燃烧的空气称为“无效的空气”,其主要成分是N2,上述实验证明空气是可分的,因此,空气不是元素;
(2)1781年,英国科学卡文迪什通过实验发现,将氢气和氧气按一定比例混合点燃后能生成水,该变化的文字表达式为:氢气+氧气水,该反应是由两种物质生成一种物质的反应,其基本类型是化合反应;水通电生成氢气和氧气,反应的文字表达式为:水氢气+氧气;
①氢气具有可燃性,在空气中能安静地燃烧,产生淡蓝色火焰,放出热量;氧气具有助燃性能使带火星的木条复燃,常用来检验氧气。
实验方案 实验现象 结论
将燃着的木条放在玻璃管a尖嘴处,慢慢打开活塞,观察现象。 气体燃烧,发出淡蓝色火焰 玻璃管a上方收集的气体H2,,不是水蒸气
将带火星的木条放在玻璃管b尖嘴处,慢慢打开活塞,观察现象。 带火星的木条复燃 玻璃管b上方收集的气体为O2,不是水蒸气
②实验表明,水通电后发生了化学变化,该化学变化过程是:构成水分子的氢原子、氧原子重新结合成氢分子、氧分子,由此可见,化学变化中不变的微粒是原子;构成物质的微粒有分子、原子和离子,原子可形成分子,原子得失电子形成离子。所以a是离子、b原子、c是分子;
(3)“木”(木材)隔绝空气加强热可得到木煤气(主要成分为CO、H2、CH4)、木焦油、木炭等,这种生产方式化工生产中称为干馏,由此判断“木”不是元素。
(4)课本上元素的概念是:把的原子归为一类,每一类原子称为一种元素。其中“一类原子”包括质子数和中子数都相同的所有原子;质子数相同,中子数不同的所有原子。故选AC;
(5)水分子中的氢原子质子数为1,中子数为0,重水(D2O)分子中的重氢原子(符号“D”)质子数和中子数均为1,氢原子和重氢原子都是氢元素的原子,这是因为氢原子和重氢原子核内质子数都是1或核内质子数相同;从宏观的角度看,重水是由氢元素和氧元素组成的;
(6)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,在氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,因此氧化铝的化学式是Al2O3,其相对分子质量=27×2+16×3=102;
(7)①自元素被发现以来,科学家一直在寻找已发现元素的排列规律,1869年,俄国化学家门捷列夫发现化学元素的周期性,排列出第一张元素周期表;
②结合图6分析镁原子不显电子的原因是原子核带的正电荷数和核外电子带的负电荷数相等或原子核和核外电子所带的电荷电量相等,电性相反;
③图5中空白处元素的原子序数为20,相对原子质量为40.08,核外电子层数是4,位于元素周期表第四周期,最外层电子数是2,在化学反应中易失去电子,若用R表示该元素,R元素在化合物中的化合价是+2,氯元素在和R总称的化合物中的化合价是-1,化合物中元素化合价代数和为零,则R与氯组成的化合物的化学式为RCl2。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
