沪教版九年级化学上册 5.1金属的性质和利用 综合训练 (WORD版,含答案)
文档属性
| 名称 | 沪教版九年级化学上册 5.1金属的性质和利用 综合训练 (WORD版,含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 268.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-01 00:00:00 | ||
图片预览



文档简介
金属的性质和利用 综合训练
一、选择题(每题只有一个正确选项)
1.X、Y、Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性顺序是( )
(1)Z+YSO4=ZSO4+Y
(2)X+YSO4=XSO4+Y
(3)Z+H2SO4=ZSO4+H2↑
(4)X+H2SO4=不发生反应
A. Z>X>Y B. X>Y>Z
C. Z>Y>X D. X>Z>Y
2.为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
3.将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,对于该图像的理解正确的组合是
①A表示锌与稀硫酸的反应 ,方程式为:
Zn + H2SO4=ZnSO4 + H2↑
②B表示铁与稀硫酸的反应,方程式为2Fe + 3H2SO4 =Fe2(SO4)3 + 3H2↑
③反应结束后两种金属一定都有剩余
④反应结束后稀硫酸都没有剩余
⑤反应结束后消耗两种金属的质量相等
⑥反应结束后所得溶液质量相等
①②③ B.②④⑤⑥
C.③⑤⑥ D.①④
4.下列图像中能正确体现所叙述变化的相关信息的是( )
向Fe(NO3)2和Cu(NO3)2的混合溶液中加入过量的锌粉
B.向等质量的镁粉和锌粉中分别同时逐滴加入相同浓度的稀盐酸至过量
C.向生铁中加入足量的稀硫酸
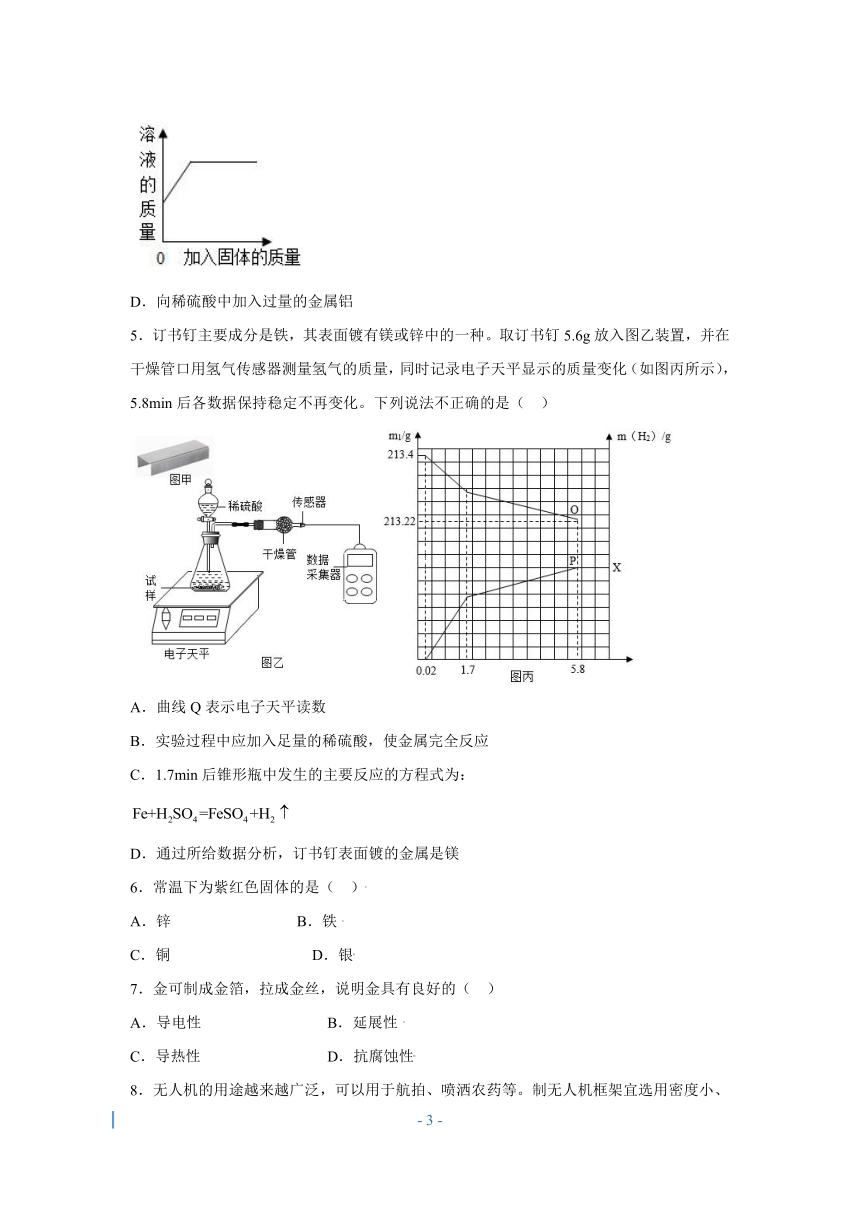
D.向稀硫酸中加入过量的金属铝
5.订书钉主要成分是铁,其表面镀有镁或锌中的一种。取订书钉5.6g放入图乙装置,并在干燥管口用氢气传感器测量氢气的质量,同时记录电子天平显示的质量变化(如图丙所示),5.8min后各数据保持稳定不再变化。下列说法不正确的是( )
A.曲线Q表示电子天平读数
B.实验过程中应加入足量的稀硫酸,使金属完全反应
C.1.7min后锥形瓶中发生的主要反应的方程式为:
D.通过所给数据分析,订书钉表面镀的金属是镁
6.常温下为紫红色固体的是( )
A.锌 B.铁
C.铜 D.银
7.金可制成金箔,拉成金丝,说明金具有良好的( )
A.导电性 B.延展性
C.导热性 D.抗腐蚀性
8.无人机的用途越来越广泛,可以用于航拍、喷洒农药等。制无人机框架宜选用密度小、强度高、硬度较大,化学稳定性好的金属材料,下列材料中最适合做无人机框架的是( )
生铁 B.黄铜
C.铝合金 D.纯铝
9.四川广汉三星堆出土的“青铜神树”让世人惊艳,史前文明或许存在。青铜属于( )
合金 B.盐
C.单质 D.化合物
10.合金和金属在生活中广泛应用,下列说法不正确的是( )
A.硬币镀镍或镀铜能提高耐腐蚀性
B.铝常常用于户外输电线,是因为铝的化学性质不活泼
C.不锈钢是通过改变金属内部结构来提高抗腐蚀和抗氧化能力
D.钛合金与人体有良好的“相容性”在医疗上可用于制造人骨替代品
11.下列有关金属的说法正确的是( )
A.所有金属都呈银白色
B.常温下所有的金属都是固体
C.合金的硬度一般比各成分金属小
D.铝制品耐腐蚀是因为表面生成致密氧化膜
12.下列反应属于置换反应的是( )
A. 3Fe+2O2 Fe3O4
B. CaCO3 CaO+CO2↑
C. 2KMnO4 K2MnO4+MnO2+O2↑
D. Cl2+2KI=2KCl+I2
13.把铁钉放入稀硫酸中,以下对该实验现象的描述不正确的是( )
①铁钉表面有气泡产生 ②溶液变为浅绿色 ③铁钉质量增加 ④溶液质量减轻
①② B.③④
C.①②③ D.①②③④
14.铜粉中含有少量的铁粉,最佳的除铁办法是( )
A.加入足量稀硫酸,过滤
B.在空气中灼烧
C.高温下加热并通入氢气
D.加入足量硝酸银溶液,过滤
15.若金属锰在金属活动性顺序中位于铝和锌之间,则下列反应不能发生的是(提示:MnSO4溶于水)( )
Mn+2HCl=MnCl2+H2↑
Fe+MnSO4=FeSO4+Mn
2Al+3MnSO4=Al2(SO4)3+3Mn
Mg+MnSO4=MgSO4+Mn
二、非选择题
16.2021年3月,四川"三星堆遗址"已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有_____
A.象牙 B.黄金
C.丝织品 D.青铜
(2)青铜的硬度比纯铜______(填大或"小")。
(3)铜制品长期暴露在空气中能与空气中的 O2、H2O 和______化合生成铜锈(主要成分是 Cu2(OH)2CO3)。
(4)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为______。
17.2020年12月,“嫦娥五号”返回器携带的月球土壤样品,对于全面科学探测月球地质、资源等方面的信息有重要意义。
(1)地球和月球上都有单质形式存在的金、银,说明它们的化学性质______。
(2)月球上存在天然的铁、铝等金属颗粒而地球上没有的原因是______。
(3)从金、银、铁、铝混合金属中回收金、银。将混合金属放入一定量的硝酸银溶液中充分反应后过滤,得到滤渣和浅绿色溶液,向滤渣中加入一定量稀盐酸,有气泡产生。
①滤渣中一定含有的金属是______。
②硝酸银溶液和铁反应的化学方程式为______。
(4)不论月球土壤材料还是地球土壤材料,人类的使用过程是相似的。已知人类冶炼和使用金属的历史年代数据如下图:
从图中,你得到的结论是______。
18.金属材料与人类生活息息相关,请回答下列问题。
(1)钛元素在元素周期表中的信息如右图所示,则钛的相对原子质量是______。
(2)家用台灯通常采用铜质插头,是利用金属铜的______性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是______。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是______;若滤液显蓝色,则滤液中溶质一定有______。
19.用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平.锌片、铁片、镁片.5%盐酸、20%盐酸.
(一)不同金属与酸反应的快慢不同
取质量相等的上述两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示。
(1)金属活动性顺序表(填元素符号)K、Ca、Na、_____、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au
(2)线B对应的金属为 _____。
(3)线A对应的金属与稀盐酸反应的化学方程式 _____。
(二)金属与不同质量分数的盐酸反应的快慢不同
(4)取质量相等的锌片,分别放入5%、20%的足量稀盐酸中.生成氢气的质量为m,反应时间为t.5%的盐酸与锌片反应m与t的关系曲线如图2所示.请在该图上补画出20%的盐酸与锌片反应m与t的关系曲线_____。实验表明,盐酸质量分数越大,与金属反应的速率越快。
(三)温度对金属与盐酸反应速率也有影响
(5)取两个烧杯,分别加入等质量的 _____(“同种”、“不同种”)金属,再分别加入足量的质量分数 _____(“相同”、“不相同”)的稀盐酸。实验表明,温度越高,盐酸与金属反应的速率越快。
答案
1-15 ABDDD CBCAB DDBAB
- 7 -
一、选择题(每题只有一个正确选项)
1.X、Y、Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性顺序是( )
(1)Z+YSO4=ZSO4+Y
(2)X+YSO4=XSO4+Y
(3)Z+H2SO4=ZSO4+H2↑
(4)X+H2SO4=不发生反应
A. Z>X>Y B. X>Y>Z
C. Z>Y>X D. X>Z>Y
2.为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
3.将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,对于该图像的理解正确的组合是
①A表示锌与稀硫酸的反应 ,方程式为:
Zn + H2SO4=ZnSO4 + H2↑
②B表示铁与稀硫酸的反应,方程式为2Fe + 3H2SO4 =Fe2(SO4)3 + 3H2↑
③反应结束后两种金属一定都有剩余
④反应结束后稀硫酸都没有剩余
⑤反应结束后消耗两种金属的质量相等
⑥反应结束后所得溶液质量相等
①②③ B.②④⑤⑥
C.③⑤⑥ D.①④
4.下列图像中能正确体现所叙述变化的相关信息的是( )
向Fe(NO3)2和Cu(NO3)2的混合溶液中加入过量的锌粉
B.向等质量的镁粉和锌粉中分别同时逐滴加入相同浓度的稀盐酸至过量
C.向生铁中加入足量的稀硫酸
D.向稀硫酸中加入过量的金属铝
5.订书钉主要成分是铁,其表面镀有镁或锌中的一种。取订书钉5.6g放入图乙装置,并在干燥管口用氢气传感器测量氢气的质量,同时记录电子天平显示的质量变化(如图丙所示),5.8min后各数据保持稳定不再变化。下列说法不正确的是( )
A.曲线Q表示电子天平读数
B.实验过程中应加入足量的稀硫酸,使金属完全反应
C.1.7min后锥形瓶中发生的主要反应的方程式为:
D.通过所给数据分析,订书钉表面镀的金属是镁
6.常温下为紫红色固体的是( )
A.锌 B.铁
C.铜 D.银
7.金可制成金箔,拉成金丝,说明金具有良好的( )
A.导电性 B.延展性
C.导热性 D.抗腐蚀性
8.无人机的用途越来越广泛,可以用于航拍、喷洒农药等。制无人机框架宜选用密度小、强度高、硬度较大,化学稳定性好的金属材料,下列材料中最适合做无人机框架的是( )
生铁 B.黄铜
C.铝合金 D.纯铝
9.四川广汉三星堆出土的“青铜神树”让世人惊艳,史前文明或许存在。青铜属于( )
合金 B.盐
C.单质 D.化合物
10.合金和金属在生活中广泛应用,下列说法不正确的是( )
A.硬币镀镍或镀铜能提高耐腐蚀性
B.铝常常用于户外输电线,是因为铝的化学性质不活泼
C.不锈钢是通过改变金属内部结构来提高抗腐蚀和抗氧化能力
D.钛合金与人体有良好的“相容性”在医疗上可用于制造人骨替代品
11.下列有关金属的说法正确的是( )
A.所有金属都呈银白色
B.常温下所有的金属都是固体
C.合金的硬度一般比各成分金属小
D.铝制品耐腐蚀是因为表面生成致密氧化膜
12.下列反应属于置换反应的是( )
A. 3Fe+2O2 Fe3O4
B. CaCO3 CaO+CO2↑
C. 2KMnO4 K2MnO4+MnO2+O2↑
D. Cl2+2KI=2KCl+I2
13.把铁钉放入稀硫酸中,以下对该实验现象的描述不正确的是( )
①铁钉表面有气泡产生 ②溶液变为浅绿色 ③铁钉质量增加 ④溶液质量减轻
①② B.③④
C.①②③ D.①②③④
14.铜粉中含有少量的铁粉,最佳的除铁办法是( )
A.加入足量稀硫酸,过滤
B.在空气中灼烧
C.高温下加热并通入氢气
D.加入足量硝酸银溶液,过滤
15.若金属锰在金属活动性顺序中位于铝和锌之间,则下列反应不能发生的是(提示:MnSO4溶于水)( )
Mn+2HCl=MnCl2+H2↑
Fe+MnSO4=FeSO4+Mn
2Al+3MnSO4=Al2(SO4)3+3Mn
Mg+MnSO4=MgSO4+Mn
二、非选择题
16.2021年3月,四川"三星堆遗址"已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有_____
A.象牙 B.黄金
C.丝织品 D.青铜
(2)青铜的硬度比纯铜______(填大或"小")。
(3)铜制品长期暴露在空气中能与空气中的 O2、H2O 和______化合生成铜锈(主要成分是 Cu2(OH)2CO3)。
(4)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为______。
17.2020年12月,“嫦娥五号”返回器携带的月球土壤样品,对于全面科学探测月球地质、资源等方面的信息有重要意义。
(1)地球和月球上都有单质形式存在的金、银,说明它们的化学性质______。
(2)月球上存在天然的铁、铝等金属颗粒而地球上没有的原因是______。
(3)从金、银、铁、铝混合金属中回收金、银。将混合金属放入一定量的硝酸银溶液中充分反应后过滤,得到滤渣和浅绿色溶液,向滤渣中加入一定量稀盐酸,有气泡产生。
①滤渣中一定含有的金属是______。
②硝酸银溶液和铁反应的化学方程式为______。
(4)不论月球土壤材料还是地球土壤材料,人类的使用过程是相似的。已知人类冶炼和使用金属的历史年代数据如下图:
从图中,你得到的结论是______。
18.金属材料与人类生活息息相关,请回答下列问题。
(1)钛元素在元素周期表中的信息如右图所示,则钛的相对原子质量是______。
(2)家用台灯通常采用铜质插头,是利用金属铜的______性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是______。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是______;若滤液显蓝色,则滤液中溶质一定有______。
19.用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平.锌片、铁片、镁片.5%盐酸、20%盐酸.
(一)不同金属与酸反应的快慢不同
取质量相等的上述两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示。
(1)金属活动性顺序表(填元素符号)K、Ca、Na、_____、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au
(2)线B对应的金属为 _____。
(3)线A对应的金属与稀盐酸反应的化学方程式 _____。
(二)金属与不同质量分数的盐酸反应的快慢不同
(4)取质量相等的锌片,分别放入5%、20%的足量稀盐酸中.生成氢气的质量为m,反应时间为t.5%的盐酸与锌片反应m与t的关系曲线如图2所示.请在该图上补画出20%的盐酸与锌片反应m与t的关系曲线_____。实验表明,盐酸质量分数越大,与金属反应的速率越快。
(三)温度对金属与盐酸反应速率也有影响
(5)取两个烧杯,分别加入等质量的 _____(“同种”、“不同种”)金属,再分别加入足量的质量分数 _____(“相同”、“不相同”)的稀盐酸。实验表明,温度越高,盐酸与金属反应的速率越快。
答案
1-15 ABDDD CBCAB DDBAB
- 7 -
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
