2021-2022学年高一上学期生物人教版(2019)必修1 5.1降低化学反应活化能的酶课件 (39张ppt)
文档属性
| 名称 | 2021-2022学年高一上学期生物人教版(2019)必修1 5.1降低化学反应活化能的酶课件 (39张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 13.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2021-12-01 20:41:53 | ||
图片预览






文档简介
(共39张PPT)
5.1降低化学反应活化能的酶
问题探讨
1773年意大利科学家斯帕兰札尼做了一个巧妙的实验:将肉块放入小巧的金属笼内,然后让鸡把小笼子吞下去。过一段时间后,他把小笼子取出来,发现笼内肉块消失了。
讨论
1.将肉块放入金属笼内可以排除物理消化还是化学消化?
收集胃内的化学物质,看看这些物质在体外是否也能将肉块分解。
结论:食物在胃中的消化,靠的是胃液中的某种物质。
3.怎样证明你的推测?
2.是什么物质使肉块消失了?
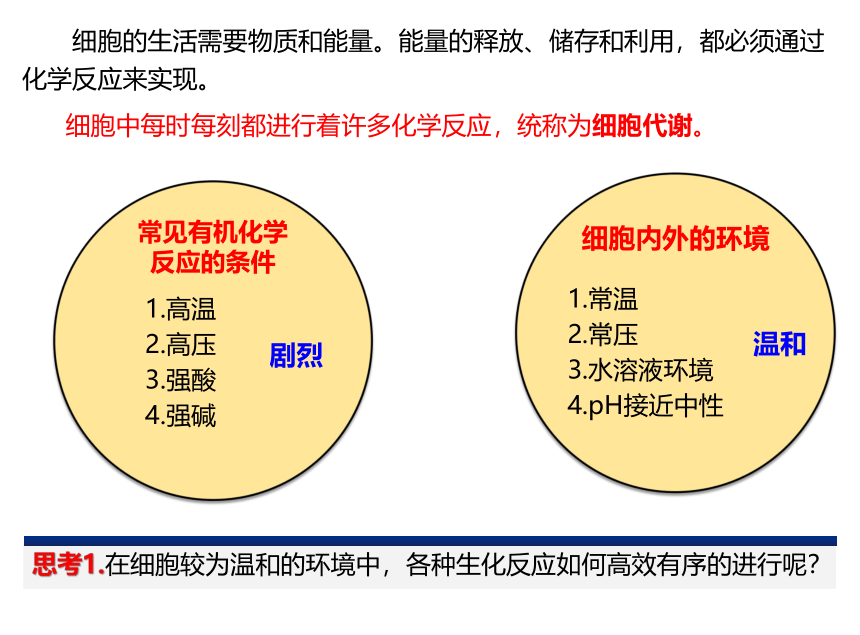
细胞内外的环境
常温
常压
水溶液环境
pH接近中性
温和
思考1.在细胞较为温和的环境中,各种生化反应如何高效有序的进行呢?
细胞的生活需要物质和能量。能量的释放、储存和利用,都必须通过化学反应来实现。
细胞中每时每刻都进行着许多化学反应,统称为细胞代谢。
常见有机化学反应的条件
高温
高压
强酸
强碱
剧烈
一、酶在代谢中的作用
1.探究实验:比较过氧化氢在不同条件下的分解
①实验原理
2H2O2 2H2O + O2
通过O2的产生量判断H2O2的分解情况
②实验目的
通过比较过氧化氢在不同条件下的分解的快慢,了解过氧化氢酶的作用。
加热是化学反应的常见条件
Fe3+是无机催化剂
新鲜的肝脏中含有过氧化氢酶
细胞代谢中也会产生代谢废物,甚至会产生对细胞有害的物质,如过氧化氢,细胞中有过氧化氢酶,能将过氧化氢及时分解为氧气和水。新鲜肝脏中有较多的过氧化氢酶。
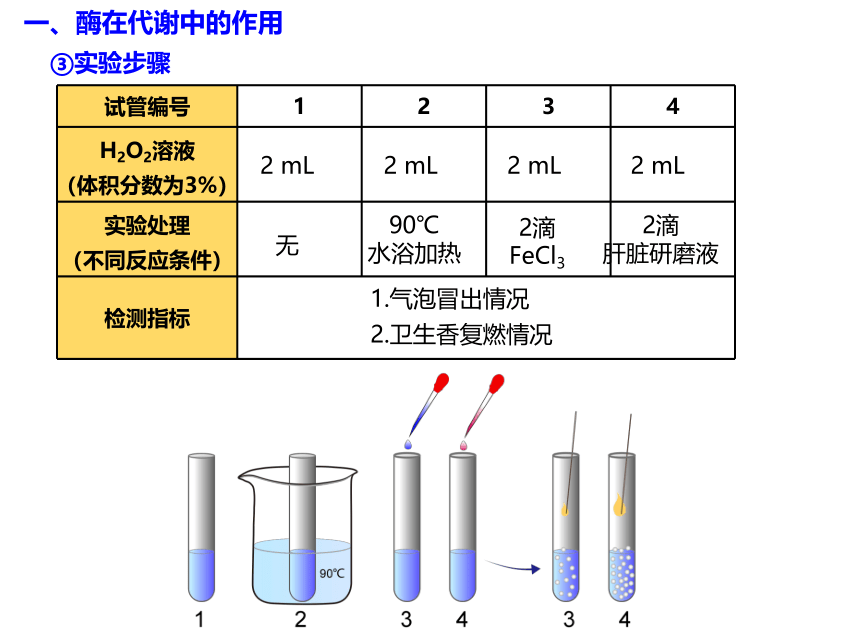
③实验步骤
一、酶在代谢中的作用
试管编号 1 2 3 4
H2O2溶液 (体积分数为3%)
实验处理 (不同反应条件)
检测指标 2 mL
2 mL
2 mL
2 mL
无
90℃
水浴加热
2滴
FeCl3
2滴
肝脏研磨液
1.气泡冒出情况
2.卫生香复燃情况
讨论
1.与1号试管相比,2号试管出现了什么不同的现象?这一现象说明什么?
2号试管放出的气泡多,这一现象说明加热促进过氧化氢的分解,提高反应速率。
2.在细胞内,能通过加热来提高反应速率吗?
不能。
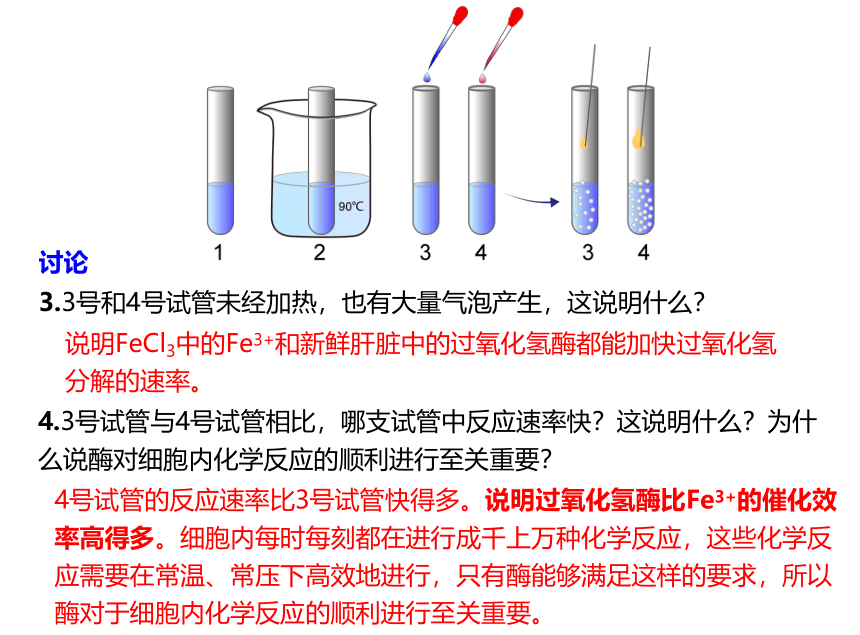
讨论
4.3号试管与4号试管相比,哪支试管中反应速率快?这说明什么?为什么说酶对细胞内化学反应的顺利进行至关重要?
3.3号和4号试管未经加热,也有大量气泡产生,这说明什么?
说明FeCl3中的Fe3+和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率。
4号试管的反应速率比3号试管快得多。说明过氧化氢酶比Fe3+的催化效率高得多。细胞内每时每刻都在进行成千上万种化学反应,这些化学反应需要在常温、常压下高效地进行,只有酶能够满足这样的要求,所以酶对于细胞内化学反应的顺利进行至关重要。
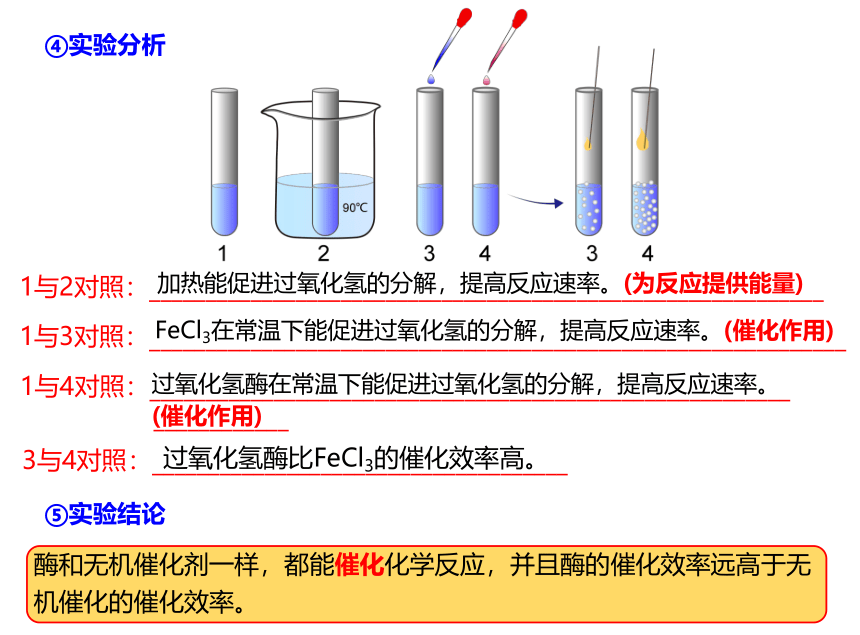
1与2对照:____________________________________________________________
加热能促进过氧化氢的分解,提高反应速率。(为反应提供能量)
1与3对照:______________________________________________________________
FeCl3在常温下能促进过氧化氢的分解,提高反应速率。(催化作用)
1与4对照:_________________________________________________________
____________
过氧化氢酶在常温下能促进过氧化氢的分解,提高反应速率。(催化作用)
④实验分析
3与4对照:_____________________________________
过氧化氢酶比FeCl3的催化效率高。
酶和无机催化剂一样,都能催化化学反应,并且酶的催化效率远高于无机催化的催化效率。
⑤实验结论
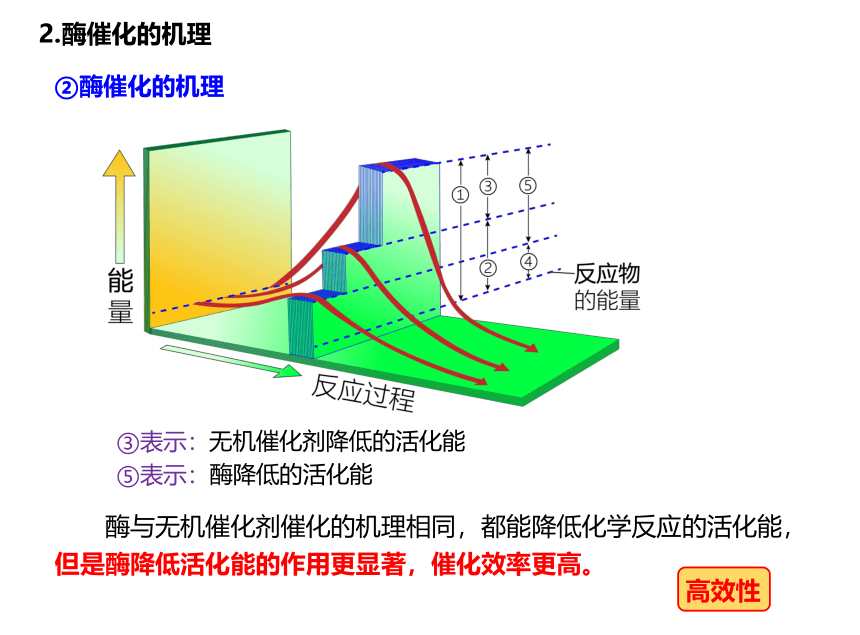
2.酶催化的机理
分子从常态转变为容易发生化学反应的活跃态所需要的能量。
①活化能
图中①表示:
图中②表示:
图中④表示:
无催化剂时化学反应所需的活化能。
无机催化剂催化时化学反应所需的活化能。
酶催化时化学反应所需的活化能。
2.酶催化的机理
②酶催化的机理
③表示:
⑤表示:
无机催化剂降低的活化能
酶降低的活化能
酶与无机催化剂催化的机理相同,都能降低化学反应的活化能,但是酶降低活化能的作用更显著,催化效率更高。
高效性
试管编号 1 2 3 4
H2O2溶液 (体积分数为3%) 2 mL 2 mL 2 mL 2 mL
实验处理 (不同反应条件) 无 90℃ 水浴加热 2滴 FeCl3 2滴
肝脏研磨液
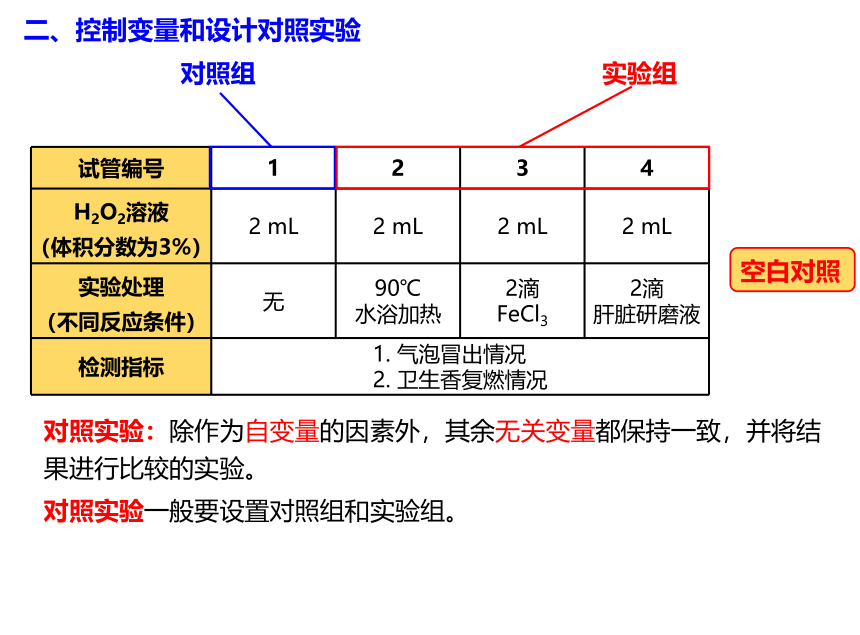
检测指标 1. 气泡冒出情况 2. 卫生香复燃情况 二、控制变量和设计对照实验
变量:实验过程中的变化因素
自变量:人为控制的对实验对象进行处理的因素
无关变量:实验过程中存在的其他一些会对实验结果造成影响的可变因素
因变量:因自变量改变而变化的变量
试管编号 1 2 3 4
H2O2溶液 (体积分数为3%) 2 mL 2 mL 2 mL 2 mL
实验处理 (不同反应条件) 无 90℃ 水浴加热 2滴 FeCl3 2滴
肝脏研磨液
检测指标 1. 气泡冒出情况 2. 卫生香复燃情况 二、控制变量和设计对照实验
对照实验:除作为自变量的因素外,其余无关变量都保持一致,并将结果进行比较的实验。
对照实验一般要设置对照组和实验组。
对照组
实验组
空白对照
空白对照
在未真正做实验之前,结果就已知的那组就是对照组;而结果未知的那组是实验组。
空白对照指不做任何实验的对照组或不给对照组以任何处理因素。
注意:不给对照组任何处理因素是相对实验组而言的,实际上对照组还是要做一定的处理,只是不加实验组的处理因素,或者说相对于实验组而言,除实验变量外,别的处理与实验组完全相同。
1.有人设计实验探究有机肥是否能提高土壤肥力并优于化肥。实验分为两组,一组农田施有机肥,一组农田施化肥。该实验设计缺少__________________________________________。
随堂练习
In-class practice
既不施用有机肥也不施用化肥的对照田
自身对照
实验处理前的对象状况为对照组,实验处理后的对象变化则为实验组。
自身对照指对照组和实验组都在同一研究对象上进行,不另设对照。自身对照方法简便,关键是看清实验处理前后现象变化的差异。
第一次对照:质壁分离状态与自然状态形成对照;
第二次对照:复原后状态与质壁分离状态形成对照
李毕希(J.V.Liebig)
巴斯德(L.Pasteur)
发酵是由酵母菌细胞的存在所致,没有活细胞的参与,糖类是不可能变成酒精的。
发酵是酵母菌细胞中的某些物质,但这些物质只有在酵母菌细胞死亡并裂解后才能发挥作用。
三、酶的本质
思考2.对于死酵母细胞,它已经失去了生命活动还有可能引起发酵吗?结合前面两位科学家的观点,还有其他的可能吗?
活酵母细胞中的物质
毕希纳(E.Buchner)
酵母细胞的某些物质能够在酵母细胞破碎后继续起作用,就像在活酵母细胞中一样。
萨姆纳从刀豆种子中提取到脲酶,并证明脲酶是蛋白质。
萨姆纳(J.B.Sumner)
切赫(T.R.Cech)和 奥尔特曼(S.Altman)
少数RNA也具有生物催化功能。
思考3.综合酶本质的探索历程,能不能给酶下一个比较完整的定义?
酶是__________产生的具有___________的_________,其中绝大多数酶是__________,少数酶是________。
活细胞
催化作用
有机物
蛋白质
RNA
标准蛋白质样液
标准RNA样液
待测酶液
均发生紫色反应
该酶是蛋白质
均呈现红色
该酶是RNA
分别加入 双缩脲试剂
分别加入 吡罗红染液
三、酶的特性
1.高效性
与无机催化剂相比,酶能更显著地降低反应的活化能。
思考4.设计实验验证酶具有高效性时,对照组和实验组应该如何设计呢?
2.专一性
思考5.口腔里有唾液淀粉酶,为什么塞进牙缝的肉丝两天后还没被消化?
三、酶的特性
探究实验:淀粉酶对淀粉和蔗糖的水解作用
序号 项目 试管1 试管2
1 注入可溶性淀粉溶液 2mL ——
2 注入蔗糖溶液 —— 2mL
3 注入淀粉酶溶液 2mL 2mL
4 保温5min 5 注入斐林试剂2mL 6 沸水浴加热1min 7 观察记录试管中有无砖红色沉淀 实验结论:
淀粉酶只能催化淀粉水解不能催化蔗糖水解。
酶具有专一性:一种酶只能催化一种或一类化学反应。
—— 保证了细胞内化学反应有序进行
2.专一性
三、酶的特性
探究实验:淀粉酶对淀粉和蔗糖的水解作用
序号 项目 试管1 试管2
1 注入可溶性淀粉溶液 2mL ——
2 注入蔗糖溶液 —— 2mL
3 注入淀粉酶溶液 2mL 2mL
4 保温5min 5 注入斐林试剂2mL 6 沸水浴加热1min 7 观察记录试管中有无砖红色沉淀
思考6.本实验中,是否可用碘液检测淀粉和蔗糖是否发生了水解?
不能;因为实验组和对照组实验现象相同,不能说明淀粉酶对蔗糖是否起作用。
方案二:
淀粉 + 蔗糖酶
蔗糖 + 蔗糖酶
方案四:
蔗糖 + 淀粉酶
蔗糖 + 蔗糖酶
方案一:
淀粉 + 淀粉酶
蔗糖 + 淀粉酶
方案三:
淀粉 + 淀粉酶
淀粉 + 蔗糖酶
思路1:底物不同,酶相同
思路2:底物相同,酶不同
用斐林试剂检测
用斐林试剂检测
用斐林试剂检测
用碘液或者斐林试剂检测
2.下图表示的是某类酶作用的模型。尝试用文字描述这个模型。这个模型能解释酶的什么特性?
这个模型中 A 代表某类酶,B 代表底物,C 和 D 代表产物。这个模型的含义是:酶 A与底物 B 专一性结合,催化反应的发生,产生了产物 C 和 D。这个模型可以类比解释酶的专一性。
随堂练习
In-class practice
锁钥学说
酶和无机催化剂在反应前后数量和性质不发生改变,一段时间内可以重复利用。
3.内质网应激时,会导致Ca2+从内质网腔释放到细胞质基质中与钙蛋白酶原结合,钙蛋白酶原被Ca2+激活后可水解多种蛋白质,诱导细胞凋亡。钙蛋白酶可水解多种蛋白质说明该酶不具有专一性( )
×
随堂练习
In-class practice
有的酶对底物的要求比绝对专一性要低一些,可以作用于一类结构相似的底物,即能催化一类化学反应。比如,胃蛋白酶催化具有苯丙氨酸、酪氨酸、色氨酸以及亮氨酸、谷氨酸、谷氨酰胺等肽键的断裂,使大分子的蛋白质变为较小分子的多肽;胰蛋白酶水解碱性氨基酸(赖氨酸、精氨酸)的残基与其他氨基酸的氨基形成的肽键,产物是以碱性氨基酸作为羧基末端的多肽和少量碱性氨基酸;这就是酶的“相对专一性”。
酶催化特定化学反应的能力称为酶活性。
酶活性可用在一定条件下酶所催化某一化学反应的速率表示。
3.酶作用条件温和
三、酶的特性
探究实验一:探究温度对酶活性的影响
阅读课本82-83页,借助课本中的材料,设计实验。
①选择哪一种酶做实验材料?为什么?
②本实验的自变量、因变量分别是什么?用什么方法控制自变量?
③你将设定哪几个温度?怎样控制温度,哪个是对照组,哪个是实验组?
④在设计这一实验中最关键的一步是什么? 提示:(在酶与反应底物接触前就应该用相应的温度处理酶和反应底物)。
⑤你所预期的对照组和实验组的现象或结果是什么?
3.酶作用条件温和
三、酶的特性
探究实验一:探究温度对酶活性的影响
操作步骤 1号试管 2号试管 3号试管 4号试管 5号试管 6号试管
0℃ 0℃ 50℃ 50℃ 100℃ 100℃
第一步 2 mL — 2 mL — 2 mL —
第二步 — 2 mL — 2 mL — 2 mL
第三步 在各自温度下保温5 min 第四步 将2号加入1号中 将4号加入3号中 将6号加入5号中 第五步 在各自温度下保温5 min 第六步 2滴 2滴 2滴 实验现象 变蓝
不变蓝
变蓝
实验结论:
温度过低或过高酶活性都较低。
思考·讨论
1.如何进一步探究淀粉酶的最适温度?
缩小温度梯度,重复进行上述实验。
酶活性受温度影响示意图
最适温度
在最适温度条件下,酶的活性最高,温度偏高或偏低,酶的活性都会明显降低。
一般来说,动物体内酶的最适温度在35~40℃之间;植物体内酶的最适温度在40~50℃之间;细菌和真菌体内酶最适温度差别较大,有的酶最适温度可高达70℃。
思考·讨论
2.为什么不能用斐林试剂对实验结果进行检测?
该实验的自变量是温度,用斐林试剂检测时需要水浴加热,
这样会干扰自变量。
3.为什么不能用过氧化氢酶和过氧化氢来探究温度对酶活性的影响?
因为过氧化氢本身受热易分解,会对实验结果造成干扰。
操作步骤 1号试管 2号试管 3号试管
第一步 加入2滴肝脏研磨液 第二步 1mL pH=7的缓冲液 1mL 盐酸溶液 1mL NaOH溶液
第三步 加入2mL的H2O2溶液 第四步 观察气泡生成速率,或插入卫生香,观察复燃所需时间 实验现象 产生大量气泡
产生少量气泡
产生少量气泡
探究实验二:探究pH对酶活性的影响
3.酶作用条件温和
三、酶的特性
实验结论:
pH过低或过高酶活性都较低。
在最适pH条件下,酶的活性最高,pH偏高或偏低,酶的活性都会明显降低。
最适pH
酶活性受pH影响示意图
1.如何进一步探究过氧化氢酶的最适pH?
思考·讨论
缩小温度梯度,重复进行上述实验。
动物体内酶的最适pH大多在6.5~8.0,但也有例外,如胃蛋白酶的最适pH为1.5;植物体内的酶的最适pH大多为4.5~6.5。
高温、强酸、强碱会使酶的空间结构遭到破坏,使酶永久失活。
温度和pH偏高或偏低,酶的活性都会明显降低。
低温使酶活性受抑制,温度恢复,酶活性可以恢复。
4.下列有关酶的实验设计思路错误的是( )
A.利用过氧化氢和过氧化氢酶探究温度对酶活性的影响
B.利用淀粉、蔗糖、淀粉酶和碘液验证酶的专一性
C.利用过氧化氢、新鲜的猪肝研磨液和蒸馏水研究酶的高效性
D.利用胃蛋白酶、蛋清和pH分别为3、7、11的缓冲液验证pH对酶活性
的影响
ABCD
随堂练习
In-class practice
四、影响酶促反应速率的因素
1.酶促反应:
由酶催化的化学反应,生物体内的化学反应绝大多数属于酶促反应。
2.酶促反应速率:
3.影响酶促反应速率的因素:
单位时间内反应物或生成物浓度的改变量。
pH
温度
抑制剂
激活剂
酶活性
酶浓度
底物浓度
酶促反应速率
底物与酶的接触面积
★酶活性≠酶促反应速率
①酶浓度(底物有限)
a
b
c
ab:
在一定的酶浓度范围内,随酶浓度的增加,反应速率增加
N
酶浓度
反应速率
0
b:
当酶浓度增大到某一值时,反应速率达到最大值,不再增加
酶浓度较低,底物没有完全被酶结合
底物完全被酶结合
②底物浓度(酶有限)
a
b
c
ab:
在一定的酶浓度范围内,随酶浓度的增加,反应速率增加
N
底物浓度
反应速率
0
b:
当酶浓度增大到某一值时,反应速率达到最大值,不再增加
酶浓度较低,底物没有完全被酶结合
底物完全被酶结合
5.酶抑制剂分竞争性抑制剂和非竞争性抑制剂,两者作用特点如图甲所示,图乙表示相应的反应速度。下列有关叙述不正确的是( )
活性中心
底物
竞争性抑制剂
A
B
C
甲
非竞争性抑制剂
底物
乙
反应速度
底物浓度
a
b
c
酶
酶
酶
B
竞争性抑制剂的抑制作用可以通过增大底物的浓度来抵消其抑制作用;
非竞争性抑制剂其抑制作用不能通过增加底物的浓度来抵消其抑制作用
A.曲线a表示没有酶抑制剂存在时的作用效果
B.曲线c表示在竞争性抑制剂作用下酶的活性降低
C.曲线a、b反应速率不再增加是受酶浓度的限制
D.竞争性抑制剂与该酶催化的底物结构相似
随堂练习
In-class practice
五、酶的应用
1.溶菌酶
溶解细菌细胞壁,具有抗菌消炎的作用。在临床上与抗生素混合使用,能增强抗生素的疗效。
五、酶的应用
2.果胶酶
分解果肉内细胞壁中的果胶,提高果汁产量,使果汁变得澄清。
五、酶的应用
3.多酶片
普通糖衣—胃蛋白酶—肠溶衣糖衣—胰酶
普通糖衣保护胃蛋白酶,在胃液中会分解,释放出胃蛋白酶。
肠溶衣保护胰酶,在胃液中不会分解,在小肠中分解,释放出胰酶。
5.1降低化学反应活化能的酶
问题探讨
1773年意大利科学家斯帕兰札尼做了一个巧妙的实验:将肉块放入小巧的金属笼内,然后让鸡把小笼子吞下去。过一段时间后,他把小笼子取出来,发现笼内肉块消失了。
讨论
1.将肉块放入金属笼内可以排除物理消化还是化学消化?
收集胃内的化学物质,看看这些物质在体外是否也能将肉块分解。
结论:食物在胃中的消化,靠的是胃液中的某种物质。
3.怎样证明你的推测?
2.是什么物质使肉块消失了?
细胞内外的环境
常温
常压
水溶液环境
pH接近中性
温和
思考1.在细胞较为温和的环境中,各种生化反应如何高效有序的进行呢?
细胞的生活需要物质和能量。能量的释放、储存和利用,都必须通过化学反应来实现。
细胞中每时每刻都进行着许多化学反应,统称为细胞代谢。
常见有机化学反应的条件
高温
高压
强酸
强碱
剧烈
一、酶在代谢中的作用
1.探究实验:比较过氧化氢在不同条件下的分解
①实验原理
2H2O2 2H2O + O2
通过O2的产生量判断H2O2的分解情况
②实验目的
通过比较过氧化氢在不同条件下的分解的快慢,了解过氧化氢酶的作用。
加热是化学反应的常见条件
Fe3+是无机催化剂
新鲜的肝脏中含有过氧化氢酶
细胞代谢中也会产生代谢废物,甚至会产生对细胞有害的物质,如过氧化氢,细胞中有过氧化氢酶,能将过氧化氢及时分解为氧气和水。新鲜肝脏中有较多的过氧化氢酶。
③实验步骤
一、酶在代谢中的作用
试管编号 1 2 3 4
H2O2溶液 (体积分数为3%)
实验处理 (不同反应条件)
检测指标 2 mL
2 mL
2 mL
2 mL
无
90℃
水浴加热
2滴
FeCl3
2滴
肝脏研磨液
1.气泡冒出情况
2.卫生香复燃情况
讨论
1.与1号试管相比,2号试管出现了什么不同的现象?这一现象说明什么?
2号试管放出的气泡多,这一现象说明加热促进过氧化氢的分解,提高反应速率。
2.在细胞内,能通过加热来提高反应速率吗?
不能。
讨论
4.3号试管与4号试管相比,哪支试管中反应速率快?这说明什么?为什么说酶对细胞内化学反应的顺利进行至关重要?
3.3号和4号试管未经加热,也有大量气泡产生,这说明什么?
说明FeCl3中的Fe3+和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率。
4号试管的反应速率比3号试管快得多。说明过氧化氢酶比Fe3+的催化效率高得多。细胞内每时每刻都在进行成千上万种化学反应,这些化学反应需要在常温、常压下高效地进行,只有酶能够满足这样的要求,所以酶对于细胞内化学反应的顺利进行至关重要。
1与2对照:____________________________________________________________
加热能促进过氧化氢的分解,提高反应速率。(为反应提供能量)
1与3对照:______________________________________________________________
FeCl3在常温下能促进过氧化氢的分解,提高反应速率。(催化作用)
1与4对照:_________________________________________________________
____________
过氧化氢酶在常温下能促进过氧化氢的分解,提高反应速率。(催化作用)
④实验分析
3与4对照:_____________________________________
过氧化氢酶比FeCl3的催化效率高。
酶和无机催化剂一样,都能催化化学反应,并且酶的催化效率远高于无机催化的催化效率。
⑤实验结论
2.酶催化的机理
分子从常态转变为容易发生化学反应的活跃态所需要的能量。
①活化能
图中①表示:
图中②表示:
图中④表示:
无催化剂时化学反应所需的活化能。
无机催化剂催化时化学反应所需的活化能。
酶催化时化学反应所需的活化能。
2.酶催化的机理
②酶催化的机理
③表示:
⑤表示:
无机催化剂降低的活化能
酶降低的活化能
酶与无机催化剂催化的机理相同,都能降低化学反应的活化能,但是酶降低活化能的作用更显著,催化效率更高。
高效性
试管编号 1 2 3 4
H2O2溶液 (体积分数为3%) 2 mL 2 mL 2 mL 2 mL
实验处理 (不同反应条件) 无 90℃ 水浴加热 2滴 FeCl3 2滴
肝脏研磨液
检测指标 1. 气泡冒出情况 2. 卫生香复燃情况 二、控制变量和设计对照实验
变量:实验过程中的变化因素
自变量:人为控制的对实验对象进行处理的因素
无关变量:实验过程中存在的其他一些会对实验结果造成影响的可变因素
因变量:因自变量改变而变化的变量
试管编号 1 2 3 4
H2O2溶液 (体积分数为3%) 2 mL 2 mL 2 mL 2 mL
实验处理 (不同反应条件) 无 90℃ 水浴加热 2滴 FeCl3 2滴
肝脏研磨液
检测指标 1. 气泡冒出情况 2. 卫生香复燃情况 二、控制变量和设计对照实验
对照实验:除作为自变量的因素外,其余无关变量都保持一致,并将结果进行比较的实验。
对照实验一般要设置对照组和实验组。
对照组
实验组
空白对照
空白对照
在未真正做实验之前,结果就已知的那组就是对照组;而结果未知的那组是实验组。
空白对照指不做任何实验的对照组或不给对照组以任何处理因素。
注意:不给对照组任何处理因素是相对实验组而言的,实际上对照组还是要做一定的处理,只是不加实验组的处理因素,或者说相对于实验组而言,除实验变量外,别的处理与实验组完全相同。
1.有人设计实验探究有机肥是否能提高土壤肥力并优于化肥。实验分为两组,一组农田施有机肥,一组农田施化肥。该实验设计缺少__________________________________________。
随堂练习
In-class practice
既不施用有机肥也不施用化肥的对照田
自身对照
实验处理前的对象状况为对照组,实验处理后的对象变化则为实验组。
自身对照指对照组和实验组都在同一研究对象上进行,不另设对照。自身对照方法简便,关键是看清实验处理前后现象变化的差异。
第一次对照:质壁分离状态与自然状态形成对照;
第二次对照:复原后状态与质壁分离状态形成对照
李毕希(J.V.Liebig)
巴斯德(L.Pasteur)
发酵是由酵母菌细胞的存在所致,没有活细胞的参与,糖类是不可能变成酒精的。
发酵是酵母菌细胞中的某些物质,但这些物质只有在酵母菌细胞死亡并裂解后才能发挥作用。
三、酶的本质
思考2.对于死酵母细胞,它已经失去了生命活动还有可能引起发酵吗?结合前面两位科学家的观点,还有其他的可能吗?
活酵母细胞中的物质
毕希纳(E.Buchner)
酵母细胞的某些物质能够在酵母细胞破碎后继续起作用,就像在活酵母细胞中一样。
萨姆纳从刀豆种子中提取到脲酶,并证明脲酶是蛋白质。
萨姆纳(J.B.Sumner)
切赫(T.R.Cech)和 奥尔特曼(S.Altman)
少数RNA也具有生物催化功能。
思考3.综合酶本质的探索历程,能不能给酶下一个比较完整的定义?
酶是__________产生的具有___________的_________,其中绝大多数酶是__________,少数酶是________。
活细胞
催化作用
有机物
蛋白质
RNA
标准蛋白质样液
标准RNA样液
待测酶液
均发生紫色反应
该酶是蛋白质
均呈现红色
该酶是RNA
分别加入 双缩脲试剂
分别加入 吡罗红染液
三、酶的特性
1.高效性
与无机催化剂相比,酶能更显著地降低反应的活化能。
思考4.设计实验验证酶具有高效性时,对照组和实验组应该如何设计呢?
2.专一性
思考5.口腔里有唾液淀粉酶,为什么塞进牙缝的肉丝两天后还没被消化?
三、酶的特性
探究实验:淀粉酶对淀粉和蔗糖的水解作用
序号 项目 试管1 试管2
1 注入可溶性淀粉溶液 2mL ——
2 注入蔗糖溶液 —— 2mL
3 注入淀粉酶溶液 2mL 2mL
4 保温5min 5 注入斐林试剂2mL 6 沸水浴加热1min 7 观察记录试管中有无砖红色沉淀 实验结论:
淀粉酶只能催化淀粉水解不能催化蔗糖水解。
酶具有专一性:一种酶只能催化一种或一类化学反应。
—— 保证了细胞内化学反应有序进行
2.专一性
三、酶的特性
探究实验:淀粉酶对淀粉和蔗糖的水解作用
序号 项目 试管1 试管2
1 注入可溶性淀粉溶液 2mL ——
2 注入蔗糖溶液 —— 2mL
3 注入淀粉酶溶液 2mL 2mL
4 保温5min 5 注入斐林试剂2mL 6 沸水浴加热1min 7 观察记录试管中有无砖红色沉淀
思考6.本实验中,是否可用碘液检测淀粉和蔗糖是否发生了水解?
不能;因为实验组和对照组实验现象相同,不能说明淀粉酶对蔗糖是否起作用。
方案二:
淀粉 + 蔗糖酶
蔗糖 + 蔗糖酶
方案四:
蔗糖 + 淀粉酶
蔗糖 + 蔗糖酶
方案一:
淀粉 + 淀粉酶
蔗糖 + 淀粉酶
方案三:
淀粉 + 淀粉酶
淀粉 + 蔗糖酶
思路1:底物不同,酶相同
思路2:底物相同,酶不同
用斐林试剂检测
用斐林试剂检测
用斐林试剂检测
用碘液或者斐林试剂检测
2.下图表示的是某类酶作用的模型。尝试用文字描述这个模型。这个模型能解释酶的什么特性?
这个模型中 A 代表某类酶,B 代表底物,C 和 D 代表产物。这个模型的含义是:酶 A与底物 B 专一性结合,催化反应的发生,产生了产物 C 和 D。这个模型可以类比解释酶的专一性。
随堂练习
In-class practice
锁钥学说
酶和无机催化剂在反应前后数量和性质不发生改变,一段时间内可以重复利用。
3.内质网应激时,会导致Ca2+从内质网腔释放到细胞质基质中与钙蛋白酶原结合,钙蛋白酶原被Ca2+激活后可水解多种蛋白质,诱导细胞凋亡。钙蛋白酶可水解多种蛋白质说明该酶不具有专一性( )
×
随堂练习
In-class practice
有的酶对底物的要求比绝对专一性要低一些,可以作用于一类结构相似的底物,即能催化一类化学反应。比如,胃蛋白酶催化具有苯丙氨酸、酪氨酸、色氨酸以及亮氨酸、谷氨酸、谷氨酰胺等肽键的断裂,使大分子的蛋白质变为较小分子的多肽;胰蛋白酶水解碱性氨基酸(赖氨酸、精氨酸)的残基与其他氨基酸的氨基形成的肽键,产物是以碱性氨基酸作为羧基末端的多肽和少量碱性氨基酸;这就是酶的“相对专一性”。
酶催化特定化学反应的能力称为酶活性。
酶活性可用在一定条件下酶所催化某一化学反应的速率表示。
3.酶作用条件温和
三、酶的特性
探究实验一:探究温度对酶活性的影响
阅读课本82-83页,借助课本中的材料,设计实验。
①选择哪一种酶做实验材料?为什么?
②本实验的自变量、因变量分别是什么?用什么方法控制自变量?
③你将设定哪几个温度?怎样控制温度,哪个是对照组,哪个是实验组?
④在设计这一实验中最关键的一步是什么? 提示:(在酶与反应底物接触前就应该用相应的温度处理酶和反应底物)。
⑤你所预期的对照组和实验组的现象或结果是什么?
3.酶作用条件温和
三、酶的特性
探究实验一:探究温度对酶活性的影响
操作步骤 1号试管 2号试管 3号试管 4号试管 5号试管 6号试管
0℃ 0℃ 50℃ 50℃ 100℃ 100℃
第一步 2 mL — 2 mL — 2 mL —
第二步 — 2 mL — 2 mL — 2 mL
第三步 在各自温度下保温5 min 第四步 将2号加入1号中 将4号加入3号中 将6号加入5号中 第五步 在各自温度下保温5 min 第六步 2滴 2滴 2滴 实验现象 变蓝
不变蓝
变蓝
实验结论:
温度过低或过高酶活性都较低。
思考·讨论
1.如何进一步探究淀粉酶的最适温度?
缩小温度梯度,重复进行上述实验。
酶活性受温度影响示意图
最适温度
在最适温度条件下,酶的活性最高,温度偏高或偏低,酶的活性都会明显降低。
一般来说,动物体内酶的最适温度在35~40℃之间;植物体内酶的最适温度在40~50℃之间;细菌和真菌体内酶最适温度差别较大,有的酶最适温度可高达70℃。
思考·讨论
2.为什么不能用斐林试剂对实验结果进行检测?
该实验的自变量是温度,用斐林试剂检测时需要水浴加热,
这样会干扰自变量。
3.为什么不能用过氧化氢酶和过氧化氢来探究温度对酶活性的影响?
因为过氧化氢本身受热易分解,会对实验结果造成干扰。
操作步骤 1号试管 2号试管 3号试管
第一步 加入2滴肝脏研磨液 第二步 1mL pH=7的缓冲液 1mL 盐酸溶液 1mL NaOH溶液
第三步 加入2mL的H2O2溶液 第四步 观察气泡生成速率,或插入卫生香,观察复燃所需时间 实验现象 产生大量气泡
产生少量气泡
产生少量气泡
探究实验二:探究pH对酶活性的影响
3.酶作用条件温和
三、酶的特性
实验结论:
pH过低或过高酶活性都较低。
在最适pH条件下,酶的活性最高,pH偏高或偏低,酶的活性都会明显降低。
最适pH
酶活性受pH影响示意图
1.如何进一步探究过氧化氢酶的最适pH?
思考·讨论
缩小温度梯度,重复进行上述实验。
动物体内酶的最适pH大多在6.5~8.0,但也有例外,如胃蛋白酶的最适pH为1.5;植物体内的酶的最适pH大多为4.5~6.5。
高温、强酸、强碱会使酶的空间结构遭到破坏,使酶永久失活。
温度和pH偏高或偏低,酶的活性都会明显降低。
低温使酶活性受抑制,温度恢复,酶活性可以恢复。
4.下列有关酶的实验设计思路错误的是( )
A.利用过氧化氢和过氧化氢酶探究温度对酶活性的影响
B.利用淀粉、蔗糖、淀粉酶和碘液验证酶的专一性
C.利用过氧化氢、新鲜的猪肝研磨液和蒸馏水研究酶的高效性
D.利用胃蛋白酶、蛋清和pH分别为3、7、11的缓冲液验证pH对酶活性
的影响
ABCD
随堂练习
In-class practice
四、影响酶促反应速率的因素
1.酶促反应:
由酶催化的化学反应,生物体内的化学反应绝大多数属于酶促反应。
2.酶促反应速率:
3.影响酶促反应速率的因素:
单位时间内反应物或生成物浓度的改变量。
pH
温度
抑制剂
激活剂
酶活性
酶浓度
底物浓度
酶促反应速率
底物与酶的接触面积
★酶活性≠酶促反应速率
①酶浓度(底物有限)
a
b
c
ab:
在一定的酶浓度范围内,随酶浓度的增加,反应速率增加
N
酶浓度
反应速率
0
b:
当酶浓度增大到某一值时,反应速率达到最大值,不再增加
酶浓度较低,底物没有完全被酶结合
底物完全被酶结合
②底物浓度(酶有限)
a
b
c
ab:
在一定的酶浓度范围内,随酶浓度的增加,反应速率增加
N
底物浓度
反应速率
0
b:
当酶浓度增大到某一值时,反应速率达到最大值,不再增加
酶浓度较低,底物没有完全被酶结合
底物完全被酶结合
5.酶抑制剂分竞争性抑制剂和非竞争性抑制剂,两者作用特点如图甲所示,图乙表示相应的反应速度。下列有关叙述不正确的是( )
活性中心
底物
竞争性抑制剂
A
B
C
甲
非竞争性抑制剂
底物
乙
反应速度
底物浓度
a
b
c
酶
酶
酶
B
竞争性抑制剂的抑制作用可以通过增大底物的浓度来抵消其抑制作用;
非竞争性抑制剂其抑制作用不能通过增加底物的浓度来抵消其抑制作用
A.曲线a表示没有酶抑制剂存在时的作用效果
B.曲线c表示在竞争性抑制剂作用下酶的活性降低
C.曲线a、b反应速率不再增加是受酶浓度的限制
D.竞争性抑制剂与该酶催化的底物结构相似
随堂练习
In-class practice
五、酶的应用
1.溶菌酶
溶解细菌细胞壁,具有抗菌消炎的作用。在临床上与抗生素混合使用,能增强抗生素的疗效。
五、酶的应用
2.果胶酶
分解果肉内细胞壁中的果胶,提高果汁产量,使果汁变得澄清。
五、酶的应用
3.多酶片
普通糖衣—胃蛋白酶—肠溶衣糖衣—胰酶
普通糖衣保护胃蛋白酶,在胃液中会分解,释放出胃蛋白酶。
肠溶衣保护胰酶,在胃液中不会分解,在小肠中分解,释放出胰酶。
同课章节目录
- 第1章 走近细胞
- 第1节 细胞是生命活动的基本单位
- 第2节 细胞的多样性和统一性
- 第2章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 细胞中的无机物
- 第3节 细胞中的糖类和脂质
- 第4节 蛋白质是生命活动的主要承担者
- 第5节 核酸是遗传信息的携带者
- 第3章 细胞的基本结构
- 第1节 细胞膜的结构和功能
- 第2节 细胞器之间的分工合作
- 第3节 细胞核的结构和功能
- 第4章 细胞的物质输入和输出
- 第1节 被动运输
- 第2节 主动运输与胞吞、胞吐
- 第5章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“货币”ATP
- 第3节 细胞呼吸的原理和应用
- 第4节 光合作用与能量转化
- 第6章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和死亡
