化合价
图片预览






文档简介
(共36张PPT)
课题4
物质
HCl
H2O
NaCl
Al2O3
原子个数比
1:1
2:1
1:1
2:3
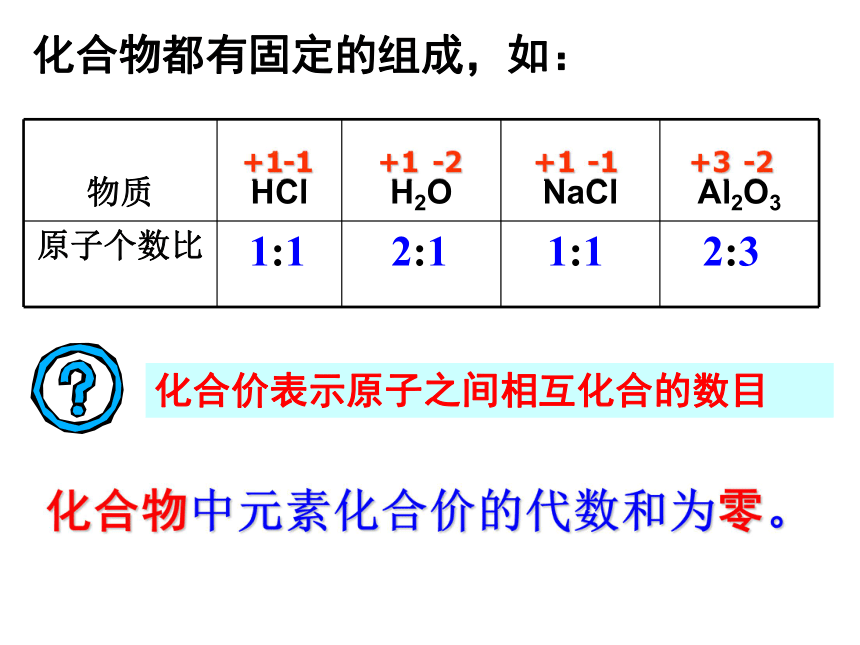
化合物都有固定的组成,如:
+1
-1
+1
-2
+1
-1
+3
-2
化合物中元素化合价的代数和为零。
化合价表示原子之间相互化合的数目
化合价规则
☆化合价是元素在形成化合物时表现出的性质,因此,单质中元素的化合价为零。
化合价的表示方法:
1、先写出元素符号;
2、然后将元素的化合价标在元素符号的正上方;
3、先写正、负号,后写数值(怎么念怎么写)
如 :
O H Na Mg Al Ca
-2 +1 +1 +2 +3 +2
思考:化合价书写与离子书写的区别
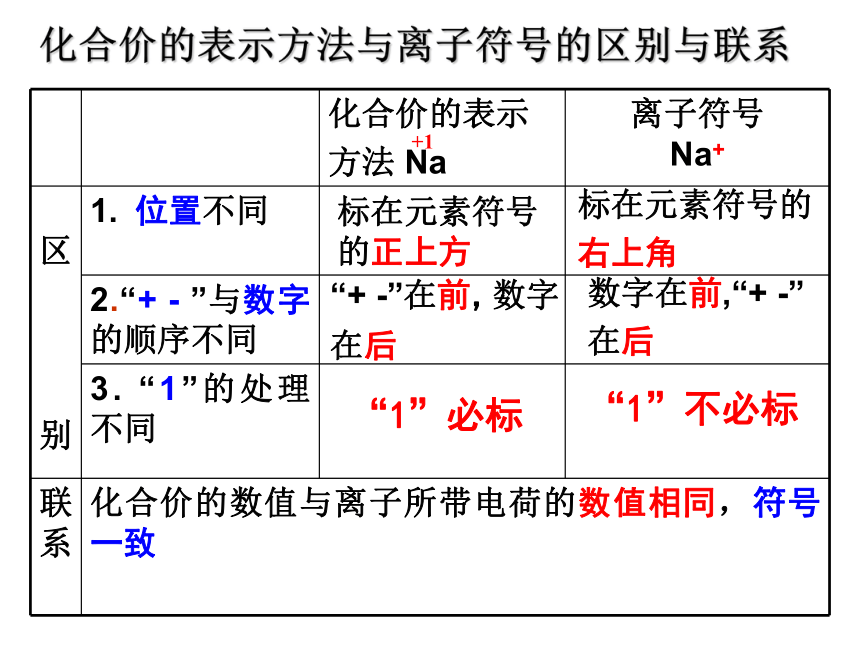
化合价的表示方法与离子符号的区别与联系
化合价的表示
方法 Na 离子符号 Na+
区
别 1. 位置不同
2.“+ - ”与数字的顺序不同
3. “1”的处理不同
联系
化合价的数值与离子所带电荷的数值相同,符号一致
+1
标在元素符号的正上方
标在元素符号的
右上角
“+ -”在前,数字
在后
数字在前,“+ -”
在后
“1”必标
“1”不必标
+
-
m
R
m
+
-
R
表示化合价的正负、数值
一个离子所带电荷的数值、正负
氢氧化钙: Ca(OH)2 碳酸钙:CaCO3
硝酸铜 : Cu(NO3)2 硫酸钡:BaSO4
氢氧化铁: Fe(OH)3
这些化学式与前面的化学式有何不同?
①这些化学式中元素种类较多,不是2种。
②这些化学式有的有括号。
原子团:做为一个整体参加反应的原子集团, 也叫根
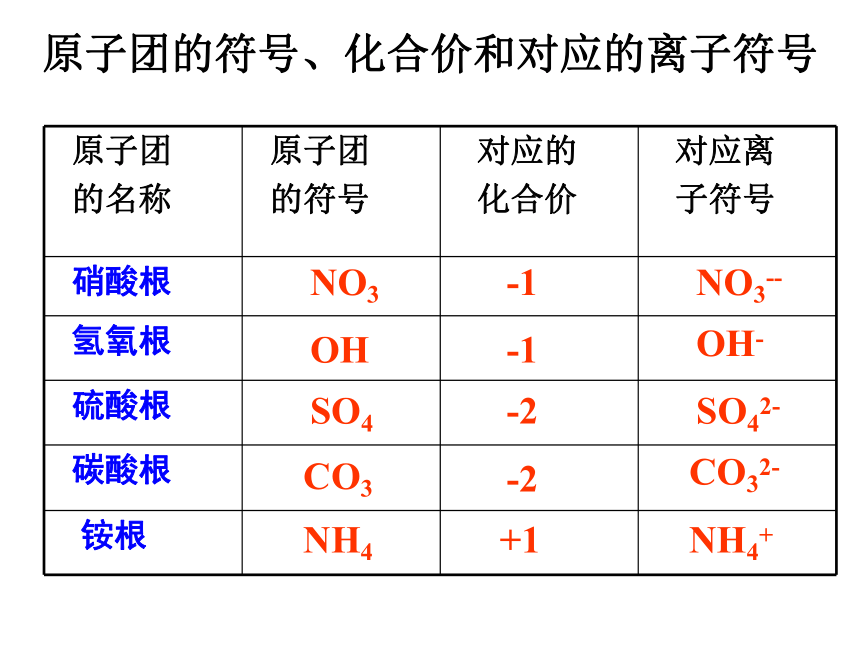
原子团的符号、化合价和对应的离子符号
原子团
的名称 原子团
的符号 对应的
化合价 对应离
子符号
硝酸根
氢氧根
硫酸根
碳酸根
铵根
NO3
OH
SO4
CO3
NH4
-1
-1
-2
-2
+1
NO3--
OH-
SO42-
CO32-
NH4+
铝离子 ,氧离子 ,
化合价为正二价的镁元素 ,
化合价为负二价的硫元素 ,
二氧化碳中的碳元素为正四价 。
Al3+
O2-
Mg
+2
S
-2
CO2
+4
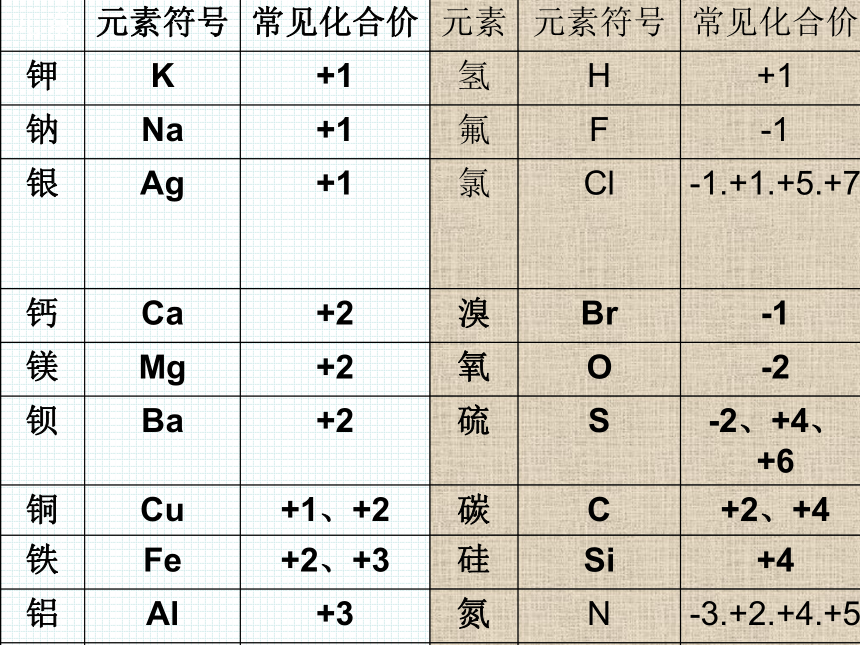
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.+7 磷 P -3、+3、+5
锌 Zn +2
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.
+7 磷 P -3、+3、+5
锌 Zn +2
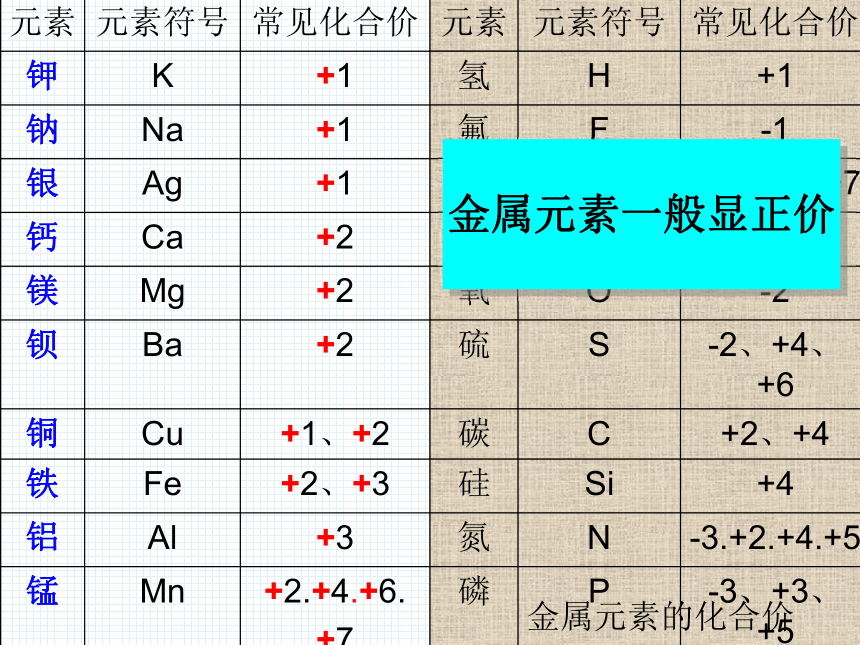
金属元素的化合价
金属元素一般显正价
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.+7 磷 P -3、+3、+5
锌 Zn +2
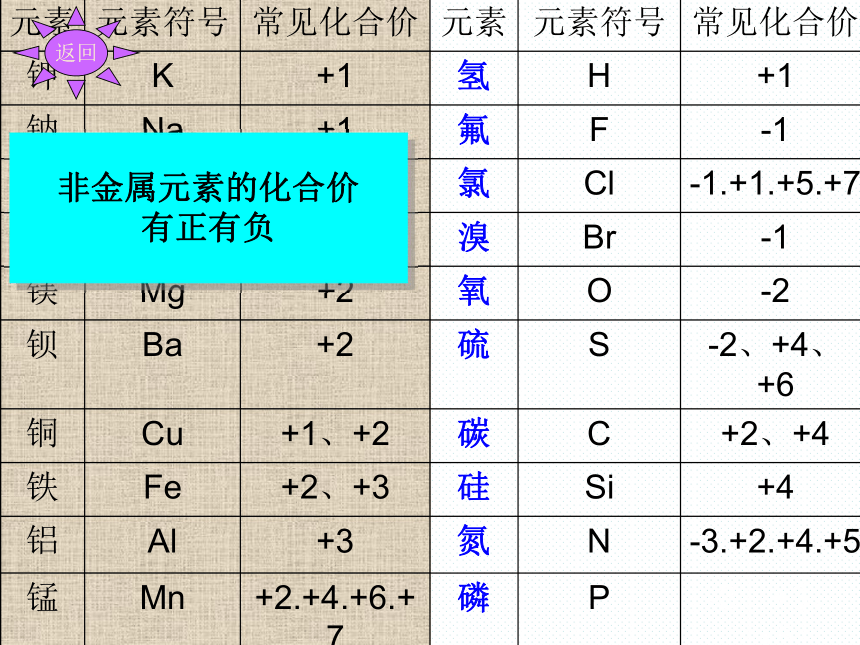
非金属元素的化合价
有正有负
返回
化合价规则
☆1. 在化合物里,氧通常显-2价
氢通常显+1价;
☆2. 金属一般显正价,非金属
有正有负。
化合价口诀:
一价氯、氢、钾、钠、银
二价氧、钡、钙、镁、锌
三铝四硅五价磷
亚铁二 价、铁三价
氯在最右负一价
二、四、六硫都齐全
硫在最右负二价
铜、汞二价最常见
帮你记忆
注:红字体元素为负价,其他均为正价。
元素的化合价由什么决定?
答:该元素原子的最外层电子数
化合物中元素化合价的判断
+1 +2 +3 -2 -2 -1
Na Mg Al O S Cl
失电子显正价 得电子显负价
失几个电子显正几价 得几个电子显负几价
元素化合价
化合价 判 断
原 子
离 子
注意:元素化合价与离子所带电荷的写法不同
易 失 电 子
易 得 电 子
化学式
判断
化合价
书写
试确定氯酸钾中氯元素的化合价
先写出化学式,标出已知元素的化合价
设未知数
列等式(正负总价和为0)
解答
根据化学式确定化合价
【例】
还记得KMnO4、K2MnO4吗?
分别读作?
怎么区分?
试分别标出锰元素的化合价。
高锰酸钾、
锰酸钾
计算下列物质中氮元素的化合价
⑴NO ⑵NO2
⑶NH3 ⑷N2
⑸HNO3
+2
+4
-3
0
同种元素在不同物质中可显不同的化合价
+5
将下列物质按氯元素的化合价由高到低的顺序排成一列:
Cl2、NaClO4、 NaCl 、KClO3、 NaClO、 NaClO2
NaClO4 KClO3 NaClO2 NaClO Cl2 NaCl
o
+7
-1
+5
+1
+3
加强练习
+7
+5
+3
+1
o
-1
①写出元素符号,正价在前边,负价在后边,化合价标在元素的正上方。
②求两种元素化合价绝对值的最小公倍数。
③求各元素的原子个数。
④把原子数写在各元素符号的右下角。
4. 根据化合价求化学式的一般步骤:
⑤按正价与负价的代数和为0的原则检查化学式书写是否正确。
(1)先写元素符号(正前负后)
(2)标出各元素的化合价(正上方)
(3) 求公倍,算个数,标个数。
(4)检查代数和是否为零
根据化合价确定化学式
【例】磷元素有两种氧化物,其中磷元素的化合价分别为+3和+5 ,写出这两种氧化物的化学式。
P O
+3 价磷的氧化物
+3 -2
2
5
+5 价磷的氧化物
P O
+5 -2
2
3
写出下列元素的氧化物的化学式:
Na ; Mg ;
Al ; S ;
Cl ; Si ;
+1
+2
+3
+6
+7
+4
Na2O
MgO
Al2O3
SO3
Cl2O7
SiO2
在表中填入正负化合价结合成化合物的化学式
K
Ca
Al
Cl
OH
SO4
负价元素
正价元素
化学式
-1
-2
+1
+2
+3
KCl
CaCl2
AlCl3
K2SO4
CaSO4
Al 2(SO4)3
-1
KOH
Ca(OH)2
Al(OH)3
某化某:指该物质中含两种元素
某酸某:指该物质中含“某酸根”原子团
氢氧化某:指该物质中含“氢氧根”原子团
某化亚铁:
某酸亚铁:
氢氧化亚铁:
注意规律:
铁元素的化合价为+2价
下列化学式如有错误请改在横线上:
氧化钙Ca2O2 ______,
氯化铁 FeCl2 ______,
氯化锌 ZnCl ______,
氢氧化铜CuOH __________,
氯化钠ClNa ____.
CaO
FeCl3
ZnCl2
Cu(OH)2
NaCl
练习:写出下列物质的化学式。
氧化钾
氯化钾
氢氧化钾
硫酸钾
K2O
KCl
KOH
K2SO4
氧化钙
氯化钙
氢氧化钙
硫酸钙
CaO
CaCl2
Ca(OH)2
CaSO4
氧化铁
氯化铁
氢氧化铁
硫酸铁
Fe2O3
FeCl3
Fe(OH)3
H2O
表示每一个水分子中有两个氢原子
2
表示2个水分子
1.化学式前面的数字表示分子的个数。
2.化学式中元素符号右下角的数字表示每一个分子中含有的这种原子的个数。
注意:
Al
3+
每个铝离子带三个单位正电荷
3
3个铝离子
说明下列符号中数字“2”的含义
2H2
2Mg2+
2O
两个氢分子
两个氧原子
两个镁离子
每一个氢分子由两个氢原子构成
每一个镁离子带两个单位正电荷
填写下列化学符号中数字“2”的含义:
①Fe2+ ;
②MgO .
+2
一个亚铁离子带两个单位的正电荷
氧化镁中镁元素的化合价为+2价
指出下列符号中数字“2”的含义。
⑴O2 ;
⑵2O ;
⑶H2O ;
⑷2H+ ;
一个氧分子中含有2个氧原子
2个氧原子
一个水分子中含有2个氢原子
2个氢离子
指出下列符号中数字“2”的含义。
⑸2P2O5 ;
;
⑹O2- ;
2个五氧化二磷分子
一个五氧化二磷分子分子中含有2个磷原子
一个氧离子带有2个单位的正电荷
用化学符号填空:
⑴水银 ;
⑵三个氢原子 ;
⑶两个五氧化二氮分子 ;
⑷3个氢氧根离子 ;
⑸ +3价的铝元素 ;
⑹硫酸铁 ;
Hg
3H
2N2O5
3OH-
Al
+3
Fe2(SO4)3
Al 表示 ;
3Al表示 ;
Al3+表示 ;
3Al3+表示 ;
Al
Al3+
失失3个电子
3 个铝离子
一个铝原子;
铝元素;
3个铝原子
一个铝离子
铝这种单质;
课题4
物质
HCl
H2O
NaCl
Al2O3
原子个数比
1:1
2:1
1:1
2:3
化合物都有固定的组成,如:
+1
-1
+1
-2
+1
-1
+3
-2
化合物中元素化合价的代数和为零。
化合价表示原子之间相互化合的数目
化合价规则
☆化合价是元素在形成化合物时表现出的性质,因此,单质中元素的化合价为零。
化合价的表示方法:
1、先写出元素符号;
2、然后将元素的化合价标在元素符号的正上方;
3、先写正、负号,后写数值(怎么念怎么写)
如 :
O H Na Mg Al Ca
-2 +1 +1 +2 +3 +2
思考:化合价书写与离子书写的区别
化合价的表示方法与离子符号的区别与联系
化合价的表示
方法 Na 离子符号 Na+
区
别 1. 位置不同
2.“+ - ”与数字的顺序不同
3. “1”的处理不同
联系
化合价的数值与离子所带电荷的数值相同,符号一致
+1
标在元素符号的正上方
标在元素符号的
右上角
“+ -”在前,数字
在后
数字在前,“+ -”
在后
“1”必标
“1”不必标
+
-
m
R
m
+
-
R
表示化合价的正负、数值
一个离子所带电荷的数值、正负
氢氧化钙: Ca(OH)2 碳酸钙:CaCO3
硝酸铜 : Cu(NO3)2 硫酸钡:BaSO4
氢氧化铁: Fe(OH)3
这些化学式与前面的化学式有何不同?
①这些化学式中元素种类较多,不是2种。
②这些化学式有的有括号。
原子团:做为一个整体参加反应的原子集团, 也叫根
原子团的符号、化合价和对应的离子符号
原子团
的名称 原子团
的符号 对应的
化合价 对应离
子符号
硝酸根
氢氧根
硫酸根
碳酸根
铵根
NO3
OH
SO4
CO3
NH4
-1
-1
-2
-2
+1
NO3--
OH-
SO42-
CO32-
NH4+
铝离子 ,氧离子 ,
化合价为正二价的镁元素 ,
化合价为负二价的硫元素 ,
二氧化碳中的碳元素为正四价 。
Al3+
O2-
Mg
+2
S
-2
CO2
+4
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.+7 磷 P -3、+3、+5
锌 Zn +2
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.
+7 磷 P -3、+3、+5
锌 Zn +2
金属元素的化合价
金属元素一般显正价
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.+7 磷 P -3、+3、+5
锌 Zn +2
非金属元素的化合价
有正有负
返回
化合价规则
☆1. 在化合物里,氧通常显-2价
氢通常显+1价;
☆2. 金属一般显正价,非金属
有正有负。
化合价口诀:
一价氯、氢、钾、钠、银
二价氧、钡、钙、镁、锌
三铝四硅五价磷
亚铁二 价、铁三价
氯在最右负一价
二、四、六硫都齐全
硫在最右负二价
铜、汞二价最常见
帮你记忆
注:红字体元素为负价,其他均为正价。
元素的化合价由什么决定?
答:该元素原子的最外层电子数
化合物中元素化合价的判断
+1 +2 +3 -2 -2 -1
Na Mg Al O S Cl
失电子显正价 得电子显负价
失几个电子显正几价 得几个电子显负几价
元素化合价
化合价 判 断
原 子
离 子
注意:元素化合价与离子所带电荷的写法不同
易 失 电 子
易 得 电 子
化学式
判断
化合价
书写
试确定氯酸钾中氯元素的化合价
先写出化学式,标出已知元素的化合价
设未知数
列等式(正负总价和为0)
解答
根据化学式确定化合价
【例】
还记得KMnO4、K2MnO4吗?
分别读作?
怎么区分?
试分别标出锰元素的化合价。
高锰酸钾、
锰酸钾
计算下列物质中氮元素的化合价
⑴NO ⑵NO2
⑶NH3 ⑷N2
⑸HNO3
+2
+4
-3
0
同种元素在不同物质中可显不同的化合价
+5
将下列物质按氯元素的化合价由高到低的顺序排成一列:
Cl2、NaClO4、 NaCl 、KClO3、 NaClO、 NaClO2
NaClO4 KClO3 NaClO2 NaClO Cl2 NaCl
o
+7
-1
+5
+1
+3
加强练习
+7
+5
+3
+1
o
-1
①写出元素符号,正价在前边,负价在后边,化合价标在元素的正上方。
②求两种元素化合价绝对值的最小公倍数。
③求各元素的原子个数。
④把原子数写在各元素符号的右下角。
4. 根据化合价求化学式的一般步骤:
⑤按正价与负价的代数和为0的原则检查化学式书写是否正确。
(1)先写元素符号(正前负后)
(2)标出各元素的化合价(正上方)
(3) 求公倍,算个数,标个数。
(4)检查代数和是否为零
根据化合价确定化学式
【例】磷元素有两种氧化物,其中磷元素的化合价分别为+3和+5 ,写出这两种氧化物的化学式。
P O
+3 价磷的氧化物
+3 -2
2
5
+5 价磷的氧化物
P O
+5 -2
2
3
写出下列元素的氧化物的化学式:
Na ; Mg ;
Al ; S ;
Cl ; Si ;
+1
+2
+3
+6
+7
+4
Na2O
MgO
Al2O3
SO3
Cl2O7
SiO2
在表中填入正负化合价结合成化合物的化学式
K
Ca
Al
Cl
OH
SO4
负价元素
正价元素
化学式
-1
-2
+1
+2
+3
KCl
CaCl2
AlCl3
K2SO4
CaSO4
Al 2(SO4)3
-1
KOH
Ca(OH)2
Al(OH)3
某化某:指该物质中含两种元素
某酸某:指该物质中含“某酸根”原子团
氢氧化某:指该物质中含“氢氧根”原子团
某化亚铁:
某酸亚铁:
氢氧化亚铁:
注意规律:
铁元素的化合价为+2价
下列化学式如有错误请改在横线上:
氧化钙Ca2O2 ______,
氯化铁 FeCl2 ______,
氯化锌 ZnCl ______,
氢氧化铜CuOH __________,
氯化钠ClNa ____.
CaO
FeCl3
ZnCl2
Cu(OH)2
NaCl
练习:写出下列物质的化学式。
氧化钾
氯化钾
氢氧化钾
硫酸钾
K2O
KCl
KOH
K2SO4
氧化钙
氯化钙
氢氧化钙
硫酸钙
CaO
CaCl2
Ca(OH)2
CaSO4
氧化铁
氯化铁
氢氧化铁
硫酸铁
Fe2O3
FeCl3
Fe(OH)3
H2O
表示每一个水分子中有两个氢原子
2
表示2个水分子
1.化学式前面的数字表示分子的个数。
2.化学式中元素符号右下角的数字表示每一个分子中含有的这种原子的个数。
注意:
Al
3+
每个铝离子带三个单位正电荷
3
3个铝离子
说明下列符号中数字“2”的含义
2H2
2Mg2+
2O
两个氢分子
两个氧原子
两个镁离子
每一个氢分子由两个氢原子构成
每一个镁离子带两个单位正电荷
填写下列化学符号中数字“2”的含义:
①Fe2+ ;
②MgO .
+2
一个亚铁离子带两个单位的正电荷
氧化镁中镁元素的化合价为+2价
指出下列符号中数字“2”的含义。
⑴O2 ;
⑵2O ;
⑶H2O ;
⑷2H+ ;
一个氧分子中含有2个氧原子
2个氧原子
一个水分子中含有2个氢原子
2个氢离子
指出下列符号中数字“2”的含义。
⑸2P2O5 ;
;
⑹O2- ;
2个五氧化二磷分子
一个五氧化二磷分子分子中含有2个磷原子
一个氧离子带有2个单位的正电荷
用化学符号填空:
⑴水银 ;
⑵三个氢原子 ;
⑶两个五氧化二氮分子 ;
⑷3个氢氧根离子 ;
⑸ +3价的铝元素 ;
⑹硫酸铁 ;
Hg
3H
2N2O5
3OH-
Al
+3
Fe2(SO4)3
Al 表示 ;
3Al表示 ;
Al3+表示 ;
3Al3+表示 ;
Al
Al3+
失失3个电子
3 个铝离子
一个铝原子;
铝元素;
3个铝原子
一个铝离子
铝这种单质;
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
