11.1 生活中常见的盐 课件——2021-2022学年人教版九年级下册(45张PPT)
文档属性
| 名称 | 11.1 生活中常见的盐 课件——2021-2022学年人教版九年级下册(45张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-03 00:00:00 | ||
图片预览











文档简介
(共45张PPT)
生活中常见的盐
日常生活中所说的盐,通常指食盐,你想一下它都有哪些物理性质呢?
盐田
盐井
盐湖
盐矿
氯化钠
物理性质:白色颗粒状固体,易溶于水,有咸味。
广泛存在于海水、盐湖、盐矿中。
用途广泛:
生理盐水
调味品和防腐剂
融雪剂
氯化钠
生活中作为调味品和防腐剂;
农业上用于选种;
医疗上用于制生理盐水;
交通上作融雪剂;
同时还是化工生产的原料等。
粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如: 等。
不能直接食用,必须除杂和提纯之后才能食用。
粗盐
粗盐中难溶性杂质的去除
粗盐中难溶性杂质的去除
实验步骤:
1、溶解:
称取5.0g食盐,用药匙将粗盐逐渐加入盛有10mL水的烧杯中,边加边用玻璃棒搅拌,一直到粗盐不再溶解为止。
称量剩下的粗盐,确定10mL水里溶解了多少克粗盐。
粗盐中难溶性杂质的去除
2、过滤:
用玻璃棒引流,过滤食盐水。仔细观察剩余物和滤液的颜色。
如果滤液仍浑浊应再过滤一次。
实验步骤:
粗盐中难溶性杂质的去除
3、蒸发结晶:
将滤液倒入蒸发皿,加热,过程中用玻璃棒不断搅拌;
实验步骤:
4、计算产率:
把蒸发皿中的晶体称量,并计算产率,最后转移到指定容器中。
粗盐中难溶性杂质的去除
上面三个实验操作,溶解、过滤、蒸发结晶,都用到了玻璃棒,他们的作用分别是什么?
溶解时:搅拌,加速溶解;
过滤时:引流;
蒸发结晶时: 搅拌,防止液体飞溅。
练习
1.下列说法正确的是( )
A.盐都能食用,故称为食盐
B.盐就是食盐,易溶于水
C.盐都有咸味,都是白色固体
D.盐是一类物质的总称
2.食盐是一种重要的化工原料,可用于生产:①金属钠②氯气③盐酸④硫酸⑤烧碱⑥纯碱等,以上正确的是( )
A.①②③⑤⑥ B.③④⑤
C.①④⑤⑥ D.①②③④⑤⑥
D
A
小结
氯化钠 :白色颗粒状固体,易溶于水,有咸味。
粗盐提纯的步骤:溶解、过滤、蒸发
有的同学说,盐就是食盐,这样说对吗?
当然是错误的!盐是由金属离子和酸根离子构成的化合物。除了氯化钠以外,还有很多,例如碳酸钙,碳酸钠等。
大理石
石灰石
贝壳
珊瑚
物理性质:白色块状固体,不溶于水。
碳酸钙
碳酸钙在自然界中广泛存在,它是大理石和石灰石的主要成分,贝壳、珊瑚、鸡蛋壳等也含有碳酸钙。
华表
建筑材料
钙片
碳酸钙
用途:重要的建筑材料,同时还可以用作补钙剂,在实验室,用于制备二氧化碳等。
化学性质:
1、与酸反应:
2、高温分解:
实验室制二氧化碳
工业制二氧化碳和生石灰
碳酸钙
化学性质:
3、与碳酸反应:
碳酸氢钙分解:
溶洞的形成
碳酸钙
碳酸钠和碳酸氢钠
碳酸钠:白色粉末状固体,易溶于水,它的水溶液呈碱性,俗名纯碱或苏打。
碳酸氢钠:白色粉末状固体,可溶于水,它的水溶液呈碱性,俗名小苏打。
碳酸钠和碳酸氢钠
物理性质相似,化学性质比较相似。他们都能与酸反应。
除此之外,碳酸钠还能和澄清石灰水发生反应
现象:澄清石灰水变浑浊。
碳酸钠
碳酸钠、碳酸钙都能与盐酸发生反应,与他们的组成有很大的关系,它们都含有碳酸根离子。
如何检验碳酸根离子?
碳酸根离子的检验
操作:取样;滴加稀盐酸;将产生的气体通入澄清石灰水。
现象:溶液中冒气泡,并且产生的气体能使澄清石灰水变浑浊。
结论:含有碳酸根离子
碳酸根离子的检验
练习
生活中,大理石地板如果不慎滴上了醋或者其他酸,擦干地板以后,表面变得没有那么光亮了,为什么?
大理石的主要成分是碳酸钙,会和酸发生反应。表面被腐蚀,反应方程式如下:
小结
碳酸钙:白色固体,不溶于水,大理石或石灰石的主要成分
碳酸钠:白色粉末状固体,易溶于水,它的水溶液呈碱性,俗名纯碱或苏打。
碳酸氢钠:白色粉末状固体,可溶于水,它的水溶液呈碱性,俗名小苏打。
之前学的这四个反应属于什么基本反应类型呢?
复分解反应
复分解反应
定义:由两种化合物相互交换成分,生成另外两种化合物的反应,这样的反应叫复分解反应。
表达式:AB + CD→ AD + CB
特点:双交换,价不变
任何两个化合物相互交换成分,都能生成新的物质吗?
实验一:CuSO4溶液+NaOH溶液
探究复分解反应发生的条件
现象:生成蓝色沉淀
反应方程式为:
探究复分解反应发生的条件
实验二:CuSO4溶液+BaCl2溶液
现象:生成白色沉淀
反应方程式为:
这两个反应有什么共同的现象?
都有沉淀产生
探究复分解反应发生的条件
下面是我们学过的几个中和反应,它们有什么共同之处?
都有水产生
探究复分解反应发生的条件
下面是我们学过的几个碳酸钠、碳酸钙与盐酸的反应,它们有什么共同的现象?
都有气体产生
只有当两种化合物交换成分,生成物中有沉淀或有气体或有水生成时,(至少满足上述条件之一),复分解反应才可以发生
复分解反应发生的条件
常见的复分解反应类型
盐的溶解性
判断一下,下面几个反应,能不能发生复分解反应?
稀硫酸
判断依据
能
能
能
不能
生成水
不能生成水、气体、沉淀
生成二氧化碳气体
生成硫酸钡沉淀
NaOH溶液
NaCl溶液
练习
下列各组物质的溶液,不能发生复分解反应的是 ( )
A、HCl,Ca(OH)2 B、Na2CO3,H2SO4C、AgNO3,BaCl2 D、KCl,CuSO4
D
练习
下列各组溶液,不加其它试剂就能鉴别的是( )(多选)
A、Na2CO3、HCl、H2SO4、NaNO3B、K2CO3、H2SO4、HNO3、BaCl2C、HCl、AgNO3、HNO3、NaCl
D、NaOH、FeCl3、MgCl2、BaCl2
BD
练习
下列化学反应属复分解反应的是( )
A、Zn+H2SO4 =ZnSO4+H2↑
B、2KMnO4 K2MnO4+MnO2+O2↑
C、CaO+H2O= Ca(OH)2
D、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
D
小结
复分解反应:由两种化合物相互交换成分,生成另外两种化合物的反应。
复分解反应条件:两种化合物交换成分,生成物中有沉淀或有气体或有水生成时复分解反应才可以发生。
课本练习
1.解释下列现象。
(1)鸡蛋壳的主要成分是碳酸钙。将一个新鲜的鸡蛋放在盛有足量稀盐酸的玻璃杯中。可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
(2)馒头、面包等发面食品的一个特点是面团中有许多小孔,它们使发面食品松软可口。根据发酵粉(含碳酸氢钠和有机酸等)可与面粉、水混合直接制作发面食品的事实,说明碳酸氢钠在其中的作用。
2.通过一个阶段的化学学习,我们已经认识了许多物质,它们有的是单质,有的是氧化物,有的是酸、碱、盐。请用化学式举几个例子。
课本练习
课本练习
3.下列反应中不属于复分解反应的是( )
课本练习
4.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们提出了如下假设:
假设一:该溶液没有变质
假设二:该溶液部分变质
假设三:该溶液全部变质
请设计实验方案,分别验证以上假设,检验叙述实验步骤和现象,并写出相关反应的化学方程式。
课本练习
5.亚硝酸钠是一种工业用盐。它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性。如果让你来鉴别亚硝酸钠和食盐,你选用什么试剂,如何操作?
课本练习
6.氯化钠在生活、生产中的用途非常广泛,请通过查阅报纸、书刊、网络和访谈等,了解氯化钠的用途,并以“氯化钠的妙用”为题编制资料卡片。
总结
常见的盐
氯化钠
碳酸钙
白色固体,易溶于水,有咸味
粗盐提纯:溶解、过滤、蒸发
白色固体,不溶于水
大理石或石灰石的主要成分
总结
常见的盐
碳酸钠
碳酸氢钠
俗名纯碱或苏打
白色固体,易溶于水
俗名小苏打
白色固体,可溶于水
生活中常见的盐
日常生活中所说的盐,通常指食盐,你想一下它都有哪些物理性质呢?
盐田
盐井
盐湖
盐矿
氯化钠
物理性质:白色颗粒状固体,易溶于水,有咸味。
广泛存在于海水、盐湖、盐矿中。
用途广泛:
生理盐水
调味品和防腐剂
融雪剂
氯化钠
生活中作为调味品和防腐剂;
农业上用于选种;
医疗上用于制生理盐水;
交通上作融雪剂;
同时还是化工生产的原料等。
粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如: 等。
不能直接食用,必须除杂和提纯之后才能食用。
粗盐
粗盐中难溶性杂质的去除
粗盐中难溶性杂质的去除
实验步骤:
1、溶解:
称取5.0g食盐,用药匙将粗盐逐渐加入盛有10mL水的烧杯中,边加边用玻璃棒搅拌,一直到粗盐不再溶解为止。
称量剩下的粗盐,确定10mL水里溶解了多少克粗盐。
粗盐中难溶性杂质的去除
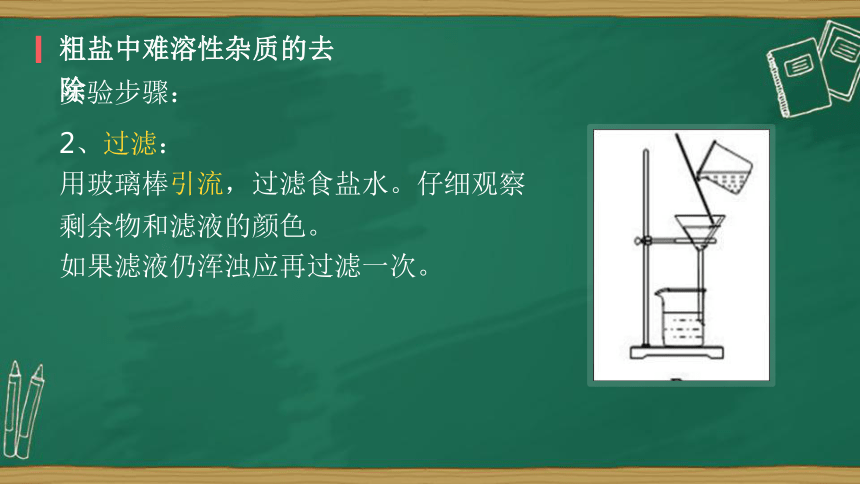
2、过滤:
用玻璃棒引流,过滤食盐水。仔细观察剩余物和滤液的颜色。
如果滤液仍浑浊应再过滤一次。
实验步骤:
粗盐中难溶性杂质的去除
3、蒸发结晶:
将滤液倒入蒸发皿,加热,过程中用玻璃棒不断搅拌;
实验步骤:
4、计算产率:
把蒸发皿中的晶体称量,并计算产率,最后转移到指定容器中。
粗盐中难溶性杂质的去除
上面三个实验操作,溶解、过滤、蒸发结晶,都用到了玻璃棒,他们的作用分别是什么?
溶解时:搅拌,加速溶解;
过滤时:引流;
蒸发结晶时: 搅拌,防止液体飞溅。
练习
1.下列说法正确的是( )
A.盐都能食用,故称为食盐
B.盐就是食盐,易溶于水
C.盐都有咸味,都是白色固体
D.盐是一类物质的总称
2.食盐是一种重要的化工原料,可用于生产:①金属钠②氯气③盐酸④硫酸⑤烧碱⑥纯碱等,以上正确的是( )
A.①②③⑤⑥ B.③④⑤
C.①④⑤⑥ D.①②③④⑤⑥
D
A
小结
氯化钠 :白色颗粒状固体,易溶于水,有咸味。
粗盐提纯的步骤:溶解、过滤、蒸发
有的同学说,盐就是食盐,这样说对吗?
当然是错误的!盐是由金属离子和酸根离子构成的化合物。除了氯化钠以外,还有很多,例如碳酸钙,碳酸钠等。
大理石
石灰石
贝壳
珊瑚
物理性质:白色块状固体,不溶于水。
碳酸钙
碳酸钙在自然界中广泛存在,它是大理石和石灰石的主要成分,贝壳、珊瑚、鸡蛋壳等也含有碳酸钙。
华表
建筑材料
钙片
碳酸钙
用途:重要的建筑材料,同时还可以用作补钙剂,在实验室,用于制备二氧化碳等。
化学性质:
1、与酸反应:
2、高温分解:
实验室制二氧化碳
工业制二氧化碳和生石灰
碳酸钙
化学性质:
3、与碳酸反应:
碳酸氢钙分解:
溶洞的形成
碳酸钙
碳酸钠和碳酸氢钠
碳酸钠:白色粉末状固体,易溶于水,它的水溶液呈碱性,俗名纯碱或苏打。
碳酸氢钠:白色粉末状固体,可溶于水,它的水溶液呈碱性,俗名小苏打。
碳酸钠和碳酸氢钠
物理性质相似,化学性质比较相似。他们都能与酸反应。
除此之外,碳酸钠还能和澄清石灰水发生反应
现象:澄清石灰水变浑浊。
碳酸钠
碳酸钠、碳酸钙都能与盐酸发生反应,与他们的组成有很大的关系,它们都含有碳酸根离子。
如何检验碳酸根离子?
碳酸根离子的检验
操作:取样;滴加稀盐酸;将产生的气体通入澄清石灰水。
现象:溶液中冒气泡,并且产生的气体能使澄清石灰水变浑浊。
结论:含有碳酸根离子
碳酸根离子的检验
练习
生活中,大理石地板如果不慎滴上了醋或者其他酸,擦干地板以后,表面变得没有那么光亮了,为什么?
大理石的主要成分是碳酸钙,会和酸发生反应。表面被腐蚀,反应方程式如下:
小结
碳酸钙:白色固体,不溶于水,大理石或石灰石的主要成分
碳酸钠:白色粉末状固体,易溶于水,它的水溶液呈碱性,俗名纯碱或苏打。
碳酸氢钠:白色粉末状固体,可溶于水,它的水溶液呈碱性,俗名小苏打。
之前学的这四个反应属于什么基本反应类型呢?
复分解反应
复分解反应
定义:由两种化合物相互交换成分,生成另外两种化合物的反应,这样的反应叫复分解反应。
表达式:AB + CD→ AD + CB
特点:双交换,价不变
任何两个化合物相互交换成分,都能生成新的物质吗?
实验一:CuSO4溶液+NaOH溶液
探究复分解反应发生的条件
现象:生成蓝色沉淀
反应方程式为:
探究复分解反应发生的条件
实验二:CuSO4溶液+BaCl2溶液
现象:生成白色沉淀
反应方程式为:
这两个反应有什么共同的现象?
都有沉淀产生
探究复分解反应发生的条件
下面是我们学过的几个中和反应,它们有什么共同之处?
都有水产生
探究复分解反应发生的条件
下面是我们学过的几个碳酸钠、碳酸钙与盐酸的反应,它们有什么共同的现象?
都有气体产生
只有当两种化合物交换成分,生成物中有沉淀或有气体或有水生成时,(至少满足上述条件之一),复分解反应才可以发生
复分解反应发生的条件
常见的复分解反应类型
盐的溶解性
判断一下,下面几个反应,能不能发生复分解反应?
稀硫酸
判断依据
能
能
能
不能
生成水
不能生成水、气体、沉淀
生成二氧化碳气体
生成硫酸钡沉淀
NaOH溶液
NaCl溶液
练习
下列各组物质的溶液,不能发生复分解反应的是 ( )
A、HCl,Ca(OH)2 B、Na2CO3,H2SO4C、AgNO3,BaCl2 D、KCl,CuSO4
D
练习
下列各组溶液,不加其它试剂就能鉴别的是( )(多选)
A、Na2CO3、HCl、H2SO4、NaNO3B、K2CO3、H2SO4、HNO3、BaCl2C、HCl、AgNO3、HNO3、NaCl
D、NaOH、FeCl3、MgCl2、BaCl2
BD
练习
下列化学反应属复分解反应的是( )
A、Zn+H2SO4 =ZnSO4+H2↑
B、2KMnO4 K2MnO4+MnO2+O2↑
C、CaO+H2O= Ca(OH)2
D、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
D
小结
复分解反应:由两种化合物相互交换成分,生成另外两种化合物的反应。
复分解反应条件:两种化合物交换成分,生成物中有沉淀或有气体或有水生成时复分解反应才可以发生。
课本练习
1.解释下列现象。
(1)鸡蛋壳的主要成分是碳酸钙。将一个新鲜的鸡蛋放在盛有足量稀盐酸的玻璃杯中。可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
(2)馒头、面包等发面食品的一个特点是面团中有许多小孔,它们使发面食品松软可口。根据发酵粉(含碳酸氢钠和有机酸等)可与面粉、水混合直接制作发面食品的事实,说明碳酸氢钠在其中的作用。
2.通过一个阶段的化学学习,我们已经认识了许多物质,它们有的是单质,有的是氧化物,有的是酸、碱、盐。请用化学式举几个例子。
课本练习
课本练习
3.下列反应中不属于复分解反应的是( )
课本练习
4.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们提出了如下假设:
假设一:该溶液没有变质
假设二:该溶液部分变质
假设三:该溶液全部变质
请设计实验方案,分别验证以上假设,检验叙述实验步骤和现象,并写出相关反应的化学方程式。
课本练习
5.亚硝酸钠是一种工业用盐。它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性。如果让你来鉴别亚硝酸钠和食盐,你选用什么试剂,如何操作?
课本练习
6.氯化钠在生活、生产中的用途非常广泛,请通过查阅报纸、书刊、网络和访谈等,了解氯化钠的用途,并以“氯化钠的妙用”为题编制资料卡片。
总结
常见的盐
氯化钠
碳酸钙
白色固体,易溶于水,有咸味
粗盐提纯:溶解、过滤、蒸发
白色固体,不溶于水
大理石或石灰石的主要成分
总结
常见的盐
碳酸钠
碳酸氢钠
俗名纯碱或苏打
白色固体,易溶于水
俗名小苏打
白色固体,可溶于水
同课章节目录
