9.2.5 溶解度曲线及其应用同步练习—2021-2022学年九年级化学人教版下册(word版 含解析)
文档属性
| 名称 | 9.2.5 溶解度曲线及其应用同步练习—2021-2022学年九年级化学人教版下册(word版 含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 203.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-03 00:00:00 | ||
图片预览




文档简介
9.2.5 溶解度曲线及其应用
一.选择题(共15小题)
1.如图是甲、乙、丙三种物质的溶解度曲线图,请据图判断下列说法正确的是( )
A.甲的溶解度大于乙和丙
B.将t1℃时甲的饱和溶液变为t2℃时甲的饱和溶液,可以采用蒸发水的方法
C.当大量甲的固体中含有少量固体丙时,可以采用蒸发结晶的方法提纯甲
D.将t2℃下甲的饱和溶液150g降温到t1℃,则可析出晶体质量为30g
2.硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。下列说法正确的是( )
A.硝酸钾的溶解度大于氯化铵的溶解度
B.只有③烧杯中溶液是R的饱和溶液
C.t1℃时,30g氯化铵加入到50g水中溶解可得80g溶液
D.硝酸钾中混有少量氯化铵可采用降温结晶的方法提纯
3.甲、乙、丙三种固体物质溶解度曲线如图所示,下列说法错误的是( )
A.a、b、c三点对应的甲溶液中,a、b一定为饱和溶液
B.阴影区域中,甲、丙均处于不饱和状态
C.t3℃时,将22g乙加入到50g水中充分搅拌后剩余7g乙未溶解
D.t2℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量:甲=乙<丙
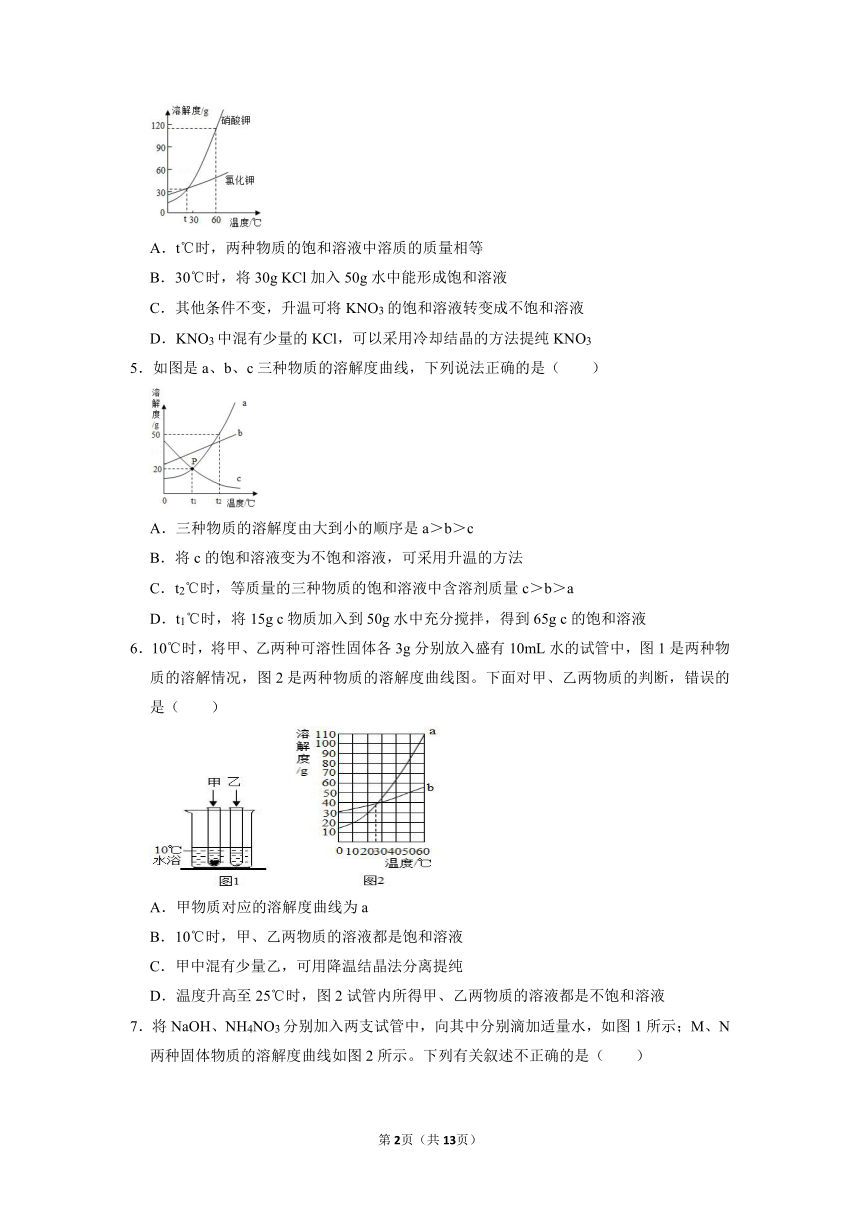
4.KNO3和KCl的溶解度曲线如图,下列说法错误的是( )
A.t℃时,两种物质的饱和溶液中溶质的质量相等
B.30℃时,将30g KCl加入50g水中能形成饱和溶液
C.其他条件不变,升温可将KNO3的饱和溶液转变成不饱和溶液
D.KNO3中混有少量的KCl,可以采用冷却结晶的方法提纯KNO3
5.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.三种物质的溶解度由大到小的顺序是a>b>c
B.将c的饱和溶液变为不饱和溶液,可采用升温的方法
C.t2℃时,等质量的三种物质的饱和溶液中含溶剂质量c>b>a
D.t1℃时,将15g c物质加入到50g水中充分搅拌,得到65g c的饱和溶液
6.10℃时,将甲、乙两种可溶性固体各3g分别放入盛有10mL水的试管中,图1是两种物质的溶解情况,图2是两种物质的溶解度曲线图。下面对甲、乙两物质的判断,错误的是( )
A.甲物质对应的溶解度曲线为a
B.10℃时,甲、乙两物质的溶液都是饱和溶液
C.甲中混有少量乙,可用降温结晶法分离提纯
D.温度升高至25℃时,图2试管内所得甲、乙两物质的溶液都是不饱和溶液
7.将NaOH、NH4NO3分别加入两支试管中,向其中分别滴加适量水,如图1所示;M、N两种固体物质的溶解度曲线如图2所示。下列有关叙述不正确的是( )
A.N的溶解度曲线为A
B.若N的饱和溶液中有少量的M,可以用降温结晶的方法提纯N
C.将t2℃时两种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:M>N
D.t2℃时,将42g B曲线所代表物质的饱和溶液降温至t1℃,需再加入7g该固体才能使溶液达到饱和
8.甲、乙两种固体的溶解度曲线如图所示。下列说法中,正确的是( )
A.甲的溶解度大于乙的溶解度
B.20℃时,甲和乙的饱和溶液中所含溶质质量相等
C.40℃时,甲的饱和溶液中溶质和溶液的质量比为1:3
D.40℃时,向100g水中加入50g乙,所得溶液的质量为150g
9.如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是( )
A.甲物质的溶解度为50克
B.甲物质的溶解度大于乙物质的溶解度
C.t2℃时,在100g饱和溶液中含有50g甲物质
D.t1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液
10.甲、乙两固体的溶解度曲线如图所示。下列说法正确的是( )
A.t1℃时,甲、乙饱和溶液中溶质的质量相等
B.t2℃时,等质量的甲、乙饱和溶液中溶剂质量:甲<乙
C.t1℃时,将30g甲加入50g水中配制成80g甲的饱和溶液
D.t2℃时,乙中混有少量的甲,用降温结晶的方法提纯乙
11.20℃时,将a克的甲和乙两种固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热至50℃时如图2(不考虑水分蒸发),甲、乙两种物质的溶解度曲线如图3。下列说法不正确的是( )
A.30℃时,向50g水中加入15g M,所得溶液为饱和溶液
B.甲物质为图3中的M
C.图2中得到的一定都是不饱和溶液
D.50℃时M、N两物质的饱和溶液降温至30℃,M析出晶体质量大
12.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲的溶解度大于丙的溶解度
B.t2℃时,若将20g的甲、乙、丙三种物质分别加入盛有50g水的烧杯中,充分溶解后,能形成饱和溶液的是甲、乙
C.t3℃时,等质量的甲、乙、丙三种物质的饱和溶液降温到t1℃,析出固体最多的是甲
D.甲中混有少量的乙,提纯甲的方法是蒸发结晶
13.a、b、c三种物质的溶解度曲线如图所示,下列说法正确的是( )
A.t1时,等质量的a、c溶液中溶质的质量相等
B.t2时,将a、b、c三种饱和溶液同时降温到t1,析出晶体的质量大小关系为a>b>c
C.将相同质量的固体a、b溶解配制成t2时的饱和溶液,得到的溶液质量为a>b
D.a物质中混有少量c,可采用降温结晶的方式提纯a
14.如图是KCl、KNO3两种固体物质的溶解度曲线,下列说法正确的是( )
A.KNO3的溶解度大于KCl的溶解度
B.t1℃时KNO3的溶解度是70
C.在t1℃时,100g KNO3饱和溶液和100g KCl饱和溶液,KCl饱和溶液中的溶剂质量大于KNO3饱和溶液中的溶剂质量
D.在t2℃时,欲使KNO3、KCl两种物质的溶液分别降到t℃时,析出晶体的质量KCl一定小于KNO3
15.结合KNO3和NH4Cl的溶解度曲线判断,下列叙述错误的是( )
A.t1℃时,两种物质的溶解度相等
B.两种物质的溶解度都随温度升高而增大
C.升高温度可将接近饱和的KNO3溶液变成饱和溶液
D.将t2℃的饱和NH4Cl溶液降温到t1℃,溶液质量减小
二.填空题(共5小题)
16.如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时,甲物质的溶解度 乙物质的溶解度(填大于、小于或等于)。
(2)甲、乙两种物质的溶解度受温度影响较小的是 物质。
(3)t2℃时,把50g乙物质放入50g水中,充分搅拌,所得溶液是 溶液(填“饱和”或“不饱和”)。
(4)t2℃时,有一接近饱和的甲溶液,使其变为饱和溶液可采用 的方法(任写一种)。
17.如图是a、b、c三种物质的溶解度曲线,请据图回答:
(1)t2℃时,a、b、c三种物质的溶解度由大到小的顺序是 ;
(2)t2℃时,将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为 g,形成的溶液是 (填“饱和溶液”或“不饱和溶液”);
(3)通过 (“升高”或“降低”)温度可将c的不饱和溶液变为饱和溶液。
18.如图为甲、乙、丙三种固体物质的溶解度曲线,请回答。
(1)P点的表示意义是 。
(2)t2℃时,将25g甲物质放入50g水中并充分搅拌,所得溶液的质量为 g。
(3)在质量不变的情况下,将丙物质的不饱和溶液变为饱和溶液的方法是 。
(4)t1℃时,甲、乙饱和溶液分别蒸发掉10g水,析出固体的质量甲 (填“>”或“<”或“=”“无法判断”)乙。
19.如图是MgCl2、KCl和MgSO4的溶解度曲线。t1℃时三种物质的饱和溶液中,溶质质量分数由大到小的顺序为 ,t2℃时的三种物质的饱和溶液分别升温至t3℃,有晶体析出的是 ,若要配制175g 20% MgCl2溶液,需t2℃时饱和的MgCl2溶液为 g。
20.20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象。
(1)20℃时, (填“A”或“B”)试管中的溶液一定是饱和溶液。
(2)图2中表示甲物质的溶解度曲线的是 (填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是 。
(3)从a、b混合物中得到较纯净的a所采用的方法是 。
参考答案与试题解析
一.选择题(共15小题)
1.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度的大小也不能确定,故A错误;
B、甲物质的溶解度随温度的升高而增大,将t1℃时甲的饱和溶液变为t2℃时甲的饱和溶液,可以采用蒸发水的方法,故B正确;
C、甲物质的溶解度随温度的降低而减小,丙物质的溶解度随温度的降低而增大,所以当大量甲的固体中含有少量固体丙时,可以采用降温结晶的方法提纯甲,故C错误;
D、t2℃时,甲物质的溶解度是50g,甲的饱和溶液150g中,含有溶质50g,溶剂100g,降温到t1℃,100g水中可以溶解30g的固体,可析出晶体质量为20g,故D错误。
故选:B。
2.【解答】解:A、不知道温度范围,不能比较两种物质溶解度大小,该选项说法不正确;
B、t2℃时硝酸钾溶解度是60g,氯化铵溶解度小于60g,②中没有析出固体,说明R是硝酸钾,②③烧杯中溶液是R的饱和溶液,该选项说法不正确;
C、t1℃时氯化铵溶解度是40g,30g氯化铵加入到50g水中溶解,能够溶解20g,可得70g溶液,该选项说法不正确;
D、硝酸钾溶解度受温度变化影响较大,氯化铵溶解度受温度变化影响较小,硝酸钾中混有少量氯化铵可采用降温结晶的方法提纯,该选项说法正确。
故选:D。
3.【解答】解:A、由溶解度曲线的意义可知,a、b、c三点对应的甲溶液中,a、b在甲的溶解度曲线上,一定为饱和溶液,c在甲的溶解度曲线下面,一定为不饱和溶液,故A正确;
B、由溶解度曲线的意义可知,阴影区域在甲、丙的溶解度曲线的下方,甲、丙均处于不饱和状态,故B正确;
C、t3℃时,乙的溶解度是30g,由溶解读的含义可知,将22g乙加入到50g水中充分搅拌后只能溶解15g,剩余乙未溶解的质量为:22g﹣15g=7g,故C正确;
D、由溶解度曲线的意义可知,t2℃时,将甲、乙、丙的饱和溶液降温到t1℃,甲、乙要析出晶体,且甲析出的晶体多;丙物质的溶解度增大,没有析出晶体,所以t2℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量:丙>乙>甲,故D错误。
故选:D。
4.【解答】解:A、t℃时,两种物质的饱和溶液的质量不能确定,所以饱和溶液中溶质的质量也不能确定,故A错误;
B、30℃时,氯化钾的溶解度小于60g,所以将30gKCl加入50g水中能形成饱和溶液,故B正确;
C、硝酸钾的溶解度随温度的升高而增大,所以其他条件不变,升温可将KNO3的饱和溶液转变成不饱和溶液,故C正确;
D、硝酸钾的溶解度受温度变化影响较大,氯化钾的溶解度受温度变化影响较小,所以KNO3中混有少量的KCl,可以采用冷却结晶的方法提纯KNO3,故D正确。
故选:A。
5.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度也不能确定,故A错误;
B、c物质的溶解度随温度的降低而增大,所以将c的饱和溶液变为不饱和溶液,可采用降温的方法,故B错误;
C、t2℃时,a物质的溶解度最大,c物质的溶解度最小,所以等质量的三种物质的饱和溶液中含溶剂质量c>b>a,故C正确;
D、t1℃时,c物质的溶解度是20g,将15gc物质加入到50g水中充分搅拌,只能溶解10g的固体,得到60gc的饱和溶液,故D错误。
故选:C。
6.【解答】解:A、10℃时,b物质的溶解度大于a物质的溶解度,将甲、乙两种可溶性固体各3g分别放入盛有10mL水的试管中,甲试管中有剩余,所以甲物质对应的溶解度曲线为a,故A正确;
B、10℃时,b物质的溶解度大于30g,因此该温度下的10g水中加入3gb物质能完全溶解,所得乙物质的溶液是不饱和溶液,故B错误;
C、甲物质的溶解度受温度变化影响较大,乙物质的溶解度受温度变化影响较小,所以甲中混有少量乙,可用降温结晶法分离提纯,故C正确;
D、温度升高至25℃时,甲、乙物质的溶解度相等,但是乙物质在10℃时就已经全部溶解了,所以图2试管内所得甲、乙两物质的溶液都是不饱和溶液,故D正确。
故选:B。
7.【解答】解:A、氢氧化钠溶于水放热,温度升高,M溶液变浑浊,说明M的溶解度随着温度升高而减小,硝酸铵溶于水吸热,温度降低,N溶液变浑浊,说明N的溶解度随着温度降低而减小,N的溶解度曲线为A,该选项说法正确;
B、若N的饱和溶液中有少量的M,可以用降温结晶的方法提纯N,该选项说法正确;
C、不能比较析出固体的质量,是因为不知道溶液质量,该选项说法不正确;
D、t2℃时B曲线所代表物质的溶解度是20g,42g B曲线所代表物质的饱和溶液中溶质质量:42g××100%=7g,溶剂质量是35g,加入7g该固体,溶质质量是14g,35g溶剂溶解14g固体恰好饱和,该选项说法正确。
故选:C。
8.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度也不能确定,故A错误;
B、20℃时,甲和乙的饱和溶液的质量不能确定,所以饱和溶液中所含溶质质量也不能确定,故B错误;
C、40℃时,甲物质的溶解度是50g,所以甲的饱和溶液中溶质和溶液的质量比为50g:150g=1:3,故C正确;
D、40℃时,乙物质的溶解度是40g,所以向100g水中加入50g乙,只能溶解40g的固体,所得溶液的质量为140g,故D错误。
故选:C。
9.【解答】解:A、不知道温度范围,不能确定物质的溶解度大小,该选项说法不正确;
B、不知道温度范围,不能比较物质的溶解度大小,该选项说法不正确;
C、t2℃时甲的溶解度是50g,在100g饱和溶液中含有:100g××100%=33.3g甲物质,该选项说法不正确;
D、t1℃时甲和乙的溶解度都是30g,甲和乙各30g分别加入100g水中,均形成饱和溶液,该选项说法正确。
故选:D。
10.【解答】解:A、t1℃时,甲、乙饱和溶液中溶质的质量不一定相等,是因为不知道溶液质量,该选项说法不正确;
B、t2℃时甲的溶解度大于乙,等质量的甲、乙饱和溶液中溶剂质量:甲<乙,该选项说法正确;
C、t1℃时甲的溶解度是30g,将30g甲加入50g水中,能够溶解15g,配制成65g甲的饱和溶液,该选项说法不正确;
D、甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响较小,t2℃时,乙中混有少量的甲,用蒸发结晶的方法提纯乙,该选项说法不正确。
故选:B。
11.【解答】解:A、30℃时M的溶解度是20g,向50g水中加入15gM,不能完全溶解,所得溶液为饱和溶液,该选项说法正确;
B、甲物质在20℃时的溶解度小于乙,为图3中的M,该选项说法正确;
C、由图中信息可知,a小于20,50℃时两种物质溶解度都大于20g,因此图2中得到的一定都是不饱和溶液,该选项说法正确;
D、不知道饱和溶液质量,不能比较析出固体质量大小,该选项说法不正确。
故选:D。
12.【解答】解:A、不知道温度范围,不能比较两种物质溶解度大小,该选项说法不正确;
B、t2℃时甲、乙溶解度大于40g,丙溶解度小于30g,若将20g的甲、乙、丙三种物质分别加入盛有50g水的烧杯中,充分溶解后,能形成饱和溶液的是丙,该选项说法不正确;
C、t3℃时,等质量的甲、乙、丙三种物质的饱和溶液降温到t1℃,析出固体最多的是甲,是因为该温度范围内,甲的溶解度质量差最大,该选项说法正确;
D、甲中混有少量的乙,提纯甲的方法是降温结晶,是因为甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响较小,该选项说法不正确。
故选:C。
13.【解答】解:A、t1时,等质量的a、c溶液的状态不能确定,所以溶液中溶质的质量不能确定,故A错误;
B、t2时,将a、b、c三种饱和溶液同时降温到t1,饱和溶液的质量不能确定,所以析出晶体的质量大小也不能确定,故B错误;
C、t2时,a物质的溶解度大于b物质的溶解度,所以将相同质量的固体a、b溶解配制成t2时的饱和溶液,得到的溶液质量为a<b,故C错误;
D、a物质的溶解度随温度的降低而减小,c物质的溶解度随温度的降低而增大,所以a物质中混有少量c,可采用降温结晶的方式提纯a,故D正确。
故选:D。
14.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度也不能确定,故A错误;
B、通过分析溶解度曲线可知,t1℃时,KNO3的溶解度是70g,故B错误;
C、在t1℃时,硝酸钾的溶解度大于氯化钾的溶解度,所以100gKNO3饱和溶液和100gKCl饱和溶液,KCl饱和溶液中的溶剂质量大于KNO3饱和溶液中的溶剂质量,故C正确;
D、在t2℃时,欲使KNO3、KCl两种物质的溶液分别降到t℃时,溶液的质量和状态不能确定,所以析出晶体的质量也不能确定,故D错误。
故选:C。
15.【解答】解:A、通过分析溶解度曲线可知,t1℃时,两种物质的溶解度相等,故A正确;
B、两种物质的溶解度都随温度升高而增大,故B正确;
C、硝酸钾的溶解度随温度的降低而减小,所以降低温度可将接近饱和的KNO3溶液变成饱和溶液,故C错误;
D、将t2℃的饱和NH4Cl溶液降温到t1℃,溶解度减小,析出晶体,所以溶液质量减小,故D正确。
故选:C。
二.填空题(共5小题)
16.【解答】解:(1)通过分析溶解度曲线可知,t1℃时,甲物质的溶解度等于乙物质的溶解;
(2)乙物质的溶解度曲线比较平缓,所以甲、乙两种物质的溶解度受温度影响较小的是乙物质;
(3)t2℃时,乙物质的溶解度是80g,所以把50g乙物质放入50g水中,充分搅拌,所得溶液是饱和溶液;
(4)甲物质的溶解度随温度的升高而增大,所以t2℃时,有一接近饱和的甲溶液变为饱和溶液,可采用增加溶质,蒸发溶剂,降低温度的方法。
故答案为:(1)等于;
(2)乙;
(3)饱和;
(4)增加溶质,蒸发溶剂,降低温度。
17.【解答】解:(1)通过分析溶解度曲线可知,t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c;
(2)t2℃时,a物质的溶解度是50g,所以将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为150g,形成的溶液是饱和溶液;
(3)c物质的溶解度随温度的升高而减小,所以通过升高温度可将c的不饱和溶液变为饱和溶液。
故答案为:(1)a>b>c;
(2)150;饱和;
(3)升高。
18.【解答】解:(1)通过分析溶解度曲线可知,P点的表示意义是:在t3℃时,甲、乙两物质的溶解度相等都为40g;
(2)t2℃时,甲物质的溶解度是25g,将25g甲物质放入50g水中并充分搅拌,只能溶解12.5g的固体,所得溶液的质量为62.5g;
(3)丙物质的溶解度随温度的升高而减小,所以在质量不变的情况下,将丙物质的不饱和溶液变为饱和溶液的方法是升高温度;
(4)t1℃时,甲物质的溶解度小于乙物质的溶解度,所以甲、乙饱和溶液分别蒸发掉10g水,析出固体的质量甲<乙。
故答案为:(1)在t3℃时,甲、乙两物质的溶解度相等都为40g;
(2)62.5;
(3)升高温度;
(4)<。
19.【解答】解:t1℃时,氯化镁的溶解度最大,氯化钾的溶解度最小,所以三种物质的饱和溶液中,溶质质量分数由大到小的顺序为:MgCl2>MgSO4>KCl;t2℃时的三种物质的饱和溶液分别升温至t3℃,硫酸镁的溶解度减小,氯化钾、氯化镁的溶解度增大,所以有晶体析出的是MgSO4;若要配制175g20% MgCl2溶液,需t2℃时饱和的MgCl2溶液为=85g。
故答案为:MgCl2>MgSO4>KCl;MgSO4;85。
20.【解答】解:(1)20℃时,A试管中有没有溶解的固体,一定是饱和溶液。
故填:A。
(2)20℃时甲的溶解度小于乙,图2中表示甲物质的溶解度曲线的是b,要使A试管中剩余的固体继续溶解可采用的方法是加热或加溶剂等。
故填:b;加热或加溶剂等。
(3)a的溶解度受温度变化影响较大,b的溶解度受温度变化影响较小,从a、b混合物中得到较纯净的a所采用的方法是降温结晶。
故填:降温结晶。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2021/12/3 9:58:34;用户:化学;邮箱:yingchuang2@xyh.com;学号:31596026
第1页(共3页)
第1页(共3页)
一.选择题(共15小题)
1.如图是甲、乙、丙三种物质的溶解度曲线图,请据图判断下列说法正确的是( )
A.甲的溶解度大于乙和丙
B.将t1℃时甲的饱和溶液变为t2℃时甲的饱和溶液,可以采用蒸发水的方法
C.当大量甲的固体中含有少量固体丙时,可以采用蒸发结晶的方法提纯甲
D.将t2℃下甲的饱和溶液150g降温到t1℃,则可析出晶体质量为30g
2.硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。下列说法正确的是( )
A.硝酸钾的溶解度大于氯化铵的溶解度
B.只有③烧杯中溶液是R的饱和溶液
C.t1℃时,30g氯化铵加入到50g水中溶解可得80g溶液
D.硝酸钾中混有少量氯化铵可采用降温结晶的方法提纯
3.甲、乙、丙三种固体物质溶解度曲线如图所示,下列说法错误的是( )
A.a、b、c三点对应的甲溶液中,a、b一定为饱和溶液
B.阴影区域中,甲、丙均处于不饱和状态
C.t3℃时,将22g乙加入到50g水中充分搅拌后剩余7g乙未溶解
D.t2℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量:甲=乙<丙
4.KNO3和KCl的溶解度曲线如图,下列说法错误的是( )
A.t℃时,两种物质的饱和溶液中溶质的质量相等
B.30℃时,将30g KCl加入50g水中能形成饱和溶液
C.其他条件不变,升温可将KNO3的饱和溶液转变成不饱和溶液
D.KNO3中混有少量的KCl,可以采用冷却结晶的方法提纯KNO3
5.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.三种物质的溶解度由大到小的顺序是a>b>c
B.将c的饱和溶液变为不饱和溶液,可采用升温的方法
C.t2℃时,等质量的三种物质的饱和溶液中含溶剂质量c>b>a
D.t1℃时,将15g c物质加入到50g水中充分搅拌,得到65g c的饱和溶液
6.10℃时,将甲、乙两种可溶性固体各3g分别放入盛有10mL水的试管中,图1是两种物质的溶解情况,图2是两种物质的溶解度曲线图。下面对甲、乙两物质的判断,错误的是( )
A.甲物质对应的溶解度曲线为a
B.10℃时,甲、乙两物质的溶液都是饱和溶液
C.甲中混有少量乙,可用降温结晶法分离提纯
D.温度升高至25℃时,图2试管内所得甲、乙两物质的溶液都是不饱和溶液
7.将NaOH、NH4NO3分别加入两支试管中,向其中分别滴加适量水,如图1所示;M、N两种固体物质的溶解度曲线如图2所示。下列有关叙述不正确的是( )
A.N的溶解度曲线为A
B.若N的饱和溶液中有少量的M,可以用降温结晶的方法提纯N
C.将t2℃时两种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:M>N
D.t2℃时,将42g B曲线所代表物质的饱和溶液降温至t1℃,需再加入7g该固体才能使溶液达到饱和
8.甲、乙两种固体的溶解度曲线如图所示。下列说法中,正确的是( )
A.甲的溶解度大于乙的溶解度
B.20℃时,甲和乙的饱和溶液中所含溶质质量相等
C.40℃时,甲的饱和溶液中溶质和溶液的质量比为1:3
D.40℃时,向100g水中加入50g乙,所得溶液的质量为150g
9.如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是( )
A.甲物质的溶解度为50克
B.甲物质的溶解度大于乙物质的溶解度
C.t2℃时,在100g饱和溶液中含有50g甲物质
D.t1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液
10.甲、乙两固体的溶解度曲线如图所示。下列说法正确的是( )
A.t1℃时,甲、乙饱和溶液中溶质的质量相等
B.t2℃时,等质量的甲、乙饱和溶液中溶剂质量:甲<乙
C.t1℃时,将30g甲加入50g水中配制成80g甲的饱和溶液
D.t2℃时,乙中混有少量的甲,用降温结晶的方法提纯乙
11.20℃时,将a克的甲和乙两种固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热至50℃时如图2(不考虑水分蒸发),甲、乙两种物质的溶解度曲线如图3。下列说法不正确的是( )
A.30℃时,向50g水中加入15g M,所得溶液为饱和溶液
B.甲物质为图3中的M
C.图2中得到的一定都是不饱和溶液
D.50℃时M、N两物质的饱和溶液降温至30℃,M析出晶体质量大
12.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲的溶解度大于丙的溶解度
B.t2℃时,若将20g的甲、乙、丙三种物质分别加入盛有50g水的烧杯中,充分溶解后,能形成饱和溶液的是甲、乙
C.t3℃时,等质量的甲、乙、丙三种物质的饱和溶液降温到t1℃,析出固体最多的是甲
D.甲中混有少量的乙,提纯甲的方法是蒸发结晶
13.a、b、c三种物质的溶解度曲线如图所示,下列说法正确的是( )
A.t1时,等质量的a、c溶液中溶质的质量相等
B.t2时,将a、b、c三种饱和溶液同时降温到t1,析出晶体的质量大小关系为a>b>c
C.将相同质量的固体a、b溶解配制成t2时的饱和溶液,得到的溶液质量为a>b
D.a物质中混有少量c,可采用降温结晶的方式提纯a
14.如图是KCl、KNO3两种固体物质的溶解度曲线,下列说法正确的是( )
A.KNO3的溶解度大于KCl的溶解度
B.t1℃时KNO3的溶解度是70
C.在t1℃时,100g KNO3饱和溶液和100g KCl饱和溶液,KCl饱和溶液中的溶剂质量大于KNO3饱和溶液中的溶剂质量
D.在t2℃时,欲使KNO3、KCl两种物质的溶液分别降到t℃时,析出晶体的质量KCl一定小于KNO3
15.结合KNO3和NH4Cl的溶解度曲线判断,下列叙述错误的是( )
A.t1℃时,两种物质的溶解度相等
B.两种物质的溶解度都随温度升高而增大
C.升高温度可将接近饱和的KNO3溶液变成饱和溶液
D.将t2℃的饱和NH4Cl溶液降温到t1℃,溶液质量减小
二.填空题(共5小题)
16.如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时,甲物质的溶解度 乙物质的溶解度(填大于、小于或等于)。
(2)甲、乙两种物质的溶解度受温度影响较小的是 物质。
(3)t2℃时,把50g乙物质放入50g水中,充分搅拌,所得溶液是 溶液(填“饱和”或“不饱和”)。
(4)t2℃时,有一接近饱和的甲溶液,使其变为饱和溶液可采用 的方法(任写一种)。
17.如图是a、b、c三种物质的溶解度曲线,请据图回答:
(1)t2℃时,a、b、c三种物质的溶解度由大到小的顺序是 ;
(2)t2℃时,将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为 g,形成的溶液是 (填“饱和溶液”或“不饱和溶液”);
(3)通过 (“升高”或“降低”)温度可将c的不饱和溶液变为饱和溶液。
18.如图为甲、乙、丙三种固体物质的溶解度曲线,请回答。
(1)P点的表示意义是 。
(2)t2℃时,将25g甲物质放入50g水中并充分搅拌,所得溶液的质量为 g。
(3)在质量不变的情况下,将丙物质的不饱和溶液变为饱和溶液的方法是 。
(4)t1℃时,甲、乙饱和溶液分别蒸发掉10g水,析出固体的质量甲 (填“>”或“<”或“=”“无法判断”)乙。
19.如图是MgCl2、KCl和MgSO4的溶解度曲线。t1℃时三种物质的饱和溶液中,溶质质量分数由大到小的顺序为 ,t2℃时的三种物质的饱和溶液分别升温至t3℃,有晶体析出的是 ,若要配制175g 20% MgCl2溶液,需t2℃时饱和的MgCl2溶液为 g。
20.20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象。
(1)20℃时, (填“A”或“B”)试管中的溶液一定是饱和溶液。
(2)图2中表示甲物质的溶解度曲线的是 (填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是 。
(3)从a、b混合物中得到较纯净的a所采用的方法是 。
参考答案与试题解析
一.选择题(共15小题)
1.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度的大小也不能确定,故A错误;
B、甲物质的溶解度随温度的升高而增大,将t1℃时甲的饱和溶液变为t2℃时甲的饱和溶液,可以采用蒸发水的方法,故B正确;
C、甲物质的溶解度随温度的降低而减小,丙物质的溶解度随温度的降低而增大,所以当大量甲的固体中含有少量固体丙时,可以采用降温结晶的方法提纯甲,故C错误;
D、t2℃时,甲物质的溶解度是50g,甲的饱和溶液150g中,含有溶质50g,溶剂100g,降温到t1℃,100g水中可以溶解30g的固体,可析出晶体质量为20g,故D错误。
故选:B。
2.【解答】解:A、不知道温度范围,不能比较两种物质溶解度大小,该选项说法不正确;
B、t2℃时硝酸钾溶解度是60g,氯化铵溶解度小于60g,②中没有析出固体,说明R是硝酸钾,②③烧杯中溶液是R的饱和溶液,该选项说法不正确;
C、t1℃时氯化铵溶解度是40g,30g氯化铵加入到50g水中溶解,能够溶解20g,可得70g溶液,该选项说法不正确;
D、硝酸钾溶解度受温度变化影响较大,氯化铵溶解度受温度变化影响较小,硝酸钾中混有少量氯化铵可采用降温结晶的方法提纯,该选项说法正确。
故选:D。
3.【解答】解:A、由溶解度曲线的意义可知,a、b、c三点对应的甲溶液中,a、b在甲的溶解度曲线上,一定为饱和溶液,c在甲的溶解度曲线下面,一定为不饱和溶液,故A正确;
B、由溶解度曲线的意义可知,阴影区域在甲、丙的溶解度曲线的下方,甲、丙均处于不饱和状态,故B正确;
C、t3℃时,乙的溶解度是30g,由溶解读的含义可知,将22g乙加入到50g水中充分搅拌后只能溶解15g,剩余乙未溶解的质量为:22g﹣15g=7g,故C正确;
D、由溶解度曲线的意义可知,t2℃时,将甲、乙、丙的饱和溶液降温到t1℃,甲、乙要析出晶体,且甲析出的晶体多;丙物质的溶解度增大,没有析出晶体,所以t2℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量:丙>乙>甲,故D错误。
故选:D。
4.【解答】解:A、t℃时,两种物质的饱和溶液的质量不能确定,所以饱和溶液中溶质的质量也不能确定,故A错误;
B、30℃时,氯化钾的溶解度小于60g,所以将30gKCl加入50g水中能形成饱和溶液,故B正确;
C、硝酸钾的溶解度随温度的升高而增大,所以其他条件不变,升温可将KNO3的饱和溶液转变成不饱和溶液,故C正确;
D、硝酸钾的溶解度受温度变化影响较大,氯化钾的溶解度受温度变化影响较小,所以KNO3中混有少量的KCl,可以采用冷却结晶的方法提纯KNO3,故D正确。
故选:A。
5.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度也不能确定,故A错误;
B、c物质的溶解度随温度的降低而增大,所以将c的饱和溶液变为不饱和溶液,可采用降温的方法,故B错误;
C、t2℃时,a物质的溶解度最大,c物质的溶解度最小,所以等质量的三种物质的饱和溶液中含溶剂质量c>b>a,故C正确;
D、t1℃时,c物质的溶解度是20g,将15gc物质加入到50g水中充分搅拌,只能溶解10g的固体,得到60gc的饱和溶液,故D错误。
故选:C。
6.【解答】解:A、10℃时,b物质的溶解度大于a物质的溶解度,将甲、乙两种可溶性固体各3g分别放入盛有10mL水的试管中,甲试管中有剩余,所以甲物质对应的溶解度曲线为a,故A正确;
B、10℃时,b物质的溶解度大于30g,因此该温度下的10g水中加入3gb物质能完全溶解,所得乙物质的溶液是不饱和溶液,故B错误;
C、甲物质的溶解度受温度变化影响较大,乙物质的溶解度受温度变化影响较小,所以甲中混有少量乙,可用降温结晶法分离提纯,故C正确;
D、温度升高至25℃时,甲、乙物质的溶解度相等,但是乙物质在10℃时就已经全部溶解了,所以图2试管内所得甲、乙两物质的溶液都是不饱和溶液,故D正确。
故选:B。
7.【解答】解:A、氢氧化钠溶于水放热,温度升高,M溶液变浑浊,说明M的溶解度随着温度升高而减小,硝酸铵溶于水吸热,温度降低,N溶液变浑浊,说明N的溶解度随着温度降低而减小,N的溶解度曲线为A,该选项说法正确;
B、若N的饱和溶液中有少量的M,可以用降温结晶的方法提纯N,该选项说法正确;
C、不能比较析出固体的质量,是因为不知道溶液质量,该选项说法不正确;
D、t2℃时B曲线所代表物质的溶解度是20g,42g B曲线所代表物质的饱和溶液中溶质质量:42g××100%=7g,溶剂质量是35g,加入7g该固体,溶质质量是14g,35g溶剂溶解14g固体恰好饱和,该选项说法正确。
故选:C。
8.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度也不能确定,故A错误;
B、20℃时,甲和乙的饱和溶液的质量不能确定,所以饱和溶液中所含溶质质量也不能确定,故B错误;
C、40℃时,甲物质的溶解度是50g,所以甲的饱和溶液中溶质和溶液的质量比为50g:150g=1:3,故C正确;
D、40℃时,乙物质的溶解度是40g,所以向100g水中加入50g乙,只能溶解40g的固体,所得溶液的质量为140g,故D错误。
故选:C。
9.【解答】解:A、不知道温度范围,不能确定物质的溶解度大小,该选项说法不正确;
B、不知道温度范围,不能比较物质的溶解度大小,该选项说法不正确;
C、t2℃时甲的溶解度是50g,在100g饱和溶液中含有:100g××100%=33.3g甲物质,该选项说法不正确;
D、t1℃时甲和乙的溶解度都是30g,甲和乙各30g分别加入100g水中,均形成饱和溶液,该选项说法正确。
故选:D。
10.【解答】解:A、t1℃时,甲、乙饱和溶液中溶质的质量不一定相等,是因为不知道溶液质量,该选项说法不正确;
B、t2℃时甲的溶解度大于乙,等质量的甲、乙饱和溶液中溶剂质量:甲<乙,该选项说法正确;
C、t1℃时甲的溶解度是30g,将30g甲加入50g水中,能够溶解15g,配制成65g甲的饱和溶液,该选项说法不正确;
D、甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响较小,t2℃时,乙中混有少量的甲,用蒸发结晶的方法提纯乙,该选项说法不正确。
故选:B。
11.【解答】解:A、30℃时M的溶解度是20g,向50g水中加入15gM,不能完全溶解,所得溶液为饱和溶液,该选项说法正确;
B、甲物质在20℃时的溶解度小于乙,为图3中的M,该选项说法正确;
C、由图中信息可知,a小于20,50℃时两种物质溶解度都大于20g,因此图2中得到的一定都是不饱和溶液,该选项说法正确;
D、不知道饱和溶液质量,不能比较析出固体质量大小,该选项说法不正确。
故选:D。
12.【解答】解:A、不知道温度范围,不能比较两种物质溶解度大小,该选项说法不正确;
B、t2℃时甲、乙溶解度大于40g,丙溶解度小于30g,若将20g的甲、乙、丙三种物质分别加入盛有50g水的烧杯中,充分溶解后,能形成饱和溶液的是丙,该选项说法不正确;
C、t3℃时,等质量的甲、乙、丙三种物质的饱和溶液降温到t1℃,析出固体最多的是甲,是因为该温度范围内,甲的溶解度质量差最大,该选项说法正确;
D、甲中混有少量的乙,提纯甲的方法是降温结晶,是因为甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响较小,该选项说法不正确。
故选:C。
13.【解答】解:A、t1时,等质量的a、c溶液的状态不能确定,所以溶液中溶质的质量不能确定,故A错误;
B、t2时,将a、b、c三种饱和溶液同时降温到t1,饱和溶液的质量不能确定,所以析出晶体的质量大小也不能确定,故B错误;
C、t2时,a物质的溶解度大于b物质的溶解度,所以将相同质量的固体a、b溶解配制成t2时的饱和溶液,得到的溶液质量为a<b,故C错误;
D、a物质的溶解度随温度的降低而减小,c物质的溶解度随温度的降低而增大,所以a物质中混有少量c,可采用降温结晶的方式提纯a,故D正确。
故选:D。
14.【解答】解:A、在比较物质的溶解度时,需要指明温度,温度不能确定,溶解度也不能确定,故A错误;
B、通过分析溶解度曲线可知,t1℃时,KNO3的溶解度是70g,故B错误;
C、在t1℃时,硝酸钾的溶解度大于氯化钾的溶解度,所以100gKNO3饱和溶液和100gKCl饱和溶液,KCl饱和溶液中的溶剂质量大于KNO3饱和溶液中的溶剂质量,故C正确;
D、在t2℃时,欲使KNO3、KCl两种物质的溶液分别降到t℃时,溶液的质量和状态不能确定,所以析出晶体的质量也不能确定,故D错误。
故选:C。
15.【解答】解:A、通过分析溶解度曲线可知,t1℃时,两种物质的溶解度相等,故A正确;
B、两种物质的溶解度都随温度升高而增大,故B正确;
C、硝酸钾的溶解度随温度的降低而减小,所以降低温度可将接近饱和的KNO3溶液变成饱和溶液,故C错误;
D、将t2℃的饱和NH4Cl溶液降温到t1℃,溶解度减小,析出晶体,所以溶液质量减小,故D正确。
故选:C。
二.填空题(共5小题)
16.【解答】解:(1)通过分析溶解度曲线可知,t1℃时,甲物质的溶解度等于乙物质的溶解;
(2)乙物质的溶解度曲线比较平缓,所以甲、乙两种物质的溶解度受温度影响较小的是乙物质;
(3)t2℃时,乙物质的溶解度是80g,所以把50g乙物质放入50g水中,充分搅拌,所得溶液是饱和溶液;
(4)甲物质的溶解度随温度的升高而增大,所以t2℃时,有一接近饱和的甲溶液变为饱和溶液,可采用增加溶质,蒸发溶剂,降低温度的方法。
故答案为:(1)等于;
(2)乙;
(3)饱和;
(4)增加溶质,蒸发溶剂,降低温度。
17.【解答】解:(1)通过分析溶解度曲线可知,t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c;
(2)t2℃时,a物质的溶解度是50g,所以将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为150g,形成的溶液是饱和溶液;
(3)c物质的溶解度随温度的升高而减小,所以通过升高温度可将c的不饱和溶液变为饱和溶液。
故答案为:(1)a>b>c;
(2)150;饱和;
(3)升高。
18.【解答】解:(1)通过分析溶解度曲线可知,P点的表示意义是:在t3℃时,甲、乙两物质的溶解度相等都为40g;
(2)t2℃时,甲物质的溶解度是25g,将25g甲物质放入50g水中并充分搅拌,只能溶解12.5g的固体,所得溶液的质量为62.5g;
(3)丙物质的溶解度随温度的升高而减小,所以在质量不变的情况下,将丙物质的不饱和溶液变为饱和溶液的方法是升高温度;
(4)t1℃时,甲物质的溶解度小于乙物质的溶解度,所以甲、乙饱和溶液分别蒸发掉10g水,析出固体的质量甲<乙。
故答案为:(1)在t3℃时,甲、乙两物质的溶解度相等都为40g;
(2)62.5;
(3)升高温度;
(4)<。
19.【解答】解:t1℃时,氯化镁的溶解度最大,氯化钾的溶解度最小,所以三种物质的饱和溶液中,溶质质量分数由大到小的顺序为:MgCl2>MgSO4>KCl;t2℃时的三种物质的饱和溶液分别升温至t3℃,硫酸镁的溶解度减小,氯化钾、氯化镁的溶解度增大,所以有晶体析出的是MgSO4;若要配制175g20% MgCl2溶液,需t2℃时饱和的MgCl2溶液为=85g。
故答案为:MgCl2>MgSO4>KCl;MgSO4;85。
20.【解答】解:(1)20℃时,A试管中有没有溶解的固体,一定是饱和溶液。
故填:A。
(2)20℃时甲的溶解度小于乙,图2中表示甲物质的溶解度曲线的是b,要使A试管中剩余的固体继续溶解可采用的方法是加热或加溶剂等。
故填:b;加热或加溶剂等。
(3)a的溶解度受温度变化影响较大,b的溶解度受温度变化影响较小,从a、b混合物中得到较纯净的a所采用的方法是降温结晶。
故填:降温结晶。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2021/12/3 9:58:34;用户:化学;邮箱:yingchuang2@xyh.com;学号:31596026
第1页(共3页)
第1页(共3页)
同课章节目录
