《化学反应速率》课件
图片预览






文档简介
(共20张PPT)
化学反应有快有慢:
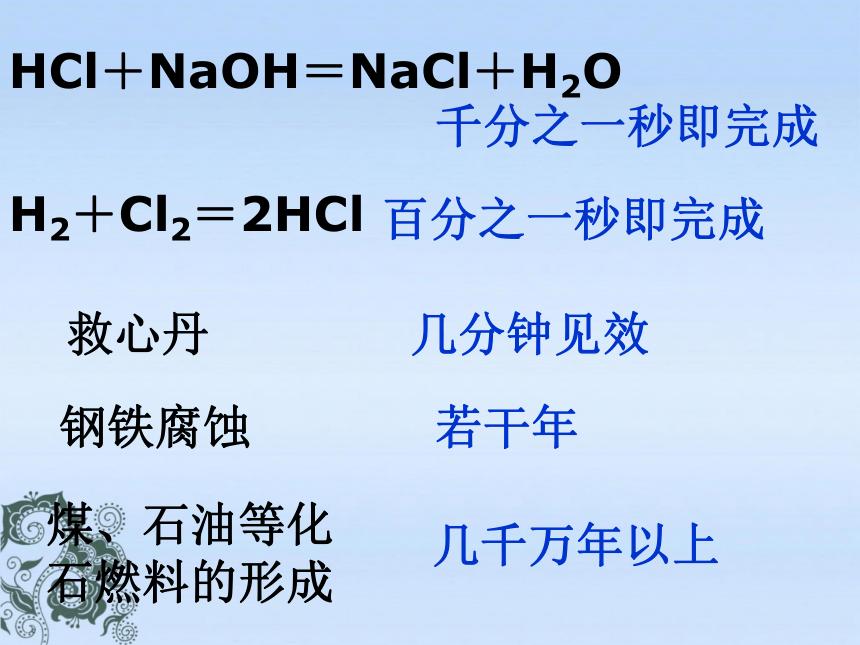
HCl+NaOH=NaCl+H2O
千分之一秒即完成
H2+Cl2=2HCl
百分之一秒即完成
救心丹
几分钟见效
钢铁腐蚀
若干年
煤、石油等化石燃料的形成
几千万年以上
第一节
化学反应速率
一个化学反应进行的快慢程度用化学反应速率来衡量。
回忆在物理学中对运动速率的定义
思考:对于反应 Zn+H2SO4=H2 +ZnSO4,可以如何定量描述其反应速率?
单位时间、某物理量的变化
1、定义:
化学反应速率用单位时间(如每秒,每分,每小时)内反应物浓度的减小或生成物浓度的增大来表示。
计算公式:
一、化学反应速率
(物质的量浓度)
常用单位:mol/(L·s) mol/(L·min)
练习巩固
在 N2 + 3H2 2 NH3反应中,自开始至2秒,氨的浓度由0变为0. 6 mol/L,则以氨气表示的化学反应速率是多少?
= 0.3mol/(L·s)
v (NH3) =
△c (NH3)
△t
=
(0. 6 – 0 )mol/L
2s
2 、计算化学反应速率的步骤:
起始浓度c(起始)
变化浓度Δ c
终了浓度c(终了)
---- 三部曲
例题:反应4NH3+5O2 4NO+6H2O 在5升的密闭容器中进行,30秒后,NO 的物质的量增加了0.3mol,此反应的平均反应速率用NO来表示为多少?
问题1:若用O2的浓度变化来表示此反应速率是多少? 若用NH3 来表示呢
问题2:此反应化学反应速率用不同物质表示为什么数值不同?数值上有何规律?
v(NO)=0.002mol/(L·s)
v(O2)=0.0025mol/(L·s)
v(NH3)=0.002mol/(L·s)
3、化学反应速率的特点—
①同一反应,可用不同物质的浓度变化来表示,数值可以不同,但必须指明是用哪种物质表示,均取正值,且是某一段时间内的平均速率。
②用不同物质的浓度变化表示时,速率比等于方程式中的系数比
③起始浓度不一定按比例,但转化浓度一定按比例。
④一般不用纯液体或固体来表示化学反应速率。
一个化学反应的速率用不同的反应物或生成物来表示,数值可能不同但含意是一致的 ,速 率之比等 于该反应方程式中对应物质的系数之比。
所以:在表示某反应速率时应注明是用哪种物质表示的。
对于反应aA+bB=cC+dD有
v(A): v(B): v(C): v(D)=a:b:c:d
比较反应速率大小时,不仅要看反应速率数值本身的大小,还要结合化学方程式中物质的化学计量数的大小来说明。
对于反应A+3B=2C+2D,下列数据表示不同条件的反应速率,其中反应进行得最快的是( )
v (A) =0.15mol/(L·S) B. v (B) =0.6mol/(L · S)
C. v (C) =1mol/(L · S) D. v (D) =2mol/(L · min)
标准一致,单位统一
例1:
例2:将等物质的量的A 、 B混合于2L密闭容器中,发生下列反应:
3 A(g)+B(g)= x C(g)+2 D(g),4min后测得C(D)=0.5mol/L,C(A):C(B)=3:5,C的平均反应速率为0.125mol/(L ·min),求:
(1)此时A的物质的量浓度
(2)B的平均反应速率
(3)x的值是多少
例4:
根据右图填空:
(1)反应物是 ;生成物是 ;
(2)在2min内A、B、C三者的反应速率值各是多少?该反应的化学方程式 .
O
2
6
8
B
A
C
4
2
c/mol·L-1
t/min
二、化学反应的速率是通过实验测定的。
测定方法有∶
1、直接观察某些性质(如释放出气体的体积和体系压强);
2、科学仪器测定(如颜色的深浅、光的吸收和发射、导电能力等);
3、溶液中,常利用颜色深浅和显色物质浓度间的正比关系来跟踪反应的过程和测量反应速率。
掌握化学反应速率的概念,数学表达式及计算步骤;
理解化学反应速率是一段时间内的平均速率,不同物质表示的同一反应的反应速率之比等于化学方程式的计量数之比。比较化学反应的快慢应以同一种物质表示的化学反应速率为标准,还应注意单位的统一。
小 结:
化学反应有快有慢:
HCl+NaOH=NaCl+H2O
千分之一秒即完成
H2+Cl2=2HCl
百分之一秒即完成
救心丹
几分钟见效
钢铁腐蚀
若干年
煤、石油等化石燃料的形成
几千万年以上
第一节
化学反应速率
一个化学反应进行的快慢程度用化学反应速率来衡量。
回忆在物理学中对运动速率的定义
思考:对于反应 Zn+H2SO4=H2 +ZnSO4,可以如何定量描述其反应速率?
单位时间、某物理量的变化
1、定义:
化学反应速率用单位时间(如每秒,每分,每小时)内反应物浓度的减小或生成物浓度的增大来表示。
计算公式:
一、化学反应速率
(物质的量浓度)
常用单位:mol/(L·s) mol/(L·min)
练习巩固
在 N2 + 3H2 2 NH3反应中,自开始至2秒,氨的浓度由0变为0. 6 mol/L,则以氨气表示的化学反应速率是多少?
= 0.3mol/(L·s)
v (NH3) =
△c (NH3)
△t
=
(0. 6 – 0 )mol/L
2s
2 、计算化学反应速率的步骤:
起始浓度c(起始)
变化浓度Δ c
终了浓度c(终了)
---- 三部曲
例题:反应4NH3+5O2 4NO+6H2O 在5升的密闭容器中进行,30秒后,NO 的物质的量增加了0.3mol,此反应的平均反应速率用NO来表示为多少?
问题1:若用O2的浓度变化来表示此反应速率是多少? 若用NH3 来表示呢
问题2:此反应化学反应速率用不同物质表示为什么数值不同?数值上有何规律?
v(NO)=0.002mol/(L·s)
v(O2)=0.0025mol/(L·s)
v(NH3)=0.002mol/(L·s)
3、化学反应速率的特点—
①同一反应,可用不同物质的浓度变化来表示,数值可以不同,但必须指明是用哪种物质表示,均取正值,且是某一段时间内的平均速率。
②用不同物质的浓度变化表示时,速率比等于方程式中的系数比
③起始浓度不一定按比例,但转化浓度一定按比例。
④一般不用纯液体或固体来表示化学反应速率。
一个化学反应的速率用不同的反应物或生成物来表示,数值可能不同但含意是一致的 ,速 率之比等 于该反应方程式中对应物质的系数之比。
所以:在表示某反应速率时应注明是用哪种物质表示的。
对于反应aA+bB=cC+dD有
v(A): v(B): v(C): v(D)=a:b:c:d
比较反应速率大小时,不仅要看反应速率数值本身的大小,还要结合化学方程式中物质的化学计量数的大小来说明。
对于反应A+3B=2C+2D,下列数据表示不同条件的反应速率,其中反应进行得最快的是( )
v (A) =0.15mol/(L·S) B. v (B) =0.6mol/(L · S)
C. v (C) =1mol/(L · S) D. v (D) =2mol/(L · min)
标准一致,单位统一
例1:
例2:将等物质的量的A 、 B混合于2L密闭容器中,发生下列反应:
3 A(g)+B(g)= x C(g)+2 D(g),4min后测得C(D)=0.5mol/L,C(A):C(B)=3:5,C的平均反应速率为0.125mol/(L ·min),求:
(1)此时A的物质的量浓度
(2)B的平均反应速率
(3)x的值是多少
例4:
根据右图填空:
(1)反应物是 ;生成物是 ;
(2)在2min内A、B、C三者的反应速率值各是多少?该反应的化学方程式 .
O
2
6
8
B
A
C
4
2
c/mol·L-1
t/min
二、化学反应的速率是通过实验测定的。
测定方法有∶
1、直接观察某些性质(如释放出气体的体积和体系压强);
2、科学仪器测定(如颜色的深浅、光的吸收和发射、导电能力等);
3、溶液中,常利用颜色深浅和显色物质浓度间的正比关系来跟踪反应的过程和测量反应速率。
掌握化学反应速率的概念,数学表达式及计算步骤;
理解化学反应速率是一段时间内的平均速率,不同物质表示的同一反应的反应速率之比等于化学方程式的计量数之比。比较化学反应的快慢应以同一种物质表示的化学反应速率为标准,还应注意单位的统一。
小 结:
