人教版九年级化学下册 8.3金属资源的利用和保护 达标训练 (WORD版含答案)
文档属性
| 名称 | 人教版九年级化学下册 8.3金属资源的利用和保护 达标训练 (WORD版含答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 206.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-06 00:00:00 | ||
图片预览


文档简介
金属资源的利用和保护 达标训练
一、选择题(每题只有一个正确选项)
1.钛合金是21世纪的重要材料,工业上制取钛的一个反应是:TiCl4+2MgTi+2MgC12,该反应类型属于( )
A. 化合反应 B.分解反应
C.置换反应 D.以上都不对
2.下列物质间比较的说法中不正确的是( )
A. 熔点:武德合金小于铅(铅为武德合金成分之一)
B. 硬度:黄铜大于铜
C. 铁元素的质量分数:Fe2O3>FeO
D. 铜和铁生锈的难易:铜比铁难
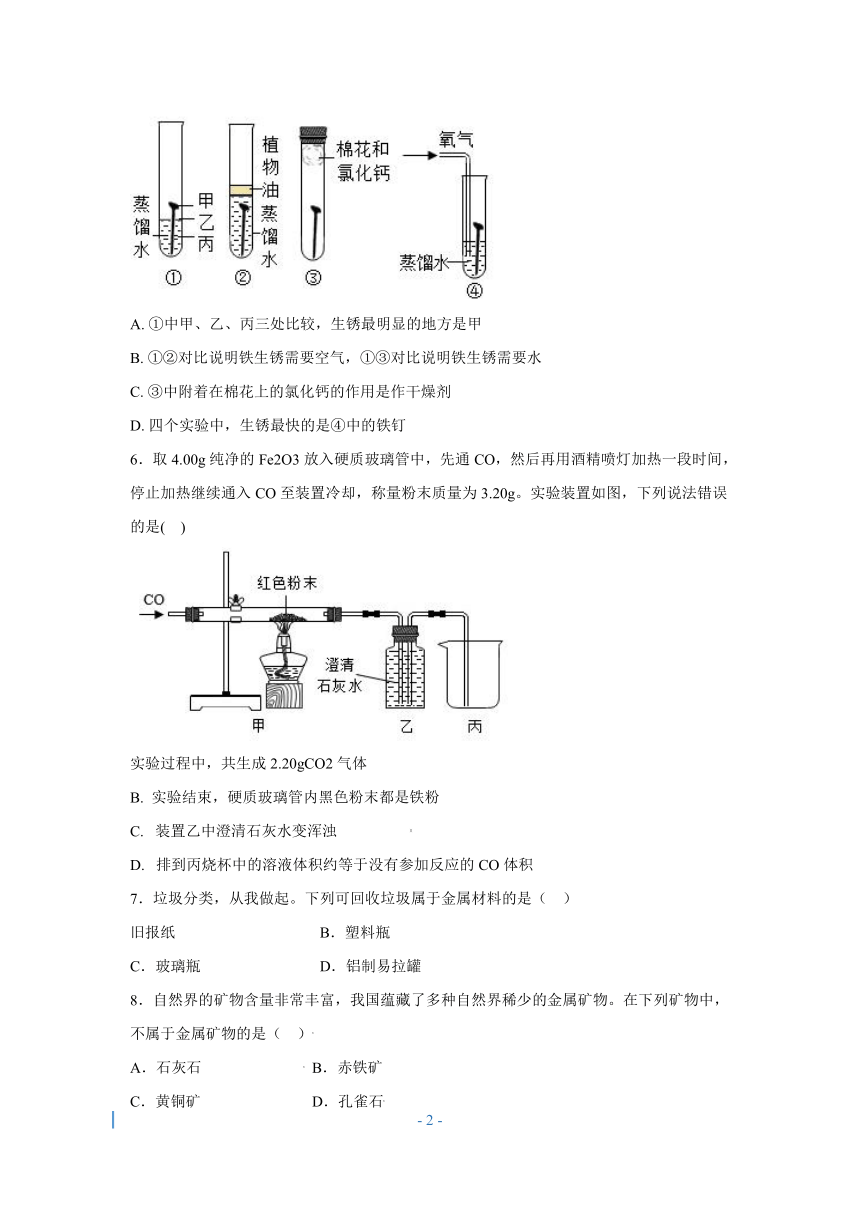
3.实验室用图装置模拟炼铁。下列说法正确的是( )
磁铁矿的主要成分是Fe2O3
B. 应先加热Fe2O3再通入CO
C. 红棕色的逐渐变黑
D. 气体通过澄清石灰水后可直接排放
4.下列措施中,不能防止金属制品锈蚀的是( )
在表面刷漆 B. 改用不锈钢
C . 在表面镀铬 D. 用湿布擦拭
5.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法错误的是( )
A. ①中甲、乙、丙三处比较,生锈最明显的地方是甲
B. ①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C. ③中附着在棉花上的氯化钙的作用是作干燥剂
D. 四个实验中,生锈最快的是④中的铁钉
6.取4.00g纯净的Fe2O3放入硬质玻璃管中,先通CO,然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却,称量粉末质量为3.20g。实验装置如图,下列说法错误的是( )
实验过程中,共生成2.20gCO2气体
B. 实验结束,硬质玻璃管内黑色粉末都是铁粉
C. 装置乙中澄清石灰水变浑浊
D. 排到丙烧杯中的溶液体积约等于没有参加反应的CO体积
7.垃圾分类,从我做起。下列可回收垃圾属于金属材料的是( )
旧报纸 B.塑料瓶
C.玻璃瓶 D.铝制易拉罐
8.自然界的矿物含量非常丰富,我国蕴藏了多种自然界稀少的金属矿物。在下列矿物中,不属于金属矿物的是( )
A.石灰石 B.赤铁矿
C.黄铜矿 D.孔雀石
9.人类利用金属的历史经历了从青铜器时代到铁器时代,再到铝合金大量使用的过程。这一事实与下列因素有关的是( )
地壳中金属元素的含量
B.金属的延展性
C.金属的导电性
D.金属冶炼的水平
10.从化学的角度对下列成语进行解释,其中不正确的是( )
A. “百炼成钢”﹣﹣降低生铁中的含碳量
B. “点石成金”﹣﹣化学反应改变了元素种类
C. “钻木取火”﹣﹣温度达到可燃物的着火点
D. “沙里淘金”﹣﹣金在自然界中以单质形式存在
11.铁是我们生活中常见的金属,有关铁的知识的认识符合实际的是( )
A.生铁和钢是混合物
B.用CO还原铁矿石的反应是置换反应
C.铁是地壳中含量最多的金属元素
D.铁丝在干燥的空气中易生锈
12.小明笔记中有一处错误,你认为是图中的哪一处( )
A. a处 B. b处
C. c处 D. d处
二、非选择题
13.钢铁在生产、生活中有广泛的用途。
(1)钢铁属于________(填“纯净物”或“混合物”);
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式________。
(3)市场上有一种含铁粉的麦片,食用后在胃酸(主要成分为盐酸)作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为________。这种麦片必须真空保存,原因是________。
14.如图是工业炼铁的流程图,根据图示回答下列问题:
(1)工业炼铁过程中,常常需要将焦炭粉碎,其目的是________, 焦炭在炼铁中的作用有________、________。
(2)上述过程中有些反应吸热,请写出一个吸热反应的化学方程式________。
(3)炼铁过程中还有一种关键原料________(填名称 ),其作用是________。
15.铜片在潮湿的空气中久置,表面会产生绿色的铜锈。某小组同学设计并进行实验,探究铜生锈的条件。
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与铜片接触的物质,利用右图装置(铜片长
8cm,宽1cm,试管容积为20mL),分别进行下列7个实验,并持续观察30天。
编号 主要实验操作 实验现象
① 充满纯净的O2 铜片均无明显变化
② 充满纯净的CO2
③ 充满经煮沸并迅速冷却的蒸馏水
④ 加入蒸馏水5mL(液面未浸没铜片),再充满O2
⑤ 加入经煮沸并迅速冷却的蒸馏水5 mL,再充满CO2
⑥ 充入10mL O2 ,再充入10mLCO2
⑦ 加入蒸馏水5ml,再依次充入10mL CO2和10mL O2 铜片生锈,且水面附近锈蚀最严重
【解释与结论】
(1)实验3中,要使用经煮沸并迅速冷却的蒸馏水,原因是________。
(2)实验5的目的是________。
(3)通过上述实验,得出铜生锈的条件是________。
(4)【反思与评价】
请写出一种防止铜制品锈蚀的方法________。
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。由此,你认为上述实验中只需进行实验(填实验编号),就可探究出铜生锈条件,理由是________。
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因可能是________。
参考答案
1-12 CCCDA BDADB AB
- 7 -
一、选择题(每题只有一个正确选项)
1.钛合金是21世纪的重要材料,工业上制取钛的一个反应是:TiCl4+2MgTi+2MgC12,该反应类型属于( )
A. 化合反应 B.分解反应
C.置换反应 D.以上都不对
2.下列物质间比较的说法中不正确的是( )
A. 熔点:武德合金小于铅(铅为武德合金成分之一)
B. 硬度:黄铜大于铜
C. 铁元素的质量分数:Fe2O3>FeO
D. 铜和铁生锈的难易:铜比铁难
3.实验室用图装置模拟炼铁。下列说法正确的是( )
磁铁矿的主要成分是Fe2O3
B. 应先加热Fe2O3再通入CO
C. 红棕色的逐渐变黑
D. 气体通过澄清石灰水后可直接排放
4.下列措施中,不能防止金属制品锈蚀的是( )
在表面刷漆 B. 改用不锈钢
C . 在表面镀铬 D. 用湿布擦拭
5.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法错误的是( )
A. ①中甲、乙、丙三处比较,生锈最明显的地方是甲
B. ①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C. ③中附着在棉花上的氯化钙的作用是作干燥剂
D. 四个实验中,生锈最快的是④中的铁钉
6.取4.00g纯净的Fe2O3放入硬质玻璃管中,先通CO,然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却,称量粉末质量为3.20g。实验装置如图,下列说法错误的是( )
实验过程中,共生成2.20gCO2气体
B. 实验结束,硬质玻璃管内黑色粉末都是铁粉
C. 装置乙中澄清石灰水变浑浊
D. 排到丙烧杯中的溶液体积约等于没有参加反应的CO体积
7.垃圾分类,从我做起。下列可回收垃圾属于金属材料的是( )
旧报纸 B.塑料瓶
C.玻璃瓶 D.铝制易拉罐
8.自然界的矿物含量非常丰富,我国蕴藏了多种自然界稀少的金属矿物。在下列矿物中,不属于金属矿物的是( )
A.石灰石 B.赤铁矿
C.黄铜矿 D.孔雀石
9.人类利用金属的历史经历了从青铜器时代到铁器时代,再到铝合金大量使用的过程。这一事实与下列因素有关的是( )
地壳中金属元素的含量
B.金属的延展性
C.金属的导电性
D.金属冶炼的水平
10.从化学的角度对下列成语进行解释,其中不正确的是( )
A. “百炼成钢”﹣﹣降低生铁中的含碳量
B. “点石成金”﹣﹣化学反应改变了元素种类
C. “钻木取火”﹣﹣温度达到可燃物的着火点
D. “沙里淘金”﹣﹣金在自然界中以单质形式存在
11.铁是我们生活中常见的金属,有关铁的知识的认识符合实际的是( )
A.生铁和钢是混合物
B.用CO还原铁矿石的反应是置换反应
C.铁是地壳中含量最多的金属元素
D.铁丝在干燥的空气中易生锈
12.小明笔记中有一处错误,你认为是图中的哪一处( )
A. a处 B. b处
C. c处 D. d处
二、非选择题
13.钢铁在生产、生活中有广泛的用途。
(1)钢铁属于________(填“纯净物”或“混合物”);
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式________。
(3)市场上有一种含铁粉的麦片,食用后在胃酸(主要成分为盐酸)作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为________。这种麦片必须真空保存,原因是________。
14.如图是工业炼铁的流程图,根据图示回答下列问题:
(1)工业炼铁过程中,常常需要将焦炭粉碎,其目的是________, 焦炭在炼铁中的作用有________、________。
(2)上述过程中有些反应吸热,请写出一个吸热反应的化学方程式________。
(3)炼铁过程中还有一种关键原料________(填名称 ),其作用是________。
15.铜片在潮湿的空气中久置,表面会产生绿色的铜锈。某小组同学设计并进行实验,探究铜生锈的条件。
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与铜片接触的物质,利用右图装置(铜片长
8cm,宽1cm,试管容积为20mL),分别进行下列7个实验,并持续观察30天。
编号 主要实验操作 实验现象
① 充满纯净的O2 铜片均无明显变化
② 充满纯净的CO2
③ 充满经煮沸并迅速冷却的蒸馏水
④ 加入蒸馏水5mL(液面未浸没铜片),再充满O2
⑤ 加入经煮沸并迅速冷却的蒸馏水5 mL,再充满CO2
⑥ 充入10mL O2 ,再充入10mLCO2
⑦ 加入蒸馏水5ml,再依次充入10mL CO2和10mL O2 铜片生锈,且水面附近锈蚀最严重
【解释与结论】
(1)实验3中,要使用经煮沸并迅速冷却的蒸馏水,原因是________。
(2)实验5的目的是________。
(3)通过上述实验,得出铜生锈的条件是________。
(4)【反思与评价】
请写出一种防止铜制品锈蚀的方法________。
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。由此,你认为上述实验中只需进行实验(填实验编号),就可探究出铜生锈条件,理由是________。
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因可能是________。
参考答案
1-12 CCCDA BDADB AB
- 7 -
同课章节目录
