高中化学人教版必修一2.1物质的分类 课件(58张ppt)
文档属性
| 名称 | 高中化学人教版必修一2.1物质的分类 课件(58张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-07 00:00:00 | ||
图片预览







文档简介
(共58张PPT)
物质的分类
简单分类法及其应用
为什么在图书馆里你很快就能找到需要的书?
因为图书进行了分类
简单分类法及其应用
简单分类法及其应用
简单分类法及其应用
在超市,我们能很快找到所需药品,为什么?
没有分类,超市会什么样?
因为商品进行了分类
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
《开心辞典》
考考你的记忆力
看看你能说出多少内容???
创原家独
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
知识点1、分类及分类的意义
2、意义:能提高人们工作、学习效率,使人们更快更便捷的达到目的。
1、分类把某些特征相似的事物,按照一定标准归类到一起;
新知讲解
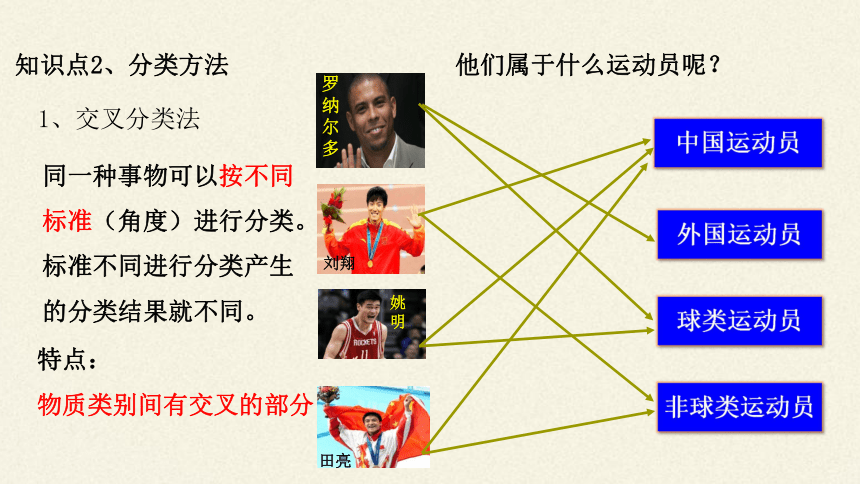
知识点2、分类方法
姚明
刘翔
田亮
罗纳尔多
中国运动员
外国运动员
球类运动员
非球类运动员
1、交叉分类法
同一种事物可以按不同标准(角度)进行分类。标准不同进行分类产生的分类结果就不同。
特点:
物质类别间有交叉的部分
他们属于什么运动员呢?
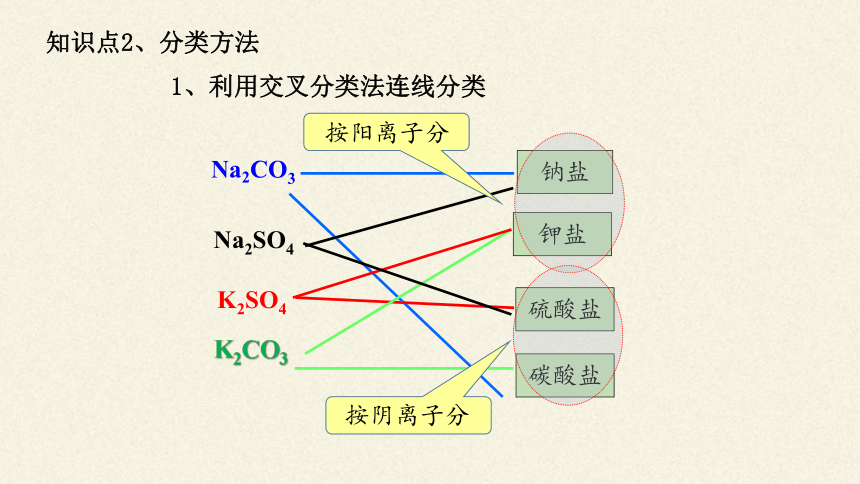
知识点2、分类方法
1、利用交叉分类法连线分类
Na2SO4
Na2CO3
K2CO3
K2SO4
钠盐
钾盐
硫酸盐
碳酸盐
按阳离子分
按阴离子分
知识点2、分类方法
2、找出一种不同于其它种的物质
A. Na2CO3 Na2SO4 NaCl K2CO3
B. Na2CO3 K2CO3 Na2SO4 CaCO3
C. Na2CO3 K2CO3 KCl K2SO4
D. Na2CO3 Na2SO4 K2SO4 MgSO4
初中学过有关物质类别的概念
知识点2、分类方法
复习回顾
物质
混合物、纯净物、单质、化合物、金属单质、非金属单质、酸、碱、盐、氧化物、酸性氧化物、碱性氧化物等。
是否由同一种分子组成
纯净物
混合物
是否由同种元素组成
单质
化合物
金属单质
非金属单质
根据组成特点和所具有的性质
酸
碱
盐
氧化物
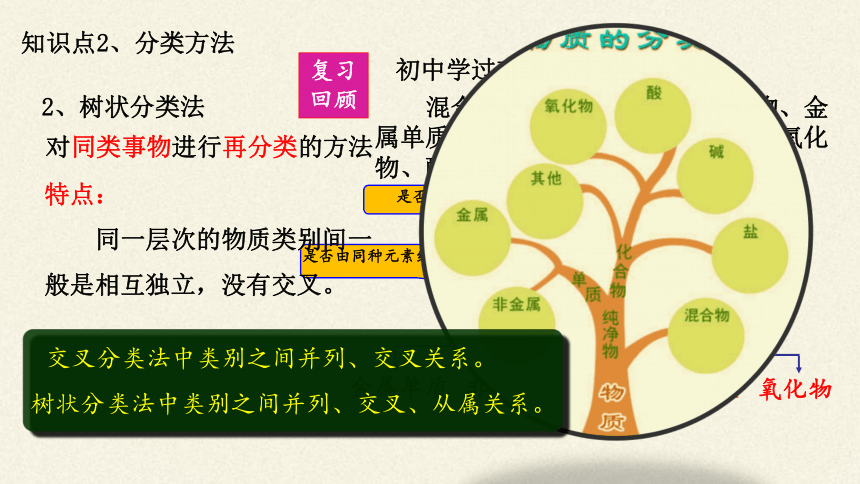
2、树状分类法
对同类事物进行再分类的方法
特点:
同一层次的物质类别间一般是相互独立,没有交叉。
交叉分类法中类别之间并列、交叉关系。
树状分类法中类别之间并列、交叉、从属关系。
知识点2、分类方法
2、树状分类法
利用树状分类法对常见化学反应分类
化学反应
按反应前后种类、类别
按得氧、失氧
化合反应 A+B=AB
分解反应 AB=A+B
置换反应 A+BC=AC+B
复分解反应 AB+CD=AD+CB
氧化反应
还原反应
物质
纯净物
混合物
单质
化合物
金属单质
非金属单质
氧化物
盐
碱
酸
无机化合物
有机化合物
根据物质组成是否单一
根据组成元素的异同
根据性质的差异
根据组成的差异
……
同素异形体: 同一种元素形成的几种性质不同的单质叫做同素异形体
(1)形成方式:
a.原子个数不同,如O2, O3
b.原子排列方式不同,如金刚石,石墨
(2)性质差异
同素异形体的物理性质差别较大。同素异形体之间的转化属于化学变化。
知识点3、分类法的应用
1、确定转化关系
酸
盐
金属
金属
盐
非金属
碱性氧化物
碱
酸
盐
碱
盐
酸性氧化物
碱
碱性氧化物
正确理解几个 “一定”“不一定”
1、碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物。
2、酸性氧化物不一定是非金属氧化物,如:Mn2O7;非金属氧化物不一定是酸性氧化物,如CO, NO。
3、酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱,如:Fe2O3。
2、分散系及其分类
(1)分散系:
分散质:
分散剂:
把一种(或多种)物质分散在另一种(或多种)物质中
所得到的体系。
被分散的物质
能分散分散质的物质
分
散
系
分散质
分散剂
气
液
固
气
液
固
按聚集状态 (气、液、固) 来分,有9种类型。
(2)分散系的分类
知识点3、分类法的应用
分散质 分散剂 实例
气 气
液 气
固 气
气 液
液 液
固 液
气 固
液 固
固 固
空气
云、雾
烟、灰尘
汽水
牛奶、酒精的水溶液
糖水、油漆、泥水
泡沫塑料
珍珠(包藏着水的碳酸钙)
有色玻璃、合金
常见的一些分散系
分散质
分散剂
气
液
固
气
液
固
分散系
胶 体
浊 液
溶 液
悬浊液
乳浊液
当分散剂是水或其他液体时,按照分散质粒子的大小来分:
树状分类法
溶液、胶体、浊液的区分
溶液、胶体、浊液的区分
三者本质特征比较:
胶体
浊液
溶液
100nm
1nm
分散质粒子直径
可以通过滤纸
胶体是以粒子直径的大小为本质特征的
溶液、胶体、浊液的区分
(1). 概念: 分散质粒子直径 1nm<d<100nm 之间的分散系
认识几种常见胶体
晨雾
、烟
、白云
烟水晶
有色玻璃
胶体
液溶胶
烟水晶
有色玻璃
固溶胶
雾
白云
气溶胶
常见的胶体
溶液、胶体、浊液的稳定性
1.取3个小烧杯,分别加入25ml蒸馏水,25mlCuSO4溶液和25ml泥水。将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5--6滴FeCl3饱和溶液。继续煮沸至溶液呈红褐色,停止加热。观察制得的Fe(OH)3胶体,并与CuSO4溶液和泥水比较。
Fe(OH)3胶体 红褐色,澄清透明
CuSO4溶液 蓝色,澄清透明
泥水 浑浊,不透明
科学探究1
2.分别用激光笔照射Fe(OH)3胶体和CuSO4溶液,在与光束垂直的方向进行观察,并记录实验现象。
CuSO4 溶液
Fe(OH)3 胶体
科学探究2
谢 谢
(2)氢氧化铁胶体的制取
反应原理:
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
△
=
重要步骤:
沸水中滴入FeCl3饱和溶液
(3)胶体的性质
丁达尔效应:
CuSO4溶液
Fe(OH)3胶体
当可见光束通过胶体时,在入射光侧面可观察到明亮的“通路”。
科学探究3
光束照射时的现象
Fe(OH)3胶体 形成一条光亮的通路
CuSO4溶液 没有光亮的通路现象产生
科学探究4
利用丁达尔效应来区分胶体和溶液是一种常用的物理方法。
当一束光线照射胶体时,从侧面观察,可看见在胶体里形成一条光亮的通路的现象。它是物质的聚集状态所表现出来的一种性质。
丁达尔效应
胶体产生丁达尔效应的原因
生活中的丁达尔效应
【练一练】下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于10-9m
D.丁达尔效应可用于区别胶体和溶液
×
×
分散质粒子直径
1nm=10-9m
×
D
课堂练习
1、分类是一种科学的学习方法,科学分类的前提是有准确的分类标准。
2、用交叉分类法、树状分类法,按物质组成对物质进行分类。
3、分散系的概念与分类
4、胶体的概念与分类
5、氢氧化铁胶体的制备
6、丁达尔效应
课堂总结
导入
上节课我们学习了物质的分类
物质
混合物
纯净物
单质
化合物
非金属单质
金属单质
无机化合物
有机化合物
氧化物
酸
碱
盐
…
导入
根据物质的分类,可以认识物质的性质、转化关系,从而制备新物质。
物质的分类
物质的性质
物质之间的转化关系
认识
认识
人类生活和生产所需要的新物质
制备
制备
同类物质往往具有相似的性质。
盐酸、硫酸
氢氧化钠、氢氧化钙
碳酸钠、碳酸钾
酸
碱
盐
新课讲解
新课讲解
酸的主要化学性质
①酸可以与活泼金属反应
②酸可以与碱性氧化物反应
③酸可以与碱反应
④酸可以与某些盐反应
注:“酸”是在水溶液中电离时产生的阳离子都是氢离子的化合物。
根据酸的主要化学性质,可以有哪些反应实例呢?
思考·讨论
酸的主要化学性质 反应实例
酸与活泼金属反应 Zn + H2SO4 == ZnSO4 + H2↑
酸与碱性氧化物反应 6HCl + Fe2O3 == 2FeCl3 + 3H2O
酸与碱反应 NaOH + HCl == NaCl + H2O
酸与某些盐反应 HCl + AgNO3 == AgCl↓ + HNO3
新课讲解
碱的主要化学性质
①碱可以与非金属氧化物反应
②碱可以与酸反应
③碱可以与某些盐反应
④碱可以使酚酞试剂变红,使紫色石蕊试剂变蓝反应
注:“碱”是在水溶液中电离时产生的阴离子都是氢氧根离子的化合物。
根据碱的主要化学性质,可以有哪些反应实例呢?
思考·讨论
碱的主要化学性质 反应实例
碱与非金属氧化物反应 2NaOH + CO2 == Na2CO3 + H2O
碱与酸反应 NaOH + HCl == NaCl + H2O
碱与某些盐反应 Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH
新课讲解
盐的主要化学性质
①盐可以与金属反应
②盐可以与酸反应
③盐可以与碱反应
④盐可以与某些盐反应
注:“盐”是在水溶液中电离时生成金属阳离子(或其他阳离子)和酸根阴离子的化合物。
根据盐的主要化学性质,可以有哪些反应实例呢?
思考·讨论
盐的主要化学性质 反应实例
盐与金属反应 Fe + CuSO4 == FeSO4 + Cu↓
盐与酸反应 BaCl2 + H2SO4 == BaSO4↓ + 2HCl
盐与碱反应 FeCl3 + 3NaOH == 3NaCl + Fe(OH)3↓
盐与某些盐反应 BaCl2 + Na2SO4 == BaSO4↓ + 2NaCl
①为什么不同的酸(或碱)具有相似的化学性质?
思考·讨论
因为它们在组成上具有相似性。
“H+”酸
“酸根离子”盐
“OH-”
碱
②酸、碱、盐的主要化学性质中,涉及哪些反应类型?
思考·讨论
从反应类型来看,初中学过的酸与金属、盐与金属的反应都属于置换反应,酸与碱、盐与酸、盐与碱、盐与盐之间的反应都属于复分解反应。
试着写出下列物质之间转化的化学方程式,体会由金属单质到盐、非金属到盐的转化关系。
Ca → CaO → Ca(OH)2 → CaSO4
思考·讨论
C → CO2 → H2CO3 → CaCO3
对于上述转化关系,从物质分类的角度看,你发现了什么规律?
思考·讨论
金属单质
碱性氧化物
碱
盐
O2
H2O
酸或酸性氧化物
非金属单质
酸性氧化物
酸
盐
O2
H2O
碱或碱性氧化物
思维启迪
制取某类物质的方法
根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制取某类物质的方法。
例如,要想制取某种碱,通常可以采取两种方法:碱性氧化物与水发生反应;盐与另一种碱发生反应。
工业生产中制取NaOH ,是怎么做的呢?
思考·讨论
工业上制取NaOH一般不采用Na2O与H2O反应,而主要采用电解饱和食盐水的方法。
因为Na2O作为原料、来源少、成本高,因此不适用用批量生产NaOH。
2NaCl + 2H2O ==== 2NaOH + H2↑ + Cl2↑
通电
根据物质的组成和性质,通过化学变化可以实现物质之间的转化。在化学变化过程中,元素是不会改变的,这是考虑如何实现物质之间的转化时最基本的依据。
在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。
新课讲解
物质的转化
思维启迪
化学科研工作者与化学工程师
化学科研工作者研究的是基本原理,例如怎么合成某种物质,某种物质的结构是什么样的,某种物质具有什么电子、光学、力学、磁学性质。
化学工程师研究的是怎么实现这些基本原理,例如怎么设计化工厂的反应器,选择反应的温度、压强、催化剂。
从基础知识来看,量子力学对化学科研工作者的重要性远远超过对化学工程师,流体力学对化学工程师的重要性远远超过对化学科研工作者。
1.下列物质分类正确的是( )
课堂达标
D
碱 酸 盐 碱性氧化物 酸性氧化物
A Na2CO3 H2SO4 NaOH SO2 CO2
B NaOH HCl NaCl Na2O CO
C NaOH CH3COOH CaF2 CO SO2
D KOH HNO3 CaCO3 CaO SO2
解析 “酸”是在水溶液中电离时产生的阳离子都是氢离子的化合物;“碱”是在水溶液中电离时产生的阴离子都是氢氧根离子的化合物;“盐”是在水溶液中电离时生成金属阳离子(或其他阳离子)和酸根阴离子的化合物;碱性氧化物是指与酸反应而成盐和水的氧化物;酸性氧化物是指与碱作用生成盐和水的氧化物。Na2CO3不是碱,NaOH不是盐,SO2不是碱性氧化物,选项A错误;CO不是酸性氧化物,选项B错误;CO不是碱性氧化物,选项C错误。因此选D。
2.下列各组物质,按照单质、化合物、混合物的顺序排列正确的是( )
A. 稀有气体、酒、冰水混合物
B. 乙醇、浓硫酸、胆矾
C.金刚石、铁矿石、大理石
D.水银、水蒸气、水煤气
课堂达标
D
解析:酒是混合物,冰水混合物是纯净物,选项A错误;乙醇是化合物,浓硫酸是混合物,胆矾是纯净物,选项B错误;铁矿石是混合物,选项C错误;水银是单质,水蒸气是化合物,水煤气是混合物,选项D正确。因此选D。
3.下列反应方程正确的是( )
A.BaCl2 + H2SO4 == BaSO4 + 2HCl
B.NaOH + CO2 == Na2CO3 + H2O
C.HCl + AgNO3 == AgCl↓ + HNO3
D.4HCl + Fe2O3 == 2FeCl2 + 2H2O
课堂达标
解析:选项A是盐和酸的反应,正确的反应式是BaCl2 + H2SO4 == BaSO4↓ + 2HCl ,选项A错误;选项B是碱和酸性氧化物的反应,正确的反应式是2NaOH + CO2 == Na2CO3 + H2O,选项B错误;选项D是酸和金属氧化物的反应,正确的反应式是6HCl + Fe2O3 == 2FeCl3 + 3H2O,选项D错误。因此选C。
C
4.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可做干燥剂的理由是什么?(用化学方程式表示)
课堂达标
4. 同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)CaO是碱性氧化物
(2)生石灰能够强烈吸收水分,是碱性干燥剂的主要成分,吸水后氧化钙与水生成氢氧化钙:
课堂达标
CaO+H2O===Ca(OH)2(放出大量热)
解析:CaO是碱性氧化物,能与水、酸、酸性氧化物、盐反应,具有碱性氧化物的通性。生石灰能够强烈吸收水分,是碱性干燥剂的主要成分,吸水后氧化钙与水生成氢氧化钙。
物质的分类及转化
课堂小结
同类物质往往具有相似的性质
酸的化学性质:
①酸可以与活泼金属反应;②酸可以与碱性氧化物反应;③酸可以与碱反应;④酸可以与某些盐反应
碱的化学性质:
①碱可以与非金属氧化物反应;②碱可以与酸反应;③碱可以与某些盐反应;④碱可以使酚酞试剂变红,使紫色石蕊试剂变蓝反应
盐的化学性质:
①盐可以与金属反应;②盐可以与酸反应;③盐可以与碱反应;④盐可以与某些盐反应
物质的转化:
根据物质的组成和性质,通过化学变化可以实现物质之间的转化。在化学变化过程中,元素是不会改变的,这是考虑如何实现物质之间的转化时最基本的依据。
作业布置
P12:6、7、8
熟记酸、碱、盐的化学性质
物质的分类
简单分类法及其应用
为什么在图书馆里你很快就能找到需要的书?
因为图书进行了分类
简单分类法及其应用
简单分类法及其应用
简单分类法及其应用
在超市,我们能很快找到所需药品,为什么?
没有分类,超市会什么样?
因为商品进行了分类
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
《开心辞典》
考考你的记忆力
看看你能说出多少内容???
创原家独
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
知识点1、分类及分类的意义
2、意义:能提高人们工作、学习效率,使人们更快更便捷的达到目的。
1、分类把某些特征相似的事物,按照一定标准归类到一起;
新知讲解
知识点2、分类方法
姚明
刘翔
田亮
罗纳尔多
中国运动员
外国运动员
球类运动员
非球类运动员
1、交叉分类法
同一种事物可以按不同标准(角度)进行分类。标准不同进行分类产生的分类结果就不同。
特点:
物质类别间有交叉的部分
他们属于什么运动员呢?
知识点2、分类方法
1、利用交叉分类法连线分类
Na2SO4
Na2CO3
K2CO3
K2SO4
钠盐
钾盐
硫酸盐
碳酸盐
按阳离子分
按阴离子分
知识点2、分类方法
2、找出一种不同于其它种的物质
A. Na2CO3 Na2SO4 NaCl K2CO3
B. Na2CO3 K2CO3 Na2SO4 CaCO3
C. Na2CO3 K2CO3 KCl K2SO4
D. Na2CO3 Na2SO4 K2SO4 MgSO4
初中学过有关物质类别的概念
知识点2、分类方法
复习回顾
物质
混合物、纯净物、单质、化合物、金属单质、非金属单质、酸、碱、盐、氧化物、酸性氧化物、碱性氧化物等。
是否由同一种分子组成
纯净物
混合物
是否由同种元素组成
单质
化合物
金属单质
非金属单质
根据组成特点和所具有的性质
酸
碱
盐
氧化物
2、树状分类法
对同类事物进行再分类的方法
特点:
同一层次的物质类别间一般是相互独立,没有交叉。
交叉分类法中类别之间并列、交叉关系。
树状分类法中类别之间并列、交叉、从属关系。
知识点2、分类方法
2、树状分类法
利用树状分类法对常见化学反应分类
化学反应
按反应前后种类、类别
按得氧、失氧
化合反应 A+B=AB
分解反应 AB=A+B
置换反应 A+BC=AC+B
复分解反应 AB+CD=AD+CB
氧化反应
还原反应
物质
纯净物
混合物
单质
化合物
金属单质
非金属单质
氧化物
盐
碱
酸
无机化合物
有机化合物
根据物质组成是否单一
根据组成元素的异同
根据性质的差异
根据组成的差异
……
同素异形体: 同一种元素形成的几种性质不同的单质叫做同素异形体
(1)形成方式:
a.原子个数不同,如O2, O3
b.原子排列方式不同,如金刚石,石墨
(2)性质差异
同素异形体的物理性质差别较大。同素异形体之间的转化属于化学变化。
知识点3、分类法的应用
1、确定转化关系
酸
盐
金属
金属
盐
非金属
碱性氧化物
碱
酸
盐
碱
盐
酸性氧化物
碱
碱性氧化物
正确理解几个 “一定”“不一定”
1、碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物。
2、酸性氧化物不一定是非金属氧化物,如:Mn2O7;非金属氧化物不一定是酸性氧化物,如CO, NO。
3、酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱,如:Fe2O3。
2、分散系及其分类
(1)分散系:
分散质:
分散剂:
把一种(或多种)物质分散在另一种(或多种)物质中
所得到的体系。
被分散的物质
能分散分散质的物质
分
散
系
分散质
分散剂
气
液
固
气
液
固
按聚集状态 (气、液、固) 来分,有9种类型。
(2)分散系的分类
知识点3、分类法的应用
分散质 分散剂 实例
气 气
液 气
固 气
气 液
液 液
固 液
气 固
液 固
固 固
空气
云、雾
烟、灰尘
汽水
牛奶、酒精的水溶液
糖水、油漆、泥水
泡沫塑料
珍珠(包藏着水的碳酸钙)
有色玻璃、合金
常见的一些分散系
分散质
分散剂
气
液
固
气
液
固
分散系
胶 体
浊 液
溶 液
悬浊液
乳浊液
当分散剂是水或其他液体时,按照分散质粒子的大小来分:
树状分类法
溶液、胶体、浊液的区分
溶液、胶体、浊液的区分
三者本质特征比较:
胶体
浊液
溶液
100nm
1nm
分散质粒子直径
可以通过滤纸
胶体是以粒子直径的大小为本质特征的
溶液、胶体、浊液的区分
(1). 概念: 分散质粒子直径 1nm<d<100nm 之间的分散系
认识几种常见胶体
晨雾
、烟
、白云
烟水晶
有色玻璃
胶体
液溶胶
烟水晶
有色玻璃
固溶胶
雾
白云
气溶胶
常见的胶体
溶液、胶体、浊液的稳定性
1.取3个小烧杯,分别加入25ml蒸馏水,25mlCuSO4溶液和25ml泥水。将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5--6滴FeCl3饱和溶液。继续煮沸至溶液呈红褐色,停止加热。观察制得的Fe(OH)3胶体,并与CuSO4溶液和泥水比较。
Fe(OH)3胶体 红褐色,澄清透明
CuSO4溶液 蓝色,澄清透明
泥水 浑浊,不透明
科学探究1
2.分别用激光笔照射Fe(OH)3胶体和CuSO4溶液,在与光束垂直的方向进行观察,并记录实验现象。
CuSO4 溶液
Fe(OH)3 胶体
科学探究2
谢 谢
(2)氢氧化铁胶体的制取
反应原理:
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
△
=
重要步骤:
沸水中滴入FeCl3饱和溶液
(3)胶体的性质
丁达尔效应:
CuSO4溶液
Fe(OH)3胶体
当可见光束通过胶体时,在入射光侧面可观察到明亮的“通路”。
科学探究3
光束照射时的现象
Fe(OH)3胶体 形成一条光亮的通路
CuSO4溶液 没有光亮的通路现象产生
科学探究4
利用丁达尔效应来区分胶体和溶液是一种常用的物理方法。
当一束光线照射胶体时,从侧面观察,可看见在胶体里形成一条光亮的通路的现象。它是物质的聚集状态所表现出来的一种性质。
丁达尔效应
胶体产生丁达尔效应的原因
生活中的丁达尔效应
【练一练】下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于10-9m
D.丁达尔效应可用于区别胶体和溶液
×
×
分散质粒子直径
1nm=10-9m
×
D
课堂练习
1、分类是一种科学的学习方法,科学分类的前提是有准确的分类标准。
2、用交叉分类法、树状分类法,按物质组成对物质进行分类。
3、分散系的概念与分类
4、胶体的概念与分类
5、氢氧化铁胶体的制备
6、丁达尔效应
课堂总结
导入
上节课我们学习了物质的分类
物质
混合物
纯净物
单质
化合物
非金属单质
金属单质
无机化合物
有机化合物
氧化物
酸
碱
盐
…
导入
根据物质的分类,可以认识物质的性质、转化关系,从而制备新物质。
物质的分类
物质的性质
物质之间的转化关系
认识
认识
人类生活和生产所需要的新物质
制备
制备
同类物质往往具有相似的性质。
盐酸、硫酸
氢氧化钠、氢氧化钙
碳酸钠、碳酸钾
酸
碱
盐
新课讲解
新课讲解
酸的主要化学性质
①酸可以与活泼金属反应
②酸可以与碱性氧化物反应
③酸可以与碱反应
④酸可以与某些盐反应
注:“酸”是在水溶液中电离时产生的阳离子都是氢离子的化合物。
根据酸的主要化学性质,可以有哪些反应实例呢?
思考·讨论
酸的主要化学性质 反应实例
酸与活泼金属反应 Zn + H2SO4 == ZnSO4 + H2↑
酸与碱性氧化物反应 6HCl + Fe2O3 == 2FeCl3 + 3H2O
酸与碱反应 NaOH + HCl == NaCl + H2O
酸与某些盐反应 HCl + AgNO3 == AgCl↓ + HNO3
新课讲解
碱的主要化学性质
①碱可以与非金属氧化物反应
②碱可以与酸反应
③碱可以与某些盐反应
④碱可以使酚酞试剂变红,使紫色石蕊试剂变蓝反应
注:“碱”是在水溶液中电离时产生的阴离子都是氢氧根离子的化合物。
根据碱的主要化学性质,可以有哪些反应实例呢?
思考·讨论
碱的主要化学性质 反应实例
碱与非金属氧化物反应 2NaOH + CO2 == Na2CO3 + H2O
碱与酸反应 NaOH + HCl == NaCl + H2O
碱与某些盐反应 Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH
新课讲解
盐的主要化学性质
①盐可以与金属反应
②盐可以与酸反应
③盐可以与碱反应
④盐可以与某些盐反应
注:“盐”是在水溶液中电离时生成金属阳离子(或其他阳离子)和酸根阴离子的化合物。
根据盐的主要化学性质,可以有哪些反应实例呢?
思考·讨论
盐的主要化学性质 反应实例
盐与金属反应 Fe + CuSO4 == FeSO4 + Cu↓
盐与酸反应 BaCl2 + H2SO4 == BaSO4↓ + 2HCl
盐与碱反应 FeCl3 + 3NaOH == 3NaCl + Fe(OH)3↓
盐与某些盐反应 BaCl2 + Na2SO4 == BaSO4↓ + 2NaCl
①为什么不同的酸(或碱)具有相似的化学性质?
思考·讨论
因为它们在组成上具有相似性。
“H+”酸
“酸根离子”盐
“OH-”
碱
②酸、碱、盐的主要化学性质中,涉及哪些反应类型?
思考·讨论
从反应类型来看,初中学过的酸与金属、盐与金属的反应都属于置换反应,酸与碱、盐与酸、盐与碱、盐与盐之间的反应都属于复分解反应。
试着写出下列物质之间转化的化学方程式,体会由金属单质到盐、非金属到盐的转化关系。
Ca → CaO → Ca(OH)2 → CaSO4
思考·讨论
C → CO2 → H2CO3 → CaCO3
对于上述转化关系,从物质分类的角度看,你发现了什么规律?
思考·讨论
金属单质
碱性氧化物
碱
盐
O2
H2O
酸或酸性氧化物
非金属单质
酸性氧化物
酸
盐
O2
H2O
碱或碱性氧化物
思维启迪
制取某类物质的方法
根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制取某类物质的方法。
例如,要想制取某种碱,通常可以采取两种方法:碱性氧化物与水发生反应;盐与另一种碱发生反应。
工业生产中制取NaOH ,是怎么做的呢?
思考·讨论
工业上制取NaOH一般不采用Na2O与H2O反应,而主要采用电解饱和食盐水的方法。
因为Na2O作为原料、来源少、成本高,因此不适用用批量生产NaOH。
2NaCl + 2H2O ==== 2NaOH + H2↑ + Cl2↑
通电
根据物质的组成和性质,通过化学变化可以实现物质之间的转化。在化学变化过程中,元素是不会改变的,这是考虑如何实现物质之间的转化时最基本的依据。
在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。
新课讲解
物质的转化
思维启迪
化学科研工作者与化学工程师
化学科研工作者研究的是基本原理,例如怎么合成某种物质,某种物质的结构是什么样的,某种物质具有什么电子、光学、力学、磁学性质。
化学工程师研究的是怎么实现这些基本原理,例如怎么设计化工厂的反应器,选择反应的温度、压强、催化剂。
从基础知识来看,量子力学对化学科研工作者的重要性远远超过对化学工程师,流体力学对化学工程师的重要性远远超过对化学科研工作者。
1.下列物质分类正确的是( )
课堂达标
D
碱 酸 盐 碱性氧化物 酸性氧化物
A Na2CO3 H2SO4 NaOH SO2 CO2
B NaOH HCl NaCl Na2O CO
C NaOH CH3COOH CaF2 CO SO2
D KOH HNO3 CaCO3 CaO SO2
解析 “酸”是在水溶液中电离时产生的阳离子都是氢离子的化合物;“碱”是在水溶液中电离时产生的阴离子都是氢氧根离子的化合物;“盐”是在水溶液中电离时生成金属阳离子(或其他阳离子)和酸根阴离子的化合物;碱性氧化物是指与酸反应而成盐和水的氧化物;酸性氧化物是指与碱作用生成盐和水的氧化物。Na2CO3不是碱,NaOH不是盐,SO2不是碱性氧化物,选项A错误;CO不是酸性氧化物,选项B错误;CO不是碱性氧化物,选项C错误。因此选D。
2.下列各组物质,按照单质、化合物、混合物的顺序排列正确的是( )
A. 稀有气体、酒、冰水混合物
B. 乙醇、浓硫酸、胆矾
C.金刚石、铁矿石、大理石
D.水银、水蒸气、水煤气
课堂达标
D
解析:酒是混合物,冰水混合物是纯净物,选项A错误;乙醇是化合物,浓硫酸是混合物,胆矾是纯净物,选项B错误;铁矿石是混合物,选项C错误;水银是单质,水蒸气是化合物,水煤气是混合物,选项D正确。因此选D。
3.下列反应方程正确的是( )
A.BaCl2 + H2SO4 == BaSO4 + 2HCl
B.NaOH + CO2 == Na2CO3 + H2O
C.HCl + AgNO3 == AgCl↓ + HNO3
D.4HCl + Fe2O3 == 2FeCl2 + 2H2O
课堂达标
解析:选项A是盐和酸的反应,正确的反应式是BaCl2 + H2SO4 == BaSO4↓ + 2HCl ,选项A错误;选项B是碱和酸性氧化物的反应,正确的反应式是2NaOH + CO2 == Na2CO3 + H2O,选项B错误;选项D是酸和金属氧化物的反应,正确的反应式是6HCl + Fe2O3 == 2FeCl3 + 3H2O,选项D错误。因此选C。
C
4.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可做干燥剂的理由是什么?(用化学方程式表示)
课堂达标
4. 同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)CaO是碱性氧化物
(2)生石灰能够强烈吸收水分,是碱性干燥剂的主要成分,吸水后氧化钙与水生成氢氧化钙:
课堂达标
CaO+H2O===Ca(OH)2(放出大量热)
解析:CaO是碱性氧化物,能与水、酸、酸性氧化物、盐反应,具有碱性氧化物的通性。生石灰能够强烈吸收水分,是碱性干燥剂的主要成分,吸水后氧化钙与水生成氢氧化钙。
物质的分类及转化
课堂小结
同类物质往往具有相似的性质
酸的化学性质:
①酸可以与活泼金属反应;②酸可以与碱性氧化物反应;③酸可以与碱反应;④酸可以与某些盐反应
碱的化学性质:
①碱可以与非金属氧化物反应;②碱可以与酸反应;③碱可以与某些盐反应;④碱可以使酚酞试剂变红,使紫色石蕊试剂变蓝反应
盐的化学性质:
①盐可以与金属反应;②盐可以与酸反应;③盐可以与碱反应;④盐可以与某些盐反应
物质的转化:
根据物质的组成和性质,通过化学变化可以实现物质之间的转化。在化学变化过程中,元素是不会改变的,这是考虑如何实现物质之间的转化时最基本的依据。
作业布置
P12:6、7、8
熟记酸、碱、盐的化学性质
