九年级上册化学 第五单元《化学方程式》综合测试卷(含答案)
文档属性
| 名称 | 九年级上册化学 第五单元《化学方程式》综合测试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 178.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-09 00:00:00 | ||
图片预览

文档简介
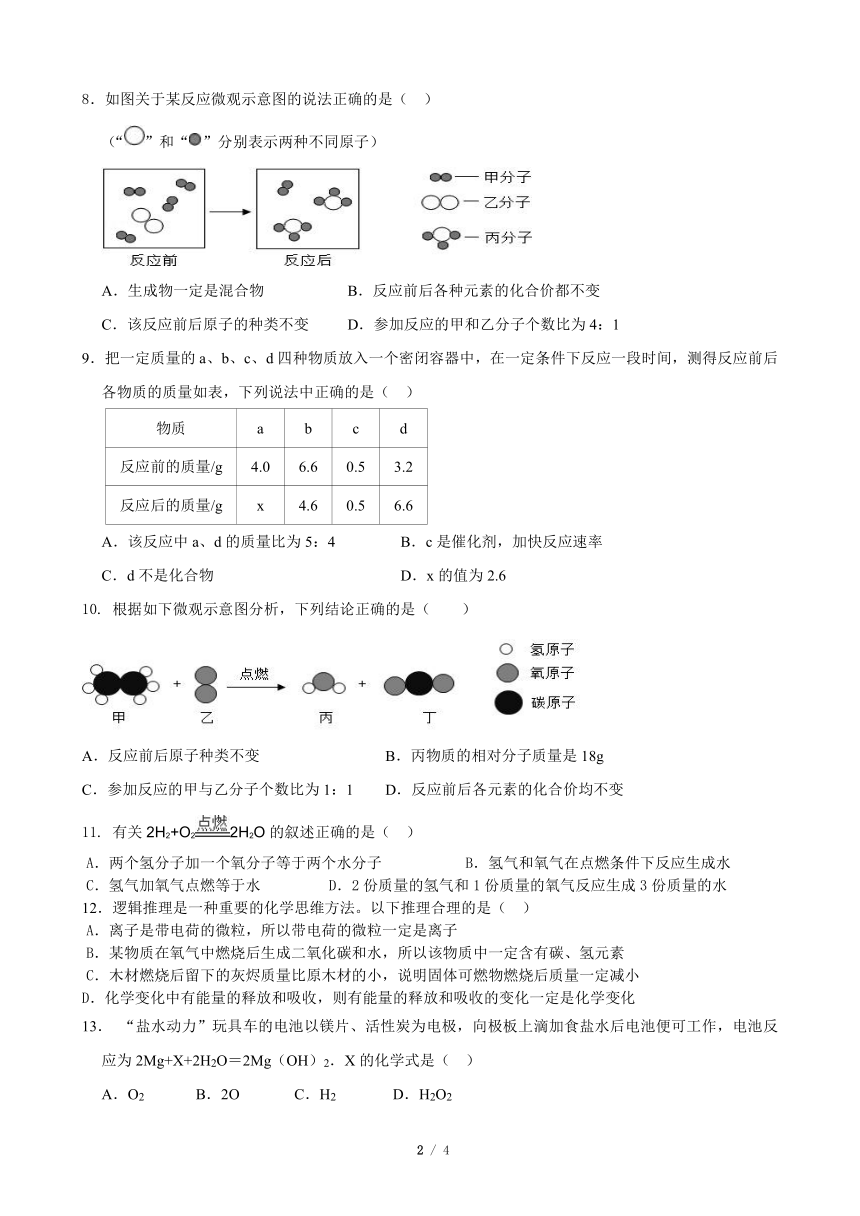
九年级化学第五单元《化学方程式》综合测试卷
附相对原子质量:H-1;C-12;N-14;O-16;
一、选择题:(153=45分)
1.下列情况中,能实现“1+1=2”这一结果的是( )
A.1毫升酒精加1毫升水得到2毫升酒精的水溶液
B.1克硫粉加1克氧气完全反应得到2克二氧化硫
C.1克氢氧化钙加1克水充分溶解后得到2克氢氧化钙溶液
D.1克氯化钡溶液加1克硫酸溶液充分反应后得到2克混合溶液
2.化学反应遵循质量守恒定律的原因是化学反应前后( )
A.分子的种类没有改变 B.分子的数目没有改变
C.原子的种类、数目和质量都没有改变 D.物质的种类没有改变
3.在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是( )
A.5g B.6g C.7g D.4g
4.下列实验能用于验证质量守恒定律的是( )
5.硝酸银通常保存在棕色的试剂瓶中,硝酸银受热分解会产生一种污染空气的有害气体,该气体可能是( )
A.O2 B.SO2 C.NH3 D.NO2
6.实验室制取氯气的反应方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2X,氯气有毒。下列说法不正确的是( )
A.X的化学式为H2O B.锰的化合价由+4降为+2
C.制取氯气时要有尾气处理装置 D.可采用制取二氧化碳的装置制取氯气
7. 草莓、香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(化学式为C4H8O2)等物质.下列关于乙酸乙酯的说法正确的是( )
A.该物质中碳、氢、氧的质量比为12:1:16 B.该物质属于氧化物
C.其分子由碳原子、氢原子和氧分子构成 D.该物质的相对分子质量为88
8.如图关于某反应微观示意图的说法正确的是( )
(“”和“”分别表示两种不同原子)
A.生成物一定是混合物 B.反应前后各种元素的化合价都不变
C.该反应前后原子的种类不变 D.参加反应的甲和乙分子个数比为4:1
9.把一定质量的a、b、c、d四种物质放入一个密闭容器中,在一定条件下反应一段时间,测得反应前后各物质的质量如表,下列说法中正确的是( )
物质 a b c d
反应前的质量/g 4.0 6.6 0.5 3.2
反应后的质量/g x 4.6 0.5 6.6
A.该反应中a、d的质量比为5:4 B.c是催化剂,加快反应速率
C.d不是化合物 D.x的值为2.6
10. 根据如下微观示意图分析,下列结论正确的是( )
A.反应前后原子种类不变 B.丙物质的相对分子质量是18g
C.参加反应的甲与乙分子个数比为1:1 D.反应前后各元素的化合价均不变
11. 有关2H2+O22H2O的叙述正确的是( )
A.两个氢分子加一个氧分子等于两个水分子 B.氢气和氧气在点燃条件下反应生成水
C.氢气加氧气点燃等于水 D.2份质量的氢气和1份质量的氧气反应生成3份质量的水
12.逻辑推理是一种重要的化学思维方法。以下推理合理的是( )
A.离子是带电荷的微粒,所以带电荷的微粒一定是离子
B.某物质在氧气中燃烧后生成二氧化碳和水,所以该物质中一定含有碳、氢元素
C.木材燃烧后留下的灰烬质量比原木材的小,说明固体可燃物燃烧后质量一定减小
D.化学变化中有能量的释放和吸收,则有能量的释放和吸收的变化一定是化学变化
13. “盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+X+2H2O=2Mg(OH)2.X的化学式是( )
A.O2 B.2O C.H2 D.H2O2
14.质量相同的下列四种物质,完全分解后制得氧气质量最多的是( )
A.H2O2 B.H2O C.KClO3 D.KMnO4
15.将16g纯净物R在足量氧气中完全燃烧,生成44g二氧化碳和36g水。下列判断正确的是( )
A.R只含碳、氢元素 B.消耗氧气32g
C.R含碳、氢、氧三种元素 D.R中碳元素的质量分数为70%
二、填空题(化学方程式每空2分,其他每空1分,共29分)
16. 化学用语可准确、简洁表达化学信息。请用恰当的化学用语填空。
(1)2个铝离子 ; (2)5个硫酸根离子 ; (3)氖气 ;
(4)保持冰、水混合物化学性质的粒子 ; (5)由Fe3+和OH﹣构成的氢氧化铁 ;
(6)地壳中含量最多的金属元素与最多的非金属元素形成化合物的化学式 。
17. “三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体.下图为该反应的微观示意图,其中“”“”“”分别代表碳原子、氮原子、氧原子.
请回答下列问题:
(1)1个A分子中含有 个原子,(2)B中碳元素和氧元素的质量比为 ,
(3)4种物质中,属于化合物的是 (填图中字母),
(4)该反应的化学方程式为 ,
(5)在该反应中,生成C和D的质量比为 (计算结果用最简整数比表示)
18. 如图是钾原子在元素周期表中的信息和结构示意图。
(1)将一小块金属钾放入水中,会与水发生剧烈反应,放出大量的热,生成一种碱和氢气。写出该反应的化学方程式 (2分)。
金属钾化学性质非常活泼的原因是 。
(2)钾元素位于元素周期表中第 周期。
19. 如图是某化学反应的微观模拟图,根据图示回答下列问题:
(1)在C图中将相关粒子图形补充完整 ① (在图中完成);补充此图形的依据是 ② ; (2)反应前后不发生改变的粒子是 (填名称);
(3)由此变化可知:在化学变化中,分子可以再分, 。
20. A、B、C、D、E、F、G、H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、H是黑色固体,D能使带火星的木条复燃,E、F都是无色液体,在②的反应前后B的质量和化学性质都不改变。
请根据上述信息,回答下列问题:
(1)物质C是 ,物质E是 。
(2)写出①、③反应的化学方程式。① 、③
(3)③反应中现象:
(4)物质B在两次反应中充当不同的角色,在①反应中它是 在②反应中它是
三、实验题(102=20分)
21. 实验小组同学规范地完成了如图所示的三个实验,验证质量守恒定律。
(1)实验甲乙中气球的作用是 ,实验结束冷却至室温后,气球比原来更瘪的原因是 ,此时将锥形瓶倒置于水中,取下气球,可观察到 ,锥形瓶底部铺一层细沙的目的是 。
(2)实验小组分别在反应结束后进行了称量,只有实验乙天平平衡,说明质量守恒,微观解释其守恒的原因是 ;在老师的引导下,也使甲实验天平平衡了,该实验初次称量不平衡的原因可能是 。
(3)碳酸钠与盐酸(HCl)反应生成氯化钠、水和二氧化碳,反应的化学方程式为 。实验B结束后天平的指针 (填“偏左”、“偏右、“不变),该反应 (填“符合”、“不符合”)质量守恒定律。
(4)教师引导学生分析了丙实验天平不平衡的原因,认为该实验要验证质量守恒定律应在 。
四、计算题(6分)
22.科学家正致力于研究光催化分解水制氢气,反应方程式为2H2O2H2↑+O2↑,用该方法制取12kg氢气至少需要分解多少千克的水?
参考答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 B C B C D D D C D A B B A B A
16. (1)2Al 3+; (2)5SO42﹣; (3)Ne; (4)H2O; (5)Fe(OH)3; (6)Al2O3。
17. (1)3; (2)3:4; (3)ABC; (4)2NO2+4CO4CO2+N2; (5)44:7.
18. (1)2K+2H2O═2KOH+H2↑; 在化学反应中易失去最外层电子; (2)4。
19. (1)①,②质量守恒定律; (2)氢原子、氧原子; (3)原子不可再分。
20.(1)C是锰酸钾,E是过氧化氢溶液
(2)①2KMnO4 K2MnO4+MnO2+O2↑;③2O2+3FeFe3O4;
(3)剧烈燃烧,火星四射,放出大量热,生成黑色固体;
(4)生成物,催化剂。
21. (1)平衡装置内外压强,防止瓶塞飞出;
锥形瓶中的氧气消耗;
水进入锥形瓶;
防止热的燃烧产物炸裂集气瓶。
(2)反应前后原子种类、原子个数和质量都不变;
没有冷却至室温就称量。
(3)Na2CO3+2HCl=2NaCl+H2O+CO2↑;
偏右;
符合。
(4)密闭体系中进行。
22. 解:设制取12kg氢气至少需要分解水的质量为x
2H2O2H2↑+O2↑
36 4
x 12kg
x=108kg。
答:制取12kg氢气至少需要分解108千克的水。
1 / 4
附相对原子质量:H-1;C-12;N-14;O-16;
一、选择题:(153=45分)
1.下列情况中,能实现“1+1=2”这一结果的是( )
A.1毫升酒精加1毫升水得到2毫升酒精的水溶液
B.1克硫粉加1克氧气完全反应得到2克二氧化硫
C.1克氢氧化钙加1克水充分溶解后得到2克氢氧化钙溶液
D.1克氯化钡溶液加1克硫酸溶液充分反应后得到2克混合溶液
2.化学反应遵循质量守恒定律的原因是化学反应前后( )
A.分子的种类没有改变 B.分子的数目没有改变
C.原子的种类、数目和质量都没有改变 D.物质的种类没有改变
3.在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是( )
A.5g B.6g C.7g D.4g
4.下列实验能用于验证质量守恒定律的是( )
5.硝酸银通常保存在棕色的试剂瓶中,硝酸银受热分解会产生一种污染空气的有害气体,该气体可能是( )
A.O2 B.SO2 C.NH3 D.NO2
6.实验室制取氯气的反应方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2X,氯气有毒。下列说法不正确的是( )
A.X的化学式为H2O B.锰的化合价由+4降为+2
C.制取氯气时要有尾气处理装置 D.可采用制取二氧化碳的装置制取氯气
7. 草莓、香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(化学式为C4H8O2)等物质.下列关于乙酸乙酯的说法正确的是( )
A.该物质中碳、氢、氧的质量比为12:1:16 B.该物质属于氧化物
C.其分子由碳原子、氢原子和氧分子构成 D.该物质的相对分子质量为88
8.如图关于某反应微观示意图的说法正确的是( )
(“”和“”分别表示两种不同原子)
A.生成物一定是混合物 B.反应前后各种元素的化合价都不变
C.该反应前后原子的种类不变 D.参加反应的甲和乙分子个数比为4:1
9.把一定质量的a、b、c、d四种物质放入一个密闭容器中,在一定条件下反应一段时间,测得反应前后各物质的质量如表,下列说法中正确的是( )
物质 a b c d
反应前的质量/g 4.0 6.6 0.5 3.2
反应后的质量/g x 4.6 0.5 6.6
A.该反应中a、d的质量比为5:4 B.c是催化剂,加快反应速率
C.d不是化合物 D.x的值为2.6
10. 根据如下微观示意图分析,下列结论正确的是( )
A.反应前后原子种类不变 B.丙物质的相对分子质量是18g
C.参加反应的甲与乙分子个数比为1:1 D.反应前后各元素的化合价均不变
11. 有关2H2+O22H2O的叙述正确的是( )
A.两个氢分子加一个氧分子等于两个水分子 B.氢气和氧气在点燃条件下反应生成水
C.氢气加氧气点燃等于水 D.2份质量的氢气和1份质量的氧气反应生成3份质量的水
12.逻辑推理是一种重要的化学思维方法。以下推理合理的是( )
A.离子是带电荷的微粒,所以带电荷的微粒一定是离子
B.某物质在氧气中燃烧后生成二氧化碳和水,所以该物质中一定含有碳、氢元素
C.木材燃烧后留下的灰烬质量比原木材的小,说明固体可燃物燃烧后质量一定减小
D.化学变化中有能量的释放和吸收,则有能量的释放和吸收的变化一定是化学变化
13. “盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+X+2H2O=2Mg(OH)2.X的化学式是( )
A.O2 B.2O C.H2 D.H2O2
14.质量相同的下列四种物质,完全分解后制得氧气质量最多的是( )
A.H2O2 B.H2O C.KClO3 D.KMnO4
15.将16g纯净物R在足量氧气中完全燃烧,生成44g二氧化碳和36g水。下列判断正确的是( )
A.R只含碳、氢元素 B.消耗氧气32g
C.R含碳、氢、氧三种元素 D.R中碳元素的质量分数为70%
二、填空题(化学方程式每空2分,其他每空1分,共29分)
16. 化学用语可准确、简洁表达化学信息。请用恰当的化学用语填空。
(1)2个铝离子 ; (2)5个硫酸根离子 ; (3)氖气 ;
(4)保持冰、水混合物化学性质的粒子 ; (5)由Fe3+和OH﹣构成的氢氧化铁 ;
(6)地壳中含量最多的金属元素与最多的非金属元素形成化合物的化学式 。
17. “三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体.下图为该反应的微观示意图,其中“”“”“”分别代表碳原子、氮原子、氧原子.
请回答下列问题:
(1)1个A分子中含有 个原子,(2)B中碳元素和氧元素的质量比为 ,
(3)4种物质中,属于化合物的是 (填图中字母),
(4)该反应的化学方程式为 ,
(5)在该反应中,生成C和D的质量比为 (计算结果用最简整数比表示)
18. 如图是钾原子在元素周期表中的信息和结构示意图。
(1)将一小块金属钾放入水中,会与水发生剧烈反应,放出大量的热,生成一种碱和氢气。写出该反应的化学方程式 (2分)。
金属钾化学性质非常活泼的原因是 。
(2)钾元素位于元素周期表中第 周期。
19. 如图是某化学反应的微观模拟图,根据图示回答下列问题:
(1)在C图中将相关粒子图形补充完整 ① (在图中完成);补充此图形的依据是 ② ; (2)反应前后不发生改变的粒子是 (填名称);
(3)由此变化可知:在化学变化中,分子可以再分, 。
20. A、B、C、D、E、F、G、H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、H是黑色固体,D能使带火星的木条复燃,E、F都是无色液体,在②的反应前后B的质量和化学性质都不改变。
请根据上述信息,回答下列问题:
(1)物质C是 ,物质E是 。
(2)写出①、③反应的化学方程式。① 、③
(3)③反应中现象:
(4)物质B在两次反应中充当不同的角色,在①反应中它是 在②反应中它是
三、实验题(102=20分)
21. 实验小组同学规范地完成了如图所示的三个实验,验证质量守恒定律。
(1)实验甲乙中气球的作用是 ,实验结束冷却至室温后,气球比原来更瘪的原因是 ,此时将锥形瓶倒置于水中,取下气球,可观察到 ,锥形瓶底部铺一层细沙的目的是 。
(2)实验小组分别在反应结束后进行了称量,只有实验乙天平平衡,说明质量守恒,微观解释其守恒的原因是 ;在老师的引导下,也使甲实验天平平衡了,该实验初次称量不平衡的原因可能是 。
(3)碳酸钠与盐酸(HCl)反应生成氯化钠、水和二氧化碳,反应的化学方程式为 。实验B结束后天平的指针 (填“偏左”、“偏右、“不变),该反应 (填“符合”、“不符合”)质量守恒定律。
(4)教师引导学生分析了丙实验天平不平衡的原因,认为该实验要验证质量守恒定律应在 。
四、计算题(6分)
22.科学家正致力于研究光催化分解水制氢气,反应方程式为2H2O2H2↑+O2↑,用该方法制取12kg氢气至少需要分解多少千克的水?
参考答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 B C B C D D D C D A B B A B A
16. (1)2Al 3+; (2)5SO42﹣; (3)Ne; (4)H2O; (5)Fe(OH)3; (6)Al2O3。
17. (1)3; (2)3:4; (3)ABC; (4)2NO2+4CO4CO2+N2; (5)44:7.
18. (1)2K+2H2O═2KOH+H2↑; 在化学反应中易失去最外层电子; (2)4。
19. (1)①,②质量守恒定律; (2)氢原子、氧原子; (3)原子不可再分。
20.(1)C是锰酸钾,E是过氧化氢溶液
(2)①2KMnO4 K2MnO4+MnO2+O2↑;③2O2+3FeFe3O4;
(3)剧烈燃烧,火星四射,放出大量热,生成黑色固体;
(4)生成物,催化剂。
21. (1)平衡装置内外压强,防止瓶塞飞出;
锥形瓶中的氧气消耗;
水进入锥形瓶;
防止热的燃烧产物炸裂集气瓶。
(2)反应前后原子种类、原子个数和质量都不变;
没有冷却至室温就称量。
(3)Na2CO3+2HCl=2NaCl+H2O+CO2↑;
偏右;
符合。
(4)密闭体系中进行。
22. 解:设制取12kg氢气至少需要分解水的质量为x
2H2O2H2↑+O2↑
36 4
x 12kg
x=108kg。
答:制取12kg氢气至少需要分解108千克的水。
1 / 4
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
