河南省漯河市临颍县第一高中2021-2022学年高二11月月考化学试卷(Word版含答案)
文档属性
| 名称 | 河南省漯河市临颍县第一高中2021-2022学年高二11月月考化学试卷(Word版含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 209.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-11 00:00:00 | ||
图片预览



文档简介
临颍县第一高中2021-2022学年高二11月月考
化学试卷
一、单选题
1.下列说法正确的是()
A. 乙烷和乙醇都属烃类化合物 B. 有机化合物一定含有碳元素
C. 丙烷和丁烷都有同分异构体 D. 含有碳元素的化合物一定是有机化合物
2.压强一定的条件下,决定气体分子间的平均距离的是( )
A. 温度 B. 气体的摩尔质量 C. 气体分子的质量 D. 气体分子的大小
3.在下列反应中,HCl作氧化剂的是( )
A. NaOH+HCl=NaCl+H2O B. Zn+2HCl=ZnCl2+H2↑
C. MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑ D. CuO+2HCl=CuCl2+H2O
4.下列溶液露置在空气中质量会变轻的是(不考虑溶剂挥发)( )
A. 澄清石灰水 B. Na2SO3溶液 C. NaOH溶液 D. 浓硫酸
5.下图是工业合成氨反应的速率-时间图像,在 t1 时刻改变某一条件,到 t2 时重新达到平衡,判断 t1 时刻可能改变条件是( )
A. 使用催化剂 B. 升高温度 C. 增大压强 D. 提高 N2 浓度
6.下列说法正确的是( )
A. 硫酸钡不溶于水,所以硫酸钡是非电解质 B. 铜可以导电,所以铜是电解质
C. 氯化钠溶液能导电,所以氯化钠溶液是电解质 D. 液态氯化氢不能导电,但氯化氢是电解质
7.有以下物质①Na2SO4溶液 ②熔融的CaCl2 ③CuSO4·5H2O固体 ④KOH固体 ⑤石墨 ⑥蔗糖。有关它们的说法正确的是( )
A. 不能导电的有③④⑥ B. 属于电解质有①②③④
C. 属于非电解质的有①⑤⑥ D. 属于混合物的有①②③⑥
8.材料是现代社会发展的重要支柱。下列材料中,不属于有机高分子材料的是( )
A.塑料
B.橡胶
C.合金
D.羊毛
9.下列有关浓硫酸的认识正确的是( )
A. 浓硫酸具有吸水性,可用来干燥H2S B. 浓硫酸在常温下不与铁和铝反应
C. 可将蒸馏水注入浓硫酸进行稀释 D. 棉花接触浓硫酸后会变黑
10.对一已经达到化学平衡的体系,下列说法符合题意的是( )
A. 化学反应速率变化时,化学平衡一定发生移动
B. 化学平衡发生移动时,化学反应速率一定变化
C. 正反应进行的程度越大,正反应速率一定越大
D. 使化学反应速率发生变化,而化学平衡不移动的影响因素,一定是催化剂
11.聚合氯化铝铁[AlFe(OH)nCl6-n]m用于生活给水及工业给水的净化处理。以工业废料(Fe、Al、FeO、Fe2O3、Al2O3)为原料生产该产品的流程如下,下列说法错误的是( )
A. 产品中铁元素的化合价为+3
B. 甲溶液中一定存在的阳离子有H+、Al3+、Fe2+、Fe3+
C. 试剂X可以用H2O2 , 目的是将Fe2+氧化为Fe3+
D. 乙溶液呈酸性
12.有机化合物种类丰富,数量繁多。乙醇和二甲醚的结构式如下图所示:
乙醇 二甲醚
下列关于上述两种物质的说法正确的是( )
A. 分子式不同 B. 碳氧键(C-O)数目相同 C. 互为同分异构体 D. 性质完全相同
13.下列烃在光照下与氯气反应,能生成多种一氯代烃的是( )
A. B.
C. D.
14.下列物质组合正确的是( )
序号 纯净物 混合物 非电解质 弱电解质 强电解质
A 盐酸 水煤气 HD 醋酸 硫酸
B 胆矾 漂白粉 NH3 HNO2 硫酸钡
C 火碱 蔗糖溶液 三氧化硫 氨水 碳酸氢钠
D 冰醋酸 福尔马林 乙醇 碘化氢 苛性钾
A. A B. B C. C D. D
15.为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
序号 不纯物 除杂试剂 分离方法
A CH4(C2H4) 酸性KMnO4溶液 洗气
B C2H5OH(乙酸) 新制生石灰 蒸馏
C 乙酸乙酯(乙醇) 饱和Na2CO3溶液 蒸馏
D NH4Cl溶液(FeCl3) NaOH溶液 过滤
A.A
B.B
C.C
D.D
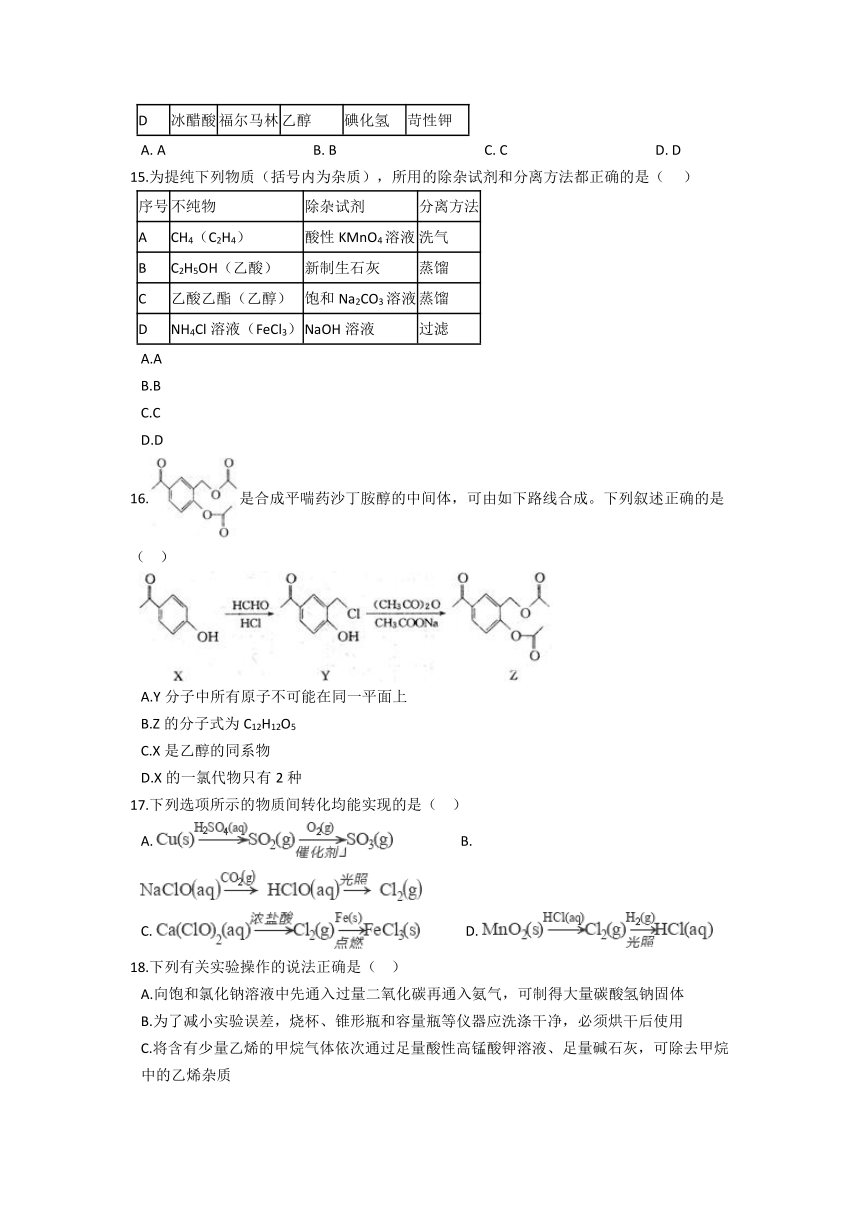
16.是合成平喘药沙丁胺醇的中间体,可由如下路线合成。下列叙述正确的是( )
A.Y分子中所有原子不可能在同一平面上
B.Z的分子式为C12H12O5
C.X是乙醇的同系物
D.X的一氯代物只有2种
17.下列选项所示的物质间转化均能实现的是( )
A. B.
C. D.
18.下列有关实验操作的说法正确是( )
A.向饱和氯化钠溶液中先通入过量二氧化碳再通入氨气,可制得大量碳酸氢钠固体
B.为了减小实验误差,烧杯、锥形瓶和容量瓶等仪器应洗涤干净,必须烘干后使用
C.将含有少量乙烯的甲烷气体依次通过足量酸性高锰酸钾溶液、足量碱石灰,可除去甲烷中的乙烯杂质
D.中和滴定实验中滴定管中液体流速宜先快后慢,滴定时眼睛注视着滴定管中液体刻度的变化
19.已知含氧酸可用通式(OH)nXOm来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大的是强酸,m小的是弱酸。下列各含氧酸中酸性最强的是( )
A. H2SeO3 B. HMnO4 C. H3BO3 D. H3PO4
20.CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列方案可以提高尾气处理效率的是( )
①提高装置温度 ②选用适当的催化剂 ③增大装置的压强 ④装置中放入碱石灰
A. ②③④ B. ①②③ C. ①③④ D. ①②③④
二、判断题
21.标准状况下,2.24L己烷含有分子的数目为0.1NA (判断对错)
22.含碳的化合物一定是有机化合物. (判断对错)
23.摩尔是七个基本物理量之一 .(判断对错)
24.某有机物燃烧后生成二氧化碳和水,所以此有机物一定含有C、H、O三种元素. (判断对错)
25.将蓝色的硫酸铜晶体放入浓硫酸属于物理变化 .(判断对错)
26.蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物 (判断对错)
27.处于金属和非金属分界线附近的元素常作催化剂(判断对错)
28.24g镁原子的最外层电子数为NA (判断对错)
29.现行的元素周期表共18个纵行,18个族,七个周期(判断对错)
30.所有的烷烃分子都存在同分异构体.(判断对错)
三、填空题
31.三大传统的硅酸盐材料指
32.下图为黑龙江省农科院种植的小麦,请填写下列空白:
如图农作物需要补充的化肥主要是________,如果作物叶片边缘发黄需要补充的化肥的作用是________,将小麦磨成面粉后,可以做一些面食,也有的在面食中加了点蔬菜做成蔬菜面条等,蔬菜面条中富含为人类提供能量的营养素是________,其化学式为________。维生素对生命活动的作用是________。
四、解答题
33.已知25℃时,Ksp(FeS)=8.1×10﹣17 , 试求FeS的溶解度(要求有计算过程Fe﹣56,S﹣32).
五、实验探究题
34.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)I.将钠、镁各2 g分别投入盛足量冷水的烧杯中,实验结果:________与冷水剧烈反应;另取镁、铝各2 g 分别投入足量0.05 mol/L盐酸中,________与盐酸反应最剧烈。
(2)向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明元素得电子能力________>________,反应的离子方程式为________。
实验结论:随原子序数增大,同周期元素失电子能力依次________(填“增强”或“减弱”,下同),得电子能力依次________。
(3)II.利用如图装置可验证同主族元素非金属性的变化规律。
仪器A的名称为________。
(4)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4.反应一段时间后,将C振荡、静置,观察到C中现象是________。此装置存在的不足之处是________。
35.某学生进行淀粉的水解实验,操作如下:
(1)取少量淀粉溶液,加入3~5滴稀硫酸,加热几分钟。淀粉水解反应的化学方程式为________
(2)取少量冷却后的水解液,向其中加入银氨溶液,水浴加热无银镜产生。他由此认为:水解产物中没有葡萄糖。他的结论是否正确 ________,理由是________
(3)用5t含淀粉80%的粮食,可以制得葡萄糖的质量为________。(假设淀粉的转化率为81%)
六、综合题
36.
(1)有以下四种物质:①22g二氧化碳②8g氢气③1.204×1024个氮气分子④4℃时18mL水它们所含分子数最多的是________,所含原子数最多的________,质量最大的是________所含电子数最多的是________(填序号)
(2)12.4 gNa2R含Na+0.4mol,则Na2R的摩尔质量为________,R的相对原子质量为________,含R的质量为1.6g的Na2R,其物质的量为________。
37.现有下列物质①NaCl晶体②干冰③HCl④铜⑤CaCO3固体⑥葡萄糖⑦酒精⑧熔融的KNO3⑨液氧⑩稀硫酸
(1)以上物质属于电解质的是:________;
(2)以上物质属于非电解质的是________;
(3)以上物质能导电的是________.
七、推断题
38.有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
请你根据上图推断:
(1)原溶液中一定存在的阴离子有________,显________(填“酸”“碱”或“中”)性。
(2)实验③中产生无色无味气体所发生的化学方程式为________。
(3)写出实验④中A点对应沉淀的化学式:________。
(4)写出实验④中,由A→B过程中所发生反应的离子方程式:________。
答案部分
一、单选题
1.【答案】 B
2.【答案】 A
3.【答案】 B
4.【答案】 A
5.【答案】 B
6.【答案】 D
7.【答案】 A
8.【答案】 C
9.【答案】 D
10.【答案】 B
11.【答案】 B
12.【答案】 C
13.【答案】 C
14.【答案】 B
15.【答案】 B
16.【答案】 A
17.【答案】 C
18.【答案】 C
19.【答案】 B
20.【答案】 A
二、判断题
21.【答案】 错误
22.【答案】 错误
23.【答案】 错误
24.【答案】 错误
25.【答案】 错误
26.【答案】 错误
27.【答案】 错误
28.【答案】 错误
29.【答案】 错误
30.【答案】 错误
三、填空题
31.【答案】 水泥;玻璃;陶瓷
32.【答案】 氮肥、磷肥、钾肥;氮肥;淀粉;(C6H10O5)n;调节新陈代谢,预防疾病,维持身体健康。
四、解答题
33.【答案】解:设达到溶解平衡时c(Fe2+)为x.
FeS(s) Fe2+(aq)+ S2﹣(aq)
x x
则x2=Ksp,x= =9×10﹣9 mol/L,
即1L溶液中含FeS的物质的量为9×10﹣9 mol,
S= ×100=7.92×10﹣8 g,
答:FeS的溶解度为7.92×10﹣8 g.
五、实验探究题
34.【答案】 (1)钠;镁
(2)C;Si;SiO +CO2+H2O=H2SiO3↓+CO ;减弱;增强
(3)分液漏斗
(4)溶液分层,上层接近无色,下层呈橙红色;无尾气处理装置,污染空气
35.【答案】 (1)(C6H10O5)n(淀粉)+nH2O nC6H12O6(葡萄糖)
(2)不正确;没有向水解液中加入NaOH溶液调节pH至碱性
(3)3.6t
六、综合题
36.【答案】 (1)②;②;③;③
(2)62 g mol-1;16;0.1 mol
37.【答案】 (1)①③⑤⑧
(2)②⑥⑦
(3)④⑧⑩
七、推断题
38.【答案】 (1)SO42-;酸
(2)2Na2O2+2H2O=4NaOH+O2↑
(3)Al(OH)3、Mg(OH)2
(4)Al(OH)3+OH-=AlO2-+2H2O
化学试卷
一、单选题
1.下列说法正确的是()
A. 乙烷和乙醇都属烃类化合物 B. 有机化合物一定含有碳元素
C. 丙烷和丁烷都有同分异构体 D. 含有碳元素的化合物一定是有机化合物
2.压强一定的条件下,决定气体分子间的平均距离的是( )
A. 温度 B. 气体的摩尔质量 C. 气体分子的质量 D. 气体分子的大小
3.在下列反应中,HCl作氧化剂的是( )
A. NaOH+HCl=NaCl+H2O B. Zn+2HCl=ZnCl2+H2↑
C. MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑ D. CuO+2HCl=CuCl2+H2O
4.下列溶液露置在空气中质量会变轻的是(不考虑溶剂挥发)( )
A. 澄清石灰水 B. Na2SO3溶液 C. NaOH溶液 D. 浓硫酸
5.下图是工业合成氨反应的速率-时间图像,在 t1 时刻改变某一条件,到 t2 时重新达到平衡,判断 t1 时刻可能改变条件是( )
A. 使用催化剂 B. 升高温度 C. 增大压强 D. 提高 N2 浓度
6.下列说法正确的是( )
A. 硫酸钡不溶于水,所以硫酸钡是非电解质 B. 铜可以导电,所以铜是电解质
C. 氯化钠溶液能导电,所以氯化钠溶液是电解质 D. 液态氯化氢不能导电,但氯化氢是电解质
7.有以下物质①Na2SO4溶液 ②熔融的CaCl2 ③CuSO4·5H2O固体 ④KOH固体 ⑤石墨 ⑥蔗糖。有关它们的说法正确的是( )
A. 不能导电的有③④⑥ B. 属于电解质有①②③④
C. 属于非电解质的有①⑤⑥ D. 属于混合物的有①②③⑥
8.材料是现代社会发展的重要支柱。下列材料中,不属于有机高分子材料的是( )
A.塑料
B.橡胶
C.合金
D.羊毛
9.下列有关浓硫酸的认识正确的是( )
A. 浓硫酸具有吸水性,可用来干燥H2S B. 浓硫酸在常温下不与铁和铝反应
C. 可将蒸馏水注入浓硫酸进行稀释 D. 棉花接触浓硫酸后会变黑
10.对一已经达到化学平衡的体系,下列说法符合题意的是( )
A. 化学反应速率变化时,化学平衡一定发生移动
B. 化学平衡发生移动时,化学反应速率一定变化
C. 正反应进行的程度越大,正反应速率一定越大
D. 使化学反应速率发生变化,而化学平衡不移动的影响因素,一定是催化剂
11.聚合氯化铝铁[AlFe(OH)nCl6-n]m用于生活给水及工业给水的净化处理。以工业废料(Fe、Al、FeO、Fe2O3、Al2O3)为原料生产该产品的流程如下,下列说法错误的是( )
A. 产品中铁元素的化合价为+3
B. 甲溶液中一定存在的阳离子有H+、Al3+、Fe2+、Fe3+
C. 试剂X可以用H2O2 , 目的是将Fe2+氧化为Fe3+
D. 乙溶液呈酸性
12.有机化合物种类丰富,数量繁多。乙醇和二甲醚的结构式如下图所示:
乙醇 二甲醚
下列关于上述两种物质的说法正确的是( )
A. 分子式不同 B. 碳氧键(C-O)数目相同 C. 互为同分异构体 D. 性质完全相同
13.下列烃在光照下与氯气反应,能生成多种一氯代烃的是( )
A. B.
C. D.
14.下列物质组合正确的是( )
序号 纯净物 混合物 非电解质 弱电解质 强电解质
A 盐酸 水煤气 HD 醋酸 硫酸
B 胆矾 漂白粉 NH3 HNO2 硫酸钡
C 火碱 蔗糖溶液 三氧化硫 氨水 碳酸氢钠
D 冰醋酸 福尔马林 乙醇 碘化氢 苛性钾
A. A B. B C. C D. D
15.为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
序号 不纯物 除杂试剂 分离方法
A CH4(C2H4) 酸性KMnO4溶液 洗气
B C2H5OH(乙酸) 新制生石灰 蒸馏
C 乙酸乙酯(乙醇) 饱和Na2CO3溶液 蒸馏
D NH4Cl溶液(FeCl3) NaOH溶液 过滤
A.A
B.B
C.C
D.D
16.是合成平喘药沙丁胺醇的中间体,可由如下路线合成。下列叙述正确的是( )
A.Y分子中所有原子不可能在同一平面上
B.Z的分子式为C12H12O5
C.X是乙醇的同系物
D.X的一氯代物只有2种
17.下列选项所示的物质间转化均能实现的是( )
A. B.
C. D.
18.下列有关实验操作的说法正确是( )
A.向饱和氯化钠溶液中先通入过量二氧化碳再通入氨气,可制得大量碳酸氢钠固体
B.为了减小实验误差,烧杯、锥形瓶和容量瓶等仪器应洗涤干净,必须烘干后使用
C.将含有少量乙烯的甲烷气体依次通过足量酸性高锰酸钾溶液、足量碱石灰,可除去甲烷中的乙烯杂质
D.中和滴定实验中滴定管中液体流速宜先快后慢,滴定时眼睛注视着滴定管中液体刻度的变化
19.已知含氧酸可用通式(OH)nXOm来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大的是强酸,m小的是弱酸。下列各含氧酸中酸性最强的是( )
A. H2SeO3 B. HMnO4 C. H3BO3 D. H3PO4
20.CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列方案可以提高尾气处理效率的是( )
①提高装置温度 ②选用适当的催化剂 ③增大装置的压强 ④装置中放入碱石灰
A. ②③④ B. ①②③ C. ①③④ D. ①②③④
二、判断题
21.标准状况下,2.24L己烷含有分子的数目为0.1NA (判断对错)
22.含碳的化合物一定是有机化合物. (判断对错)
23.摩尔是七个基本物理量之一 .(判断对错)
24.某有机物燃烧后生成二氧化碳和水,所以此有机物一定含有C、H、O三种元素. (判断对错)
25.将蓝色的硫酸铜晶体放入浓硫酸属于物理变化 .(判断对错)
26.蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物 (判断对错)
27.处于金属和非金属分界线附近的元素常作催化剂(判断对错)
28.24g镁原子的最外层电子数为NA (判断对错)
29.现行的元素周期表共18个纵行,18个族,七个周期(判断对错)
30.所有的烷烃分子都存在同分异构体.(判断对错)
三、填空题
31.三大传统的硅酸盐材料指
32.下图为黑龙江省农科院种植的小麦,请填写下列空白:
如图农作物需要补充的化肥主要是________,如果作物叶片边缘发黄需要补充的化肥的作用是________,将小麦磨成面粉后,可以做一些面食,也有的在面食中加了点蔬菜做成蔬菜面条等,蔬菜面条中富含为人类提供能量的营养素是________,其化学式为________。维生素对生命活动的作用是________。
四、解答题
33.已知25℃时,Ksp(FeS)=8.1×10﹣17 , 试求FeS的溶解度(要求有计算过程Fe﹣56,S﹣32).
五、实验探究题
34.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)I.将钠、镁各2 g分别投入盛足量冷水的烧杯中,实验结果:________与冷水剧烈反应;另取镁、铝各2 g 分别投入足量0.05 mol/L盐酸中,________与盐酸反应最剧烈。
(2)向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明元素得电子能力________>________,反应的离子方程式为________。
实验结论:随原子序数增大,同周期元素失电子能力依次________(填“增强”或“减弱”,下同),得电子能力依次________。
(3)II.利用如图装置可验证同主族元素非金属性的变化规律。
仪器A的名称为________。
(4)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4.反应一段时间后,将C振荡、静置,观察到C中现象是________。此装置存在的不足之处是________。
35.某学生进行淀粉的水解实验,操作如下:
(1)取少量淀粉溶液,加入3~5滴稀硫酸,加热几分钟。淀粉水解反应的化学方程式为________
(2)取少量冷却后的水解液,向其中加入银氨溶液,水浴加热无银镜产生。他由此认为:水解产物中没有葡萄糖。他的结论是否正确 ________,理由是________
(3)用5t含淀粉80%的粮食,可以制得葡萄糖的质量为________。(假设淀粉的转化率为81%)
六、综合题
36.
(1)有以下四种物质:①22g二氧化碳②8g氢气③1.204×1024个氮气分子④4℃时18mL水它们所含分子数最多的是________,所含原子数最多的________,质量最大的是________所含电子数最多的是________(填序号)
(2)12.4 gNa2R含Na+0.4mol,则Na2R的摩尔质量为________,R的相对原子质量为________,含R的质量为1.6g的Na2R,其物质的量为________。
37.现有下列物质①NaCl晶体②干冰③HCl④铜⑤CaCO3固体⑥葡萄糖⑦酒精⑧熔融的KNO3⑨液氧⑩稀硫酸
(1)以上物质属于电解质的是:________;
(2)以上物质属于非电解质的是________;
(3)以上物质能导电的是________.
七、推断题
38.有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
请你根据上图推断:
(1)原溶液中一定存在的阴离子有________,显________(填“酸”“碱”或“中”)性。
(2)实验③中产生无色无味气体所发生的化学方程式为________。
(3)写出实验④中A点对应沉淀的化学式:________。
(4)写出实验④中,由A→B过程中所发生反应的离子方程式:________。
答案部分
一、单选题
1.【答案】 B
2.【答案】 A
3.【答案】 B
4.【答案】 A
5.【答案】 B
6.【答案】 D
7.【答案】 A
8.【答案】 C
9.【答案】 D
10.【答案】 B
11.【答案】 B
12.【答案】 C
13.【答案】 C
14.【答案】 B
15.【答案】 B
16.【答案】 A
17.【答案】 C
18.【答案】 C
19.【答案】 B
20.【答案】 A
二、判断题
21.【答案】 错误
22.【答案】 错误
23.【答案】 错误
24.【答案】 错误
25.【答案】 错误
26.【答案】 错误
27.【答案】 错误
28.【答案】 错误
29.【答案】 错误
30.【答案】 错误
三、填空题
31.【答案】 水泥;玻璃;陶瓷
32.【答案】 氮肥、磷肥、钾肥;氮肥;淀粉;(C6H10O5)n;调节新陈代谢,预防疾病,维持身体健康。
四、解答题
33.【答案】解:设达到溶解平衡时c(Fe2+)为x.
FeS(s) Fe2+(aq)+ S2﹣(aq)
x x
则x2=Ksp,x= =9×10﹣9 mol/L,
即1L溶液中含FeS的物质的量为9×10﹣9 mol,
S= ×100=7.92×10﹣8 g,
答:FeS的溶解度为7.92×10﹣8 g.
五、实验探究题
34.【答案】 (1)钠;镁
(2)C;Si;SiO +CO2+H2O=H2SiO3↓+CO ;减弱;增强
(3)分液漏斗
(4)溶液分层,上层接近无色,下层呈橙红色;无尾气处理装置,污染空气
35.【答案】 (1)(C6H10O5)n(淀粉)+nH2O nC6H12O6(葡萄糖)
(2)不正确;没有向水解液中加入NaOH溶液调节pH至碱性
(3)3.6t
六、综合题
36.【答案】 (1)②;②;③;③
(2)62 g mol-1;16;0.1 mol
37.【答案】 (1)①③⑤⑧
(2)②⑥⑦
(3)④⑧⑩
七、推断题
38.【答案】 (1)SO42-;酸
(2)2Na2O2+2H2O=4NaOH+O2↑
(3)Al(OH)3、Mg(OH)2
(4)Al(OH)3+OH-=AlO2-+2H2O
同课章节目录
