2021年北京高考化学第15题分析和思考
图片预览








文档简介
(共35张PPT)
2021年北京高考第15题的分析和思考
主要内容
1. 素材赏析和解题思路
2. 定量计算
3. 教学启示
1. 素材赏析和解题思路
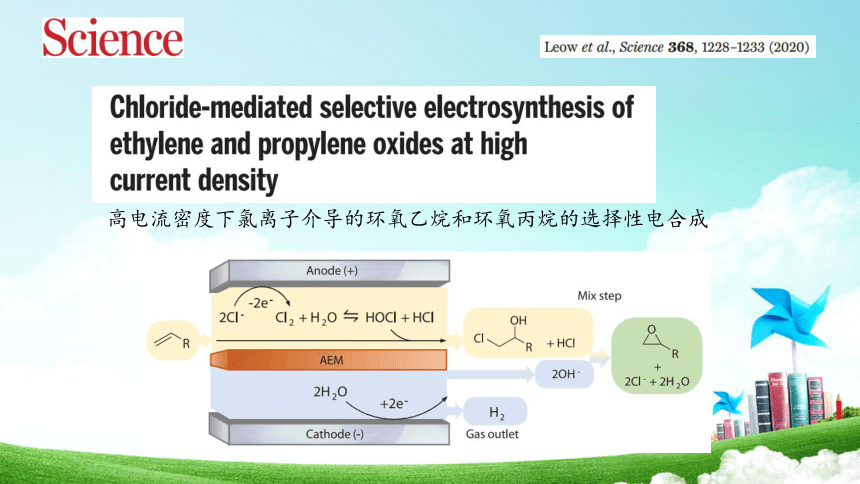
高电流密度下氯离子介导的环氧乙烷和环氧丙烷的选择性电合成
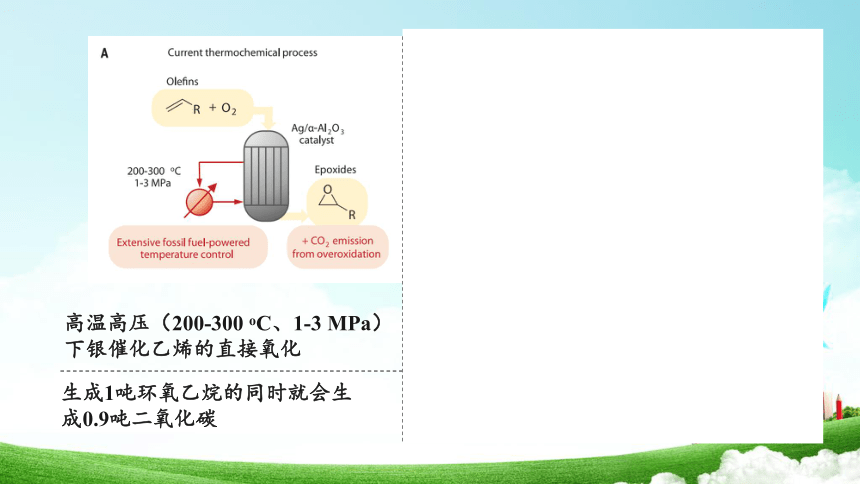
高温高压(200-300 oC、1-3 MPa)下银催化乙烯的直接氧化
生成1吨环氧乙烷的同时就会生成0.9吨二氧化碳
电化学合成法将乙烯转化为环氧乙烷
容易造成乙烯的过氧化
高电流密度下的法拉第效率较低
阴极
阳极
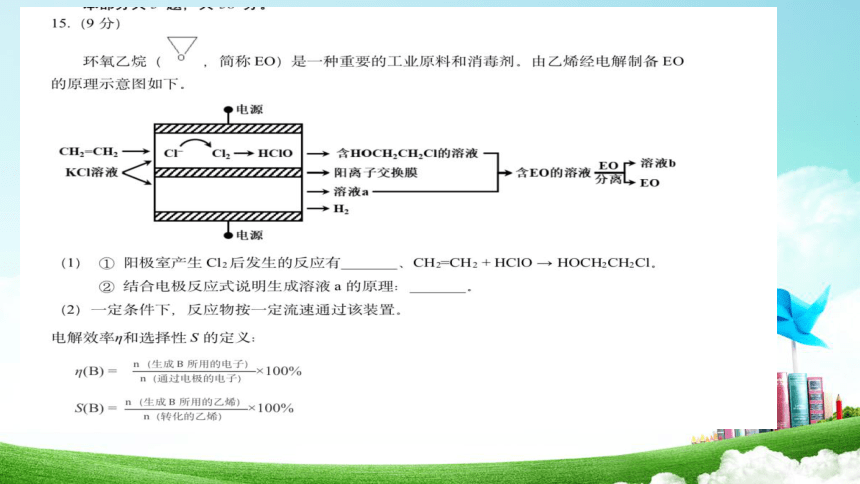
(1)
(2)
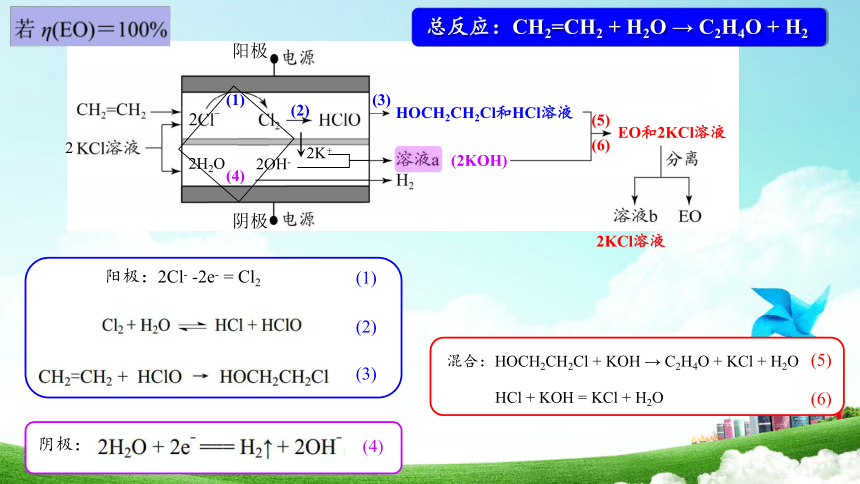
阳极:2Cl- -2e- = Cl2
阴极:
2
2K+
(4)
2H2O
2OH-
(1)
(2)
(3)
(4)
(3)
阴离子交换膜
2
阴极
阳极
(1)
(2)
阳极:2Cl- -2e- = Cl2
阴极:
2
2K+
(4)
2H2O
2OH-
HOCH2CH2Cl和HCl溶液
(2KOH)
EO和2KCl溶液
2KCl溶液
(5)
(6)
(1)
(2)
(3)
(4)
混合:HOCH2CH2Cl + KOH → C2H4O + KCl + H2O
HCl + KOH = KCl + H2O
总反应:CH2=CH2 + H2O → C2H4O + H2
(5)
(6)
(3)
2
猜想
实证
文献
2. 必须验证同时有
Cl2和HClO
检验Cl2和HClO
其中的一种即可
文献
反应可逆,Cl2和HClO一定共存
学生思路
检验Cl2和HClO
其中的一种即可
学生思路
实验方案
由(2)和(3),阳极流出液中一定含有Cl-,所以不能用AgNO3溶液
利用HClO的漂白性
利用Cl2和HClO的强氧化性
检验Cl2和H2O反应生成的Cl-
文献
加入过量 10% KI 溶液后阳极电解液的照片。 由于 I- 氧化形成 I2,观察到棕色。
加入淀粉溶液后相同阳极电解液的照片,形成深蓝色淀粉碘包合物。
用 Na2S2O3 滴定后阳极电解液的照片,得到澄清的无色溶液。
电流密度
(mA/cm2) 加入的Na2S2O3的量
(mmol) 未反应的Cl2或
HClO的量(mmol)
环氧乙烷
2-氯乙醇
法拉第效率
电流密度
阳极电解液和阴极电解液混合:
HOCH2CH2Cl + KOH → C2H4O + KCl + H2O
(5)
2. 定量计算
思路1:
η(CO2) = 1- 70% = 30%
η(EO) = 70%,
前结构层次
思路2:
e-
H2O
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
单一结构层次
思路3:多元结构层次
e-
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
3%
97%
过程1:C2H4放电生成CO2
C2H4 – 12e- + 4H2O = 2CO2 + 12H+
3% n(C2H4)
所用的电子为 3% n(C2H4) 12
97% n(C2H4)
所用的电子为 97% n(C2H4) 2
过程2:Cl-放电生成EO
C2H4 ~ 2e- ~ EO
= 15.6%
思路4:关联结构层次
过程1:C2H4放电生成CO2
过程2:Cl-放电生成EO
所用的电子为 3% n(C2H4) 12
所用的电子为 97% n(C2H4) 2
e-
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
3%
97%
思路5:拓展抽象结构层次
e-
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
3%
97%
过程1:C2H4放电生成CO2
过程2:Cl-放电生成EO
所用的电子为 3% n(C2H4) 12
所用的电子为 97% n(C2H4) 2
e-
O2
CO2
C2H4
Cl-
总Cl2
EO
C2H4
H2O
3%
97%
Cl2
HClO
HClO
3. 教学启示
1. 夯实基础
2. 培养关键能力
近10年北京高考中的化学计算:
3.氧化还原反应相关计算和速率平衡计算间隔出现。
2.连续热点是在真实情境下应用滴定方法测定物质的含量。
1.热化学方程式的反应热计算高频出现。
3. 定量计算问题
〖讨论2.关系式法在滴定计算中的应用〗
寻找联系
确定反应
建立关系式
列方程求n、%
快速浏览题干及设问,明确计算目标,找出反应。
标注反应过程的已知数据,确定滴定类型和计算类型。
根据反应原理和三大守恒,建立关系式。
规范方程式或方程组,计算目标物的物质的量,计算含量或纯度。
定性分析。正确书写方程式并配平是基础。
定性和定量结合。是难点,是关键。
解题思维模型:
小结:物质转化建立定性关系 守恒思想建立定量关系
已知量
找关系
待求量
元素
守恒
得失电子守恒
分析反应
e-
H2O
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
思路一:
思路二:
“关系”的外显和可视化
废水中苯酚含量的测定
化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol L-1标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
V.用b mol L-1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3 mL。
KBrO3
过量KBr
Br2
含苯酚废水
过量KI
Na2S2O3
滴定
至终点
I2
KBrO3
过量KBr
Br2
含苯酚废水
过量KI
Na2S2O3
滴定
至终点
I2
思路一:
思路二:
“关系”的外显和可视化
合成8-羟基喹啉时,反应时还生成了水,则L与G物质的量之比为 。
L
G
J
去2H
去2O
加2H
+ 2H2O
共需6H
8-羟基喹啉
×3
“关系”的外显和可视化
4. 注重模拟考试的难度调控
2021年北京高考第15题的分析和思考
主要内容
1. 素材赏析和解题思路
2. 定量计算
3. 教学启示
1. 素材赏析和解题思路
高电流密度下氯离子介导的环氧乙烷和环氧丙烷的选择性电合成
高温高压(200-300 oC、1-3 MPa)下银催化乙烯的直接氧化
生成1吨环氧乙烷的同时就会生成0.9吨二氧化碳
电化学合成法将乙烯转化为环氧乙烷
容易造成乙烯的过氧化
高电流密度下的法拉第效率较低
阴极
阳极
(1)
(2)
阳极:2Cl- -2e- = Cl2
阴极:
2
2K+
(4)
2H2O
2OH-
(1)
(2)
(3)
(4)
(3)
阴离子交换膜
2
阴极
阳极
(1)
(2)
阳极:2Cl- -2e- = Cl2
阴极:
2
2K+
(4)
2H2O
2OH-
HOCH2CH2Cl和HCl溶液
(2KOH)
EO和2KCl溶液
2KCl溶液
(5)
(6)
(1)
(2)
(3)
(4)
混合:HOCH2CH2Cl + KOH → C2H4O + KCl + H2O
HCl + KOH = KCl + H2O
总反应:CH2=CH2 + H2O → C2H4O + H2
(5)
(6)
(3)
2
猜想
实证
文献
2. 必须验证同时有
Cl2和HClO
检验Cl2和HClO
其中的一种即可
文献
反应可逆,Cl2和HClO一定共存
学生思路
检验Cl2和HClO
其中的一种即可
学生思路
实验方案
由(2)和(3),阳极流出液中一定含有Cl-,所以不能用AgNO3溶液
利用HClO的漂白性
利用Cl2和HClO的强氧化性
检验Cl2和H2O反应生成的Cl-
文献
加入过量 10% KI 溶液后阳极电解液的照片。 由于 I- 氧化形成 I2,观察到棕色。
加入淀粉溶液后相同阳极电解液的照片,形成深蓝色淀粉碘包合物。
用 Na2S2O3 滴定后阳极电解液的照片,得到澄清的无色溶液。
电流密度
(mA/cm2) 加入的Na2S2O3的量
(mmol) 未反应的Cl2或
HClO的量(mmol)
环氧乙烷
2-氯乙醇
法拉第效率
电流密度
阳极电解液和阴极电解液混合:
HOCH2CH2Cl + KOH → C2H4O + KCl + H2O
(5)
2. 定量计算
思路1:
η(CO2) = 1- 70% = 30%
η(EO) = 70%,
前结构层次
思路2:
e-
H2O
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
单一结构层次
思路3:多元结构层次
e-
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
3%
97%
过程1:C2H4放电生成CO2
C2H4 – 12e- + 4H2O = 2CO2 + 12H+
3% n(C2H4)
所用的电子为 3% n(C2H4) 12
97% n(C2H4)
所用的电子为 97% n(C2H4) 2
过程2:Cl-放电生成EO
C2H4 ~ 2e- ~ EO
= 15.6%
思路4:关联结构层次
过程1:C2H4放电生成CO2
过程2:Cl-放电生成EO
所用的电子为 3% n(C2H4) 12
所用的电子为 97% n(C2H4) 2
e-
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
3%
97%
思路5:拓展抽象结构层次
e-
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
3%
97%
过程1:C2H4放电生成CO2
过程2:Cl-放电生成EO
所用的电子为 3% n(C2H4) 12
所用的电子为 97% n(C2H4) 2
e-
O2
CO2
C2H4
Cl-
总Cl2
EO
C2H4
H2O
3%
97%
Cl2
HClO
HClO
3. 教学启示
1. 夯实基础
2. 培养关键能力
近10年北京高考中的化学计算:
3.氧化还原反应相关计算和速率平衡计算间隔出现。
2.连续热点是在真实情境下应用滴定方法测定物质的含量。
1.热化学方程式的反应热计算高频出现。
3. 定量计算问题
〖讨论2.关系式法在滴定计算中的应用〗
寻找联系
确定反应
建立关系式
列方程求n、%
快速浏览题干及设问,明确计算目标,找出反应。
标注反应过程的已知数据,确定滴定类型和计算类型。
根据反应原理和三大守恒,建立关系式。
规范方程式或方程组,计算目标物的物质的量,计算含量或纯度。
定性分析。正确书写方程式并配平是基础。
定性和定量结合。是难点,是关键。
解题思维模型:
小结:物质转化建立定性关系 守恒思想建立定量关系
已知量
找关系
待求量
元素
守恒
得失电子守恒
分析反应
e-
H2O
O2
CO2
C2H4
Cl-
Cl2
EO
C2H4
H2O
思路一:
思路二:
“关系”的外显和可视化
废水中苯酚含量的测定
化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol L-1标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
V.用b mol L-1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3 mL。
KBrO3
过量KBr
Br2
含苯酚废水
过量KI
Na2S2O3
滴定
至终点
I2
KBrO3
过量KBr
Br2
含苯酚废水
过量KI
Na2S2O3
滴定
至终点
I2
思路一:
思路二:
“关系”的外显和可视化
合成8-羟基喹啉时,反应时还生成了水,则L与G物质的量之比为 。
L
G
J
去2H
去2O
加2H
+ 2H2O
共需6H
8-羟基喹啉
×3
“关系”的外显和可视化
4. 注重模拟考试的难度调控
同课章节目录
