9.2.2 溶解度(课件26页)
图片预览






文档简介
(共26张PPT)
第九单元 课题2 溶解度
课时2 溶解度
在课题1溶液的学习中,我们就明白:不同溶质在同种溶剂中的溶解能力不同。同种溶质在不同溶剂中的溶解能力也不同。这节课我们就来从量的角度研究物质的溶解能力。
导入新课
1.了解溶解度含义,初步学习绘制溶解度曲线和查阅溶解度曲线。
2.了解溶解度的主要外界影响因素和应用。
3.了解气体溶解度定义和影响因素。
学习目标
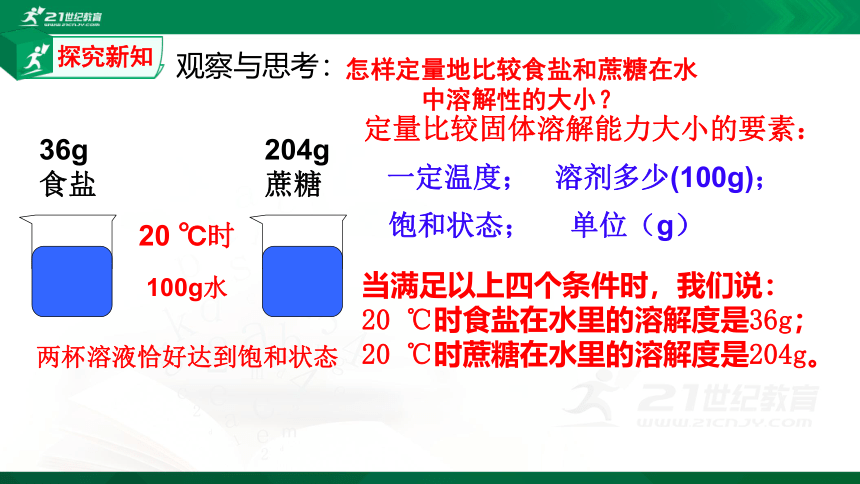
怎样定量地比较食盐和蔗糖在水中溶解性的大小?
观察与思考:
20 ℃时
100g水
36g食盐
204g蔗糖
两杯溶液恰好达到饱和状态
定量比较固体溶解能力大小的要素:
一定温度;
溶剂多少(100g);
饱和状态;
单位(g)
当满足以上四个条件时,我们说:
20 ℃时食盐在水里的溶解度是36g;
20 ℃时蔗糖在水里的溶解度是204g。
探究新知
一、固体物质的溶解度
观察与思考:
1.固体物质溶解度(通常用S表示)
在一定温度下,某固体物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
四要素
条件:一定温度
标准:100克溶剂(未说明的情况下通常指水)
状态:饱和状态(最大值)
单位:质量(克)
影响因素
内部因素:溶质和溶剂本身的性质。
外部因素:________。
温度
什么是固体溶解度?
观察与思考:
20℃时,硝酸钾的溶解度是31.6克的意义?
20℃时,100克水中最多能溶解硝酸钾的质量为31.6克;
20℃时,100克水中溶解31.6克的硝
酸钾就达到饱和状态。
学以致用
(1)20克A物质溶解在100克水中恰好配成饱和溶液,A的溶解度是20克。( )
(2) 20℃ ,20克A物质溶解在水中配成饱和溶液, 20℃ 时A的溶解度是20克。( )
(3)20℃ ,20克A物质溶解在水中配成100克饱和溶液,则 20℃ 时A的溶解度是20克。( )
(4)20℃ ,20克A物质溶解在100克水中配成饱和溶液,则 20℃ 时A的溶解度是20克。( )
你会判断吗?
×
×
×
√
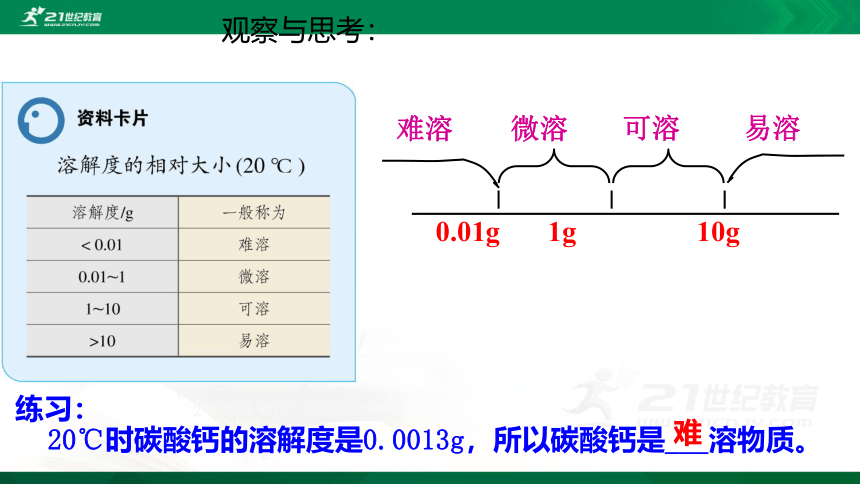
观察与思考:
难溶
微溶
可溶
易溶
0.01g
10g
1g
练习: 20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。
难
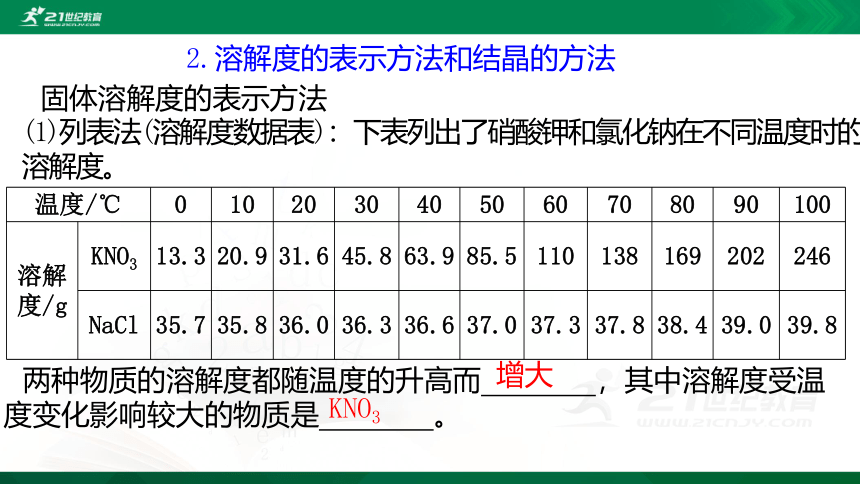
2.溶解度的表示方法和结晶的方法
固体溶解度的表示方法
(1)列表法(溶解度数据表):下表列出了硝酸钾和氯化钠在不同温度时的溶解度。
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
溶解 度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8
两种物质的溶解度都随温度的升高而 ,其中溶解度受温度变化影响较大的物质是 。
增大
KNO3
(2)作图法(溶解度曲线):用纵坐标表示 ,横坐标表示 ,得到物质的溶解度随温度变化的曲线。
溶解度
温度
根据下面表格中列出的溶解度,在
右边坐标纸内画出溶解度曲线图。
温度/℃ 0 10 20 30 40 50
溶解 度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
温度/℃ 60 70 80 90 100
溶解 度/g KNO3 110 138 169 202 246
NaCl 37.3 37.8 38.4 39.0 39.8
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
KNO3
NaCl
2.溶解度曲线的变化规律和结晶方法的选择
(1)多数固体物质的溶解度随温度的升高而增大(陡升型),
如 、 等。此类物质结晶方法选择
。
(2)少数固体物质的溶解度受温度变化影响很小(缓升型),
如________。此类物质结晶方法选择____________。
(3)极少数固体物质的溶解度随温度的升高而减小(下降
型),如____________。
KNO3
NaNO3
降温结晶
NaCl
蒸发结晶
Ca(OH)2
归纳与小结:
(1)曲线上的点均表示某物质在该温度下的溶解度。
(2)曲线下方的点表示这种物质在该温度下的不饱和溶液。
(3)曲线上方的点表示这种物质在该温度下的饱和溶液。
(4)曲线的交点表示不同物质在该温度下的溶解度相等。
(5)结晶法提纯物质(适宜于溶解度随温度变化趋势有差异的物质):
①降温结晶法(蒸发浓缩→降温结晶→过滤),如提纯NaCl和KNO3混合溶液中的KNO3;
②蒸发结晶法(蒸发结晶而不蒸干→趁热过滤),
如提纯NaCl和KNO3混合溶液中的NaCl。
归纳与小结:
(6)固体物质溶解度受温度变化影响情况:
1.大多数固体物质溶解度随温度升高而增大, 如硝酸钾等。
2.少数固体物质溶解度受温度影响不大,如食盐。
3.极少数固体物质溶解度随温度升高反而减小,如熟石灰。
二、气体物质的溶解度
观察与思考:
天气闷热时,鱼儿为什么总爱跳出水面上进行呼吸?
1.概念:某气体的压强为________kPa和一定________时,在_____体积水里溶解达到________状态时的气体______。如氮气的压强为101kPa和温度为0 ℃时,1体积水里最多能溶解0.024体积的氮气,则在0 ℃时,氮气的溶解度为________。
101
温度
1
饱和
体积
0.024
探究新知
交流与讨论:
讨论回答下列问题,归纳影响气体溶解度的因素和影响规律。
(1)打开汽水(含有二氧化碳的饮料)瓶盖后,汽水会自动喷出来。
这说明气体在水中的溶解度与什么有关?它是怎样影响气体溶解度的?
_____________________________________________________。
(2)喝了汽水以后,常常会打嗝。这说明气体在水中的溶解度与什
么有关?它是怎样影响气体溶解度的? ________________________________________________________。
气体在水中的溶解度与压强有关;压强越小,气体溶解度越小
气体在水中的溶解度与温度有关;温度越高,气体溶解度越小
(3)天气闷热时,鱼儿为什么总爱跳出水面上进行呼吸?
温度越高,气体溶解度越小。
溶解性
同种溶质在不同的溶 剂中的溶解能力不同
不同的溶质在同种溶 剂中的溶解能力不同
①一定温度
②100克溶剂
③溶液饱和
④单位是克
定量描述
易溶 、可溶 、 微溶 、 难(不)溶
物质的溶解度
固体的溶解度
气体的溶解度
影响因素(温度)
表示方法
影响因素 (温度、压强)
表示方法
课堂小结
1.下图是甲、乙两种物质的溶解度曲线。t3℃时,将取ag甲和ag乙分别放入100g水中,充分搅拌,然后降温,下列说法不正确的是( )
A.t1℃时,甲的溶解度小于乙的溶解度
B.降温至t2℃时,甲溶液和乙溶液均饱和
C.降温至t1℃时,两种溶液中溶质的质量分数相等
D.若甲中混有少量的乙,可用降温结晶的方法提纯甲
C
课堂练习
2.甲、乙两种固体的溶解度曲线如图所示,下列说法不正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙饱和溶液中溶质的质量分数相等
C.常采用冷却热饱和溶液的方法从溶液中获得甲物质晶体
D.将t1℃时相等质量的甲、乙的饱和溶液升温到t2℃,溶液中溶质的质量甲等于乙
A
3.0℃时,向100g水中不断加入硝酸钾固体或改变温度,得到相应的溶液①~⑤。
③中溶液的质量为( )
A.60g B.100g C.160g D.163.9g
C
4.40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。①中溶液的质量为( )
A.30 g B.100 g C.130 g 140 g
C
5.A、B、C三种物质的溶解度曲线如图所示,下列分析正确的是( )
A.t1℃时,A、C两种物质的饱和溶液中溶质的质量分数相等
B.使t1℃时A、B的饱和溶液升温至t2℃时仍为饱和溶液,需加入的A比B多
C.B中含有少量A时,可通过降温结晶提纯B
D.t2℃时,在50g水中得到A的饱和溶液,其中溶质和溶液的质量比为1:2
A
6.已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法不正确的是( )
A.溶液中溶质质量分数的大小关系为丁>丙>甲
B.丙中溶液溶质与溶剂的质量比为8:25
C.丁溶液一定是饱和溶液
D.CuSO4 50℃时的溶解度比20℃时的大
C
A
7.60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,析出固体质量的变化如图1,结合图2,下列说法正确的是( )
A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.蒸发溶剂可将M点的溶液转化到N点
D.20℃时,100g KNO3饱和溶液中有KNO331. 6g
8.下列是硼酸在水中的溶解度表,下列说法不正确的是( )
温度/℃ 10 20 40 60 80 100
在水中溶解度/g 3 5 9 15 23 37
在水中滴入稀盐酸后的溶解度/g 3.3 5.6 10.1 16.6 25.1 41.3
A.硼酸属于可溶物质
B.硼酸在盐酸中溶解形成的水溶液,溶质只有硼酸
C.60℃时硼酸在水中的最大浓度不会超过15%
D.40℃时配制50g5%的硼酸溶液需加水47.5mL
B
谢谢
21世纪教育网(www.21cnjy.com) 中小学教育资源网站
有大把高质量资料?一线教师?一线教研员?
欢迎加入21世纪教育网教师合作团队!!月薪过万不是梦!!
详情请看:
https://www.21cnjy.com/help/help_extract.php
第九单元 课题2 溶解度
课时2 溶解度
在课题1溶液的学习中,我们就明白:不同溶质在同种溶剂中的溶解能力不同。同种溶质在不同溶剂中的溶解能力也不同。这节课我们就来从量的角度研究物质的溶解能力。
导入新课
1.了解溶解度含义,初步学习绘制溶解度曲线和查阅溶解度曲线。
2.了解溶解度的主要外界影响因素和应用。
3.了解气体溶解度定义和影响因素。
学习目标
怎样定量地比较食盐和蔗糖在水中溶解性的大小?
观察与思考:
20 ℃时
100g水
36g食盐
204g蔗糖
两杯溶液恰好达到饱和状态
定量比较固体溶解能力大小的要素:
一定温度;
溶剂多少(100g);
饱和状态;
单位(g)
当满足以上四个条件时,我们说:
20 ℃时食盐在水里的溶解度是36g;
20 ℃时蔗糖在水里的溶解度是204g。
探究新知
一、固体物质的溶解度
观察与思考:
1.固体物质溶解度(通常用S表示)
在一定温度下,某固体物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
四要素
条件:一定温度
标准:100克溶剂(未说明的情况下通常指水)
状态:饱和状态(最大值)
单位:质量(克)
影响因素
内部因素:溶质和溶剂本身的性质。
外部因素:________。
温度
什么是固体溶解度?
观察与思考:
20℃时,硝酸钾的溶解度是31.6克的意义?
20℃时,100克水中最多能溶解硝酸钾的质量为31.6克;
20℃时,100克水中溶解31.6克的硝
酸钾就达到饱和状态。
学以致用
(1)20克A物质溶解在100克水中恰好配成饱和溶液,A的溶解度是20克。( )
(2) 20℃ ,20克A物质溶解在水中配成饱和溶液, 20℃ 时A的溶解度是20克。( )
(3)20℃ ,20克A物质溶解在水中配成100克饱和溶液,则 20℃ 时A的溶解度是20克。( )
(4)20℃ ,20克A物质溶解在100克水中配成饱和溶液,则 20℃ 时A的溶解度是20克。( )
你会判断吗?
×
×
×
√
观察与思考:
难溶
微溶
可溶
易溶
0.01g
10g
1g
练习: 20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。
难
2.溶解度的表示方法和结晶的方法
固体溶解度的表示方法
(1)列表法(溶解度数据表):下表列出了硝酸钾和氯化钠在不同温度时的溶解度。
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
溶解 度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8
两种物质的溶解度都随温度的升高而 ,其中溶解度受温度变化影响较大的物质是 。
增大
KNO3
(2)作图法(溶解度曲线):用纵坐标表示 ,横坐标表示 ,得到物质的溶解度随温度变化的曲线。
溶解度
温度
根据下面表格中列出的溶解度,在
右边坐标纸内画出溶解度曲线图。
温度/℃ 0 10 20 30 40 50
溶解 度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
温度/℃ 60 70 80 90 100
溶解 度/g KNO3 110 138 169 202 246
NaCl 37.3 37.8 38.4 39.0 39.8
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
KNO3
NaCl
2.溶解度曲线的变化规律和结晶方法的选择
(1)多数固体物质的溶解度随温度的升高而增大(陡升型),
如 、 等。此类物质结晶方法选择
。
(2)少数固体物质的溶解度受温度变化影响很小(缓升型),
如________。此类物质结晶方法选择____________。
(3)极少数固体物质的溶解度随温度的升高而减小(下降
型),如____________。
KNO3
NaNO3
降温结晶
NaCl
蒸发结晶
Ca(OH)2
归纳与小结:
(1)曲线上的点均表示某物质在该温度下的溶解度。
(2)曲线下方的点表示这种物质在该温度下的不饱和溶液。
(3)曲线上方的点表示这种物质在该温度下的饱和溶液。
(4)曲线的交点表示不同物质在该温度下的溶解度相等。
(5)结晶法提纯物质(适宜于溶解度随温度变化趋势有差异的物质):
①降温结晶法(蒸发浓缩→降温结晶→过滤),如提纯NaCl和KNO3混合溶液中的KNO3;
②蒸发结晶法(蒸发结晶而不蒸干→趁热过滤),
如提纯NaCl和KNO3混合溶液中的NaCl。
归纳与小结:
(6)固体物质溶解度受温度变化影响情况:
1.大多数固体物质溶解度随温度升高而增大, 如硝酸钾等。
2.少数固体物质溶解度受温度影响不大,如食盐。
3.极少数固体物质溶解度随温度升高反而减小,如熟石灰。
二、气体物质的溶解度
观察与思考:
天气闷热时,鱼儿为什么总爱跳出水面上进行呼吸?
1.概念:某气体的压强为________kPa和一定________时,在_____体积水里溶解达到________状态时的气体______。如氮气的压强为101kPa和温度为0 ℃时,1体积水里最多能溶解0.024体积的氮气,则在0 ℃时,氮气的溶解度为________。
101
温度
1
饱和
体积
0.024
探究新知
交流与讨论:
讨论回答下列问题,归纳影响气体溶解度的因素和影响规律。
(1)打开汽水(含有二氧化碳的饮料)瓶盖后,汽水会自动喷出来。
这说明气体在水中的溶解度与什么有关?它是怎样影响气体溶解度的?
_____________________________________________________。
(2)喝了汽水以后,常常会打嗝。这说明气体在水中的溶解度与什
么有关?它是怎样影响气体溶解度的? ________________________________________________________。
气体在水中的溶解度与压强有关;压强越小,气体溶解度越小
气体在水中的溶解度与温度有关;温度越高,气体溶解度越小
(3)天气闷热时,鱼儿为什么总爱跳出水面上进行呼吸?
温度越高,气体溶解度越小。
溶解性
同种溶质在不同的溶 剂中的溶解能力不同
不同的溶质在同种溶 剂中的溶解能力不同
①一定温度
②100克溶剂
③溶液饱和
④单位是克
定量描述
易溶 、可溶 、 微溶 、 难(不)溶
物质的溶解度
固体的溶解度
气体的溶解度
影响因素(温度)
表示方法
影响因素 (温度、压强)
表示方法
课堂小结
1.下图是甲、乙两种物质的溶解度曲线。t3℃时,将取ag甲和ag乙分别放入100g水中,充分搅拌,然后降温,下列说法不正确的是( )
A.t1℃时,甲的溶解度小于乙的溶解度
B.降温至t2℃时,甲溶液和乙溶液均饱和
C.降温至t1℃时,两种溶液中溶质的质量分数相等
D.若甲中混有少量的乙,可用降温结晶的方法提纯甲
C
课堂练习
2.甲、乙两种固体的溶解度曲线如图所示,下列说法不正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙饱和溶液中溶质的质量分数相等
C.常采用冷却热饱和溶液的方法从溶液中获得甲物质晶体
D.将t1℃时相等质量的甲、乙的饱和溶液升温到t2℃,溶液中溶质的质量甲等于乙
A
3.0℃时,向100g水中不断加入硝酸钾固体或改变温度,得到相应的溶液①~⑤。
③中溶液的质量为( )
A.60g B.100g C.160g D.163.9g
C
4.40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。①中溶液的质量为( )
A.30 g B.100 g C.130 g 140 g
C
5.A、B、C三种物质的溶解度曲线如图所示,下列分析正确的是( )
A.t1℃时,A、C两种物质的饱和溶液中溶质的质量分数相等
B.使t1℃时A、B的饱和溶液升温至t2℃时仍为饱和溶液,需加入的A比B多
C.B中含有少量A时,可通过降温结晶提纯B
D.t2℃时,在50g水中得到A的饱和溶液,其中溶质和溶液的质量比为1:2
A
6.已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法不正确的是( )
A.溶液中溶质质量分数的大小关系为丁>丙>甲
B.丙中溶液溶质与溶剂的质量比为8:25
C.丁溶液一定是饱和溶液
D.CuSO4 50℃时的溶解度比20℃时的大
C
A
7.60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,析出固体质量的变化如图1,结合图2,下列说法正确的是( )
A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.蒸发溶剂可将M点的溶液转化到N点
D.20℃时,100g KNO3饱和溶液中有KNO331. 6g
8.下列是硼酸在水中的溶解度表,下列说法不正确的是( )
温度/℃ 10 20 40 60 80 100
在水中溶解度/g 3 5 9 15 23 37
在水中滴入稀盐酸后的溶解度/g 3.3 5.6 10.1 16.6 25.1 41.3
A.硼酸属于可溶物质
B.硼酸在盐酸中溶解形成的水溶液,溶质只有硼酸
C.60℃时硼酸在水中的最大浓度不会超过15%
D.40℃时配制50g5%的硼酸溶液需加水47.5mL
B
谢谢
21世纪教育网(www.21cnjy.com) 中小学教育资源网站
有大把高质量资料?一线教师?一线教研员?
欢迎加入21世纪教育网教师合作团队!!月薪过万不是梦!!
详情请看:
https://www.21cnjy.com/help/help_extract.php
同课章节目录
