苏教版高一化学1《氯气的生产原理》课件
文档属性
| 名称 | 苏教版高一化学1《氯气的生产原理》课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 395.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-10-20 00:00:00 | ||
图片预览









文档简介
(共31张PPT)
你知道浩瀚的大海中究竟蕴藏着哪些物质吗?请查阅有关资料了解海水中主要含有的物质和各元素的含量。
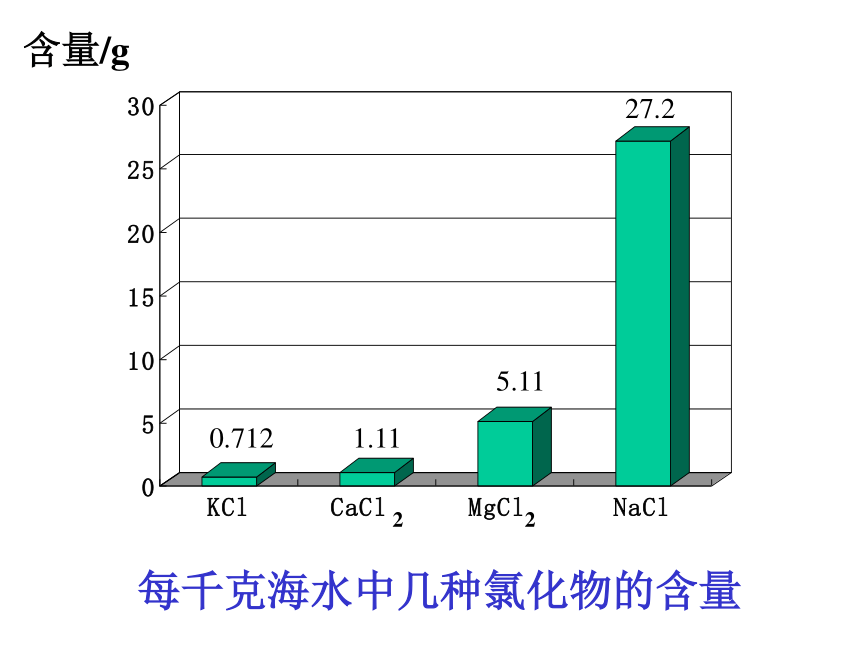
每千克海水中几种氯化物的含量
含量/g
0.712
1.11
5.11
27.2
2
2
2
你知道人们是如何从海水中获得氯化钠并生产氯气的吗?
氯气的生产原理
(一)氯气的工业制法
(二)氯气的实验室制法
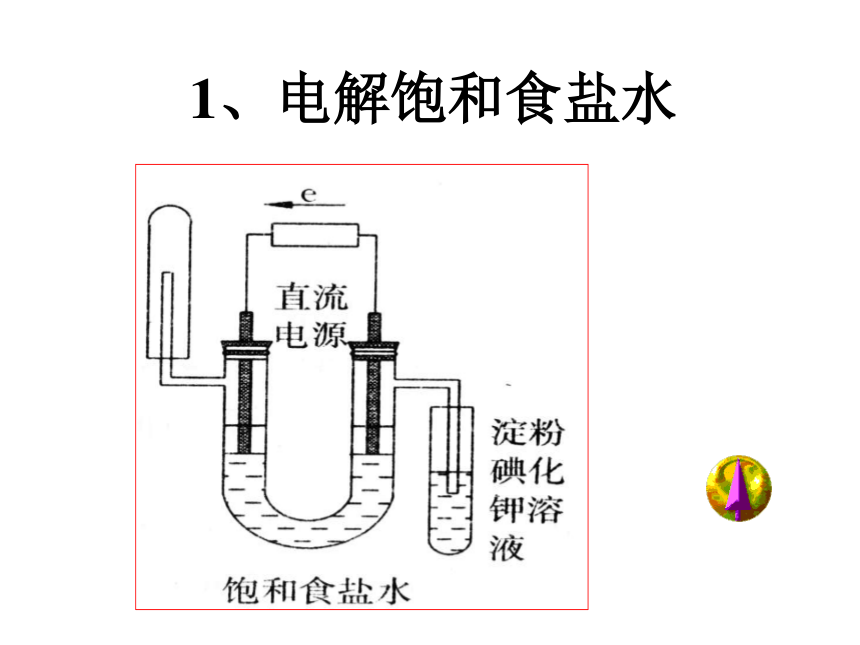
1、电解饱和食盐水
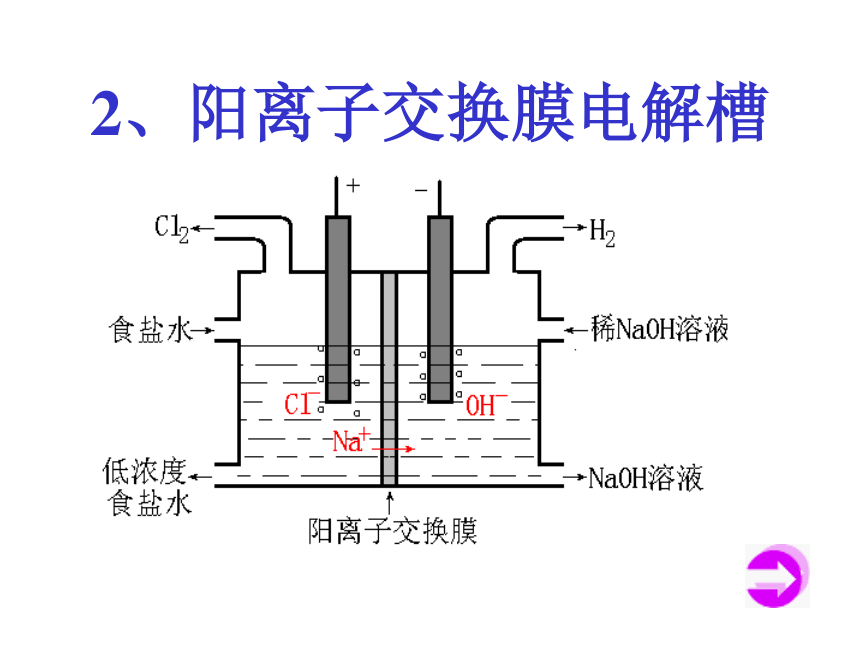
2、阳离子交换膜电解槽
(一)氯气的工业制法
1、电解饱和食盐水
实验现象 结论
1
2
3
4
两极均产生气泡
通电后有新的气体物质生成
将铁棒上方收集到的气体靠近火焰,有轻微的爆鸣声
有氢气生成
黄绿色、刺激性气味的气体产生,湿润的淀粉碘化钾试纸变蓝
有氯气生成
铁棒周围的颜色变红
有碱性物质生成
实验原理:
氯化钠和水发生电解反应,在阳极生成氯气,在阴极生成氢气和氢氧化钠。
电解氯化钠溶液的化学方程式:
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
通电
电极反应式:
阳极:2Cl--2e- = Cl2↑
(氧化反应)
阴极 :2H+ + 2e - = H2↑
(还原反应)
2、阳离子交换膜电解槽
由阳极、阴极、
阳离子交换膜
(或石棉隔膜)、
电解槽框和
导电铜棒等组成
(1)电解槽的组成:
(2)阳离子交换膜的作用 :
①能防止阴极产生的H2和阳极产 生的Cl2相混合而引起爆炸
②能避免Cl2和NaOH溶液作用生成NaClO而影响烧碱的质量
氯 气
化学式:Cl2
1774年,瑞典化学家舍勒发现氯气。
1810年,英国化学家戴维将这种元素命名为Chlorine,这个名称来自希腊文,有“绿色”的意思。我国早年译文将其译成“绿气”,后改为氯气。
戴维
(二)氯气的实验室制法
1、主要仪器:分液漏斗、圆底烧瓶、铁架台、石棉网、酒精灯、集气瓶、烧杯、导管、双孔橡皮塞等
2、实验原理:
3、装置类型
4、净化:
先通过饱和食盐水:除HCl 再通过浓硫酸:除水蒸气
5、收集:
向上排空气法:密度比空气大
排饱和食盐水法:在饱和食盐水中溶解度很小
6、尾气处理:
MnO2 + 4HCl(浓) = MnCl2 + Cl2↑ + 2H2O
2NaOH+Cl2=NaCl+NaClO+H2O
固体(二氧化锰)+液体(浓盐酸)加热制取气体
强调:
MnO2跟浓盐酸在共热的条件下才反应生成Cl2,稀盐酸不与MnO2反应。
由于稀盐酸的还原性比浓盐酸弱,不能被MnO2氧化。
问:1L 4mol/L的浓盐酸与足量的MnO2充分
反应后,被氧化的HCl是多少mol?
A、4mol B、2mol C、大于2mol小于4mol
D、小于2mol
稀盐酸与MnO2不反应,随着反应的进行,
浓盐酸的物质的量浓度逐渐变小。
实验室还可用KMnO4或KClO3代替MnO2与浓盐酸反应制氯气:
2KMnO4+16HCl=2KCl+2MnCl2 +5Cl2 ↑+8H2O
KClO3+6HCl=KCl+3Cl2 ↑ + 3H2O
思考
上述反应的氧化剂、还原剂分别是何物质?电子转移的方向和数目能标出吗?
1、用单双线桥标明电子得失情况
得2e-
失2e-
2e-
MnO2 + 4HCl(浓)== MnCl2 + Cl2 ↑ + 2H2O
△
MnO2 + 4HCl(浓)== MnCl2 + Cl2 ↑ + 2H2O
△
(氧化剂)
(还原剂)
2、在该反应中,氧化剂和还原剂
的物质的量比为 。
1 : 2
烧瓶、分液漏斗、导管、双孔橡皮塞、铁圈、铁夹、铁架台、石棉网、酒精灯
主要仪器
制Cl2
试管、带导管的单孔橡皮塞、酒精灯、铁夹、铁架台
主要仪器
制O2
试管、带导管的单孔橡皮塞、铁夹、铁架台
(或启普发生器)
主要仪器
制H2
项目
装配发生装置的主要仪器
收集气体方法
发生装置类型
Cl2
O2
H2
向上排空集气法(或排饱和食盐水法)
排水法(或向上排空集气法
排水法(或向下排空集气法
固液加热
固液不加热
固固加热
选择气体发生装置的原则是反应物的状态和反应条件
1、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
稀盐酸与MnO2不反应,随着反应的进行,
浓盐酸的物质的量浓度逐渐变小。
2、下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2,请指出装置中的错误。
1、实验室制氯气时,二氧化锰的作用是 ( )
BD
A.催化剂 B.氧化剂
C.还原剂 D.反应物
2、实验室用KMnO4制氧气,为除去粘附在试管壁上的MnO2,可用试剂是( )
A.汽油 B.水
C.稀盐酸 D.浓盐酸
D
3、实验室制氯气时有如下操作,操作顺序正确的是 ( ) ①连接好装置,检查气密性
②缓缓加热,加快反应,使气体均匀逸出
③在烧瓶中加入二氧化锰粉末
④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中
⑤用向上排空气法收集氯气,尾气导入吸收剂中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤
C
4、工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。
Cl2
H2
NaOH
淀粉碘化钾试纸
Cl2
H2
变红
NaOH
0.4g
H2
16g
NaOH
升高
5、某学生设计如下实验装置用于制备纯净的氯气。
(1)装置中有六处错误,请指出。
① ,
② ,
③ ,
④ ,
⑤ ,
⑥ 。
烧瓶下面缺石棉网
铁圈下面缺酒精灯
原料使用了稀盐酸
不应使用长颈漏斗
盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了
洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞
你知道浩瀚的大海中究竟蕴藏着哪些物质吗?请查阅有关资料了解海水中主要含有的物质和各元素的含量。
每千克海水中几种氯化物的含量
含量/g
0.712
1.11
5.11
27.2
2
2
2
你知道人们是如何从海水中获得氯化钠并生产氯气的吗?
氯气的生产原理
(一)氯气的工业制法
(二)氯气的实验室制法
1、电解饱和食盐水
2、阳离子交换膜电解槽
(一)氯气的工业制法
1、电解饱和食盐水
实验现象 结论
1
2
3
4
两极均产生气泡
通电后有新的气体物质生成
将铁棒上方收集到的气体靠近火焰,有轻微的爆鸣声
有氢气生成
黄绿色、刺激性气味的气体产生,湿润的淀粉碘化钾试纸变蓝
有氯气生成
铁棒周围的颜色变红
有碱性物质生成
实验原理:
氯化钠和水发生电解反应,在阳极生成氯气,在阴极生成氢气和氢氧化钠。
电解氯化钠溶液的化学方程式:
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
通电
电极反应式:
阳极:2Cl--2e- = Cl2↑
(氧化反应)
阴极 :2H+ + 2e - = H2↑
(还原反应)
2、阳离子交换膜电解槽
由阳极、阴极、
阳离子交换膜
(或石棉隔膜)、
电解槽框和
导电铜棒等组成
(1)电解槽的组成:
(2)阳离子交换膜的作用 :
①能防止阴极产生的H2和阳极产 生的Cl2相混合而引起爆炸
②能避免Cl2和NaOH溶液作用生成NaClO而影响烧碱的质量
氯 气
化学式:Cl2
1774年,瑞典化学家舍勒发现氯气。
1810年,英国化学家戴维将这种元素命名为Chlorine,这个名称来自希腊文,有“绿色”的意思。我国早年译文将其译成“绿气”,后改为氯气。
戴维
(二)氯气的实验室制法
1、主要仪器:分液漏斗、圆底烧瓶、铁架台、石棉网、酒精灯、集气瓶、烧杯、导管、双孔橡皮塞等
2、实验原理:
3、装置类型
4、净化:
先通过饱和食盐水:除HCl 再通过浓硫酸:除水蒸气
5、收集:
向上排空气法:密度比空气大
排饱和食盐水法:在饱和食盐水中溶解度很小
6、尾气处理:
MnO2 + 4HCl(浓) = MnCl2 + Cl2↑ + 2H2O
2NaOH+Cl2=NaCl+NaClO+H2O
固体(二氧化锰)+液体(浓盐酸)加热制取气体
强调:
MnO2跟浓盐酸在共热的条件下才反应生成Cl2,稀盐酸不与MnO2反应。
由于稀盐酸的还原性比浓盐酸弱,不能被MnO2氧化。
问:1L 4mol/L的浓盐酸与足量的MnO2充分
反应后,被氧化的HCl是多少mol?
A、4mol B、2mol C、大于2mol小于4mol
D、小于2mol
稀盐酸与MnO2不反应,随着反应的进行,
浓盐酸的物质的量浓度逐渐变小。
实验室还可用KMnO4或KClO3代替MnO2与浓盐酸反应制氯气:
2KMnO4+16HCl=2KCl+2MnCl2 +5Cl2 ↑+8H2O
KClO3+6HCl=KCl+3Cl2 ↑ + 3H2O
思考
上述反应的氧化剂、还原剂分别是何物质?电子转移的方向和数目能标出吗?
1、用单双线桥标明电子得失情况
得2e-
失2e-
2e-
MnO2 + 4HCl(浓)== MnCl2 + Cl2 ↑ + 2H2O
△
MnO2 + 4HCl(浓)== MnCl2 + Cl2 ↑ + 2H2O
△
(氧化剂)
(还原剂)
2、在该反应中,氧化剂和还原剂
的物质的量比为 。
1 : 2
烧瓶、分液漏斗、导管、双孔橡皮塞、铁圈、铁夹、铁架台、石棉网、酒精灯
主要仪器
制Cl2
试管、带导管的单孔橡皮塞、酒精灯、铁夹、铁架台
主要仪器
制O2
试管、带导管的单孔橡皮塞、铁夹、铁架台
(或启普发生器)
主要仪器
制H2
项目
装配发生装置的主要仪器
收集气体方法
发生装置类型
Cl2
O2
H2
向上排空集气法(或排饱和食盐水法)
排水法(或向上排空集气法
排水法(或向下排空集气法
固液加热
固液不加热
固固加热
选择气体发生装置的原则是反应物的状态和反应条件
1、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
稀盐酸与MnO2不反应,随着反应的进行,
浓盐酸的物质的量浓度逐渐变小。
2、下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2,请指出装置中的错误。
1、实验室制氯气时,二氧化锰的作用是 ( )
BD
A.催化剂 B.氧化剂
C.还原剂 D.反应物
2、实验室用KMnO4制氧气,为除去粘附在试管壁上的MnO2,可用试剂是( )
A.汽油 B.水
C.稀盐酸 D.浓盐酸
D
3、实验室制氯气时有如下操作,操作顺序正确的是 ( ) ①连接好装置,检查气密性
②缓缓加热,加快反应,使气体均匀逸出
③在烧瓶中加入二氧化锰粉末
④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中
⑤用向上排空气法收集氯气,尾气导入吸收剂中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤
C
4、工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。
Cl2
H2
NaOH
淀粉碘化钾试纸
Cl2
H2
变红
NaOH
0.4g
H2
16g
NaOH
升高
5、某学生设计如下实验装置用于制备纯净的氯气。
(1)装置中有六处错误,请指出。
① ,
② ,
③ ,
④ ,
⑤ ,
⑥ 。
烧瓶下面缺石棉网
铁圈下面缺酒精灯
原料使用了稀盐酸
不应使用长颈漏斗
盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了
洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞
