第一节 物质的分类 第1课时 简单分类法及其应用(共34张PPT)
文档属性
| 名称 | 第一节 物质的分类 第1课时 简单分类法及其应用(共34张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-10-21 17:59:54 | ||
图片预览








文档简介
(共36张PPT)
第一节 物质的分类
第1课时 简单分类法及其应用
生活中有哪些用到了分类法的例子?
书
店
图书馆
超市
资料分享
据统计,目前人类发现和合成的化学物质已超过3000万种,人类社会是在化学发展的基础上构筑起现代物质文明的。
那么对于数以千万计的化学物质和化学反应,我们是怎样认识的呢?是不是对每一种物质都详细地研究呢?
用分类法研究化学物质,可以使化学知识系统化、条
理化,还可以通过分门别类的研究,发现物质及其变
化的规律。
分类的定义
把大量事物按照事先设定的标准进行归类分组
的一种方法。
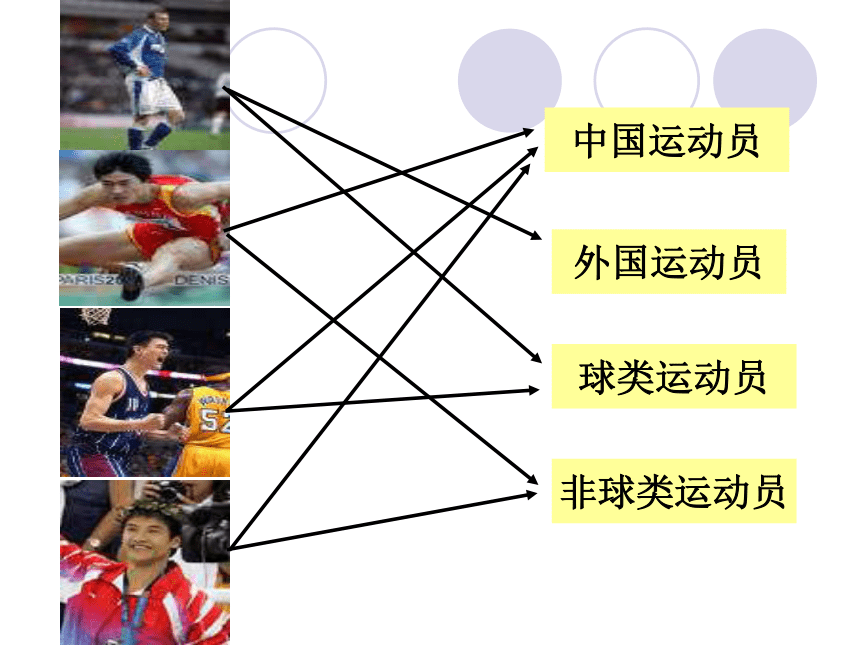
田亮
刘翔
姚明
罗纳尔多
中国运动员
外国运动员
球类运动员
非球类运动员
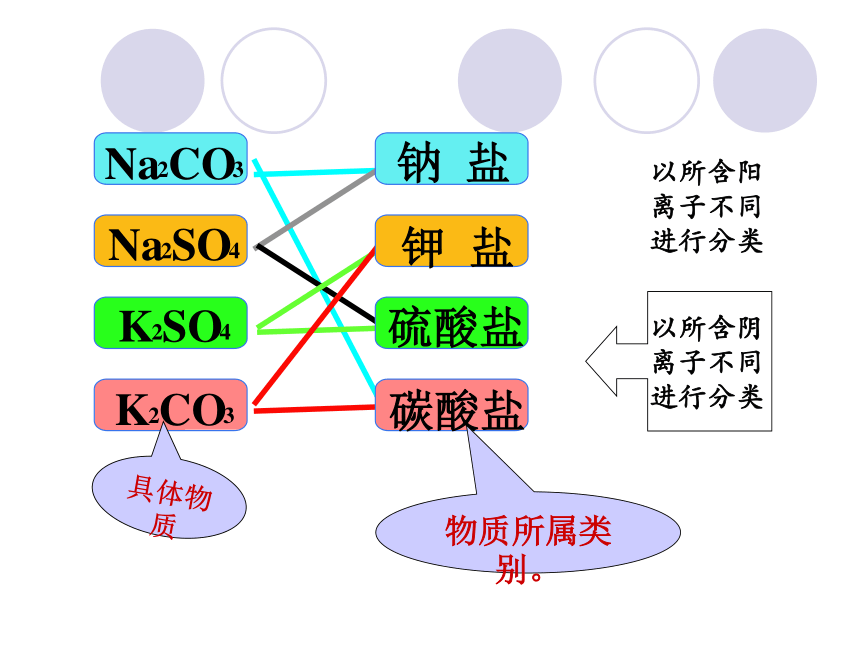
以所含阳离子不同进行分类
以所含阴离子不同进行分类
Na
2
CO
3
K
2
CO
3
K
2
SO
4
Na
2
SO
4
钠 盐
钾 盐
硫酸盐
碳酸盐
具体物质
物质所属类别。
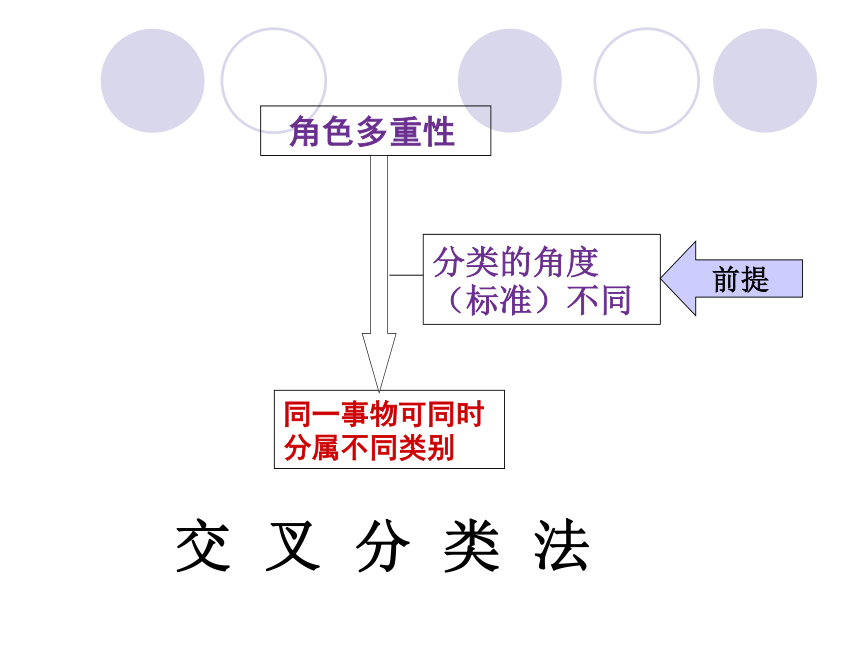
角色多重性
前提
同一事物可同时分属不同类别
分类的角度(标准)不同
交 叉 分 类 法
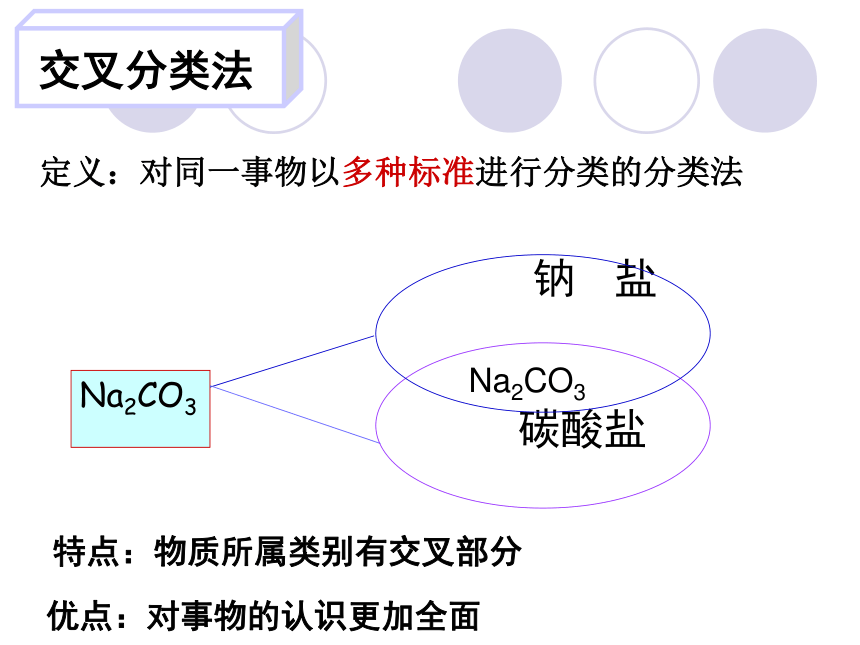
定义:对同一事物以多种标准进行分类的分类法
优点:对事物的认识更加全面
交叉分类法
钠 盐
碳酸盐
Na2CO3
Na2CO3
特点:物质所属类别有交叉部分
Na2CO3
K2SO4
钠 盐
钾 盐
这是交叉分类么 为什么
伪交叉
含氧酸
无氧酸
一元酸
二元酸
用交叉分类法对下列物质进行分类
H2SO4
HCl
HNO3
H2CO3
课堂练习
物
质
混
合
物
纯
净
物
化
合
物
单
质
碱
酸
氧化物
盐
物质的分类
知识回顾
由一种元素组成的纯净物
由几种元素组成的纯净物
金属单质
非金属单质
由非金属元素构成的单质
由金属元素构成的单质
由金属离子或NH4+的化合物与酸根离子或非金属离子组成
在水溶液中电离出的阴离子全部是OH-的化合物
在水溶液中电离出的阳离子全部是H+的化合物
氧元素和另一种元素所组成的化合物
树状分类法
对于同类事物,为了做进一步的研究,有时我们对它作多层次的分类。
树状分类法的分类原则:同一层次的物质类别间一般是相互独立,没有交叉的。
树状分类法
优点:能清楚地看到事物种类的从属关系。
定义:对同类事物按照某种属性进行 再分类的分类法
没有绝对严密的分类,人们对于物质的认识本来就是不断更新的,我们往往选择一种有利于我们研究物质的方法来分,分类不是目的,而是归类系统研究物质的一种科学方法,分类是为了更系统的研究物质,对其加深了解。
化合物
无机化合物
有机化合物
一般指组成里含C的化合物,碳的氧化物、碳酸(氢)盐、金属碳化物除外
一般指组成里不含C的化合物,碳的氧化物、碳酸(氢)盐、金属碳化物除外
物
质
混
合
物
纯
净
物
化
合
物
单
质
金属单质
非金属单质
碱
酸
氧化物
盐
物质的分类
对这个分类结果,还可以做进一步分类吗?
?
?
氧化物
酸性氧化物
碱性氧化物
不成盐氧化物
CuO、Fe2O3、Na2O等
CO、P2O5、H2O等
CO2、P2O5、SO3等
CaO、CuO、K2O等
CO、NO等
从组成元素分
非金属氧化物
金属氧化物
从性质分
氧化物的分类
成盐氧化物
能跟酸或碱反应生成盐和水的氧化物
不能跟酸或碱反应生成盐和水的氧化物
能跟碱反应生成盐和水的氧化物
两性氧化物
Al2O3等
能跟酸反应生成盐和水的氧化物
酸的分类
碱
从是否溶于水分
从碱性强弱分
难溶碱
弱碱
可溶碱
强碱
NaOH、KOH、Ca(OH) 2、Ba(OH)2、NH3·H2O等
NaOH、KOH、Ca(OH) 2、Ba(OH)2等
Cu(OH)2、Mg(OH)2、Fe(OH) 3等
NH3·H2O 、Cu(OH)2、Mg(OH)2、Fe(OH) 3等
电离产生的OH-数
碱的分类
一元碱
二 元碱
多元碱
NaOH、KOH等
Ca(OH) 2、Ba(OH)2等
Fe(OH) 3等
盐
从是否溶于水分
按组成离子分
无氧酸盐
正盐
酸式盐
碱式盐
NaCl、AgNO3、CuSO4等
NaHSO4、KHSO4等
Cu2(OH)2CO3等
按酸根是否含氧分
含氧酸盐
可溶盐
难溶盐
NaCl、AgNO3、CuSO4等
CaCO3、BaSO4、ZnS等
KNO3、KMnO4、FeSO4等
NaCl、ZnS、CaCl2等
盐的分类
……
电离时产生的阳离子全为金属离子或NH4+,阴离子全部为酸根离子的盐
电离时产生的阴离子除酸根离子外还有OH-,阳离子全为金属离子或NH4+。
电离时产生的阳离子除金属离子或NH4+外还有H+,阴离子全部为酸根离子的盐
用树状分类法对 HCl,CO2 , CaO ,NaOH,
Na2SO4 , CaCO3 , Ca(OH)2 ,H2SO4进行分类
化合物
酸
碱
盐
氧化物
HCl H2SO4
NaOH Ca(OH)2
Na2SO4 CaCO3
CO2 CaO
思考与交流
1.用化学方程式表示下列转化关系。
实践活动
分类法的应用及其意义
2.通过以上活动,你发现了什么规律?请尝试用
图表示出单质、碱性氧化物、酸性氧化物、酸、
碱、盐之间的转化关系。
金属单质 碱性氧化物 碱 盐
非金属单质 酸性氧化物 酸 盐
物质转化规律
+ O2
+ O2
+ H2O
+ H2O
盐
盐
+ H2O
总结:规律1——不同类物质可以相互转化。
规律2——同类物质具有相似性质(通性)。
一、简单分类法及其应用
1.交叉分类法:
2.树状分类法:
3.分类法的应用及意义
举一反三 由此及彼
知识小结
对同类事物作多层次的分类
对一种事物以多种标准进行分类
对于工作和生活而言,则提供便利,实现高效;
对于化学研究而言,便于了解各类物质的共性和各类反应的本质 。
1.下列反应方程式中有一个与其他三个在分类上不同,这个反应方程式是( )
A.3Fe+2O2=Fe3O4
B.CO2+C=2CO
C.NH4HS=NH3+H2S
D.Na2CO3+CO2+H2O=2NaHCO3
课堂练习
C
2.下列有五组物质,每组中有一种物质从某种角度分析与其它三种不同。请找出该物质,并说明理由。
⑴Fe、S、C、P
⑵H2、O2、N2、S
⑶Fe2O3、NaCl、CuO、H2O
⑷AgCl、BaSO4、KNO3、CaCO3 ⑸CuSO4、FeCl3、KMnO4、K2CO3
Fe
S
NaCl
KNO3
K2CO3
课堂练习
3.下列各组物质中按单质、化合物、混合物顺序排列的是( )
A.氧气 碱式碳酸铜 空气
B.胆矾 矿泉水 氖气
C.水银 水煤气 冰水混合物
D. 稀硫酸 火碱 金刚石
课堂练习
A
4.某种物质经检测,只含有一种元素,则该物质( )
A. 一定是纯净物
B.一定是单质
C.一定不是化合物
D.一定是混合物
C
5.已知“o”、“●”表示质子数不同的原子.下图中表示的气体物质中,属于化合物的是( )
A.
B.
C.
D.
B
6.下列各组物质中,从物质分类的角度看,后者从属于前者的是( )
A.纯净物、混合物
B.金属、非金属
C.纯净物、化合物
D.含氧酸、无氧酸
C
7.现有Ba、H、C、O四种元素.请你从中选择适当的元素组成符合下列要求的化合物(填化学式)
(1)氧化物
(2)碱
(3)酸
(4)盐
CO2;BaO;H2O;H2O2;CO
Ba(OH)2
H2CO3
BaCO3
第一节 物质的分类
第1课时 简单分类法及其应用
生活中有哪些用到了分类法的例子?
书
店
图书馆
超市
资料分享
据统计,目前人类发现和合成的化学物质已超过3000万种,人类社会是在化学发展的基础上构筑起现代物质文明的。
那么对于数以千万计的化学物质和化学反应,我们是怎样认识的呢?是不是对每一种物质都详细地研究呢?
用分类法研究化学物质,可以使化学知识系统化、条
理化,还可以通过分门别类的研究,发现物质及其变
化的规律。
分类的定义
把大量事物按照事先设定的标准进行归类分组
的一种方法。
田亮
刘翔
姚明
罗纳尔多
中国运动员
外国运动员
球类运动员
非球类运动员
以所含阳离子不同进行分类
以所含阴离子不同进行分类
Na
2
CO
3
K
2
CO
3
K
2
SO
4
Na
2
SO
4
钠 盐
钾 盐
硫酸盐
碳酸盐
具体物质
物质所属类别。
角色多重性
前提
同一事物可同时分属不同类别
分类的角度(标准)不同
交 叉 分 类 法
定义:对同一事物以多种标准进行分类的分类法
优点:对事物的认识更加全面
交叉分类法
钠 盐
碳酸盐
Na2CO3
Na2CO3
特点:物质所属类别有交叉部分
Na2CO3
K2SO4
钠 盐
钾 盐
这是交叉分类么 为什么
伪交叉
含氧酸
无氧酸
一元酸
二元酸
用交叉分类法对下列物质进行分类
H2SO4
HCl
HNO3
H2CO3
课堂练习
物
质
混
合
物
纯
净
物
化
合
物
单
质
碱
酸
氧化物
盐
物质的分类
知识回顾
由一种元素组成的纯净物
由几种元素组成的纯净物
金属单质
非金属单质
由非金属元素构成的单质
由金属元素构成的单质
由金属离子或NH4+的化合物与酸根离子或非金属离子组成
在水溶液中电离出的阴离子全部是OH-的化合物
在水溶液中电离出的阳离子全部是H+的化合物
氧元素和另一种元素所组成的化合物
树状分类法
对于同类事物,为了做进一步的研究,有时我们对它作多层次的分类。
树状分类法的分类原则:同一层次的物质类别间一般是相互独立,没有交叉的。
树状分类法
优点:能清楚地看到事物种类的从属关系。
定义:对同类事物按照某种属性进行 再分类的分类法
没有绝对严密的分类,人们对于物质的认识本来就是不断更新的,我们往往选择一种有利于我们研究物质的方法来分,分类不是目的,而是归类系统研究物质的一种科学方法,分类是为了更系统的研究物质,对其加深了解。
化合物
无机化合物
有机化合物
一般指组成里含C的化合物,碳的氧化物、碳酸(氢)盐、金属碳化物除外
一般指组成里不含C的化合物,碳的氧化物、碳酸(氢)盐、金属碳化物除外
物
质
混
合
物
纯
净
物
化
合
物
单
质
金属单质
非金属单质
碱
酸
氧化物
盐
物质的分类
对这个分类结果,还可以做进一步分类吗?
?
?
氧化物
酸性氧化物
碱性氧化物
不成盐氧化物
CuO、Fe2O3、Na2O等
CO、P2O5、H2O等
CO2、P2O5、SO3等
CaO、CuO、K2O等
CO、NO等
从组成元素分
非金属氧化物
金属氧化物
从性质分
氧化物的分类
成盐氧化物
能跟酸或碱反应生成盐和水的氧化物
不能跟酸或碱反应生成盐和水的氧化物
能跟碱反应生成盐和水的氧化物
两性氧化物
Al2O3等
能跟酸反应生成盐和水的氧化物
酸的分类
碱
从是否溶于水分
从碱性强弱分
难溶碱
弱碱
可溶碱
强碱
NaOH、KOH、Ca(OH) 2、Ba(OH)2、NH3·H2O等
NaOH、KOH、Ca(OH) 2、Ba(OH)2等
Cu(OH)2、Mg(OH)2、Fe(OH) 3等
NH3·H2O 、Cu(OH)2、Mg(OH)2、Fe(OH) 3等
电离产生的OH-数
碱的分类
一元碱
二 元碱
多元碱
NaOH、KOH等
Ca(OH) 2、Ba(OH)2等
Fe(OH) 3等
盐
从是否溶于水分
按组成离子分
无氧酸盐
正盐
酸式盐
碱式盐
NaCl、AgNO3、CuSO4等
NaHSO4、KHSO4等
Cu2(OH)2CO3等
按酸根是否含氧分
含氧酸盐
可溶盐
难溶盐
NaCl、AgNO3、CuSO4等
CaCO3、BaSO4、ZnS等
KNO3、KMnO4、FeSO4等
NaCl、ZnS、CaCl2等
盐的分类
……
电离时产生的阳离子全为金属离子或NH4+,阴离子全部为酸根离子的盐
电离时产生的阴离子除酸根离子外还有OH-,阳离子全为金属离子或NH4+。
电离时产生的阳离子除金属离子或NH4+外还有H+,阴离子全部为酸根离子的盐
用树状分类法对 HCl,CO2 , CaO ,NaOH,
Na2SO4 , CaCO3 , Ca(OH)2 ,H2SO4进行分类
化合物
酸
碱
盐
氧化物
HCl H2SO4
NaOH Ca(OH)2
Na2SO4 CaCO3
CO2 CaO
思考与交流
1.用化学方程式表示下列转化关系。
实践活动
分类法的应用及其意义
2.通过以上活动,你发现了什么规律?请尝试用
图表示出单质、碱性氧化物、酸性氧化物、酸、
碱、盐之间的转化关系。
金属单质 碱性氧化物 碱 盐
非金属单质 酸性氧化物 酸 盐
物质转化规律
+ O2
+ O2
+ H2O
+ H2O
盐
盐
+ H2O
总结:规律1——不同类物质可以相互转化。
规律2——同类物质具有相似性质(通性)。
一、简单分类法及其应用
1.交叉分类法:
2.树状分类法:
3.分类法的应用及意义
举一反三 由此及彼
知识小结
对同类事物作多层次的分类
对一种事物以多种标准进行分类
对于工作和生活而言,则提供便利,实现高效;
对于化学研究而言,便于了解各类物质的共性和各类反应的本质 。
1.下列反应方程式中有一个与其他三个在分类上不同,这个反应方程式是( )
A.3Fe+2O2=Fe3O4
B.CO2+C=2CO
C.NH4HS=NH3+H2S
D.Na2CO3+CO2+H2O=2NaHCO3
课堂练习
C
2.下列有五组物质,每组中有一种物质从某种角度分析与其它三种不同。请找出该物质,并说明理由。
⑴Fe、S、C、P
⑵H2、O2、N2、S
⑶Fe2O3、NaCl、CuO、H2O
⑷AgCl、BaSO4、KNO3、CaCO3 ⑸CuSO4、FeCl3、KMnO4、K2CO3
Fe
S
NaCl
KNO3
K2CO3
课堂练习
3.下列各组物质中按单质、化合物、混合物顺序排列的是( )
A.氧气 碱式碳酸铜 空气
B.胆矾 矿泉水 氖气
C.水银 水煤气 冰水混合物
D. 稀硫酸 火碱 金刚石
课堂练习
A
4.某种物质经检测,只含有一种元素,则该物质( )
A. 一定是纯净物
B.一定是单质
C.一定不是化合物
D.一定是混合物
C
5.已知“o”、“●”表示质子数不同的原子.下图中表示的气体物质中,属于化合物的是( )
A.
B.
C.
D.
B
6.下列各组物质中,从物质分类的角度看,后者从属于前者的是( )
A.纯净物、混合物
B.金属、非金属
C.纯净物、化合物
D.含氧酸、无氧酸
C
7.现有Ba、H、C、O四种元素.请你从中选择适当的元素组成符合下列要求的化合物(填化学式)
(1)氧化物
(2)碱
(3)酸
(4)盐
CO2;BaO;H2O;H2O2;CO
Ba(OH)2
H2CO3
BaCO3
