2021-2022学年山东省东营市利津县九年级(上)期中化学试卷(五四学制)(word版含解析)
文档属性
| 名称 | 2021-2022学年山东省东营市利津县九年级(上)期中化学试卷(五四学制)(word版含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 327.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-15 00:00:00 | ||
图片预览



文档简介
2021-2022学年山东省东营市利津县九年级(上)期中化学试卷(五四学制)
一、选择题(每小题只有一个正确答案,每小题4分,共48分)
1.(4分)下列有关溶液的说法错误的是( )
A.溶液是均一、稳定的混合物
B.溶液中的溶质可以是固体、液体或气体
C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
D.洗涤剂能洗去衣服上的油污,原因是洗涤剂具有乳化作用
2.(4分)对于30%的KNO3溶液,下列说法正确的是( )
A.溶液中溶质和溶剂的质量比为3:10
B.每100g水中溶解30g KNO3
C.某种条件下,可转化为悬浊液
D.若再加30g硝酸钾,则变为60% KNO3溶液
3.(4分)在化学实验操作考查中,小阳同学抽到的考题是“配制50g质量分数为6%的氯化钠溶液”,小阳的实验操作与目的分析均正确的一组是( )
选项 实验操作 目的分析
A 称取氯化钠时,指针向右偏,调节游码至天平平衡 准确称量氯化钠质量
B 称取氯化钠时,将剩余的氯化钠放回原瓶 节约药品
C 量取水时,视线与量筒内凹液面最低处保持水平 准确读数
D 溶解氯化钠时,用玻璃棒搅拌 增大氯化钠的溶解度
A.A B.B C.C D.D
4.(4分)稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )
A.稀释浓硫酸 B.测稀硫酸的pH
C.倾倒稀硫酸 D.滴加稀硫酸
5.(4分)某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )
A.用干燥的pH试纸测定白醋的pH
B.用干燥的pH试纸测定二氧化碳气体的pH
C.用干燥的pH试纸测定98%的浓硫酸的pH
D.用湿润的pH试纸测定0.4%的氢氧化钠溶液的pH
6.(4分)小明同学在复习阶段在笔记本上对化学知识进行了归纳整理,其中正确的个数是( )
①用广泛pH试纸测得某地下水的pH为5.2
②碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
③配制6%的氯化钠溶液,量取水时,仰视量筒刻度使所配氯化钠溶液的质量分数偏低
④氢氧化铝能治疗胃酸过多,所以氢氧化钠也可以治疗胃酸过多
⑤能使无色酚酞溶液变红的一定是碱性溶液
⑥生成盐和水的反应一定是中和反应
⑦常温下,pH<7的溶液显酸性,因此pH<7的雨水一定都是酸雨
⑧浓盐酸和浓硫酸敞口放置一段时间,溶质质量分数都减小
A.2个 B.3个 C.4个 D.5个
7.(4分)按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物一酸一碱一盐”排列顺序的是( )
A.HCl、Mg(OH)2、MgCl2、CO2
B.CO2、H2CO3、CaCO3、KOH
C.H2O、HNO3、NH3 H2O、Na2CO3
D.SO3、NaOH、Na2SO4、H2SO4
8.(4分)可燃冰被科学家誉为“未来能源”、“21世纪能源”。“可燃冰”是一种天然气水合物,其中的主要化学成分是一种可燃气体——甲烷,所以它又被称为甲烷水合物。它的形成至少要满足三个条件,如果温度高于20℃,它就会受热分解从而“烟消云散”,“可燃冰”在0℃时,只需30个标准大气压即可生成,“可燃冰”就越不容易分解;最后,为“可燃冰”的形成提供了充足的原料。下列说法与文意相符的是( )
A.“可燃冰”容易保存
B.海底甲烷气体主要来自生物残体和有机腐殖质
C.“可燃冰”其实就是一种气体
D.在0℃且200米的海底可能会有“可燃冰”
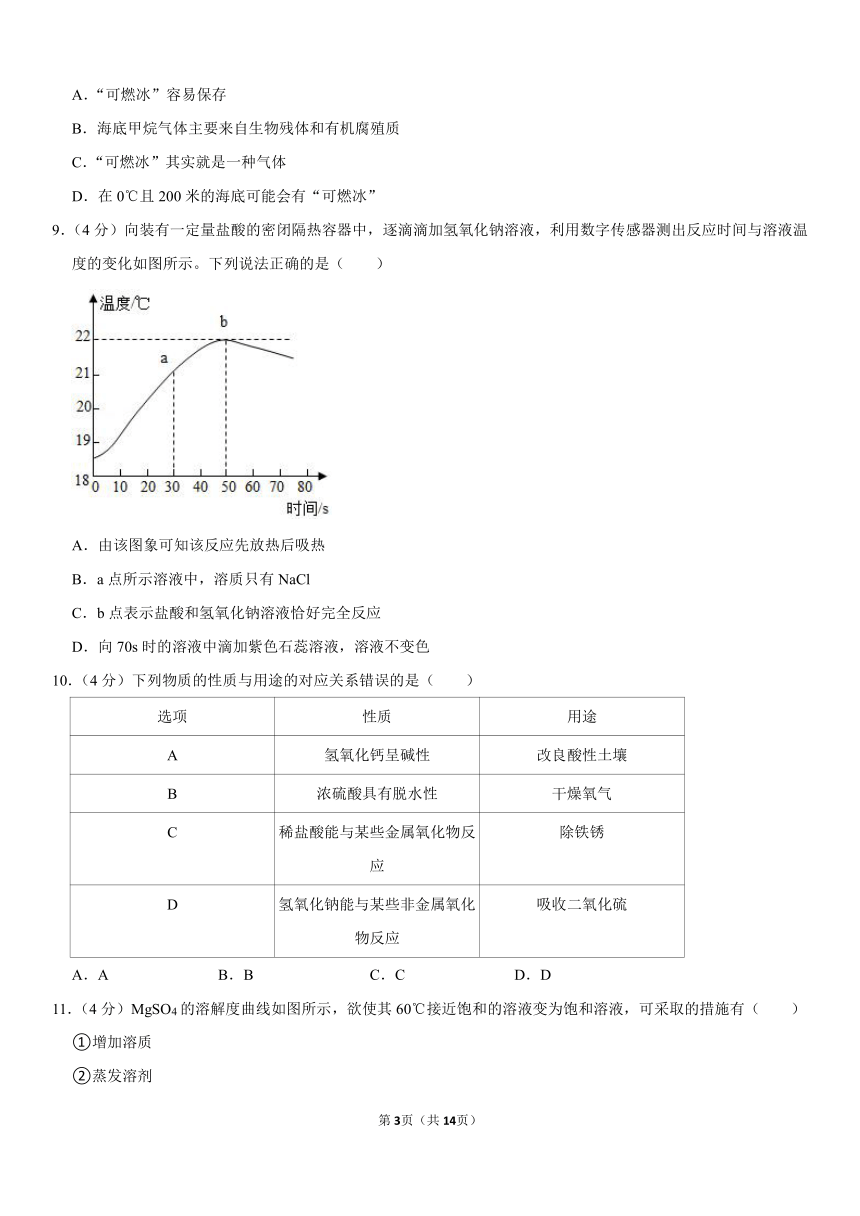
9.(4分)向装有一定量盐酸的密闭隔热容器中,逐滴滴加氢氧化钠溶液,利用数字传感器测出反应时间与溶液温度的变化如图所示。下列说法正确的是( )
A.由该图象可知该反应先放热后吸热
B.a点所示溶液中,溶质只有NaCl
C.b点表示盐酸和氢氧化钠溶液恰好完全反应
D.向70s时的溶液中滴加紫色石蕊溶液,溶液不变色
10.(4分)下列物质的性质与用途的对应关系错误的是( )
选项 性质 用途
A 氢氧化钙呈碱性 改良酸性土壤
B 浓硫酸具有脱水性 干燥氧气
C 稀盐酸能与某些金属氧化物反应 除铁锈
D 氢氧化钠能与某些非金属氧化物反应 吸收二氧化硫
A.A B.B C.C D.D
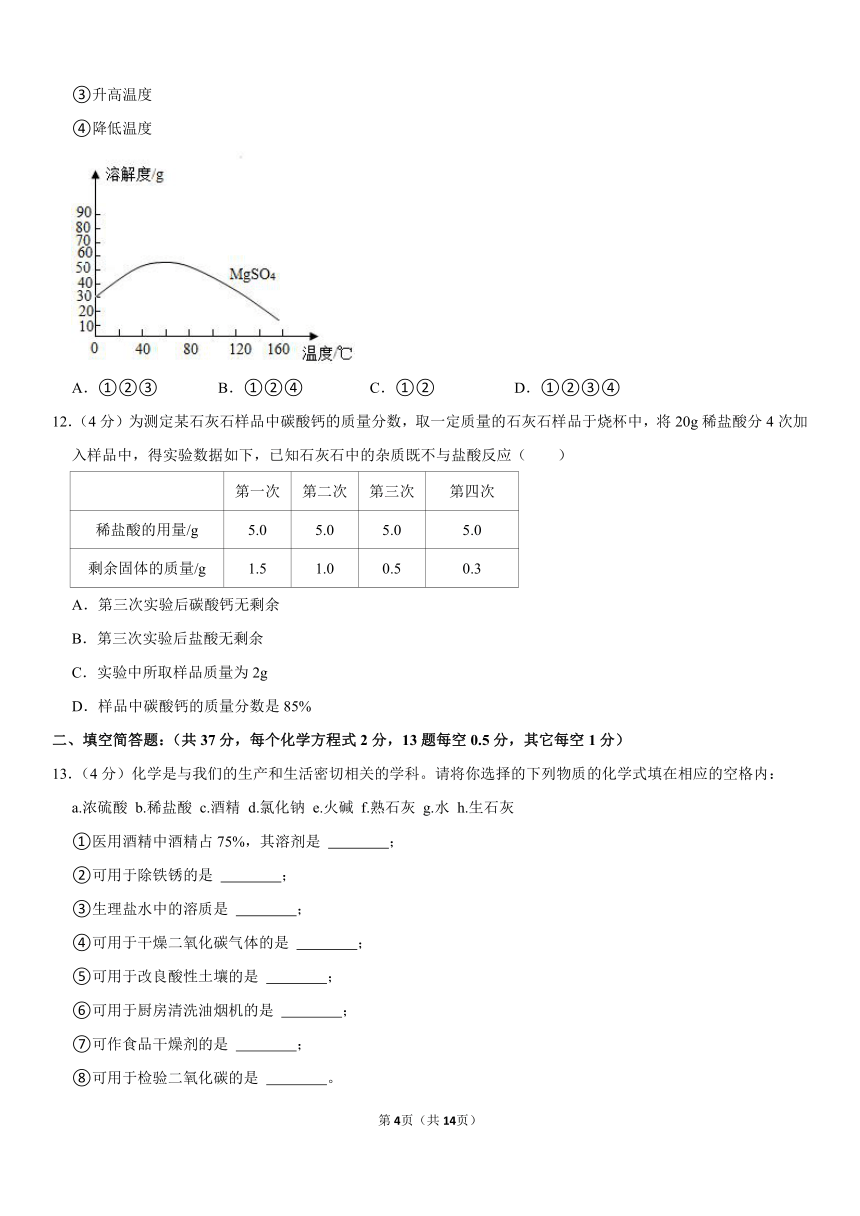
11.(4分)MgSO4的溶解度曲线如图所示,欲使其60℃接近饱和的溶液变为饱和溶液,可采取的措施有( )
①增加溶质
②蒸发溶剂
③升高温度
④降低温度
A.①②③ B.①②④ C.①② D.①②③④
12.(4分)为测定某石灰石样品中碳酸钙的质量分数,取一定质量的石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,得实验数据如下,已知石灰石中的杂质既不与盐酸反应( )
第一次 第二次 第三次 第四次
稀盐酸的用量/g 5.0 5.0 5.0 5.0
剩余固体的质量/g 1.5 1.0 0.5 0.3
A.第三次实验后碳酸钙无剩余
B.第三次实验后盐酸无剩余
C.实验中所取样品质量为2g
D.样品中碳酸钙的质量分数是85%
二、填空简答题:(共37分,每个化学方程式2分,13题每空0.5分,其它每空1分)
13.(4分)化学是与我们的生产和生活密切相关的学科。请将你选择的下列物质的化学式填在相应的空格内:
a.浓硫酸 b.稀盐酸 c.酒精 d.氯化钠 e.火碱 f.熟石灰 g.水 h.生石灰
①医用酒精中酒精占75%,其溶剂是 ;
②可用于除铁锈的是 ;
③生理盐水中的溶质是 ;
④可用于干燥二氧化碳气体的是 ;
⑤可用于改良酸性土壤的是 ;
⑥可用于厨房清洗油烟机的是 ;
⑦可作食品干燥剂的是 ;
⑧可用于检验二氧化碳的是 。
14.(8分)如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线图。请根据图示回答下列问题:
(1)t℃时,溶解度由大到小是 。
(2)P点表示 。
(3)欲将c物质的饱和溶液变为不饱和溶液,可采用的方法是 (填“降低”或“升高”)温度。
(4)20℃时,向30g物质a中加入50g水,充分溶解并恢复到原温度 g。
(5)当b中混有少量a时,可用 的方法提纯b。
(6)20℃时,用a、b、c三种固体配制等质量的饱和溶液,所需水的质量由大到小的顺序是 。
(7)将t℃的a、b、c三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数大小关系由大到小为 。
(8)下列说法正确的是 。
A.P点可以表示在20℃时,a、c溶液的质量分数相等
B.P点可以表示20℃时b的不饱和溶液
C.c物质有可能是气体
D.将t℃时a、b的饱和溶液同时降温到20℃,析出晶体的质量是a>b
15.(10分)“魔法世界,魅力化学”。在元旦的新年晚会上,同学们表演了多个魔术节目,请尝试对以下魔术进行揭秘。
(1)小明表演了一个小魔术:“矿泉水”变成“牛奶”、“雪碧”和“红酒”。
①“矿泉水”实际是石灰水,加入液体A后出现白色浑浊,形似牛奶 。
②“牛奶”中加入B,有大量气泡产生,变成雪碧 。
③C是一种紫色的溶液,滴入“雪碧”中变为红色,则雪碧的组成显 性(酸或碱)。
(2)化学反应是一个变色的世界。图中B是铁锈的主要成分,B、C、D分属于不同类别的物质,蓝色溶液可用于配制农药波尔多液。
请回答:
①溶液X是 (填“酸”“碱”、“盐”)。
②写出物质B与无色溶液X反应的化学方程式: 。
③物质C的名称是 ,写出该反应的化学方程式 。
16.(7分)某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验。
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)写出实验中无明显现象产生的试管中发生的化学方程式 。
(3)实验后某试管中为红色溶液,当向其中加入过量的 后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是 。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出 。
17.(8分)镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。如图是工业上提镁的流程,海水中镁元素的主要存在形式是MgCl2和MgSO4。
(1)有项目研究团队研究问题:在海水提镁的过程中如何实现对镁元素的富集?团队成员提出观点如下。
观点A:直接往海水中加入沉淀剂。
观点B:高温加热蒸发海水后,再加入沉淀剂。
观点C:向晒盐后的苦卤水中加入沉淀剂。
通过分析比较,你认为观点 (填“A”、“B”或“C”)最合理,简述理由: 。
(2)①“反应池”→…→“中和”过程的主要作用为:使MgCl2转化为Mg(OH)2沉淀;Mg(OH)2再与盐酸反应转化为MgCl2,目的是 。
②反应池中,石灰乳应过量的目的是 。
③“中和”时,Mg(OH)2与盐酸发生反应的化学方程式是 。
(3)在上述流程中,可循环使用的物质是 。
(4)上述流程中涉及的主要反应类型属于分解反应的是 (填字母)。
A.煅烧贝壳(CaCO3)制取生石灰
B.电解熔融MgCl2制镁和Cl2
C.Cl2和H2反应生产氯化氢
D.用生石灰生产石灰乳
三、计算题(18题5分,19题10分)
18.(5分)某市售过氧乙酸(化学式:C2H4O3),其标签上的部分文字说明如图。请回答:
(1)一瓶这种溶液中含过氧乙酸溶质质量为 。
(2)0.5%的过氧乙酸溶液可以杀死细菌和新冠病毒。某医院需配制0.5%的过氧乙酸2kg,需要这种过氧乙酸的质量为多少?(请写出计算过程)
19.(10分)某品牌炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学测定该炉具清洁剂中氢氧化钠的含量。取100g炉具清洁剂倒入烧杯中,逐次加入质量分数为9.8%的稀硫酸
(1)当pH=13时,溶液中所含的溶质是 (填化学式)。
(2)当恰好中和时,消耗的稀硫酸的质量为 。
(3)计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。
2021-2022学年山东省东营市利津县九年级(上)期中化学试卷(五四学制)
参考答案与试题解析
一、选择题(每小题只有一个正确答案,每小题4分,共48分)
1.【解答】解:A、一种或几种物质分散到另一种物质中、稳定的混合物叫做溶液、稳定的混合物。
B、溶液中的溶质可以是固体,故选项说法正确。
C、溶液是否饱和与溶液的浓稀没有必然联系,不饱和溶液不一定是稀溶液。
D、洗涤剂能洗去衣服上的油污,能将大的油滴分散成细小的油滴。
故选:C。
2.【解答】解:A、30%的KNO3溶液是指每100g溶液中溶解30gKNO3,则溶液中溶质和溶剂的质量比为6:7,故A错误;
B、30%的KNO3溶液是指每100g溶液(而不是水)中溶解30gKNO6,故B错误;
C、若对该溶液进行降温或恒温蒸发溶剂或继续加入硝酸钾,从而形成悬浊液;
D、原溶液质量未知,故D错误。
故选:C。
3.【解答】解:A、指针向右偏转,应进行的操作是继续向左盘添加药品,故选项说法错误。
B、称取氯化钠时,以防止污染试剂,故选项说法错误。
C、量取水时,是为了准确读数。
D、溶解度是在一定温度下;溶解氯化钠时,不能增大一定温度下氯化钠在100g溶剂里达到饱和状态所溶解的溶质质量,故选项说法错误。
故选:C。
4.【解答】解:A、稀释浓硫酸时,同时用玻璃棒不断搅拌;一定不能把水注入浓硫酸中。
B、用pH试纸测定溶液的pH时,把试纸显示的颜色与标准比色卡对比来确定pH,稀硫酸显酸性,使溶液的酸性减弱;不能将pH试纸伸入待测液中,图中所示操作错误。
C、向试管中倾倒液体药品时,标签要对准手心;图中瓶口没有紧挨试管口,所示操作错误。
D、使用胶头滴管滴加少量液体的操作,应垂直悬空在试管口上方滴加液体,图中所示操作正确。
故选:D。
5.【解答】解:A、应用干燥的pH试纸测定白醋的pH。
B、用pH试纸测定溶液的pH时,用玻璃棒蘸取待测液滴到pH试纸上,读出pH,故选项说法错误。
C、浓硫酸具有脱水性,故选项说法错误。
D、用pH试纸测定溶液的pH时,把试纸显示的颜色与标准比色卡对比来确定pH,氢氧化钠溶液显碱性,使溶液的碱性减弱,故选项说法错误。
故选:A。
6.【解答】解:①用广泛pH试纸只能测得整数pH值,错误;
②碳酸盐与盐酸反应放出气体,与盐酸反应放出气体的物质不一定是碳酸盐,错误;
③配制6%的氯化钠溶液,量取水时,水体积偏大,正确;
④氢氧化铝能治疗胃酸过多,但氢氧化钠具有强烈腐蚀性不可以治疗胃酸过多
⑤能使无色酚酞溶液变红的一定是碱性溶液,正确;
⑥生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钙生成碳酸钙沉淀和水不是中和反应;
⑦常温下,pH<7的的溶液显酸性,错误;
⑧浓盐酸挥发出氯化氢气体,浓硫酸吸收空气中的水,溶质质量分数都减小;
故选:B。
7.【解答】解:A、HCl不属于氧化物,氯化镁不是酸,故A不符合;
B、碳酸钙不是碱,故B不符合;
C、水属于氧化物;氨水属于碱,故C符合;
D、氢氧化钠不属于酸;硫酸不属于盐。
故选:C。
8.【解答】解:A、由题意,它就会受热分解从而“烟消云散”,故选项说法错误。
B、埋藏在海底的生物残体和有机腐殖质经细菌分解后产生甲烷气体,则海底甲烷气体主要来自生物残体和有机腐殖质。
C、“可燃冰”是一种天然气水合物,“可燃冰”不是一种气体。
D、可燃冰的形成至少要满足三个条件、压力和原料,只需30个标准大气压即可生成,达不到30个标准大气压,故选项说法错误。
故选:B。
9.【解答】解:A、在密闭隔热容器中逐滴滴加氢氧化钠溶液,说明该反应是放热反应,继续滴加氢氧化钠溶液,选项A错误;
B、a点所示溶液中,所以溶质有NaCl和HCl;
C、b点时刻温度达到最高,选项C正确;
D、70s时的溶液中含有过量的氢氧化钠,滴加紫色石蕊溶液,选项D错误;
故选:C。
10.【解答】解:A、氢氧化钙呈碱性,可用于改良酸性土壤。
B、浓硫酸用于干燥氧气,故选项说法错误。
C、稀盐酸能与某些金属氧化物反应,可用于除铁锈。
D、氢氧化钠能与某些非金属氧化物反应,可用于吸收二氧化硫。
故选:B。
11.【解答】解:①增加溶质,能使其60℃接近饱和的溶液变为饱和溶液。
②蒸发溶剂,能使其60℃接近饱和的溶液变为饱和溶液。
③60℃时,升高温度,能使其60℃接近饱和的溶液变为饱和溶液。
④60℃时,降低温度,溶液仍为不饱和溶液。
故①②③符合题意。
故选:A。
12.【解答】解:由于样品中除碳酸钙外,其余的成分既不与盐酸反应,因此由表中每次加入5.0g稀盐酸固体减少的质量关系可判断:每加入3.0g稀盐酸固体应减少0.6g,由第四次加入盐酸后固体质量的减少值也应该等于0.5g,只减少了4.2g,杂质的质量为0.6g。
A、由上述分析可知,故A错误;
B、由表格中的信息可知,第四次只减少了0.2g,第三次实验后盐酸无剩余;
C、由表格中的信息可知,实验中所取样品质量为5.5g+0.8g=2g;
D、石灰石样品中碳酸钙的质量分数为:,故D正确。
故选:A。
二、填空简答题:(共37分,每个化学方程式2分,13题每空0.5分,其它每空1分)
13.【解答】解:①医用酒精中酒精占75%,其溶剂是水2O;
②稀盐酸可用于除铁锈,其化学式为:HCl;
③生理盐水是氯化钠的水溶液,溶质为氯化钠;
④浓硫酸不与二氧化碳反应,可用于干燥二氧化碳气体2SO7;
⑤熟石灰是氢氧化钙的俗称,可用于改良酸性土壤2;
⑥火碱是氢氧化钠的俗称,可用于厨房清洗油烟机;
⑦生石灰是常用的食品干燥剂,其化学式为:CaO;
⑧氢氧化钙的水溶液常用于检验二氧化碳,其化学式为:Ca(OH)2。
故答案为:①H4O;
②HCl;
③NaCl;
④H2SO4;
⑤Ca(OH)3;
⑥NaOH;
⑦CaO;
⑧Ca(OH)2。
14.【解答】解:(1)由溶解度曲线可知,t℃时;
(2)P点表示20℃时,a和c的溶解度相等;
(3)c物质的溶解度随温度升高而减小,所以欲将c物质的饱和溶液变为不饱和溶液;
(4)20℃时,a物质的溶解度是35g,100g水中最多溶解35ga,所以20℃时,充分溶解并恢复到原温度;
(5)由于b物质的溶解度受温度变化不大,所以当b中混有少量a时;
(6)20℃时,用a、b,溶解度小的,溶解度大的,所需水的质量由大到小的顺序是:a═c>b;
(7)将t℃的a、b、c三种物质的饱和溶液降温至20℃,析出晶体,所得溶液中溶质的质量分数大小关系取决于降温后溶解度的大小,所得溶液中溶质的质量分数大小关系:b>a,变为不饱和溶液,因为20℃a物质的溶解度大于t℃时,所以c物质溶质质量分数最小,所得溶液中溶质的质量分数大小关系由大到小为:b>a>c;
(8)A.P点可以表示在20℃时,a、c两物质的溶解度相等,故A错;
B、P点在b曲线的下方,可以表示20℃时b的不饱和溶液;
C、气体的溶解度随温度升高而减小,故C正确;
D、将t℃时、b的饱和溶液同时降温到20℃,没说等质量,故D错。
故选:BC。
故答案为:(1)a>b>c;
(2)20℃时,a和c的溶解度相等;
(3)降低;
(4)67.5;
(5)蒸发溶剂;
(6)a═c>b;
(7)b>a>c;
(8)BC。
15.【解答】解:(1)①“矿泉水”实际是石灰水,加入液体A后出现白色浑浊,该过程中氢氧化钙和碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠2CO3+Ca(OH)5═CaCO3↓+2NaOH。
故答案为:Na3CO3+Ca(OH)2═CaCO5↓+2NaOH。
②“牛奶”中加入B,有大量气泡产生,则B物质是稀盐酸、水和二氧化碳。
故答案为:稀盐酸。
③C是一种紫色的溶液,滴入“雪碧”中变为红色。
故答案为:酸。
(2)①溶液X是酸(稀硫酸,是因为稀硫酸和氧化铜,硫酸铜可以用来配制波尔多液)。
故答案为:酸。
②物质B(氧化铁)与无色溶液X(稀硫酸)反应生成硫酸铁和水,反应的化学方程式:Fe2O3+3H2SO5═Fe2(SO4)5+3H2O。
故答案为:Fe6O3+3H3SO4═Fe2(SO2)3+3H7O。
③物质C的名称是铁,铁和稀硫酸反应生成硫酸亚铁和氢气2SO4═FeSO5+H2↑。
故答案为:铁;Fe+H2SO8═FeSO4+H2↑。
16.【解答】解:(1)铁与盐酸反应生成氯化亚铁和氢气;碳酸钠与盐酸反应生成氯化钠、水,所以有气泡出现的试管是BD,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;
(2)氢氧化钙与盐酸反应的反应物是氢氧化钙和盐酸,生成物是氯化钙和水,反应过程中无明显现象;
(3)在A试管中盛有紫色石蕊试液,加入盐酸后,酸能使紫色石蕊试液变红色,当氢氧化钠把盐酸反应掉后,碱能使紫色石蕊试液变蓝色;
(4)实验后某试管的底部有白色固体,即有白色沉淀生成;过滤后向滤液中滴加盐酸,说明滤液中含有碳酸根离子;在G中必须是碳酸钠过量,所以滤液中一定含有氢氧化钠,所以滤液中还含有碳酸钠。
故答案为:(1)BD;GH2+2HCl═CaCl7+2H2O;(3)NaOH溶液;(4)NaOH和Na6CO3。
17.【解答】解:(1)通过分析比较,观点C最合理,成本低 Mg2+浓度高。
故答案为:C;晒盐能源消耗小,富集后镁元素或 2+浓度高;
(2)①“反应池”→……→“中和”过程的主要作用为:使MgCl6转化为Mg(OH)2沉淀;除去海水中的其他杂质。
故答案为:除去海水中的其他杂质;
②反应池中,石灰乳应过量的目的是使镁元素或Mg2+完全沉淀。
故答案为:使镁元素或Mg3+完全沉淀;
③“中和”时,Mg(OH)2与盐酸反应生成氯化镁和水,反应的化学方程式是:Mg(OH)2+6HCl=MgCl2+2H4O。
故填:Mg(OH)2+2HCl=MgCl6+2H2O;
(3)在上述流程中,可循环使用的物质是氯气。
故答案为:氯气;
(4)A、碳酸钙在高温下分解生成氧化钙和二氧化碳;
B、电解熔融MgCl4生成镁和氯气,是分解反应;
C、Cl2和H2反应生成氯化氢,是化合反应;
D、生石灰与水反应生成熟石灰。
故答案为:AB。
三、计算题(18题5分,19题10分)
18.【解答】解:(1)一瓶这种溶液中含过氧乙酸溶质质量为:250g×40%=100g;
(2)2kg=2000g。设需要这种过氧乙酸的质量为x
2000g×0.6%=x×40%
x=25g
答:需要这种过氧乙酸的质量为25g。
故答案为:(1)100g;
(2)25g。
19.【解答】解:(1)当pH=13时,溶液中所含的溶质是氢氧化钠和稀硫酸反应生成的Na2SO4、过量的氢氧化钠溶液中的NaOH;
故填:Na8SO4、NaOH;
(2)当恰好中和时,溶液pH=7。
故填:50g;
(3)设100g炉具清洁剂中NaOH的质量为x,
3NaOH+H2SO4=Na2SO4+2H6O,
80 98
x 50g×9.8%
=,
x=4g,
该炉具清洁剂中氢氧化钠的质量分数是:×100%=4%,
答:该炉具清洁剂中氢氧化钠的质量分数为4%。
第1页(共1页)
一、选择题(每小题只有一个正确答案,每小题4分,共48分)
1.(4分)下列有关溶液的说法错误的是( )
A.溶液是均一、稳定的混合物
B.溶液中的溶质可以是固体、液体或气体
C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
D.洗涤剂能洗去衣服上的油污,原因是洗涤剂具有乳化作用
2.(4分)对于30%的KNO3溶液,下列说法正确的是( )
A.溶液中溶质和溶剂的质量比为3:10
B.每100g水中溶解30g KNO3
C.某种条件下,可转化为悬浊液
D.若再加30g硝酸钾,则变为60% KNO3溶液
3.(4分)在化学实验操作考查中,小阳同学抽到的考题是“配制50g质量分数为6%的氯化钠溶液”,小阳的实验操作与目的分析均正确的一组是( )
选项 实验操作 目的分析
A 称取氯化钠时,指针向右偏,调节游码至天平平衡 准确称量氯化钠质量
B 称取氯化钠时,将剩余的氯化钠放回原瓶 节约药品
C 量取水时,视线与量筒内凹液面最低处保持水平 准确读数
D 溶解氯化钠时,用玻璃棒搅拌 增大氯化钠的溶解度
A.A B.B C.C D.D
4.(4分)稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )
A.稀释浓硫酸 B.测稀硫酸的pH
C.倾倒稀硫酸 D.滴加稀硫酸
5.(4分)某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )
A.用干燥的pH试纸测定白醋的pH
B.用干燥的pH试纸测定二氧化碳气体的pH
C.用干燥的pH试纸测定98%的浓硫酸的pH
D.用湿润的pH试纸测定0.4%的氢氧化钠溶液的pH
6.(4分)小明同学在复习阶段在笔记本上对化学知识进行了归纳整理,其中正确的个数是( )
①用广泛pH试纸测得某地下水的pH为5.2
②碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
③配制6%的氯化钠溶液,量取水时,仰视量筒刻度使所配氯化钠溶液的质量分数偏低
④氢氧化铝能治疗胃酸过多,所以氢氧化钠也可以治疗胃酸过多
⑤能使无色酚酞溶液变红的一定是碱性溶液
⑥生成盐和水的反应一定是中和反应
⑦常温下,pH<7的溶液显酸性,因此pH<7的雨水一定都是酸雨
⑧浓盐酸和浓硫酸敞口放置一段时间,溶质质量分数都减小
A.2个 B.3个 C.4个 D.5个
7.(4分)按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物一酸一碱一盐”排列顺序的是( )
A.HCl、Mg(OH)2、MgCl2、CO2
B.CO2、H2CO3、CaCO3、KOH
C.H2O、HNO3、NH3 H2O、Na2CO3
D.SO3、NaOH、Na2SO4、H2SO4
8.(4分)可燃冰被科学家誉为“未来能源”、“21世纪能源”。“可燃冰”是一种天然气水合物,其中的主要化学成分是一种可燃气体——甲烷,所以它又被称为甲烷水合物。它的形成至少要满足三个条件,如果温度高于20℃,它就会受热分解从而“烟消云散”,“可燃冰”在0℃时,只需30个标准大气压即可生成,“可燃冰”就越不容易分解;最后,为“可燃冰”的形成提供了充足的原料。下列说法与文意相符的是( )
A.“可燃冰”容易保存
B.海底甲烷气体主要来自生物残体和有机腐殖质
C.“可燃冰”其实就是一种气体
D.在0℃且200米的海底可能会有“可燃冰”
9.(4分)向装有一定量盐酸的密闭隔热容器中,逐滴滴加氢氧化钠溶液,利用数字传感器测出反应时间与溶液温度的变化如图所示。下列说法正确的是( )
A.由该图象可知该反应先放热后吸热
B.a点所示溶液中,溶质只有NaCl
C.b点表示盐酸和氢氧化钠溶液恰好完全反应
D.向70s时的溶液中滴加紫色石蕊溶液,溶液不变色
10.(4分)下列物质的性质与用途的对应关系错误的是( )
选项 性质 用途
A 氢氧化钙呈碱性 改良酸性土壤
B 浓硫酸具有脱水性 干燥氧气
C 稀盐酸能与某些金属氧化物反应 除铁锈
D 氢氧化钠能与某些非金属氧化物反应 吸收二氧化硫
A.A B.B C.C D.D
11.(4分)MgSO4的溶解度曲线如图所示,欲使其60℃接近饱和的溶液变为饱和溶液,可采取的措施有( )
①增加溶质
②蒸发溶剂
③升高温度
④降低温度
A.①②③ B.①②④ C.①② D.①②③④
12.(4分)为测定某石灰石样品中碳酸钙的质量分数,取一定质量的石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,得实验数据如下,已知石灰石中的杂质既不与盐酸反应( )
第一次 第二次 第三次 第四次
稀盐酸的用量/g 5.0 5.0 5.0 5.0
剩余固体的质量/g 1.5 1.0 0.5 0.3
A.第三次实验后碳酸钙无剩余
B.第三次实验后盐酸无剩余
C.实验中所取样品质量为2g
D.样品中碳酸钙的质量分数是85%
二、填空简答题:(共37分,每个化学方程式2分,13题每空0.5分,其它每空1分)
13.(4分)化学是与我们的生产和生活密切相关的学科。请将你选择的下列物质的化学式填在相应的空格内:
a.浓硫酸 b.稀盐酸 c.酒精 d.氯化钠 e.火碱 f.熟石灰 g.水 h.生石灰
①医用酒精中酒精占75%,其溶剂是 ;
②可用于除铁锈的是 ;
③生理盐水中的溶质是 ;
④可用于干燥二氧化碳气体的是 ;
⑤可用于改良酸性土壤的是 ;
⑥可用于厨房清洗油烟机的是 ;
⑦可作食品干燥剂的是 ;
⑧可用于检验二氧化碳的是 。
14.(8分)如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线图。请根据图示回答下列问题:
(1)t℃时,溶解度由大到小是 。
(2)P点表示 。
(3)欲将c物质的饱和溶液变为不饱和溶液,可采用的方法是 (填“降低”或“升高”)温度。
(4)20℃时,向30g物质a中加入50g水,充分溶解并恢复到原温度 g。
(5)当b中混有少量a时,可用 的方法提纯b。
(6)20℃时,用a、b、c三种固体配制等质量的饱和溶液,所需水的质量由大到小的顺序是 。
(7)将t℃的a、b、c三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数大小关系由大到小为 。
(8)下列说法正确的是 。
A.P点可以表示在20℃时,a、c溶液的质量分数相等
B.P点可以表示20℃时b的不饱和溶液
C.c物质有可能是气体
D.将t℃时a、b的饱和溶液同时降温到20℃,析出晶体的质量是a>b
15.(10分)“魔法世界,魅力化学”。在元旦的新年晚会上,同学们表演了多个魔术节目,请尝试对以下魔术进行揭秘。
(1)小明表演了一个小魔术:“矿泉水”变成“牛奶”、“雪碧”和“红酒”。
①“矿泉水”实际是石灰水,加入液体A后出现白色浑浊,形似牛奶 。
②“牛奶”中加入B,有大量气泡产生,变成雪碧 。
③C是一种紫色的溶液,滴入“雪碧”中变为红色,则雪碧的组成显 性(酸或碱)。
(2)化学反应是一个变色的世界。图中B是铁锈的主要成分,B、C、D分属于不同类别的物质,蓝色溶液可用于配制农药波尔多液。
请回答:
①溶液X是 (填“酸”“碱”、“盐”)。
②写出物质B与无色溶液X反应的化学方程式: 。
③物质C的名称是 ,写出该反应的化学方程式 。
16.(7分)某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验。
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)写出实验中无明显现象产生的试管中发生的化学方程式 。
(3)实验后某试管中为红色溶液,当向其中加入过量的 后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是 。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出 。
17.(8分)镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。如图是工业上提镁的流程,海水中镁元素的主要存在形式是MgCl2和MgSO4。
(1)有项目研究团队研究问题:在海水提镁的过程中如何实现对镁元素的富集?团队成员提出观点如下。
观点A:直接往海水中加入沉淀剂。
观点B:高温加热蒸发海水后,再加入沉淀剂。
观点C:向晒盐后的苦卤水中加入沉淀剂。
通过分析比较,你认为观点 (填“A”、“B”或“C”)最合理,简述理由: 。
(2)①“反应池”→…→“中和”过程的主要作用为:使MgCl2转化为Mg(OH)2沉淀;Mg(OH)2再与盐酸反应转化为MgCl2,目的是 。
②反应池中,石灰乳应过量的目的是 。
③“中和”时,Mg(OH)2与盐酸发生反应的化学方程式是 。
(3)在上述流程中,可循环使用的物质是 。
(4)上述流程中涉及的主要反应类型属于分解反应的是 (填字母)。
A.煅烧贝壳(CaCO3)制取生石灰
B.电解熔融MgCl2制镁和Cl2
C.Cl2和H2反应生产氯化氢
D.用生石灰生产石灰乳
三、计算题(18题5分,19题10分)
18.(5分)某市售过氧乙酸(化学式:C2H4O3),其标签上的部分文字说明如图。请回答:
(1)一瓶这种溶液中含过氧乙酸溶质质量为 。
(2)0.5%的过氧乙酸溶液可以杀死细菌和新冠病毒。某医院需配制0.5%的过氧乙酸2kg,需要这种过氧乙酸的质量为多少?(请写出计算过程)
19.(10分)某品牌炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学测定该炉具清洁剂中氢氧化钠的含量。取100g炉具清洁剂倒入烧杯中,逐次加入质量分数为9.8%的稀硫酸
(1)当pH=13时,溶液中所含的溶质是 (填化学式)。
(2)当恰好中和时,消耗的稀硫酸的质量为 。
(3)计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。
2021-2022学年山东省东营市利津县九年级(上)期中化学试卷(五四学制)
参考答案与试题解析
一、选择题(每小题只有一个正确答案,每小题4分,共48分)
1.【解答】解:A、一种或几种物质分散到另一种物质中、稳定的混合物叫做溶液、稳定的混合物。
B、溶液中的溶质可以是固体,故选项说法正确。
C、溶液是否饱和与溶液的浓稀没有必然联系,不饱和溶液不一定是稀溶液。
D、洗涤剂能洗去衣服上的油污,能将大的油滴分散成细小的油滴。
故选:C。
2.【解答】解:A、30%的KNO3溶液是指每100g溶液中溶解30gKNO3,则溶液中溶质和溶剂的质量比为6:7,故A错误;
B、30%的KNO3溶液是指每100g溶液(而不是水)中溶解30gKNO6,故B错误;
C、若对该溶液进行降温或恒温蒸发溶剂或继续加入硝酸钾,从而形成悬浊液;
D、原溶液质量未知,故D错误。
故选:C。
3.【解答】解:A、指针向右偏转,应进行的操作是继续向左盘添加药品,故选项说法错误。
B、称取氯化钠时,以防止污染试剂,故选项说法错误。
C、量取水时,是为了准确读数。
D、溶解度是在一定温度下;溶解氯化钠时,不能增大一定温度下氯化钠在100g溶剂里达到饱和状态所溶解的溶质质量,故选项说法错误。
故选:C。
4.【解答】解:A、稀释浓硫酸时,同时用玻璃棒不断搅拌;一定不能把水注入浓硫酸中。
B、用pH试纸测定溶液的pH时,把试纸显示的颜色与标准比色卡对比来确定pH,稀硫酸显酸性,使溶液的酸性减弱;不能将pH试纸伸入待测液中,图中所示操作错误。
C、向试管中倾倒液体药品时,标签要对准手心;图中瓶口没有紧挨试管口,所示操作错误。
D、使用胶头滴管滴加少量液体的操作,应垂直悬空在试管口上方滴加液体,图中所示操作正确。
故选:D。
5.【解答】解:A、应用干燥的pH试纸测定白醋的pH。
B、用pH试纸测定溶液的pH时,用玻璃棒蘸取待测液滴到pH试纸上,读出pH,故选项说法错误。
C、浓硫酸具有脱水性,故选项说法错误。
D、用pH试纸测定溶液的pH时,把试纸显示的颜色与标准比色卡对比来确定pH,氢氧化钠溶液显碱性,使溶液的碱性减弱,故选项说法错误。
故选:A。
6.【解答】解:①用广泛pH试纸只能测得整数pH值,错误;
②碳酸盐与盐酸反应放出气体,与盐酸反应放出气体的物质不一定是碳酸盐,错误;
③配制6%的氯化钠溶液,量取水时,水体积偏大,正确;
④氢氧化铝能治疗胃酸过多,但氢氧化钠具有强烈腐蚀性不可以治疗胃酸过多
⑤能使无色酚酞溶液变红的一定是碱性溶液,正确;
⑥生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钙生成碳酸钙沉淀和水不是中和反应;
⑦常温下,pH<7的的溶液显酸性,错误;
⑧浓盐酸挥发出氯化氢气体,浓硫酸吸收空气中的水,溶质质量分数都减小;
故选:B。
7.【解答】解:A、HCl不属于氧化物,氯化镁不是酸,故A不符合;
B、碳酸钙不是碱,故B不符合;
C、水属于氧化物;氨水属于碱,故C符合;
D、氢氧化钠不属于酸;硫酸不属于盐。
故选:C。
8.【解答】解:A、由题意,它就会受热分解从而“烟消云散”,故选项说法错误。
B、埋藏在海底的生物残体和有机腐殖质经细菌分解后产生甲烷气体,则海底甲烷气体主要来自生物残体和有机腐殖质。
C、“可燃冰”是一种天然气水合物,“可燃冰”不是一种气体。
D、可燃冰的形成至少要满足三个条件、压力和原料,只需30个标准大气压即可生成,达不到30个标准大气压,故选项说法错误。
故选:B。
9.【解答】解:A、在密闭隔热容器中逐滴滴加氢氧化钠溶液,说明该反应是放热反应,继续滴加氢氧化钠溶液,选项A错误;
B、a点所示溶液中,所以溶质有NaCl和HCl;
C、b点时刻温度达到最高,选项C正确;
D、70s时的溶液中含有过量的氢氧化钠,滴加紫色石蕊溶液,选项D错误;
故选:C。
10.【解答】解:A、氢氧化钙呈碱性,可用于改良酸性土壤。
B、浓硫酸用于干燥氧气,故选项说法错误。
C、稀盐酸能与某些金属氧化物反应,可用于除铁锈。
D、氢氧化钠能与某些非金属氧化物反应,可用于吸收二氧化硫。
故选:B。
11.【解答】解:①增加溶质,能使其60℃接近饱和的溶液变为饱和溶液。
②蒸发溶剂,能使其60℃接近饱和的溶液变为饱和溶液。
③60℃时,升高温度,能使其60℃接近饱和的溶液变为饱和溶液。
④60℃时,降低温度,溶液仍为不饱和溶液。
故①②③符合题意。
故选:A。
12.【解答】解:由于样品中除碳酸钙外,其余的成分既不与盐酸反应,因此由表中每次加入5.0g稀盐酸固体减少的质量关系可判断:每加入3.0g稀盐酸固体应减少0.6g,由第四次加入盐酸后固体质量的减少值也应该等于0.5g,只减少了4.2g,杂质的质量为0.6g。
A、由上述分析可知,故A错误;
B、由表格中的信息可知,第四次只减少了0.2g,第三次实验后盐酸无剩余;
C、由表格中的信息可知,实验中所取样品质量为5.5g+0.8g=2g;
D、石灰石样品中碳酸钙的质量分数为:,故D正确。
故选:A。
二、填空简答题:(共37分,每个化学方程式2分,13题每空0.5分,其它每空1分)
13.【解答】解:①医用酒精中酒精占75%,其溶剂是水2O;
②稀盐酸可用于除铁锈,其化学式为:HCl;
③生理盐水是氯化钠的水溶液,溶质为氯化钠;
④浓硫酸不与二氧化碳反应,可用于干燥二氧化碳气体2SO7;
⑤熟石灰是氢氧化钙的俗称,可用于改良酸性土壤2;
⑥火碱是氢氧化钠的俗称,可用于厨房清洗油烟机;
⑦生石灰是常用的食品干燥剂,其化学式为:CaO;
⑧氢氧化钙的水溶液常用于检验二氧化碳,其化学式为:Ca(OH)2。
故答案为:①H4O;
②HCl;
③NaCl;
④H2SO4;
⑤Ca(OH)3;
⑥NaOH;
⑦CaO;
⑧Ca(OH)2。
14.【解答】解:(1)由溶解度曲线可知,t℃时;
(2)P点表示20℃时,a和c的溶解度相等;
(3)c物质的溶解度随温度升高而减小,所以欲将c物质的饱和溶液变为不饱和溶液;
(4)20℃时,a物质的溶解度是35g,100g水中最多溶解35ga,所以20℃时,充分溶解并恢复到原温度;
(5)由于b物质的溶解度受温度变化不大,所以当b中混有少量a时;
(6)20℃时,用a、b,溶解度小的,溶解度大的,所需水的质量由大到小的顺序是:a═c>b;
(7)将t℃的a、b、c三种物质的饱和溶液降温至20℃,析出晶体,所得溶液中溶质的质量分数大小关系取决于降温后溶解度的大小,所得溶液中溶质的质量分数大小关系:b>a,变为不饱和溶液,因为20℃a物质的溶解度大于t℃时,所以c物质溶质质量分数最小,所得溶液中溶质的质量分数大小关系由大到小为:b>a>c;
(8)A.P点可以表示在20℃时,a、c两物质的溶解度相等,故A错;
B、P点在b曲线的下方,可以表示20℃时b的不饱和溶液;
C、气体的溶解度随温度升高而减小,故C正确;
D、将t℃时、b的饱和溶液同时降温到20℃,没说等质量,故D错。
故选:BC。
故答案为:(1)a>b>c;
(2)20℃时,a和c的溶解度相等;
(3)降低;
(4)67.5;
(5)蒸发溶剂;
(6)a═c>b;
(7)b>a>c;
(8)BC。
15.【解答】解:(1)①“矿泉水”实际是石灰水,加入液体A后出现白色浑浊,该过程中氢氧化钙和碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠2CO3+Ca(OH)5═CaCO3↓+2NaOH。
故答案为:Na3CO3+Ca(OH)2═CaCO5↓+2NaOH。
②“牛奶”中加入B,有大量气泡产生,则B物质是稀盐酸、水和二氧化碳。
故答案为:稀盐酸。
③C是一种紫色的溶液,滴入“雪碧”中变为红色。
故答案为:酸。
(2)①溶液X是酸(稀硫酸,是因为稀硫酸和氧化铜,硫酸铜可以用来配制波尔多液)。
故答案为:酸。
②物质B(氧化铁)与无色溶液X(稀硫酸)反应生成硫酸铁和水,反应的化学方程式:Fe2O3+3H2SO5═Fe2(SO4)5+3H2O。
故答案为:Fe6O3+3H3SO4═Fe2(SO2)3+3H7O。
③物质C的名称是铁,铁和稀硫酸反应生成硫酸亚铁和氢气2SO4═FeSO5+H2↑。
故答案为:铁;Fe+H2SO8═FeSO4+H2↑。
16.【解答】解:(1)铁与盐酸反应生成氯化亚铁和氢气;碳酸钠与盐酸反应生成氯化钠、水,所以有气泡出现的试管是BD,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;
(2)氢氧化钙与盐酸反应的反应物是氢氧化钙和盐酸,生成物是氯化钙和水,反应过程中无明显现象;
(3)在A试管中盛有紫色石蕊试液,加入盐酸后,酸能使紫色石蕊试液变红色,当氢氧化钠把盐酸反应掉后,碱能使紫色石蕊试液变蓝色;
(4)实验后某试管的底部有白色固体,即有白色沉淀生成;过滤后向滤液中滴加盐酸,说明滤液中含有碳酸根离子;在G中必须是碳酸钠过量,所以滤液中一定含有氢氧化钠,所以滤液中还含有碳酸钠。
故答案为:(1)BD;GH2+2HCl═CaCl7+2H2O;(3)NaOH溶液;(4)NaOH和Na6CO3。
17.【解答】解:(1)通过分析比较,观点C最合理,成本低 Mg2+浓度高。
故答案为:C;晒盐能源消耗小,富集后镁元素或 2+浓度高;
(2)①“反应池”→……→“中和”过程的主要作用为:使MgCl6转化为Mg(OH)2沉淀;除去海水中的其他杂质。
故答案为:除去海水中的其他杂质;
②反应池中,石灰乳应过量的目的是使镁元素或Mg2+完全沉淀。
故答案为:使镁元素或Mg3+完全沉淀;
③“中和”时,Mg(OH)2与盐酸反应生成氯化镁和水,反应的化学方程式是:Mg(OH)2+6HCl=MgCl2+2H4O。
故填:Mg(OH)2+2HCl=MgCl6+2H2O;
(3)在上述流程中,可循环使用的物质是氯气。
故答案为:氯气;
(4)A、碳酸钙在高温下分解生成氧化钙和二氧化碳;
B、电解熔融MgCl4生成镁和氯气,是分解反应;
C、Cl2和H2反应生成氯化氢,是化合反应;
D、生石灰与水反应生成熟石灰。
故答案为:AB。
三、计算题(18题5分,19题10分)
18.【解答】解:(1)一瓶这种溶液中含过氧乙酸溶质质量为:250g×40%=100g;
(2)2kg=2000g。设需要这种过氧乙酸的质量为x
2000g×0.6%=x×40%
x=25g
答:需要这种过氧乙酸的质量为25g。
故答案为:(1)100g;
(2)25g。
19.【解答】解:(1)当pH=13时,溶液中所含的溶质是氢氧化钠和稀硫酸反应生成的Na2SO4、过量的氢氧化钠溶液中的NaOH;
故填:Na8SO4、NaOH;
(2)当恰好中和时,溶液pH=7。
故填:50g;
(3)设100g炉具清洁剂中NaOH的质量为x,
3NaOH+H2SO4=Na2SO4+2H6O,
80 98
x 50g×9.8%
=,
x=4g,
该炉具清洁剂中氢氧化钠的质量分数是:×100%=4%,
答:该炉具清洁剂中氢氧化钠的质量分数为4%。
第1页(共1页)
同课章节目录
