8.3.2金属资源的利用与保护-2021-2022学年九年级化学人教版下册(25张PPT)
文档属性
| 名称 | 8.3.2金属资源的利用与保护-2021-2022学年九年级化学人教版下册(25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-16 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
课题3 金属资源的利用和保护
1、知道钢铁锈蚀的条件
2、掌握防止金属锈蚀的简单方法
3、了解废弃金属对环境的污染,认识保护金属资源的重要性。
学习目标
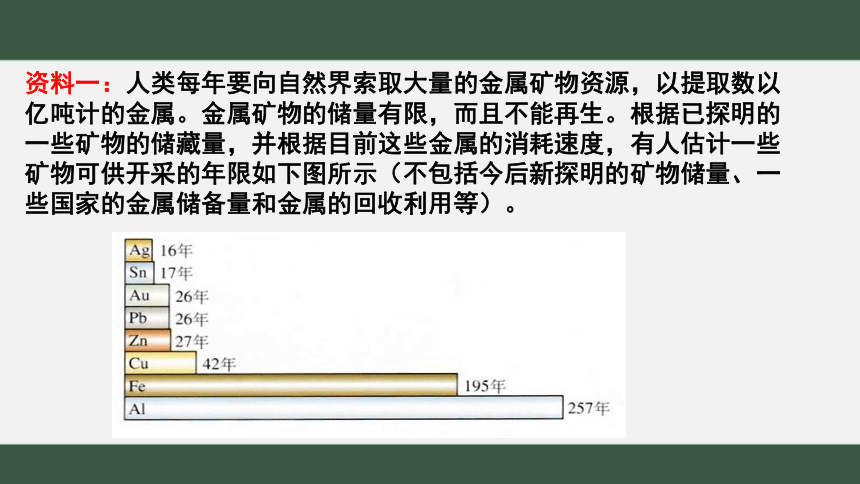
资料一:人类每年要向自然界索取大量的金属矿物资源,以提取数以亿吨计的金属。金属矿物的储量有限,而且不能再生。根据已探明的一些矿物的储藏量,并根据目前这些金属的消耗速度,有人估计一些矿物可供开采的年限如下图所示(不包括今后新探明的矿物储量、一些国家的金属储备量和金属的回收利用等)。
议一议
如果我们的生活中没有了金属,我们的生活会变成怎么样?
资料二:据有关资料报道,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20% ~ 40%。
二、金属资源保护
1、金属的腐蚀和防护
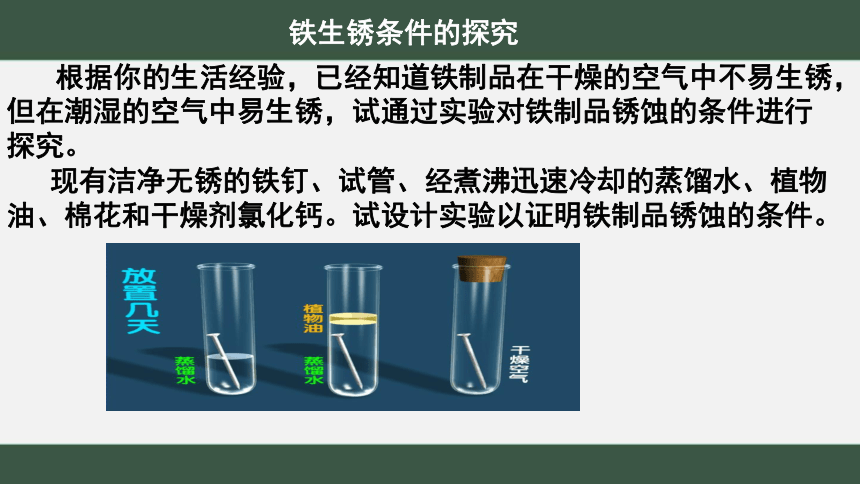
(1)铁制品锈蚀条件的探究
根据你的生活经验,已经知道铁制品在干燥的空气中不易生锈,但在潮湿的空气中易生锈,试通过实验对铁制品锈蚀的条件进行探究。
现有洁净无锈的铁钉、试管、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙。试设计实验以证明铁制品锈蚀的条件。
铁生锈条件的探究
试管Ⅰ 试管Ⅱ 试管Ⅲ
现象
分析
生锈
不生锈
不生锈
铁既与水接触,又与氧气接触
铁只与水接触
铁只与氧气接触
结论:在水、氧气同时存在的环境中铁能生锈
铁生锈条件的探究
阅读教材P19页,回答下列问题:
1、试管Ⅱ中为什么要用煮沸过的蒸馏水,且要加入植物油?
2、铝与氧气反应生成的氧化铝能起到保护里层铝的作用。铁锈是否也能保护里层的铁呢?
3、你能否根据铁生锈的条件提出防止铁制品生锈的原理吗?
为了防止蒸馏水中溶有氧气。
不能,因为铁锈是疏松的。
想一想
二、金属资源保护
1、金属的腐蚀和防护
(1)铁制品锈蚀条件的探究
铁生锈的过程是:铁与空气和水(或水蒸气)发生化学反应的过程。
铁锈的主要成分是Fe2O3 · xH2O
(2)铁制品的防护措施
防止铁生锈的原理
①隔绝空气
②隔绝水
--就是破坏铁生锈的条件
1、在实际生活和生产中我们应该采取哪些具体方法来防止铁制品生锈呢?
保持铁制品表面干燥和洁净
在铁制品表面涂一层保护膜如:刷油漆、涂油、镀上一层耐磨、耐腐蚀的金属铬等
制成合金,如不锈钢
使用后请及时擦干并挂起
刷油漆
镀铬
我是不锈钢
3、对于金属资源除了采取防止金属腐蚀的措施外,还可以通过什么途径来使金属资源得到保护呢?
废品收购站为什么要收购废铁、废铜、和易拉罐等金属?
?
据估算,回收一个铝制饮料罐比制造一个新饮料罐要便宜20%,而且还可节约金属资源和95%的能源。
废旧金属的回收利用还可以减少对环境的污染。例如,废旧电池中含有汞等,如果废旧电池随意丢弃,汞等渗出会造成地下水和土壤的污染,威胁人类健康。
将汞等回收利用,不仅可以节约金属资源,而且还可以减少对环境的污染。
你知道吗?
三、金属资源保护1.铁制品锈蚀:(1)条件:与空气中的_____和___ 接触。(2)铁锈的主要成分:Fe2O3·xH2O,结构很疏松,不能阻碍里层的铁继续被锈蚀。2.防止铁制品锈蚀的方法:(1)保持铁制品表面的___________。(2)在铁制品表面覆盖_______,如在铁制品表面涂油、刷漆、电镀等。(3)改变铁的组成和结构,制成耐腐蚀的_____,如不锈钢。
水分
氧气
洁净与干燥
保护膜
合金
【自主合作2】
3.金属资源保护:(1)保护金属资源的原因。 ①金属矿物的储量有限,而且不能再生。 ②废旧金属的随意丢弃会污染环境。(2)保护金属资源的措施。 ①防止金属_____。
②_______ 废旧金属。
③________ 地开采矿物。 ④寻找金属的_______。
锈蚀
回收利用
有计划、合理
替代品
1.据估计每年因生锈而损失的钢铁约占世界年产量的1/4,下列防锈措施中正确的是( )
①涂油 ②刷漆 ③砂纸 ④镀金属
⑤经常用雨水冲洗 ⑥烤蓝
A.③⑤ B.①②④⑥ C.①②③④⑥ D.①④
2.在下列情况下,埋在地下的铸铁管道腐蚀最慢 的是( )
A.在干燥、致密、不透气的土壤中
B.在潮湿、疏松、透气的土壤中
C.在潮湿、致密、不透气的土壤中
D.在潮湿、疏松、透气的酸性土壤中
B
A
课堂检测
1.(2017·衡阳中考)实验室模拟炼铁的实验装置如下图所示。
试回答下列问题:(1)写出有标号仪器的名称:a.________,b.________。(2)实验中看到的实验现象为玻璃管中的粉末______;试管里的澄清石灰水______。(3)玻璃管中反应的化学方程式为________________。(4)加热氧化铁之前,先通一会儿一氧化碳的作用是____________。(5)该实验设计装置C的目的是________________。
铁架台
导管
排尽管内空气,防止发生爆炸
变浑浊
3CO+Fe2O3=2Fe+3CO2
高温
逐渐变为黑色
除去未反应的CO。防止污染空气
【展示质疑】
2.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示。请回答有关问题:
1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是C和D,导管接口的连接顺序a→ → → C装置中NaOH的 。2)实验开始时,应(填“先加热再通CO”或“先通CO再加热”),目的是 。
b d e
吸收二氧化碳
排尽管内空气,防止发生爆炸
【展示质疑】
3)实验进行一段时间后,玻璃管A中出现的现象为 ,反应方程式为 。4)除CO外,还有哪些物质可以还原Fe2O3 (请写一物质的化学式)。
C\H2
3CO+Fe2O3=2Fe+3CO2
高温
红色粉末逐渐变为黑色
【巩固构建】
【巩固建构】1.判断正误: (1)赤铁矿主要成分是四氧化三铁。( ) (2)工业炼铁的原理是用焦炭把铁还原出来。( ) (3)工业炼铁得到的是含杂质的生铁,不是纯铁。( ) (4)保留铁制品上的铁锈可以防止铁的进一步锈蚀。( ) (5)回收利用废旧金属、寻找金属代用品都是保护金属资源的有效途径。( )2.铁钉在下列情况中,最容易生锈的是( ) A.在干燥的空气中 B.在潮湿的空气中 C.浸没在自来水中 D.浸没在植物油中
×
×
√
×
√
B
【巩固构建】
.如图所示,光亮的铁钉在下列几种情况下,锈蚀速率由快到慢的顺序为( )
A.①②③ B.①③② C.②③① D.②①③
B
【巩固构建】
4.实验室里用如图所示装置还原氧化铁。关于该实验,下列说法错误的是( )
A.实验时,试管中澄清的石灰水变浑浊,证明该反应中有二氧化碳生成B.实验开始时,点燃酒精灯给玻璃管加热的同时通入纯净的一氧化碳C.为了减少空气污染,应增加尾气处理装置D.实验中观察到玻璃管中红棕色固体变为黑色,并且澄清的石灰水变浑浊
B
【巩固构建】
5.自行车是日常生活中常用的交通工具,其中的支架、链条等部位经常会生锈。(1)自行车在哪种情况下使用易生锈?_________________________(2)自行车的各个部分通常采取了怎样的防锈措施?(列举两个不同部位的不同措施)_________________________________________。4.(2017·兰州中考)下列说法中正确的是( ) A.废旧电池可以随意丢弃
B.铁矿石可以随意开采 C.被腐蚀的铁制品应该加以回收利用
D.铁丝在氧气中燃烧生成氧化铁
潮湿的空气中
刷油
C
【巩固构建】
5.下列关于铁的说法正确的是( )A.铁部分锈蚀后没有回收价值 B.铁是地壳中含量最丰富的金属元素C.铁生锈,产生的铁锈能阻止铁继续被锈蚀D.铁生锈是铁在有氧气和水等物质存在的条件下,发生复杂化学反应的过程
D
【巩固构建】
6.(2017·海南中考)海南石碌铁矿,其矿石主要成分为Fe2O3。炼铁的化学方程式为Fe2O3+3CO 2Fe+3CO2,请计算:某铁矿石,其中含Fe2O3的质量为16 t,理论上可以炼出铁的质量为多少?
解:理论上可以炼出铁的质量为X
3CO+Fe2O3=2Fe+3CO2
高温
160 112
16t X
x=11.2t
答:理论上可以炼出铁的质量为11.2t
160 112
16t x
=
【巩固构建】
7.用800 t含氧化铁80%的赤铁矿石,理论可以炼出含铁99%的生铁多少吨?
解:理论上可以炼出含铁99%的生铁质量为X
3CO+Fe2O3=2Fe+3CO2
高温
160 112
800t×80% 99%X
x=452.5t
答:理论上可以炼出含铁99%的生铁质量为452.5t
160 112
800t×80% 99% x
=
【巩固构建】
课题3 金属资源的利用和保护
1、知道钢铁锈蚀的条件
2、掌握防止金属锈蚀的简单方法
3、了解废弃金属对环境的污染,认识保护金属资源的重要性。
学习目标
资料一:人类每年要向自然界索取大量的金属矿物资源,以提取数以亿吨计的金属。金属矿物的储量有限,而且不能再生。根据已探明的一些矿物的储藏量,并根据目前这些金属的消耗速度,有人估计一些矿物可供开采的年限如下图所示(不包括今后新探明的矿物储量、一些国家的金属储备量和金属的回收利用等)。
议一议
如果我们的生活中没有了金属,我们的生活会变成怎么样?
资料二:据有关资料报道,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20% ~ 40%。
二、金属资源保护
1、金属的腐蚀和防护
(1)铁制品锈蚀条件的探究
根据你的生活经验,已经知道铁制品在干燥的空气中不易生锈,但在潮湿的空气中易生锈,试通过实验对铁制品锈蚀的条件进行探究。
现有洁净无锈的铁钉、试管、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙。试设计实验以证明铁制品锈蚀的条件。
铁生锈条件的探究
试管Ⅰ 试管Ⅱ 试管Ⅲ
现象
分析
生锈
不生锈
不生锈
铁既与水接触,又与氧气接触
铁只与水接触
铁只与氧气接触
结论:在水、氧气同时存在的环境中铁能生锈
铁生锈条件的探究
阅读教材P19页,回答下列问题:
1、试管Ⅱ中为什么要用煮沸过的蒸馏水,且要加入植物油?
2、铝与氧气反应生成的氧化铝能起到保护里层铝的作用。铁锈是否也能保护里层的铁呢?
3、你能否根据铁生锈的条件提出防止铁制品生锈的原理吗?
为了防止蒸馏水中溶有氧气。
不能,因为铁锈是疏松的。
想一想
二、金属资源保护
1、金属的腐蚀和防护
(1)铁制品锈蚀条件的探究
铁生锈的过程是:铁与空气和水(或水蒸气)发生化学反应的过程。
铁锈的主要成分是Fe2O3 · xH2O
(2)铁制品的防护措施
防止铁生锈的原理
①隔绝空气
②隔绝水
--就是破坏铁生锈的条件
1、在实际生活和生产中我们应该采取哪些具体方法来防止铁制品生锈呢?
保持铁制品表面干燥和洁净
在铁制品表面涂一层保护膜如:刷油漆、涂油、镀上一层耐磨、耐腐蚀的金属铬等
制成合金,如不锈钢
使用后请及时擦干并挂起
刷油漆
镀铬
我是不锈钢
3、对于金属资源除了采取防止金属腐蚀的措施外,还可以通过什么途径来使金属资源得到保护呢?
废品收购站为什么要收购废铁、废铜、和易拉罐等金属?
?
据估算,回收一个铝制饮料罐比制造一个新饮料罐要便宜20%,而且还可节约金属资源和95%的能源。
废旧金属的回收利用还可以减少对环境的污染。例如,废旧电池中含有汞等,如果废旧电池随意丢弃,汞等渗出会造成地下水和土壤的污染,威胁人类健康。
将汞等回收利用,不仅可以节约金属资源,而且还可以减少对环境的污染。
你知道吗?
三、金属资源保护1.铁制品锈蚀:(1)条件:与空气中的_____和___ 接触。(2)铁锈的主要成分:Fe2O3·xH2O,结构很疏松,不能阻碍里层的铁继续被锈蚀。2.防止铁制品锈蚀的方法:(1)保持铁制品表面的___________。(2)在铁制品表面覆盖_______,如在铁制品表面涂油、刷漆、电镀等。(3)改变铁的组成和结构,制成耐腐蚀的_____,如不锈钢。
水分
氧气
洁净与干燥
保护膜
合金
【自主合作2】
3.金属资源保护:(1)保护金属资源的原因。 ①金属矿物的储量有限,而且不能再生。 ②废旧金属的随意丢弃会污染环境。(2)保护金属资源的措施。 ①防止金属_____。
②_______ 废旧金属。
③________ 地开采矿物。 ④寻找金属的_______。
锈蚀
回收利用
有计划、合理
替代品
1.据估计每年因生锈而损失的钢铁约占世界年产量的1/4,下列防锈措施中正确的是( )
①涂油 ②刷漆 ③砂纸 ④镀金属
⑤经常用雨水冲洗 ⑥烤蓝
A.③⑤ B.①②④⑥ C.①②③④⑥ D.①④
2.在下列情况下,埋在地下的铸铁管道腐蚀最慢 的是( )
A.在干燥、致密、不透气的土壤中
B.在潮湿、疏松、透气的土壤中
C.在潮湿、致密、不透气的土壤中
D.在潮湿、疏松、透气的酸性土壤中
B
A
课堂检测
1.(2017·衡阳中考)实验室模拟炼铁的实验装置如下图所示。
试回答下列问题:(1)写出有标号仪器的名称:a.________,b.________。(2)实验中看到的实验现象为玻璃管中的粉末______;试管里的澄清石灰水______。(3)玻璃管中反应的化学方程式为________________。(4)加热氧化铁之前,先通一会儿一氧化碳的作用是____________。(5)该实验设计装置C的目的是________________。
铁架台
导管
排尽管内空气,防止发生爆炸
变浑浊
3CO+Fe2O3=2Fe+3CO2
高温
逐渐变为黑色
除去未反应的CO。防止污染空气
【展示质疑】
2.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示。请回答有关问题:
1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是C和D,导管接口的连接顺序a→ → → C装置中NaOH的 。2)实验开始时,应(填“先加热再通CO”或“先通CO再加热”),目的是 。
b d e
吸收二氧化碳
排尽管内空气,防止发生爆炸
【展示质疑】
3)实验进行一段时间后,玻璃管A中出现的现象为 ,反应方程式为 。4)除CO外,还有哪些物质可以还原Fe2O3 (请写一物质的化学式)。
C\H2
3CO+Fe2O3=2Fe+3CO2
高温
红色粉末逐渐变为黑色
【巩固构建】
【巩固建构】1.判断正误: (1)赤铁矿主要成分是四氧化三铁。( ) (2)工业炼铁的原理是用焦炭把铁还原出来。( ) (3)工业炼铁得到的是含杂质的生铁,不是纯铁。( ) (4)保留铁制品上的铁锈可以防止铁的进一步锈蚀。( ) (5)回收利用废旧金属、寻找金属代用品都是保护金属资源的有效途径。( )2.铁钉在下列情况中,最容易生锈的是( ) A.在干燥的空气中 B.在潮湿的空气中 C.浸没在自来水中 D.浸没在植物油中
×
×
√
×
√
B
【巩固构建】
.如图所示,光亮的铁钉在下列几种情况下,锈蚀速率由快到慢的顺序为( )
A.①②③ B.①③② C.②③① D.②①③
B
【巩固构建】
4.实验室里用如图所示装置还原氧化铁。关于该实验,下列说法错误的是( )
A.实验时,试管中澄清的石灰水变浑浊,证明该反应中有二氧化碳生成B.实验开始时,点燃酒精灯给玻璃管加热的同时通入纯净的一氧化碳C.为了减少空气污染,应增加尾气处理装置D.实验中观察到玻璃管中红棕色固体变为黑色,并且澄清的石灰水变浑浊
B
【巩固构建】
5.自行车是日常生活中常用的交通工具,其中的支架、链条等部位经常会生锈。(1)自行车在哪种情况下使用易生锈?_________________________(2)自行车的各个部分通常采取了怎样的防锈措施?(列举两个不同部位的不同措施)_________________________________________。4.(2017·兰州中考)下列说法中正确的是( ) A.废旧电池可以随意丢弃
B.铁矿石可以随意开采 C.被腐蚀的铁制品应该加以回收利用
D.铁丝在氧气中燃烧生成氧化铁
潮湿的空气中
刷油
C
【巩固构建】
5.下列关于铁的说法正确的是( )A.铁部分锈蚀后没有回收价值 B.铁是地壳中含量最丰富的金属元素C.铁生锈,产生的铁锈能阻止铁继续被锈蚀D.铁生锈是铁在有氧气和水等物质存在的条件下,发生复杂化学反应的过程
D
【巩固构建】
6.(2017·海南中考)海南石碌铁矿,其矿石主要成分为Fe2O3。炼铁的化学方程式为Fe2O3+3CO 2Fe+3CO2,请计算:某铁矿石,其中含Fe2O3的质量为16 t,理论上可以炼出铁的质量为多少?
解:理论上可以炼出铁的质量为X
3CO+Fe2O3=2Fe+3CO2
高温
160 112
16t X
x=11.2t
答:理论上可以炼出铁的质量为11.2t
160 112
16t x
=
【巩固构建】
7.用800 t含氧化铁80%的赤铁矿石,理论可以炼出含铁99%的生铁多少吨?
解:理论上可以炼出含铁99%的生铁质量为X
3CO+Fe2O3=2Fe+3CO2
高温
160 112
800t×80% 99%X
x=452.5t
答:理论上可以炼出含铁99%的生铁质量为452.5t
160 112
800t×80% 99% x
=
【巩固构建】
同课章节目录
