第九单元 实验活动5 一定溶质质量分数的氯化钠溶液的配制(课件14页)
文档属性
| 名称 | 第九单元 实验活动5 一定溶质质量分数的氯化钠溶液的配制(课件14页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-19 10:22:48 | ||
图片预览






文档简介
(共14张PPT)
一、情景引入,导入新知
1、有关溶质的质量分数计算公式有哪几个?
2、有关溶液稀释计算的原理和公式是怎样的?
回顾:
实验活动5 一定溶质质量分数的
氯化钠溶液的配制
第九单元 溶液
二、自主学习,发现疑问
阅读教材P47-48一定溶质质量分数的氯化钠溶液的配制
二、自主学习,发现疑问
01
疑问一
溶液配制过程中有哪些主要步骤?每个步骤需要哪些仪器?各步骤又有哪些注意事项?
通过稀释配制溶液过程中有哪些主要步骤?每一步用到哪些仪器?与用固体溶质和水配制溶液有什么区别?
02
疑问二
步骤 1、 2、 3、 4、 5、
仪器
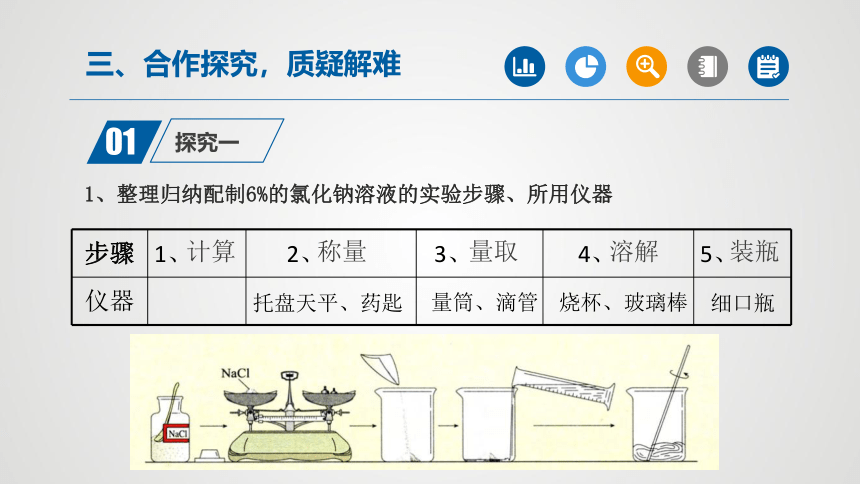
1、整理归纳配制6%的氯化钠溶液的实验步骤、所用仪器
计算
称量
量取
溶解
装瓶
托盘天平、药匙
量筒、滴管
烧杯、玻璃棒
细口瓶
三、合作探究,质疑解难
01
探究一
2、回顾讨论
⑴如何计算配制溶液所需溶质和溶剂的质量?
⑵用托盘天平称量氯化钠固体时应注意哪些问题?
⑶用量筒量取水时应注意哪些问题?
⑷溶解过程中玻璃棒有什么作用?
还有哪些方法可以加速溶解?
三、合作探究,质疑解难
01
探究一
3、学生分组实验
步骤 1、 2、 3、 4、
仪器
1、整理归纳配制6%的氯化钠溶液的实验步骤、所用仪器
计算
量取
混匀
量筒、滴管
烧杯、玻璃棒
细口瓶
装瓶
2、对比讨论
与用固体溶质和水配制溶液有什么区别?
三、合作探究,质疑解难
02
探究二
3、学生分组实验
四、展示归纳,点拨提升
实验步骤与仪器
溶质溶剂配制溶液
注意事项
天平使用注意事项
使用注意事项
稀释配制溶液
一定溶质质量分数的氯化钠溶液的配制
实验步骤与仪器
1、引导总结
⑴根据溶质的质量分数计算公式,溶质质量、溶剂质量偏大或偏小对溶质的质量分数有何影响?
偏大 偏小
溶质质量 溶质的质量分数 。 溶质的质量分数 。
溶剂质量 溶质的质量分数 。 溶质的质量分数 。
偏大
偏大
偏小
偏小
四、展示归纳,点拨提升
2、讨论点拨
⑵下列因素对配制一定溶质质量分数的氯化钠溶液有何影响?
①氯化钠不纯 溶质质量分数 。
②称量氯化钠时天平指针向左偏 溶质质量分数 。
③砝码生锈 溶质质量分数 。
④氯化钠和砝码放反 溶质质量分数 。
⑤氯化钠倒入灯杯时撒落到烧杯外 溶质质量分数 。
⑥量取水时俯视刻度线 溶质质量分数 。
⑦溶解前,烧杯内壁沾有水滴 溶质质量分数 。
⑧溶液配制完毕,部分溶液未倒入试剂瓶 溶质质量分数 。
偏大
偏小
偏大
偏小
偏小
偏大
无影响
偏小
四、展示归纳,点拨提升
2、讨论点拨
五、目标检测,检查效果
01
练习一
某化学课外兴趣小组欲配制80g质量分数为12%的氢氧化钠溶液来制作“叶脉书签”。
(1)需要氢氧化钠固体的质量为 g。
(2)称量时,氢氧化钠固体应放在 (填“滤纸”或“烧杯”)中。
(3)下列说法或操作正确的是 (填字母序号)。
A.配制该溶液时所需的玻璃仪器中只有量筒、烧杯
B.用量程为100mL的量筒量取所需要的水
C.将称量好的固体倒入装有水的量筒中溶解
(4)在量取水的体积时,若采用仰视的方法读数,则所配制的氢氧化钠溶液中溶质的质量分数将 (填“偏大”或“偏小”)。
9.6
烧杯
B
偏小
五、目标检测,检查效果
02
练习二
配制50g质量分数5%的KNO3溶液,作为无土栽培所需的营养液,溶解过程中KNO3的质量分数随时间变化关系如图所示,观察图象,分析形成这种结果的原因是( )
A.所用KNO3固体中含有水分
B.量简量水时俯视刻度线
C.KNO3固体溶解前所用烧杯内有水
D.配好的溶液装瓶时部分液体洒落在试剂瓶外
B
五、目标检测,检查效果
03
练习三
在实验室里,用溶质质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液,回答下列问题:
(1)需溶质质量分数为6%的氯化钠溶液的质量为 g,水的质量为 g ;
(2)实验过程主要步骤有计算、 、混匀、装瓶等;
(3)若用量筒量取水时仰视读数,而其它操作均正确,则所得溶液中溶质质量分数 (选填“大于”“小于”或“等于”)3%;
(4)混匀时用到的玻璃仪器有烧杯、 。
25
25
量取
小于
玻璃棒
再见!
一、情景引入,导入新知
1、有关溶质的质量分数计算公式有哪几个?
2、有关溶液稀释计算的原理和公式是怎样的?
回顾:
实验活动5 一定溶质质量分数的
氯化钠溶液的配制
第九单元 溶液
二、自主学习,发现疑问
阅读教材P47-48一定溶质质量分数的氯化钠溶液的配制
二、自主学习,发现疑问
01
疑问一
溶液配制过程中有哪些主要步骤?每个步骤需要哪些仪器?各步骤又有哪些注意事项?
通过稀释配制溶液过程中有哪些主要步骤?每一步用到哪些仪器?与用固体溶质和水配制溶液有什么区别?
02
疑问二
步骤 1、 2、 3、 4、 5、
仪器
1、整理归纳配制6%的氯化钠溶液的实验步骤、所用仪器
计算
称量
量取
溶解
装瓶
托盘天平、药匙
量筒、滴管
烧杯、玻璃棒
细口瓶
三、合作探究,质疑解难
01
探究一
2、回顾讨论
⑴如何计算配制溶液所需溶质和溶剂的质量?
⑵用托盘天平称量氯化钠固体时应注意哪些问题?
⑶用量筒量取水时应注意哪些问题?
⑷溶解过程中玻璃棒有什么作用?
还有哪些方法可以加速溶解?
三、合作探究,质疑解难
01
探究一
3、学生分组实验
步骤 1、 2、 3、 4、
仪器
1、整理归纳配制6%的氯化钠溶液的实验步骤、所用仪器
计算
量取
混匀
量筒、滴管
烧杯、玻璃棒
细口瓶
装瓶
2、对比讨论
与用固体溶质和水配制溶液有什么区别?
三、合作探究,质疑解难
02
探究二
3、学生分组实验
四、展示归纳,点拨提升
实验步骤与仪器
溶质溶剂配制溶液
注意事项
天平使用注意事项
使用注意事项
稀释配制溶液
一定溶质质量分数的氯化钠溶液的配制
实验步骤与仪器
1、引导总结
⑴根据溶质的质量分数计算公式,溶质质量、溶剂质量偏大或偏小对溶质的质量分数有何影响?
偏大 偏小
溶质质量 溶质的质量分数 。 溶质的质量分数 。
溶剂质量 溶质的质量分数 。 溶质的质量分数 。
偏大
偏大
偏小
偏小
四、展示归纳,点拨提升
2、讨论点拨
⑵下列因素对配制一定溶质质量分数的氯化钠溶液有何影响?
①氯化钠不纯 溶质质量分数 。
②称量氯化钠时天平指针向左偏 溶质质量分数 。
③砝码生锈 溶质质量分数 。
④氯化钠和砝码放反 溶质质量分数 。
⑤氯化钠倒入灯杯时撒落到烧杯外 溶质质量分数 。
⑥量取水时俯视刻度线 溶质质量分数 。
⑦溶解前,烧杯内壁沾有水滴 溶质质量分数 。
⑧溶液配制完毕,部分溶液未倒入试剂瓶 溶质质量分数 。
偏大
偏小
偏大
偏小
偏小
偏大
无影响
偏小
四、展示归纳,点拨提升
2、讨论点拨
五、目标检测,检查效果
01
练习一
某化学课外兴趣小组欲配制80g质量分数为12%的氢氧化钠溶液来制作“叶脉书签”。
(1)需要氢氧化钠固体的质量为 g。
(2)称量时,氢氧化钠固体应放在 (填“滤纸”或“烧杯”)中。
(3)下列说法或操作正确的是 (填字母序号)。
A.配制该溶液时所需的玻璃仪器中只有量筒、烧杯
B.用量程为100mL的量筒量取所需要的水
C.将称量好的固体倒入装有水的量筒中溶解
(4)在量取水的体积时,若采用仰视的方法读数,则所配制的氢氧化钠溶液中溶质的质量分数将 (填“偏大”或“偏小”)。
9.6
烧杯
B
偏小
五、目标检测,检查效果
02
练习二
配制50g质量分数5%的KNO3溶液,作为无土栽培所需的营养液,溶解过程中KNO3的质量分数随时间变化关系如图所示,观察图象,分析形成这种结果的原因是( )
A.所用KNO3固体中含有水分
B.量简量水时俯视刻度线
C.KNO3固体溶解前所用烧杯内有水
D.配好的溶液装瓶时部分液体洒落在试剂瓶外
B
五、目标检测,检查效果
03
练习三
在实验室里,用溶质质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液,回答下列问题:
(1)需溶质质量分数为6%的氯化钠溶液的质量为 g,水的质量为 g ;
(2)实验过程主要步骤有计算、 、混匀、装瓶等;
(3)若用量筒量取水时仰视读数,而其它操作均正确,则所得溶液中溶质质量分数 (选填“大于”“小于”或“等于”)3%;
(4)混匀时用到的玻璃仪器有烧杯、 。
25
25
量取
小于
玻璃棒
再见!
同课章节目录
