高中化学人教版必修1第一章第一节《化学实验安全、过滤和蒸发》教学课件(29张ppt)
文档属性
| 名称 | 高中化学人教版必修1第一章第一节《化学实验安全、过滤和蒸发》教学课件(29张ppt) |
|
|
| 格式 | ppt | ||
| 文件大小 | 13.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-19 00:00:00 | ||
图片预览






文档简介
(共29张PPT)
成
化学与材料
化学与能源
化学与环境
化学与医药
美B-2隐形轰炸机
火箭升空
光化学烟雾
结晶牛胰岛素
为什么要学化学?
第一节:化学实验基本方法 第1课时:化学实验安全、过滤和蒸发
学习目标
一.了解实验安全措施和一般事故处理方法,能识别化学品安全使用标志
二.掌握过滤、蒸发的原理和实验操作
三.掌握检验SO42-的原理和方法
化学实验室爆炸
危险化学品运输车辆起火
思考:我们做实验时应注意哪些问题?
1.了解实验室的安全守则
一、化学实验安全
2.了解安全措施
(如药品安全存放,意外事故的处理)
3.掌握正确的操作方法
(如仪器和药品的使用)
4.重视并逐步熟悉污染物和废弃物的处理方法
浓硫酸
固体NaOH
亚硫酸钠
常见的药品安全存放
一、化学实验安全
固体
液体
密封保存
钾
(
)
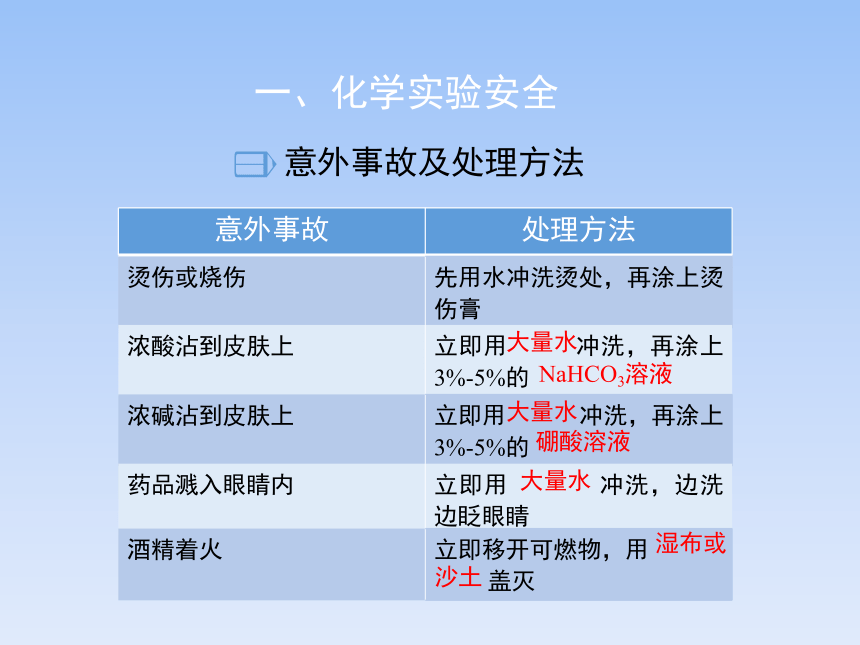
意外事故及处理方法
一、化学实验安全
意外事故 处理方法
烫伤或烧伤 先用水冲洗烫处,再涂上烫伤膏
浓酸沾到皮肤上 立即用 冲洗,再涂上3%-5%的
大量水
NaHCO3溶液
浓碱沾到皮肤上 立即用 冲洗,再涂上3%-5%的
大量水
硼酸溶液
药品溅入眼睛内 立即用 冲洗,边洗边眨眼睛
大量水
酒精着火 立即移开可燃物,用
盖灭
湿布或
沙土
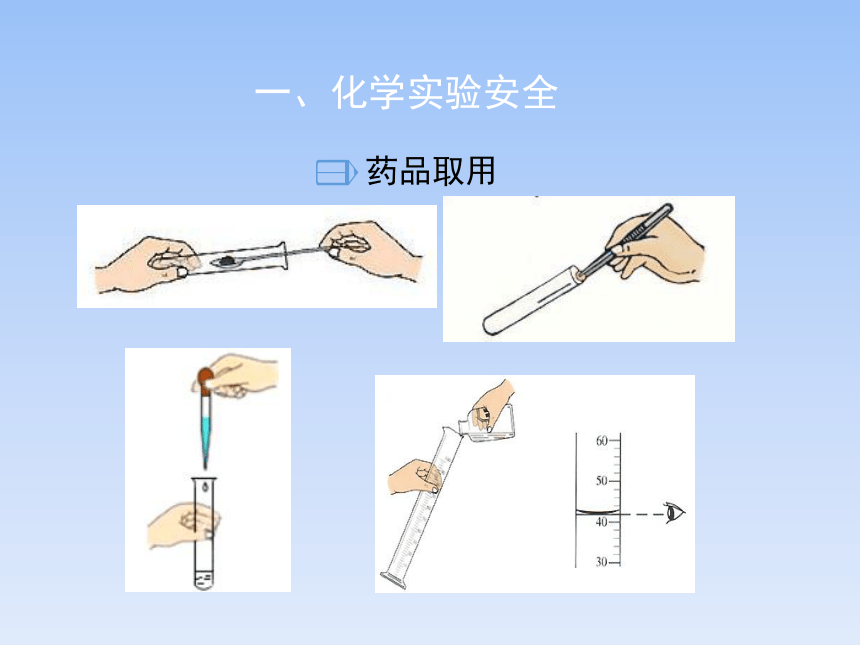
药品取用
一、化学实验安全
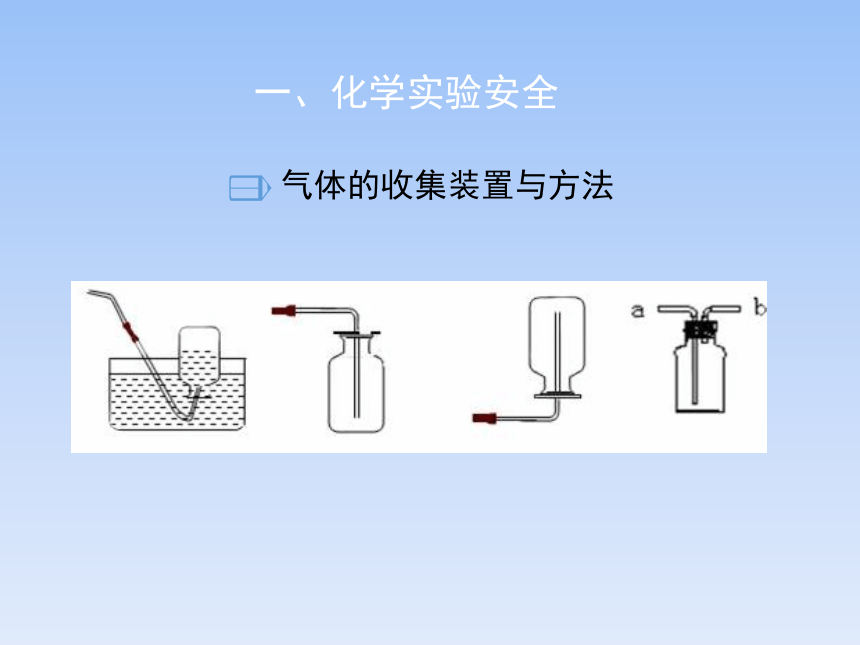
气体的收集装置与方法
一、化学实验安全
常用危险化学品的标志
一、化学实验安全
你知道金子是从哪里来的吗?
千淘万漉虽辛苦,
吹尽狂沙始到金。
——唐 刘禹锡《浪淘沙》
思考与交流
“吹尽狂沙始到金”,那淘金者又是利用什么性质和方法将金子从沙子里分离出来的呢?
将混合物中各组成物质分开,得到比较纯净的物质,并且要求恢复到原来状态(或指定的状态)称为物质的分离。
将混合物中的主要成分(或某种指定物质)净化,而把其他杂质除去,称为物质的提纯。
二.混合物的分离和提纯
(一)混合物质的分离
(二)混合物质的提纯
操作要点:一贴、二低、三靠
①过滤:
利用物质的溶解性不同分离难溶物与可溶物。
二.混合物的分离和提纯
过滤、蒸发的概念及原理
②蒸发:
利用溶液中溶质与溶剂沸点不同加热使溶剂挥发,分离溶质与溶剂。
操作要点:搅拌,大量晶体析出时,余热蒸干。
二.混合物的分离和提纯
过滤、蒸发的概念及原理
实验1-1
观察并思考:实验采用了哪些分离和提纯的方法?玻璃棒的作用是什么?
粗盐的提纯
二.混合物的分离和提纯
点击图片观看视频
优教提示:点击工具栏中课件素材,也能播放视频。
玻璃棒的4个作用:
粗盐的提纯
搅拌,加速溶解
引流
转移固体
搅拌,使受热均匀,防止液体飞溅
二.混合物的分离和提纯
粗盐的提纯
过滤
蒸发
溶解
步骤
目的
从溶液中得到食盐晶体
除去粗盐水中的不溶性杂质
使可溶性物质溶解
现象
不溶物留在滤纸上,液体沿漏斗颈流入另一个烧杯中
水分蒸发,逐渐析出晶体
粗盐逐渐溶解得到浑浊的食盐水
认真完成
根据现象完成课本P6页表格填写
二.混合物的分离和提纯
想一想:我们所得到的产物是纯净物吗?可能还含有什么杂质没有除去?
粗盐的提纯
二.混合物的分离和提纯
粗盐
溶解
悬浊液(泥沙、NaCl、MgCl2、CaCl2、硫酸盐)
过滤
不溶性杂质
(除去)
NaCl、MgCl2、CaCl2、硫酸盐的溶液
粗盐的提纯
如何检验SO42-
二.混合物的分离和提纯
实验1-2:
SO42-的检验及除杂
产生白色沉淀
加HCl
排除CO32-等离子的干扰!
无现象
粗盐水(NaCl)
结论:存在SO42-。
加BaCl2溶液
二.混合物的分离和提纯
要除去可溶杂质离子是:
Ca2+
Mg2+
SO42-
选择要加入的除杂试剂:
Na2CO3
NaOH
BaCl2
引入了新的离子:
CO32-
OH-
Ba2+
BaCO3↓
HCl
SO42-的检验及除杂
二.混合物的分离和提纯
1.BaCl2→NaOH →Na2CO3 HCl
过滤
3.NaOH→BaCl2→Na2CO3 HCl
过滤
2.BaCl2→Na2CO3→NaOH HCl
过滤
注意:Na2CO3要加在BaCl2之后
过滤后的滤液中加稀盐酸
SO42-的检验及除杂
加入除杂试剂的顺序可以是:
二.混合物的分离和提纯
应用-硫酸根离子的检验:
SO42-的检验及除杂
1.检验 Na2CO3中是否含有 Na2SO4
应排除 CO32-干扰——用酸
HCl和 BaCl2或 HNO3 和 BaCl2
2.混合物中可能含有CO32-、 SO42-、Ag+ ,检验是否含有SO42-
应排除CO32-、Ag+干扰
先加 HCl 检验是否有Ag+,且排除 CO 32-干扰;再加 BaCl2
3.检验Na2SO3中是否含有SO42-
排除SO32-的干扰——用酸,但避免引入HNO3
一般用BaCl2和HCl
4.检验一未知溶液中是否含有SO42-
考虑CO32-、Ag+ 、 SO32-的干扰
最佳方法——HCl酸化的 BaCl 2
二.混合物的分离和提纯
在设计除杂方案时,应考虑哪些方面内容,才能顺利完成实验设计?
1)选择所加试剂
2)试剂加入的先后顺序
3)试剂用量
4)试剂过量后如何处理
SO42-的检验及除杂
二.混合物的分离和提纯
不增
不减
易分
不增加新的杂质
不消耗被提纯的物质
如:不能减少NaCl成分
杂质转换为沉淀、气体等易分离
除去。如:将NaCl溶液中可能存
在的Na2SO4转换为沉淀BaSO4
复原
除去各种杂质,还原到目标产物
SO42-的检验及除杂
除杂原则:
二.混合物的分离和提纯
1、向某工厂排放出的澄清废液中,加入BaCl2溶液,产生白色沉淀,再加入足量的硝酸,沉淀部分溶解并产生能使澄清石灰水变浑浊的气体,则下列说法中正确的是( )
A.废液中一定含有Ag+
B.废液中一定含有CO32-
C.废液中一定含有SO42-
D.废液中一定含有H2SO4
课堂练习
B
课堂练习
3、为除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,再进行下列操作:①过滤②加过量的NaOH溶液③加适量的盐酸④加过量的Na2CO3溶液⑤加过量的BaCl2溶液。正确的排列顺序是
___________ _
①⑤②④①③
或①②⑤④①③
2、下列各组固体混合物中,适宜用溶解、过滤、蒸发的操作顺序进行分离的是( )
A.NaCl和NaNO3 B.CaCO3和MnO2
C.NaOH和NaNO3 D.CaCO3和Na2CO3
D
End
Thank
you
结束
成
化学与材料
化学与能源
化学与环境
化学与医药
美B-2隐形轰炸机
火箭升空
光化学烟雾
结晶牛胰岛素
为什么要学化学?
第一节:化学实验基本方法 第1课时:化学实验安全、过滤和蒸发
学习目标
一.了解实验安全措施和一般事故处理方法,能识别化学品安全使用标志
二.掌握过滤、蒸发的原理和实验操作
三.掌握检验SO42-的原理和方法
化学实验室爆炸
危险化学品运输车辆起火
思考:我们做实验时应注意哪些问题?
1.了解实验室的安全守则
一、化学实验安全
2.了解安全措施
(如药品安全存放,意外事故的处理)
3.掌握正确的操作方法
(如仪器和药品的使用)
4.重视并逐步熟悉污染物和废弃物的处理方法
浓硫酸
固体NaOH
亚硫酸钠
常见的药品安全存放
一、化学实验安全
固体
液体
密封保存
钾
(
)
意外事故及处理方法
一、化学实验安全
意外事故 处理方法
烫伤或烧伤 先用水冲洗烫处,再涂上烫伤膏
浓酸沾到皮肤上 立即用 冲洗,再涂上3%-5%的
大量水
NaHCO3溶液
浓碱沾到皮肤上 立即用 冲洗,再涂上3%-5%的
大量水
硼酸溶液
药品溅入眼睛内 立即用 冲洗,边洗边眨眼睛
大量水
酒精着火 立即移开可燃物,用
盖灭
湿布或
沙土
药品取用
一、化学实验安全
气体的收集装置与方法
一、化学实验安全
常用危险化学品的标志
一、化学实验安全
你知道金子是从哪里来的吗?
千淘万漉虽辛苦,
吹尽狂沙始到金。
——唐 刘禹锡《浪淘沙》
思考与交流
“吹尽狂沙始到金”,那淘金者又是利用什么性质和方法将金子从沙子里分离出来的呢?
将混合物中各组成物质分开,得到比较纯净的物质,并且要求恢复到原来状态(或指定的状态)称为物质的分离。
将混合物中的主要成分(或某种指定物质)净化,而把其他杂质除去,称为物质的提纯。
二.混合物的分离和提纯
(一)混合物质的分离
(二)混合物质的提纯
操作要点:一贴、二低、三靠
①过滤:
利用物质的溶解性不同分离难溶物与可溶物。
二.混合物的分离和提纯
过滤、蒸发的概念及原理
②蒸发:
利用溶液中溶质与溶剂沸点不同加热使溶剂挥发,分离溶质与溶剂。
操作要点:搅拌,大量晶体析出时,余热蒸干。
二.混合物的分离和提纯
过滤、蒸发的概念及原理
实验1-1
观察并思考:实验采用了哪些分离和提纯的方法?玻璃棒的作用是什么?
粗盐的提纯
二.混合物的分离和提纯
点击图片观看视频
优教提示:点击工具栏中课件素材,也能播放视频。
玻璃棒的4个作用:
粗盐的提纯
搅拌,加速溶解
引流
转移固体
搅拌,使受热均匀,防止液体飞溅
二.混合物的分离和提纯
粗盐的提纯
过滤
蒸发
溶解
步骤
目的
从溶液中得到食盐晶体
除去粗盐水中的不溶性杂质
使可溶性物质溶解
现象
不溶物留在滤纸上,液体沿漏斗颈流入另一个烧杯中
水分蒸发,逐渐析出晶体
粗盐逐渐溶解得到浑浊的食盐水
认真完成
根据现象完成课本P6页表格填写
二.混合物的分离和提纯
想一想:我们所得到的产物是纯净物吗?可能还含有什么杂质没有除去?
粗盐的提纯
二.混合物的分离和提纯
粗盐
溶解
悬浊液(泥沙、NaCl、MgCl2、CaCl2、硫酸盐)
过滤
不溶性杂质
(除去)
NaCl、MgCl2、CaCl2、硫酸盐的溶液
粗盐的提纯
如何检验SO42-
二.混合物的分离和提纯
实验1-2:
SO42-的检验及除杂
产生白色沉淀
加HCl
排除CO32-等离子的干扰!
无现象
粗盐水(NaCl)
结论:存在SO42-。
加BaCl2溶液
二.混合物的分离和提纯
要除去可溶杂质离子是:
Ca2+
Mg2+
SO42-
选择要加入的除杂试剂:
Na2CO3
NaOH
BaCl2
引入了新的离子:
CO32-
OH-
Ba2+
BaCO3↓
HCl
SO42-的检验及除杂
二.混合物的分离和提纯
1.BaCl2→NaOH →Na2CO3 HCl
过滤
3.NaOH→BaCl2→Na2CO3 HCl
过滤
2.BaCl2→Na2CO3→NaOH HCl
过滤
注意:Na2CO3要加在BaCl2之后
过滤后的滤液中加稀盐酸
SO42-的检验及除杂
加入除杂试剂的顺序可以是:
二.混合物的分离和提纯
应用-硫酸根离子的检验:
SO42-的检验及除杂
1.检验 Na2CO3中是否含有 Na2SO4
应排除 CO32-干扰——用酸
HCl和 BaCl2或 HNO3 和 BaCl2
2.混合物中可能含有CO32-、 SO42-、Ag+ ,检验是否含有SO42-
应排除CO32-、Ag+干扰
先加 HCl 检验是否有Ag+,且排除 CO 32-干扰;再加 BaCl2
3.检验Na2SO3中是否含有SO42-
排除SO32-的干扰——用酸,但避免引入HNO3
一般用BaCl2和HCl
4.检验一未知溶液中是否含有SO42-
考虑CO32-、Ag+ 、 SO32-的干扰
最佳方法——HCl酸化的 BaCl 2
二.混合物的分离和提纯
在设计除杂方案时,应考虑哪些方面内容,才能顺利完成实验设计?
1)选择所加试剂
2)试剂加入的先后顺序
3)试剂用量
4)试剂过量后如何处理
SO42-的检验及除杂
二.混合物的分离和提纯
不增
不减
易分
不增加新的杂质
不消耗被提纯的物质
如:不能减少NaCl成分
杂质转换为沉淀、气体等易分离
除去。如:将NaCl溶液中可能存
在的Na2SO4转换为沉淀BaSO4
复原
除去各种杂质,还原到目标产物
SO42-的检验及除杂
除杂原则:
二.混合物的分离和提纯
1、向某工厂排放出的澄清废液中,加入BaCl2溶液,产生白色沉淀,再加入足量的硝酸,沉淀部分溶解并产生能使澄清石灰水变浑浊的气体,则下列说法中正确的是( )
A.废液中一定含有Ag+
B.废液中一定含有CO32-
C.废液中一定含有SO42-
D.废液中一定含有H2SO4
课堂练习
B
课堂练习
3、为除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,再进行下列操作:①过滤②加过量的NaOH溶液③加适量的盐酸④加过量的Na2CO3溶液⑤加过量的BaCl2溶液。正确的排列顺序是
___________ _
①⑤②④①③
或①②⑤④①③
2、下列各组固体混合物中,适宜用溶解、过滤、蒸发的操作顺序进行分离的是( )
A.NaCl和NaNO3 B.CaCO3和MnO2
C.NaOH和NaNO3 D.CaCO3和Na2CO3
D
End
Thank
you
结束
