基态原子的核外电子排布
图片预览







文档简介
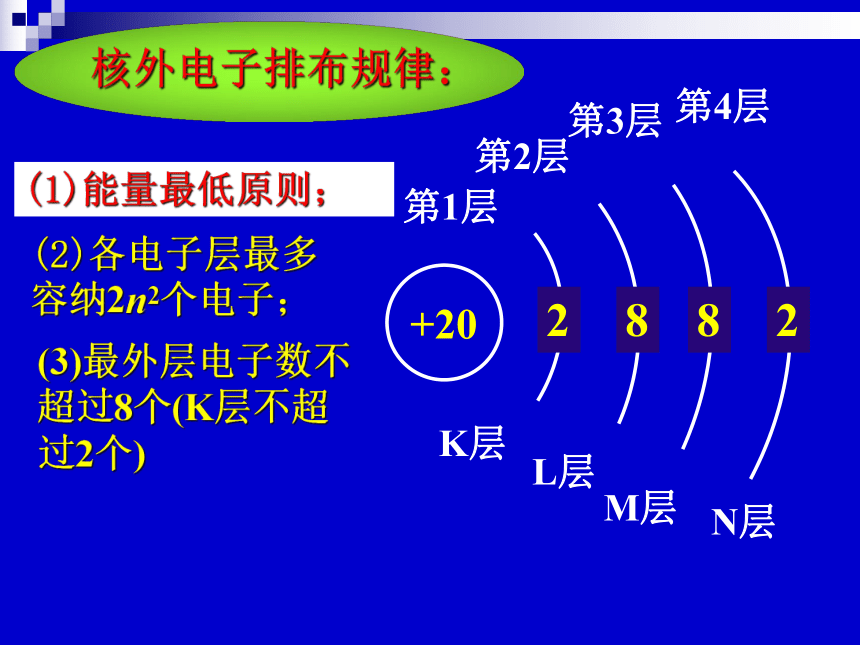
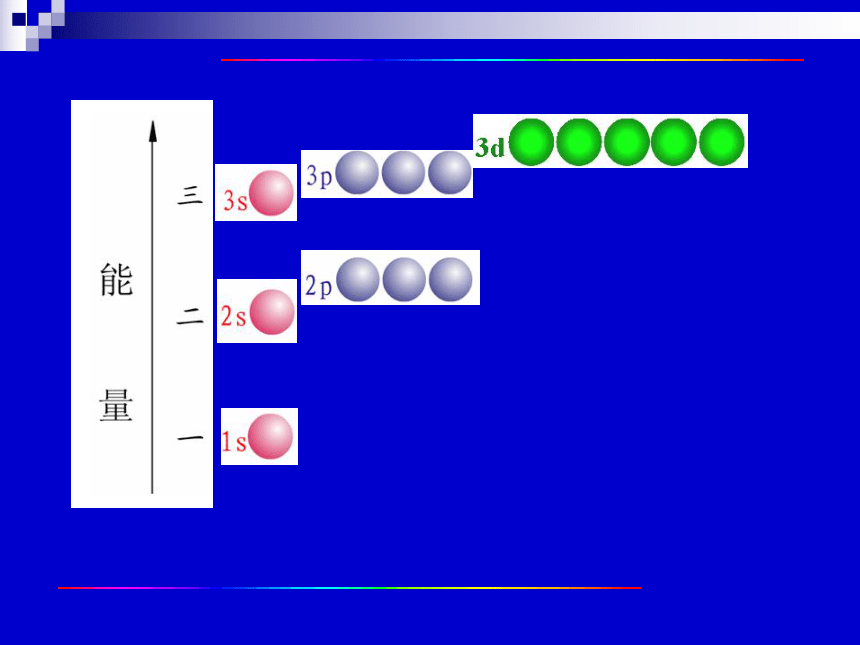
课件29张PPT。基态原子的核外电子排布集美中学 唐兵 Ca的原子核外电子排布情况如何? 核外电子排布规律:(3)最外层电子数不超过8个(K层不超过2个)(2)各电子层最多容纳2n2个电子;核外电子排布规律:(1)能量最低原则;?核外电子排布规律: 从能级的角度看,能量由低到高的顺序是怎样的?试以第一、二、三能层所含能级加以说明。 ↑ H: 1s1H: 1s1电子层数电子排布式nl x轨道类型电子个数He的核外电子排布式是怎样的?一个原子轨道最多可以容纳几个电子?泡利不相容原理 一个原子轨道中最多只能容纳两个电子,且这两个电子的自旋方向必须相反,此时体系最稳定,原子的总能量最低。 核外电子排布规律: 泡利(Pauli),奥地利科学家,对于量子力学的形成以及原子结构理论的发展有重大的贡献,获得1945年诺贝尔物理奖。他对科学理论有着很深刻的洞察力,语锋犀利,被称为“理论物理学的心脏” 。 泡利不相容原理电子排布式1s 轨道表示式 用一个○表示一个原子轨道,在○中用“↑”或“↓”表示该轨道上排入的电子。He: 1s2原子结构示意图电子排布式Li: 1s22s1请写出4~10号元素原子的电子排布式。 4 铍Be 1s2 2s2
5 硼B 1s2 2s22p1
6 碳C 1s2 2s22p2
7 氮N 1s2 2s22p3
8 氧O 1s2 2s22p4
9 氟F 1s2 2s22p5
10氖Ne 1s2 2s22p6总结第二周期元素原子核外电子排布特点C 1s2 2s22p2
依据能量最低原则和泡利不相容原理,画出C原子可能的轨道表示式洪特规则 对于基态原子,电子在能量相同的轨道上排布时,将尽可能分占不同的轨道并且自旋方向相同。 C 1s2 2s22p2
核外电子排布规律:洪特规则 对于基态原子,电子在能量相同的轨道上排布时,将尽可能分占不同的轨道并且自旋方向相同。 C 1s2 2s22p2
请写出11~18号元素原子的电子排布式。 11钠Na [Ne] 3s1
12镁Mg [Ne] 3s2
13铝Al [Ne] 3s23p1
14硅Si [Ne] 3s23p2
15磷P [Ne] 3s23p3
16硫S [Ne] 3s23p4
17氯Cl [Ne] 3s23p5
18氩Ar [Ne] 3s23p6 电子排布简式:总结第三周期元素原子核外电子排布特点请画出S元素的轨道表示式钙Ca [Ar] 4s2钙Ca能级交错核 外 电 子 填 充 顺 序 图能级顺序:ns、(n-2)f、(n-1)d、np 请写出19~36号的电子排布式的简式,并仔细对照周期表,观察是否所有原子电子排布都符合前面的排布规律。
洪特规则的特例: 对于能量相同的轨道(同一电子亚层),当电子排布处于全满(p6、d10、f14)、半满(p3、d5、f7)、全空(p0、d0、f0)时比较稳定,整个体系的能量最低。 24Cr: [Ar]3d54s129Cu:[Ar]3d104s1小结:一、原子核外电子排布遵循的原理和规则二、原子核外电子排布的表示式能量最低原则泡利不相容原理洪特规则(特例)电子排布式轨道表示式三、能级顺序ns、(n-2)f、(n-1)d、np巩固练习:1、E代表能量,请将下列轨道按能量由低到高的顺序排列:
E3s、 E3p、E3d、E4s答案: E3s ﹤E3p ﹤ E4s ﹤ E3d2、以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断正误,若错误,哪些违反了泡利不相容原理,哪些违反了洪特规则?
(1) (2) (3)
(4)
(5)
(6)答案:(1)(6)违反泡利不相容原理、 (2)(4)(5)违反洪特规则、(3)正确3、填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为——。
(2)B元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,B的元素符号为——,其基态原子的电子排布简式为——。答案:(1)N
(2)Cu,[Ar]3d104s1谢谢大家!
5 硼B 1s2 2s22p1
6 碳C 1s2 2s22p2
7 氮N 1s2 2s22p3
8 氧O 1s2 2s22p4
9 氟F 1s2 2s22p5
10氖Ne 1s2 2s22p6总结第二周期元素原子核外电子排布特点C 1s2 2s22p2
依据能量最低原则和泡利不相容原理,画出C原子可能的轨道表示式洪特规则 对于基态原子,电子在能量相同的轨道上排布时,将尽可能分占不同的轨道并且自旋方向相同。 C 1s2 2s22p2
核外电子排布规律:洪特规则 对于基态原子,电子在能量相同的轨道上排布时,将尽可能分占不同的轨道并且自旋方向相同。 C 1s2 2s22p2
请写出11~18号元素原子的电子排布式。 11钠Na [Ne] 3s1
12镁Mg [Ne] 3s2
13铝Al [Ne] 3s23p1
14硅Si [Ne] 3s23p2
15磷P [Ne] 3s23p3
16硫S [Ne] 3s23p4
17氯Cl [Ne] 3s23p5
18氩Ar [Ne] 3s23p6 电子排布简式:总结第三周期元素原子核外电子排布特点请画出S元素的轨道表示式钙Ca [Ar] 4s2钙Ca能级交错核 外 电 子 填 充 顺 序 图能级顺序:ns、(n-2)f、(n-1)d、np 请写出19~36号的电子排布式的简式,并仔细对照周期表,观察是否所有原子电子排布都符合前面的排布规律。
洪特规则的特例: 对于能量相同的轨道(同一电子亚层),当电子排布处于全满(p6、d10、f14)、半满(p3、d5、f7)、全空(p0、d0、f0)时比较稳定,整个体系的能量最低。 24Cr: [Ar]3d54s129Cu:[Ar]3d104s1小结:一、原子核外电子排布遵循的原理和规则二、原子核外电子排布的表示式能量最低原则泡利不相容原理洪特规则(特例)电子排布式轨道表示式三、能级顺序ns、(n-2)f、(n-1)d、np巩固练习:1、E代表能量,请将下列轨道按能量由低到高的顺序排列:
E3s、 E3p、E3d、E4s答案: E3s ﹤E3p ﹤ E4s ﹤ E3d2、以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断正误,若错误,哪些违反了泡利不相容原理,哪些违反了洪特规则?
(1) (2) (3)
(4)
(5)
(6)答案:(1)(6)违反泡利不相容原理、 (2)(4)(5)违反洪特规则、(3)正确3、填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为——。
(2)B元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,B的元素符号为——,其基态原子的电子排布简式为——。答案:(1)N
(2)Cu,[Ar]3d104s1谢谢大家!
