九年级化学人教版上册 第七单元 《燃料及其利用》 综合复习测试题(WORD版,含答案)
文档属性
| 名称 | 九年级化学人教版上册 第七单元 《燃料及其利用》 综合复习测试题(WORD版,含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 966.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-21 00:00:00 | ||
图片预览



文档简介
第七单元《燃料及其利用》综合复习测试题
可能用到的相对原子质量:H-1 C-12 O-16 Mg-24
一、选择题(共15小题,每小题只有一个选项符合题意。每小题2分,共30分)
1.2020年5月31日是第33个世界无烟日。下列图标中表示禁止吸烟的是( )
A B C D
2.土星是太阳系里气态行星,约含有92.4%H2、7.4%He和0.2%CH4等,平均温度为-150℃。它没燃烧成火球的原因可能有①可燃物种类太多,②氦气含量太高,③没有适宜的温度,④没有支持燃烧的氧气。其中分析正确的一项是( )
A.①② B.①③ C.②④ D.③④
3.下列关于能源的说法不正确的是( )
A.氢气是 21世纪的理想能源
B.科技发展可促进能源的开发利用
C.由于新能源的开发,可以无节制地使用石油资源
D.能源结构向多元、清洁和低碳方向转型
4.下列熄灭蜡烛的方法,其对应原理错误的是( )
A.扇灭——隔绝氧气 B.剪掉灯芯——隔离可燃物
C.湿抹布盖灭——隔绝氧气 D.水浇灭——降低温度至着火点以下
5.2020年5月12日是我国第12个“防灾减灾日”,了解防灾减灾的相关知识,有利于保护人们的生命、财产安全。下列关于火灾、灭火与逃生的说法错误的是( )
A.严禁携带易燃、易爆物品乘坐火车
B.遇火灾,如果火势较大,立即拨打 119 电话报警
C.生活中常用水来灭火,其原理是降低可燃物的着火点
D.从火场中逃生时,应有序撤离着火区域
6.化学反应不仅有新物质生成,而且还伴随能量变化。以下能量变化不是由化学变化引起的是( )
A.鞭炮爆炸发声 B.蜡烛燃烧发光 C.煤燃烧火力发电 D.电水壶通电放热
7.将酒精灯的灯芯拨得松散一些,可使燃烧更旺的原因是( )
A.减少酒精的挥发 B.降低可燃物的着火点
C.增加空气中氧气含量 D.增大可燃物与空气的接触面积
8.页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。下列说法错误的是( )
A.页岩气的主要成分是甲烷
B.页岩气是不可再生能源
C.其完全燃烧的化学方程式为2CH4+3O22CO+4H2O
D.页岩气燃烧放出热量
9.危险化学品泄漏或爆炸事件常给我们敲响安全警钟,操作不当就会存在安全隐患。下列做法不正确的是( )
A.点燃氢气,提前验纯 B.燃气泄漏,点火检查
C.矿井作业,注意通风 D.油库重地,严禁烟火
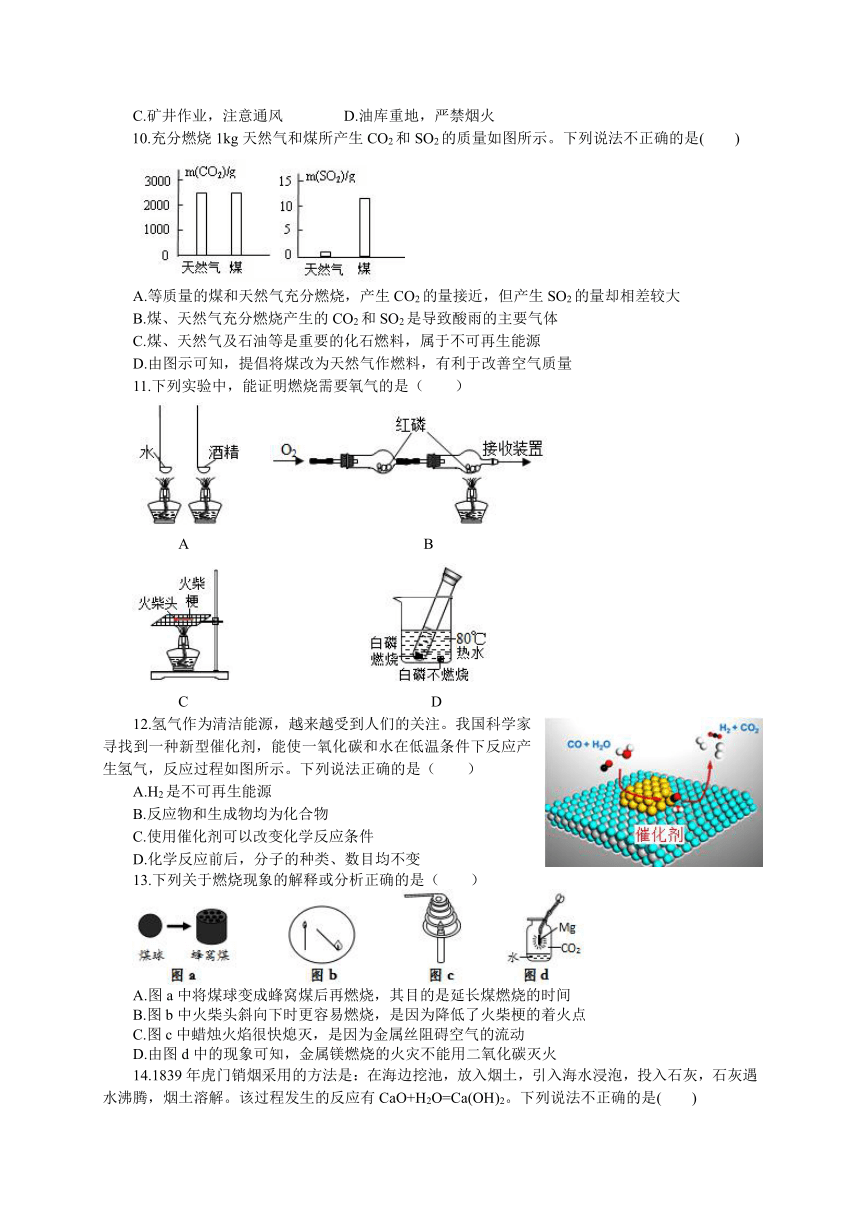
10.充分燃烧1kg天然气和煤所产生CO2和SO2的质量如图所示。下列说法不正确的是( )
A.等质量的煤和天然气充分燃烧,产生CO2的量接近,但产生SO2的量却相差较大
B.煤、天然气充分燃烧产生的CO2和SO2是导致酸雨的主要气体
C.煤、天然气及石油等是重要的化石燃料,属于不可再生能源
D.由图示可知,提倡将煤改为天然气作燃料,有利于改善空气质量
11.下列实验中,能证明燃烧需要氧气的是( )
A B
C D
12.氢气作为清洁能源,越来越受到人们的关注。我国科学家寻找到一种新型催化剂,能使一氧化碳和水在低温条件下反应产生氢气,反应过程如图所示。下列说法正确的是( )
A.H2是不可再生能源
B.反应物和生成物均为化合物
C.使用催化剂可以改变化学反应条件
D.化学反应前后,分子的种类、数目均不变
13.下列关于燃烧现象的解释或分析正确的是( )
A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B.图b中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C.图c中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D.由图d中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
14.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2O=Ca(OH)2。下列说法不正确的是( )
A.该反应属于化合反应
B.该反应会放出热量
C.由此反应推测氧化钙可干燥氯化氢气体
D.此反应可制备氢氧化钙
15.资源、能源利用和环境保护是人类共同关注的问题。下列说法错误的是
A.氢气是一种清洁高能燃料
B.煤、石油、天然气是不可再生的化石能源
C.废旧金属、纸张、塑料的回收利用可以节约相应资源,减少对环境的污染
D.地球上淡水约占全球水储量的96.5%,所以可利用的淡水资源取之不尽用之不竭
二、填空题(共7小题,共44分)
16.(6分)打火机给人们的生活带来了方便,如图为普通打火机的示意图,请回答下列问题:
(1)打火机的制作材料中属于金属材料的是______(填物质的编号)。
(2)打火机打着火时,挡风不锈钢罩并没有燃烧起来,据此说明燃烧需要的条件之一是_______________;而将打火机的开关松开即可熄灭火焰,这种灭火方法的原理是_____________。
(3)打火机中的燃料是丁烷(化学式为C4H10),丁烷完全燃烧产生二氧化碳和水,写出该反应的化学方程式:_____________。
(4)用分子、原子的观点解释丁烷气体能被压缩成液体的原因:_________________。
17.(8分)合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要。
(1)2020年6月17日,湖南省娄底市嘉信华庭小区商住楼一个仓库发生火灾,造成7人死亡。
①从物质燃烧的条件来年看,仓库内存放的纺织品、塑料制品属于___________。
②某商户慌忙打开门窗大声呼救,导致火势迅速扩大。请解释出现这种情况的原因是______________。
③消防队员赶到现场并用高压水枪灭火,水灭火的原理是___________。
④如果你遇到类似的火情,应一边自救,一边拨打火警电话。正确的自救方法是___________,火警电话是___________(均填序号)。
A.用湿手巾捂住口鼻迅速逃离 B.120 C.站原地等待消防队员营救 D.119
(2)分析下表中的数据,回答问题:
物质代号 L M N P
熔点/℃ -117 3550 44 -259
沸点/℃ 78 4827 257 -253
着火点/℃ 510 370 40 580
①有人认为“物质的熔、沸点越高,着火点越高”,该结论_________(填“合理”或“不合理”)。
②已知酒精灯火焰的温度约为500℃。利用上图装置,验证达到可燃物着火点是燃烧的条件之一,上表中可用于完成该实验的两种可燃物是_________和________(填代号)。
18.(5分)合理利用化石燃料资源,是人类不断探索的课题。某城市家用燃料的使用经历了下图所示的过程,并将逐步向理想燃料发展。
(注:括号中的物质是对应燃料的主要成分)
(1)CH4、C3H8两种物质中,氢元素的质量分数较大的是__________(填化学式)。
(2)倡导“家用燃料低碳化”的意义是__________。
(3)一定条件下,仅用一个置换反应即可制得CO和H2,反应的化学方程式为__________。
(4)随着全球能源使用量的增长,化石燃料等不可再生能源将日趋枯竭。请提出一个缓解能源危机的设想:__________。
19.(6分)能源、环境和安全已成为人类日益关注的问题。请回答下列问题。
(1)目前世界上多数国家利用的能量主要来自煤、石油和_______等化石燃料的燃烧。
(2)科技发展可促进新能源的开发利用。下列能源不属于新能源的是_______(选填字母序号)。
A.煤 B.地热能 C.太阳能 D.核能
(3)2020年6月23日,北斗三号最后一颗全球组网卫星发射成功。此次卫星发射用的火箭推进剂为液氢和液氧,其反应产物无污染。写出氢气在氧气中燃烧的化学方程式______。
(4)燃料的充分燃烧对于节约能源、减少环境污染非常重要。汽车化油器将汽油喷成雾状进入内燃机气缸,使汽油充分燃烧。这是通过_______的方法使汽油充分燃烧。
(5)加油站、化工厂、面粉厂等场所的空气中含有较多可燃性气体或粉尘,因此这些场所一定要严禁烟火,防止发生_________。
20.(2015 烟台)(5分)2020年10月20日,山西省左权县发生煤矿瓦斯爆炸事故,造成4人遇难,1人受伤。瓦斯是煤矿矿井下有害气体的总称,它已成为煤矿事故的“头号杀手”。
(1)瓦斯的主要成分是甲烷。甲烷在空气中完全燃烧的化学方程式为______________。
(2)为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是________(填序号,下同)。
A.进矿井前先做灯火实验 B.工人必须戴安全帽才能进入矿井
C.矿井内要加强通风 D.安装瓦斯探头传感器监测瓦斯浓度
(3)矿井下特大瓦斯爆炸事故发生后,专家提出了注入液氮灭火的方案。液氮可用于矿井灭火的原因是__________________、__________________(写出两条)。
21.(8分)目前全球正面临着能源、环境、水资源等方面的危机。因此,开发利用新能源显得格外重要。据报道,太阳能光伏发电在当代得到了大规模的应用和发展。太阳能光伏发电最关键的材料是高纯硅。如图是工业上以石英砂(SiO2)为主要原料制取纯硅的一种方法,请回答下列问题:
(1)发展太阳能产业的主要优点是_________(答一点即可)。
(2)将石英砂粉碎的目的是_________。
(3)焦炭在反应①中体现出来的化学性质是_________。
(4)写出流程中两种氧化物的名称_________、_________。
(5)写出步骤②中发生反应的化学方程式_________。
(6)整个制备硅过程必须达到无水无氧。在反应②的过程中若混入O2,可能引起的后果是_________。
22.(6分)氢气被看作是理想的能源。氢气的制取和储存是氢能源利用领域的研究热点
Ⅰ.氢气的制取
(1)科学家正致力于研究在催化剂和光照条件下分解水制氢气。写出该反应的化学方程式:_____,该反应_______(填“放出”或“吸收”)能量。
(2)水热分解可得氢气,高温下水分解体系中微粒含量与温度的关系如图所示。
图中曲线A、B对应的微粒依次是________(填符号)。
Ⅱ.氢气的储存
(3)一种镁铜合金可用于储氢。
①将镁、铜单质按比例在一定温度下熔炼得到上述合金。熔炼时须通入氩气,其目的是__________。
②350℃时,该镁铜合金与氢气反应,生成了一种仅含Mg、H两种元素的化合物,其中氢元素的质量分数为7.7%。该化合物的化学式为__________。
三、实验探究题(共2小题,共16分)
23.(10分)燃烧既能给人类带来光明和幸福,也能给人类带来灾难和痛苦。某小组在学习物质燃烧条件时进行了探究。老师提供了如下物品:①酒精灯 ②铜片 ③火柴头 ④火柴梗 ⑤沙土 ⑥三脚架。
【查阅资料】火柴头的着火点是260~280℃,火柴梗的着火点为350~400℃。
【实验探究】
探究的内容 实验设计与操作 实验现象 实验结论
探究一燃烧与物质的关系 _________ 可燃物才能燃烧
探究二燃烧与温度的关系 注意:火柴头和火柴梗的位置相对于火焰中心_________(填“对称”或“不对称”) _________ 物质燃烧条件之一是:_________
探究三燃烧与氧气的关系 ①_________ ②_________ _________ 物质燃烧条件之一是:_________
【拓展与应用】
(1)炭火烤羊肉串,是利用了木炭燃烧放出的_________。
(2)下面三个实验都是利用红磷燃烧测定空气中氧气的含量。
实验一是在点燃条件下发生的,实验二是在聚光光照条件下发生的,实验三是在电热丝加热条件下发生的,这三个实验的条件虽然不同,但其实质都是使_________。
24.(6分)化学实验社团在老师的指导下开展了“模拟酸雨形成”的相关实验。
【联想与实验】模仿二氧化碳与水反应进行如图一所示实验:
【问题与猜想】亚硫酸不稳定,为什么红色液体微热后不变为紫色?其原因可能为:
猜想1:加热不够充分
猜想2:与空气中的氮气有关
猜想3:与空气中的氧气有关
【实验与验证】填写表格中的空格。
编号 操作 现象 结论
1 将图一中红色液体继续加热至沸腾 仍为红色 猜想1不成立
2 如图二所示,先通入适量的SO2,然后用酒精灯微热 先变红后变紫 猜想2不成立
3 如图二所示,先通入适量的SO2,再改通入氮气,最后用酒精灯微热 _________
4 如图二所示,先通入适量的SO2,再改通入________,最后用酒精灯微热 _________ 猜想3成立
【分析与结论】红色液体微热后不变为紫色的原因是:H2SO3在空气中会被氧化成另一种酸,进一步实验证明是硫酸。
【应用与拓展】收集某硫酸厂(生产过程中产生SO2)附近刚降到地面的雨水水样,用pH计测得每隔十分钟数据如下表:
测定时间 5:05 5:15 5:25 5:35 5:45
pH 4.95 4.94 4.86 4.85 4.85
(1)分析表中数据,5:15至5:25时间段内水样中主要酸性溶质有_________。
(2)实验社团提出一种处理废气的方案如右图,利用CaCO3粉末、空气为原料在高温下吸收SO2,写出该反应的化学方程式:_________。
四、计算题(共10分)
25.推广车用乙醇汽油,可以减少汽车尾气污染。利用秸秆为原料可生产乙醇(C2H6O),其中包含葡萄糖(C6H12O6)转化为乙醇的反应(C6H12O62C2H6O+2CO2↑)。
(1)请再写出使用乙醇汽油的一点好处:__________。
(2)每生产2.3t乙醇,计算理论上参加反应的葡萄糖的质量(写出计算过程)。
参考答案
1.C
2.D 提示:根据物质燃烧的条件,可燃物燃烧需要与氧气接触并且温度达到着火点,土星中没有氧气,且平均温度为-150℃,温度没有达到氢气、甲烷的着火点,所以不能燃烧。
3.C
4.A
5.C 用水来灭火,其原理是降低可燃物温度到着火点以下,而不能降低可燃物的着火点。
6.D
7.D 提示:将酒精灯的灯芯拨得松散一些,可以增大酒精与空气的接触面积,以促进酒精燃烧。
8.C
9.B
10.B 二氧化硫是造成酸雨的主要气体,而二氧化碳不会导致酸雨,而是导致温室效应,B错误。
11.D 提示:酒精和水分别放在酒精灯上加热,均能与氧气接触,酒精能燃烧,水不能,能证明燃烧需要有可燃物,A错误;红磷均能与氧气接触,左边的红磷不能燃烧,右边的红磷能燃烧,能证明燃烧需要温度达到着火点,B错误;火柴头先燃烧,火柴梗后燃烧,能证明燃烧需要温度达到着火点,C错误;试管中的白磷能与氧气接触,能燃烧,水中的白磷不能与氧气接触,不能燃烧,能证明燃烧需要氧气,D正确。
12.C 提示:由图可知,该反应是一氧化碳和水在催化剂的作用下反应生成氢气和二氧化碳,该反应的化学方程式为。氢气可通过一氧化碳和水在催化剂的作用下制得,故氢气属于可再生能源,A错误;由化学方程式可知,反应物是一氧化碳和水,它们都是由不同种元素组成的化合物,生成物是氢气和二氧化碳,氢气是由同种元素组成的单质,二氧化碳是由不同种元素组成的化合物,B错误;由题干信息可知,使用催化剂后,可使一氧化碳和水在低温的条件下反应,故催化剂可以改变化学反应条件,C正确;由化学方程式可知,分子的种类发生了改变,数目不变,D错误。
13.D
14.C 提示:化合反应的特征是“多变一”,该反应的反应物是两种,生成物是一种,符合化合反应的特征,属于化合反应,A正确;此处的“石灰”是生石灰,“石灰遇水沸腾”,就是说生石灰和水反应能使水沸腾,说明该反应会放出热量,B正确;根据反应CaO+H2O=Ca(OH)2,氧化钙能吸收水分,可用来干燥某些气体,但氧化钙不能干燥氯化氢气体,因为氧化钙会和氯化氢气体发生化学反应,C错误;生石灰和水反应生成氢氧化钙,因此该反应可制备氢氧化钙,D正确。
15.D
16.(1)③④ (2)温度达到着火点 隔离可燃物 (3)2C4H10+13O28CO2+10H2O (4)分子间有间隔(或受压时气体分子间隔缩小等)
17.(1)①可燃物 ②空气进入房间内氧气浓度增大,氧气助火势更旺 ③降低温度到可燃物的着火点以下 ④A D (2)①不合理 ②N M
18.(1)CH4 (2)缓解温室效应(或其他合理答案) (3)C+H2O一定条件CO+H2(或“2CH4+O2一定条件2CO+4H2”等其他合理答案) (4)开发使用新能源(或其他合理答案)
提示:(1)“CH4”中氢、碳原子个数比为4“1,“C3H8”中氢、碳原子个数比为8:3,比较可知,“CH4”中氢元素的质量分数较大。(2)大气中二氧化碳的含量增加,会加剧温室效应,倡导“家用燃料低碳化”可有效减少二氧化碳的排放,从而可减缓温室效应。(3)置换反应指的是一种单质与一种化合物生成另一种单质和另一种化合物的反应,若生成物为CO和H2,可逆推反应物可为C、H2O或CH4、O2,据此可写出反应的化学方程式。(4)缓解能源危机的方法有很多,主要是寻找替代能源,即开发新能源,如太阳能、水能、地热能、潮汐能等。
19.(1)天然气 (2)A (3)2H2+O22H2O (4)增大汽油与氧气的接触面积 (5)爆炸
20.(1)CH4+2O2CO2+2H2O (2)CD (3)氮气不燃烧也不支持燃烧、液氮汽化使温度降低
21.(1)取之不尽(合理即可) (2)增大与焦炭的接触面积,使反应更充分 (3)还原性 (4)一氧化碳、二氧化硅 (5)SiCl4+2H2Si+4HCl (6)氢气和氧气反应引发爆炸
22.(1)2H2O2H2↑+O2 吸收 (2)H、O (3)①防止熔炼时镁、铜与空气反应 ②MgH2
提示:(1)水在催化剂和光照的条件下分解生成氢气和氧气,由于该反应需要在光照条件下进行,说明反应需要吸收能量。(2)水分解生成氢气和氧气,结合反应的化学方程式可知氢、氧原子的个数比为(2×2):(1×2)=2:1,由图像可知,A、B微粒个数比约为2:1,因此A为氢原子、B为氧原子。(3)①由金属单质的化学性质可知镁和铜在加热条件下都易被氧化,因此通入氩气作保护气,可防止高温熔炼时镁和铜与空气反应。②因为氢元素的质量分数为7.7%,则化合物中镁元素的质量分数为1-7.7%=92.3%,所以化合物中镁原子和氧原子的个数比为:=1:2,则化合物的化学式为MgH2。
23.【实验探究】火柴头燃烧,沙土和铜片不能燃烧 对称 火柴头、火柴梗先后燃烧 温度达到着火点 ①隔绝氧气的火柴头 ②暴露在空气中的火柴头 ①处火柴头不能燃烧,②处火柴头燃烧 与氧气接触(与①②对应) 【拓展与应用】(1)热量 (2)红磷燃烧,消耗氧气
24.【探究与验证】先变红后变紫 氧气(或O2) 先变红色,后仍为红色
【应用与拓展】(1)H2SO3和H2SO4 (2)2CaCO3+2SO2+2O22CaSO4+2CO2
提示:【探究与验证】根据结论猜想2不成立,可以分析出观察到的现象为先变红后变紫。根据结论猜想3成立。分析出操作:通入O2,观察到的现象为:先变红,加热后仍为红色。【应用与拓展】(1)5:15-5:25,从表格可以看出酸性在增强,结合资料信息与探究与验证可以分析出水样中主要酸性溶质有H2SO3、H2SO4。(2)结合题干与废气处理方案图可知反应物为SO2、空气中O2、CaCO3;生成物CO2为CaSO4;反应条件高温。该反应的方程式为2CaCO3+2SO2+2O22CaSO4+2CO2。
25.(1)节约化石燃料
(2)设参加反应的葡萄糖的质量为x。
C6H12O62C2H6O+2CO2↑
180 92
x 2.3t
x=4.5t
答:理论上参加反应的葡萄糖的质量为4.5t。
薄铜片
可能用到的相对原子质量:H-1 C-12 O-16 Mg-24
一、选择题(共15小题,每小题只有一个选项符合题意。每小题2分,共30分)
1.2020年5月31日是第33个世界无烟日。下列图标中表示禁止吸烟的是( )
A B C D
2.土星是太阳系里气态行星,约含有92.4%H2、7.4%He和0.2%CH4等,平均温度为-150℃。它没燃烧成火球的原因可能有①可燃物种类太多,②氦气含量太高,③没有适宜的温度,④没有支持燃烧的氧气。其中分析正确的一项是( )
A.①② B.①③ C.②④ D.③④
3.下列关于能源的说法不正确的是( )
A.氢气是 21世纪的理想能源
B.科技发展可促进能源的开发利用
C.由于新能源的开发,可以无节制地使用石油资源
D.能源结构向多元、清洁和低碳方向转型
4.下列熄灭蜡烛的方法,其对应原理错误的是( )
A.扇灭——隔绝氧气 B.剪掉灯芯——隔离可燃物
C.湿抹布盖灭——隔绝氧气 D.水浇灭——降低温度至着火点以下
5.2020年5月12日是我国第12个“防灾减灾日”,了解防灾减灾的相关知识,有利于保护人们的生命、财产安全。下列关于火灾、灭火与逃生的说法错误的是( )
A.严禁携带易燃、易爆物品乘坐火车
B.遇火灾,如果火势较大,立即拨打 119 电话报警
C.生活中常用水来灭火,其原理是降低可燃物的着火点
D.从火场中逃生时,应有序撤离着火区域
6.化学反应不仅有新物质生成,而且还伴随能量变化。以下能量变化不是由化学变化引起的是( )
A.鞭炮爆炸发声 B.蜡烛燃烧发光 C.煤燃烧火力发电 D.电水壶通电放热
7.将酒精灯的灯芯拨得松散一些,可使燃烧更旺的原因是( )
A.减少酒精的挥发 B.降低可燃物的着火点
C.增加空气中氧气含量 D.增大可燃物与空气的接触面积
8.页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。下列说法错误的是( )
A.页岩气的主要成分是甲烷
B.页岩气是不可再生能源
C.其完全燃烧的化学方程式为2CH4+3O22CO+4H2O
D.页岩气燃烧放出热量
9.危险化学品泄漏或爆炸事件常给我们敲响安全警钟,操作不当就会存在安全隐患。下列做法不正确的是( )
A.点燃氢气,提前验纯 B.燃气泄漏,点火检查
C.矿井作业,注意通风 D.油库重地,严禁烟火
10.充分燃烧1kg天然气和煤所产生CO2和SO2的质量如图所示。下列说法不正确的是( )
A.等质量的煤和天然气充分燃烧,产生CO2的量接近,但产生SO2的量却相差较大
B.煤、天然气充分燃烧产生的CO2和SO2是导致酸雨的主要气体
C.煤、天然气及石油等是重要的化石燃料,属于不可再生能源
D.由图示可知,提倡将煤改为天然气作燃料,有利于改善空气质量
11.下列实验中,能证明燃烧需要氧气的是( )
A B
C D
12.氢气作为清洁能源,越来越受到人们的关注。我国科学家寻找到一种新型催化剂,能使一氧化碳和水在低温条件下反应产生氢气,反应过程如图所示。下列说法正确的是( )
A.H2是不可再生能源
B.反应物和生成物均为化合物
C.使用催化剂可以改变化学反应条件
D.化学反应前后,分子的种类、数目均不变
13.下列关于燃烧现象的解释或分析正确的是( )
A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B.图b中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C.图c中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D.由图d中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
14.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2O=Ca(OH)2。下列说法不正确的是( )
A.该反应属于化合反应
B.该反应会放出热量
C.由此反应推测氧化钙可干燥氯化氢气体
D.此反应可制备氢氧化钙
15.资源、能源利用和环境保护是人类共同关注的问题。下列说法错误的是
A.氢气是一种清洁高能燃料
B.煤、石油、天然气是不可再生的化石能源
C.废旧金属、纸张、塑料的回收利用可以节约相应资源,减少对环境的污染
D.地球上淡水约占全球水储量的96.5%,所以可利用的淡水资源取之不尽用之不竭
二、填空题(共7小题,共44分)
16.(6分)打火机给人们的生活带来了方便,如图为普通打火机的示意图,请回答下列问题:
(1)打火机的制作材料中属于金属材料的是______(填物质的编号)。
(2)打火机打着火时,挡风不锈钢罩并没有燃烧起来,据此说明燃烧需要的条件之一是_______________;而将打火机的开关松开即可熄灭火焰,这种灭火方法的原理是_____________。
(3)打火机中的燃料是丁烷(化学式为C4H10),丁烷完全燃烧产生二氧化碳和水,写出该反应的化学方程式:_____________。
(4)用分子、原子的观点解释丁烷气体能被压缩成液体的原因:_________________。
17.(8分)合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要。
(1)2020年6月17日,湖南省娄底市嘉信华庭小区商住楼一个仓库发生火灾,造成7人死亡。
①从物质燃烧的条件来年看,仓库内存放的纺织品、塑料制品属于___________。
②某商户慌忙打开门窗大声呼救,导致火势迅速扩大。请解释出现这种情况的原因是______________。
③消防队员赶到现场并用高压水枪灭火,水灭火的原理是___________。
④如果你遇到类似的火情,应一边自救,一边拨打火警电话。正确的自救方法是___________,火警电话是___________(均填序号)。
A.用湿手巾捂住口鼻迅速逃离 B.120 C.站原地等待消防队员营救 D.119
(2)分析下表中的数据,回答问题:
物质代号 L M N P
熔点/℃ -117 3550 44 -259
沸点/℃ 78 4827 257 -253
着火点/℃ 510 370 40 580
①有人认为“物质的熔、沸点越高,着火点越高”,该结论_________(填“合理”或“不合理”)。
②已知酒精灯火焰的温度约为500℃。利用上图装置,验证达到可燃物着火点是燃烧的条件之一,上表中可用于完成该实验的两种可燃物是_________和________(填代号)。
18.(5分)合理利用化石燃料资源,是人类不断探索的课题。某城市家用燃料的使用经历了下图所示的过程,并将逐步向理想燃料发展。
(注:括号中的物质是对应燃料的主要成分)
(1)CH4、C3H8两种物质中,氢元素的质量分数较大的是__________(填化学式)。
(2)倡导“家用燃料低碳化”的意义是__________。
(3)一定条件下,仅用一个置换反应即可制得CO和H2,反应的化学方程式为__________。
(4)随着全球能源使用量的增长,化石燃料等不可再生能源将日趋枯竭。请提出一个缓解能源危机的设想:__________。
19.(6分)能源、环境和安全已成为人类日益关注的问题。请回答下列问题。
(1)目前世界上多数国家利用的能量主要来自煤、石油和_______等化石燃料的燃烧。
(2)科技发展可促进新能源的开发利用。下列能源不属于新能源的是_______(选填字母序号)。
A.煤 B.地热能 C.太阳能 D.核能
(3)2020年6月23日,北斗三号最后一颗全球组网卫星发射成功。此次卫星发射用的火箭推进剂为液氢和液氧,其反应产物无污染。写出氢气在氧气中燃烧的化学方程式______。
(4)燃料的充分燃烧对于节约能源、减少环境污染非常重要。汽车化油器将汽油喷成雾状进入内燃机气缸,使汽油充分燃烧。这是通过_______的方法使汽油充分燃烧。
(5)加油站、化工厂、面粉厂等场所的空气中含有较多可燃性气体或粉尘,因此这些场所一定要严禁烟火,防止发生_________。
20.(2015 烟台)(5分)2020年10月20日,山西省左权县发生煤矿瓦斯爆炸事故,造成4人遇难,1人受伤。瓦斯是煤矿矿井下有害气体的总称,它已成为煤矿事故的“头号杀手”。
(1)瓦斯的主要成分是甲烷。甲烷在空气中完全燃烧的化学方程式为______________。
(2)为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是________(填序号,下同)。
A.进矿井前先做灯火实验 B.工人必须戴安全帽才能进入矿井
C.矿井内要加强通风 D.安装瓦斯探头传感器监测瓦斯浓度
(3)矿井下特大瓦斯爆炸事故发生后,专家提出了注入液氮灭火的方案。液氮可用于矿井灭火的原因是__________________、__________________(写出两条)。
21.(8分)目前全球正面临着能源、环境、水资源等方面的危机。因此,开发利用新能源显得格外重要。据报道,太阳能光伏发电在当代得到了大规模的应用和发展。太阳能光伏发电最关键的材料是高纯硅。如图是工业上以石英砂(SiO2)为主要原料制取纯硅的一种方法,请回答下列问题:
(1)发展太阳能产业的主要优点是_________(答一点即可)。
(2)将石英砂粉碎的目的是_________。
(3)焦炭在反应①中体现出来的化学性质是_________。
(4)写出流程中两种氧化物的名称_________、_________。
(5)写出步骤②中发生反应的化学方程式_________。
(6)整个制备硅过程必须达到无水无氧。在反应②的过程中若混入O2,可能引起的后果是_________。
22.(6分)氢气被看作是理想的能源。氢气的制取和储存是氢能源利用领域的研究热点
Ⅰ.氢气的制取
(1)科学家正致力于研究在催化剂和光照条件下分解水制氢气。写出该反应的化学方程式:_____,该反应_______(填“放出”或“吸收”)能量。
(2)水热分解可得氢气,高温下水分解体系中微粒含量与温度的关系如图所示。
图中曲线A、B对应的微粒依次是________(填符号)。
Ⅱ.氢气的储存
(3)一种镁铜合金可用于储氢。
①将镁、铜单质按比例在一定温度下熔炼得到上述合金。熔炼时须通入氩气,其目的是__________。
②350℃时,该镁铜合金与氢气反应,生成了一种仅含Mg、H两种元素的化合物,其中氢元素的质量分数为7.7%。该化合物的化学式为__________。
三、实验探究题(共2小题,共16分)
23.(10分)燃烧既能给人类带来光明和幸福,也能给人类带来灾难和痛苦。某小组在学习物质燃烧条件时进行了探究。老师提供了如下物品:①酒精灯 ②铜片 ③火柴头 ④火柴梗 ⑤沙土 ⑥三脚架。
【查阅资料】火柴头的着火点是260~280℃,火柴梗的着火点为350~400℃。
【实验探究】
探究的内容 实验设计与操作 实验现象 实验结论
探究一燃烧与物质的关系 _________ 可燃物才能燃烧
探究二燃烧与温度的关系 注意:火柴头和火柴梗的位置相对于火焰中心_________(填“对称”或“不对称”) _________ 物质燃烧条件之一是:_________
探究三燃烧与氧气的关系 ①_________ ②_________ _________ 物质燃烧条件之一是:_________
【拓展与应用】
(1)炭火烤羊肉串,是利用了木炭燃烧放出的_________。
(2)下面三个实验都是利用红磷燃烧测定空气中氧气的含量。
实验一是在点燃条件下发生的,实验二是在聚光光照条件下发生的,实验三是在电热丝加热条件下发生的,这三个实验的条件虽然不同,但其实质都是使_________。
24.(6分)化学实验社团在老师的指导下开展了“模拟酸雨形成”的相关实验。
【联想与实验】模仿二氧化碳与水反应进行如图一所示实验:
【问题与猜想】亚硫酸不稳定,为什么红色液体微热后不变为紫色?其原因可能为:
猜想1:加热不够充分
猜想2:与空气中的氮气有关
猜想3:与空气中的氧气有关
【实验与验证】填写表格中的空格。
编号 操作 现象 结论
1 将图一中红色液体继续加热至沸腾 仍为红色 猜想1不成立
2 如图二所示,先通入适量的SO2,然后用酒精灯微热 先变红后变紫 猜想2不成立
3 如图二所示,先通入适量的SO2,再改通入氮气,最后用酒精灯微热 _________
4 如图二所示,先通入适量的SO2,再改通入________,最后用酒精灯微热 _________ 猜想3成立
【分析与结论】红色液体微热后不变为紫色的原因是:H2SO3在空气中会被氧化成另一种酸,进一步实验证明是硫酸。
【应用与拓展】收集某硫酸厂(生产过程中产生SO2)附近刚降到地面的雨水水样,用pH计测得每隔十分钟数据如下表:
测定时间 5:05 5:15 5:25 5:35 5:45
pH 4.95 4.94 4.86 4.85 4.85
(1)分析表中数据,5:15至5:25时间段内水样中主要酸性溶质有_________。
(2)实验社团提出一种处理废气的方案如右图,利用CaCO3粉末、空气为原料在高温下吸收SO2,写出该反应的化学方程式:_________。
四、计算题(共10分)
25.推广车用乙醇汽油,可以减少汽车尾气污染。利用秸秆为原料可生产乙醇(C2H6O),其中包含葡萄糖(C6H12O6)转化为乙醇的反应(C6H12O62C2H6O+2CO2↑)。
(1)请再写出使用乙醇汽油的一点好处:__________。
(2)每生产2.3t乙醇,计算理论上参加反应的葡萄糖的质量(写出计算过程)。
参考答案
1.C
2.D 提示:根据物质燃烧的条件,可燃物燃烧需要与氧气接触并且温度达到着火点,土星中没有氧气,且平均温度为-150℃,温度没有达到氢气、甲烷的着火点,所以不能燃烧。
3.C
4.A
5.C 用水来灭火,其原理是降低可燃物温度到着火点以下,而不能降低可燃物的着火点。
6.D
7.D 提示:将酒精灯的灯芯拨得松散一些,可以增大酒精与空气的接触面积,以促进酒精燃烧。
8.C
9.B
10.B 二氧化硫是造成酸雨的主要气体,而二氧化碳不会导致酸雨,而是导致温室效应,B错误。
11.D 提示:酒精和水分别放在酒精灯上加热,均能与氧气接触,酒精能燃烧,水不能,能证明燃烧需要有可燃物,A错误;红磷均能与氧气接触,左边的红磷不能燃烧,右边的红磷能燃烧,能证明燃烧需要温度达到着火点,B错误;火柴头先燃烧,火柴梗后燃烧,能证明燃烧需要温度达到着火点,C错误;试管中的白磷能与氧气接触,能燃烧,水中的白磷不能与氧气接触,不能燃烧,能证明燃烧需要氧气,D正确。
12.C 提示:由图可知,该反应是一氧化碳和水在催化剂的作用下反应生成氢气和二氧化碳,该反应的化学方程式为。氢气可通过一氧化碳和水在催化剂的作用下制得,故氢气属于可再生能源,A错误;由化学方程式可知,反应物是一氧化碳和水,它们都是由不同种元素组成的化合物,生成物是氢气和二氧化碳,氢气是由同种元素组成的单质,二氧化碳是由不同种元素组成的化合物,B错误;由题干信息可知,使用催化剂后,可使一氧化碳和水在低温的条件下反应,故催化剂可以改变化学反应条件,C正确;由化学方程式可知,分子的种类发生了改变,数目不变,D错误。
13.D
14.C 提示:化合反应的特征是“多变一”,该反应的反应物是两种,生成物是一种,符合化合反应的特征,属于化合反应,A正确;此处的“石灰”是生石灰,“石灰遇水沸腾”,就是说生石灰和水反应能使水沸腾,说明该反应会放出热量,B正确;根据反应CaO+H2O=Ca(OH)2,氧化钙能吸收水分,可用来干燥某些气体,但氧化钙不能干燥氯化氢气体,因为氧化钙会和氯化氢气体发生化学反应,C错误;生石灰和水反应生成氢氧化钙,因此该反应可制备氢氧化钙,D正确。
15.D
16.(1)③④ (2)温度达到着火点 隔离可燃物 (3)2C4H10+13O28CO2+10H2O (4)分子间有间隔(或受压时气体分子间隔缩小等)
17.(1)①可燃物 ②空气进入房间内氧气浓度增大,氧气助火势更旺 ③降低温度到可燃物的着火点以下 ④A D (2)①不合理 ②N M
18.(1)CH4 (2)缓解温室效应(或其他合理答案) (3)C+H2O一定条件CO+H2(或“2CH4+O2一定条件2CO+4H2”等其他合理答案) (4)开发使用新能源(或其他合理答案)
提示:(1)“CH4”中氢、碳原子个数比为4“1,“C3H8”中氢、碳原子个数比为8:3,比较可知,“CH4”中氢元素的质量分数较大。(2)大气中二氧化碳的含量增加,会加剧温室效应,倡导“家用燃料低碳化”可有效减少二氧化碳的排放,从而可减缓温室效应。(3)置换反应指的是一种单质与一种化合物生成另一种单质和另一种化合物的反应,若生成物为CO和H2,可逆推反应物可为C、H2O或CH4、O2,据此可写出反应的化学方程式。(4)缓解能源危机的方法有很多,主要是寻找替代能源,即开发新能源,如太阳能、水能、地热能、潮汐能等。
19.(1)天然气 (2)A (3)2H2+O22H2O (4)增大汽油与氧气的接触面积 (5)爆炸
20.(1)CH4+2O2CO2+2H2O (2)CD (3)氮气不燃烧也不支持燃烧、液氮汽化使温度降低
21.(1)取之不尽(合理即可) (2)增大与焦炭的接触面积,使反应更充分 (3)还原性 (4)一氧化碳、二氧化硅 (5)SiCl4+2H2Si+4HCl (6)氢气和氧气反应引发爆炸
22.(1)2H2O2H2↑+O2 吸收 (2)H、O (3)①防止熔炼时镁、铜与空气反应 ②MgH2
提示:(1)水在催化剂和光照的条件下分解生成氢气和氧气,由于该反应需要在光照条件下进行,说明反应需要吸收能量。(2)水分解生成氢气和氧气,结合反应的化学方程式可知氢、氧原子的个数比为(2×2):(1×2)=2:1,由图像可知,A、B微粒个数比约为2:1,因此A为氢原子、B为氧原子。(3)①由金属单质的化学性质可知镁和铜在加热条件下都易被氧化,因此通入氩气作保护气,可防止高温熔炼时镁和铜与空气反应。②因为氢元素的质量分数为7.7%,则化合物中镁元素的质量分数为1-7.7%=92.3%,所以化合物中镁原子和氧原子的个数比为:=1:2,则化合物的化学式为MgH2。
23.【实验探究】火柴头燃烧,沙土和铜片不能燃烧 对称 火柴头、火柴梗先后燃烧 温度达到着火点 ①隔绝氧气的火柴头 ②暴露在空气中的火柴头 ①处火柴头不能燃烧,②处火柴头燃烧 与氧气接触(与①②对应) 【拓展与应用】(1)热量 (2)红磷燃烧,消耗氧气
24.【探究与验证】先变红后变紫 氧气(或O2) 先变红色,后仍为红色
【应用与拓展】(1)H2SO3和H2SO4 (2)2CaCO3+2SO2+2O22CaSO4+2CO2
提示:【探究与验证】根据结论猜想2不成立,可以分析出观察到的现象为先变红后变紫。根据结论猜想3成立。分析出操作:通入O2,观察到的现象为:先变红,加热后仍为红色。【应用与拓展】(1)5:15-5:25,从表格可以看出酸性在增强,结合资料信息与探究与验证可以分析出水样中主要酸性溶质有H2SO3、H2SO4。(2)结合题干与废气处理方案图可知反应物为SO2、空气中O2、CaCO3;生成物CO2为CaSO4;反应条件高温。该反应的方程式为2CaCO3+2SO2+2O22CaSO4+2CO2。
25.(1)节约化石燃料
(2)设参加反应的葡萄糖的质量为x。
C6H12O62C2H6O+2CO2↑
180 92
x 2.3t
x=4.5t
答:理论上参加反应的葡萄糖的质量为4.5t。
薄铜片
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
