第三单元物质构成的奥秘测试题- 2021-2022学年九年级化学人教版上册(有答案)
文档属性
| 名称 | 第三单元物质构成的奥秘测试题- 2021-2022学年九年级化学人教版上册(有答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 240.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-21 00:00:00 | ||
图片预览


文档简介
第三单元 物质构成的奥秘
一 选择题
1.分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )
A.分子由原子构成,分子比原子大
B.水遇冷凝结成冰,水分子停止了运动
C.原子是最小的粒子,不可再分
D.氯化钠是由钠离子和氯离子构成的
2.元素观和微粒观是化学核心观念。下列说法不正确的是( )
A.构成物质的微粒有分子、原子和离子
B.质子数相同的微粒一定是由同种元素形成的
C.化学变化前后原子的种类和个数一定不变
D.原子序数与元素原子核电荷数在数值上相等
3.下列有关元素、原子、分子和离子的说法正确的是( )
A.决定元素化学性质的主要是原子的最外层电子数
B.原子可以构成分子,但不能直接构成物质
C.分子是化学变化中的最小微粒
D.微粒得到或失去电子变成离子
4.元素观、微粒观是化学的重要观念。下列有关元素和微粒的说法不正确的是( )
A.分子、原子和离子都是构成物质的粒子
B.同种元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子的核电荷数在数值上相同
D.在物质发生化学变化时,原子的种类不变,元素的种类也不会改变
5.下列化学用语所表达的意义正确的是( )
A.C60—60个碳原子 B.2O—2个氧原子
C.Fe2+—1个铁离子 D.3N—3个氮元素
6.某微粒M的结构示意图如图所示,关于该微粒的说法正确的是( )
A.M的原子易失电子
B.x只能为7
C.M为金属元素
D.x为8时,M为阴离子
7.下面是四种粒子的结构示意图,下列分析错误的是( )
A.①③化学性质相似 B.②为阴离子
C.③④属于同一种元素 D.③为第三周期元素的原子
8.如图是四种粒子的结构示意图,下列有关说法正确的是( )
A.④表示的粒子属于金属元素
B.①表示的粒子在化学反应中易失电子
C.①②③④表示四种不同元素
D.②④所表示的粒子化学性质相似
9.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是( )
A.铁的相对原子质量为55.85 g
B.锰元素为非金属元素
C.铬原子的原子核内有52个质子
D.等质量的铬、锰、铁中,含原子个数最多的是铬
二 非选择题
1.用元素、原子、分子或离子填空:
(1)水是由氢、氧两种________组成的。
(2)带电的原子或原子团叫________。
(3)保持氢气化学性质的最小粒子是氢________。
(4)化学变化中的最小粒子是________。
(5)二氧化碳、氯酸钾、氧气中都含有氧________。
(6)汞由_________构成,氯化钠由________构成。
2.在宏观、微观和符号之间建立联系是化学学科的特点。
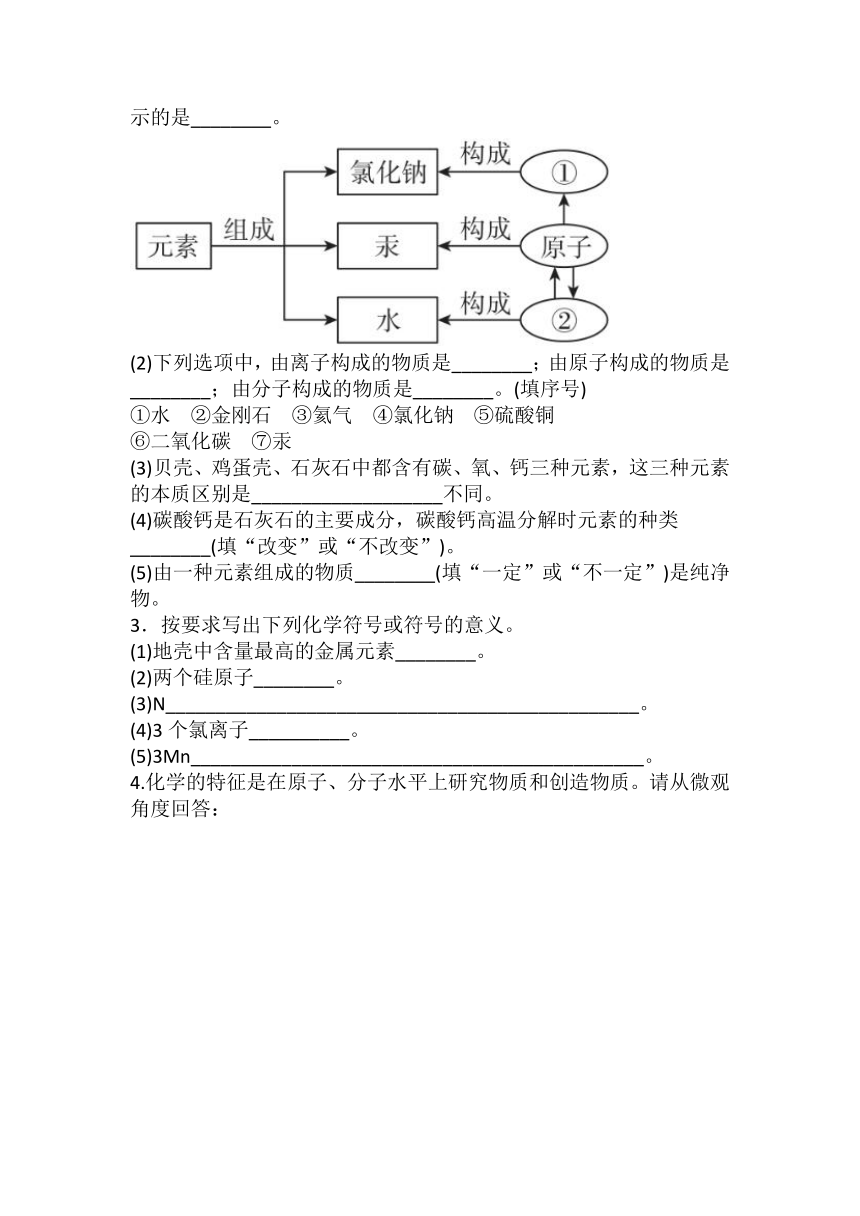
(1)物质的组成及构成关系如图所示,图中①表示的是________,②表示的是________。
(2)下列选项中,由离子构成的物质是________;由原子构成的物质是________;由分子构成的物质是________。(填序号)
①水 ②金刚石 ③氦气 ④氯化钠 ⑤硫酸铜
⑥二氧化碳 ⑦汞
(3)贝壳、鸡蛋壳、石灰石中都含有碳、氧、钙三种元素,这三种元素的本质区别是___________________不同。
(4)碳酸钙是石灰石的主要成分,碳酸钙高温分解时元素的种类________(填“改变”或“不改变”)。
(5)由一种元素组成的物质________(填“一定”或“不一定”)是纯净物。
3.按要求写出下列化学符号或符号的意义。
(1)地壳中含量最高的金属元素________。
(2)两个硅原子________。
(3)N_______________________________________________。
(4)3个氯离子__________。
(5)3Mn_____________________________________________。
4.化学的特征是在原子、分子水平上研究物质和创造物质。请从微观角度回答:
(1)“遥知不是雪,为有暗香来”。花香入鼻的原因是________
_________________________________________________。
(2)由图1推知水和过氧化氢化学性质不同的原因是_________
_________________________________________________。
(3)由图2可知,水分解过程中,没有发生变化的微粒是_____(填微粒符号)。
(4)由图2可知,该反应的基本反应类型是_________________。
(5)从图2还可得出的结论有______________________________
_______________________________________________________________________________________________________。
5.一些粒子的结构都可用示意图 来表示,且0(1)若x=12时对应的元素为A,则A的元素符号为________。
(2)当上述示意图表示的粒子均具有稳定的电子层结构时:
①若某粒子带一个单位正电荷,则该粒子的化学符号为________;
②若某粒子带两个单位负电荷,则该粒子的化学符号为________。
6.元素周期表是学习化学的重要工具,如图为元素周期表中部分元素的相关信息,利用如图所示回答相关问题。
(1)原子序数为4的元素符号为________。
(2)C、N、O排在同一周期是因为__________(填“质子数”“电子层数”或“最外层电子数”)相同。
(3)He和Mg的化学性质________(填“相似”或“不相似”)。
(4)钠离子核外电子排布与____(填元素符号)原子核外电子排布相同。
(5)一个磷原子含有____个质子,一个NH4+含有_____个电子。
16.(2020·乐山)元素周期表是学习和研究化学的重要工具。请根据下图(元素周期表的部分内容)回答有关问题:
(1)请从上图中查出关于氟元素的一条信息:______________
_____________________________________________。
(2)写出该结构简图的微粒符号________。
(3)第13号元素与第17号元素组成的化合物的化学式是_____。
(4)在元素周期表中,同一族(纵行)的元素一般具有相似的化学性质。则下列各组元素具有相似化学性质的是______(填字母序号)。
A.Be和Mg B.C和Ne
C.Al和Si D.F和Cl
参考答案
一 选择题
DBAB BDBAD
二 非选择题
1.元素 离子 分子 原子 元素 原子 离子
2. 离子 分子 ④⑤ ②③⑦ ①⑥ 质子数(或核电荷数) 不改变 不一定
3. Al 2Si 氮元素,一个氮原子 3Cl- 3个锰原子
4.分子在不停地运动 分子的构成不同 H、O 分解反应 化学反应前后,分子的种类改变,原子的种类不变(或原子是化学变化中的最小粒子,其他答案合理亦可) Mg
①Na+ ②O2-。
5.Be 电子层数 不相似 Ne 15 10
6. 氟元素相对原子质量为19.00(合理即可) Mg2+ AlCl3 A、D
一 选择题
1.分子、原子和离子都是构成物质的基本粒子,下列说法正确的是( )
A.分子由原子构成,分子比原子大
B.水遇冷凝结成冰,水分子停止了运动
C.原子是最小的粒子,不可再分
D.氯化钠是由钠离子和氯离子构成的
2.元素观和微粒观是化学核心观念。下列说法不正确的是( )
A.构成物质的微粒有分子、原子和离子
B.质子数相同的微粒一定是由同种元素形成的
C.化学变化前后原子的种类和个数一定不变
D.原子序数与元素原子核电荷数在数值上相等
3.下列有关元素、原子、分子和离子的说法正确的是( )
A.决定元素化学性质的主要是原子的最外层电子数
B.原子可以构成分子,但不能直接构成物质
C.分子是化学变化中的最小微粒
D.微粒得到或失去电子变成离子
4.元素观、微粒观是化学的重要观念。下列有关元素和微粒的说法不正确的是( )
A.分子、原子和离子都是构成物质的粒子
B.同种元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子的核电荷数在数值上相同
D.在物质发生化学变化时,原子的种类不变,元素的种类也不会改变
5.下列化学用语所表达的意义正确的是( )
A.C60—60个碳原子 B.2O—2个氧原子
C.Fe2+—1个铁离子 D.3N—3个氮元素
6.某微粒M的结构示意图如图所示,关于该微粒的说法正确的是( )
A.M的原子易失电子
B.x只能为7
C.M为金属元素
D.x为8时,M为阴离子
7.下面是四种粒子的结构示意图,下列分析错误的是( )
A.①③化学性质相似 B.②为阴离子
C.③④属于同一种元素 D.③为第三周期元素的原子
8.如图是四种粒子的结构示意图,下列有关说法正确的是( )
A.④表示的粒子属于金属元素
B.①表示的粒子在化学反应中易失电子
C.①②③④表示四种不同元素
D.②④所表示的粒子化学性质相似
9.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是( )
A.铁的相对原子质量为55.85 g
B.锰元素为非金属元素
C.铬原子的原子核内有52个质子
D.等质量的铬、锰、铁中,含原子个数最多的是铬
二 非选择题
1.用元素、原子、分子或离子填空:
(1)水是由氢、氧两种________组成的。
(2)带电的原子或原子团叫________。
(3)保持氢气化学性质的最小粒子是氢________。
(4)化学变化中的最小粒子是________。
(5)二氧化碳、氯酸钾、氧气中都含有氧________。
(6)汞由_________构成,氯化钠由________构成。
2.在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图所示,图中①表示的是________,②表示的是________。
(2)下列选项中,由离子构成的物质是________;由原子构成的物质是________;由分子构成的物质是________。(填序号)
①水 ②金刚石 ③氦气 ④氯化钠 ⑤硫酸铜
⑥二氧化碳 ⑦汞
(3)贝壳、鸡蛋壳、石灰石中都含有碳、氧、钙三种元素,这三种元素的本质区别是___________________不同。
(4)碳酸钙是石灰石的主要成分,碳酸钙高温分解时元素的种类________(填“改变”或“不改变”)。
(5)由一种元素组成的物质________(填“一定”或“不一定”)是纯净物。
3.按要求写出下列化学符号或符号的意义。
(1)地壳中含量最高的金属元素________。
(2)两个硅原子________。
(3)N_______________________________________________。
(4)3个氯离子__________。
(5)3Mn_____________________________________________。
4.化学的特征是在原子、分子水平上研究物质和创造物质。请从微观角度回答:
(1)“遥知不是雪,为有暗香来”。花香入鼻的原因是________
_________________________________________________。
(2)由图1推知水和过氧化氢化学性质不同的原因是_________
_________________________________________________。
(3)由图2可知,水分解过程中,没有发生变化的微粒是_____(填微粒符号)。
(4)由图2可知,该反应的基本反应类型是_________________。
(5)从图2还可得出的结论有______________________________
_______________________________________________________________________________________________________。
5.一些粒子的结构都可用示意图 来表示,且0
(2)当上述示意图表示的粒子均具有稳定的电子层结构时:
①若某粒子带一个单位正电荷,则该粒子的化学符号为________;
②若某粒子带两个单位负电荷,则该粒子的化学符号为________。
6.元素周期表是学习化学的重要工具,如图为元素周期表中部分元素的相关信息,利用如图所示回答相关问题。
(1)原子序数为4的元素符号为________。
(2)C、N、O排在同一周期是因为__________(填“质子数”“电子层数”或“最外层电子数”)相同。
(3)He和Mg的化学性质________(填“相似”或“不相似”)。
(4)钠离子核外电子排布与____(填元素符号)原子核外电子排布相同。
(5)一个磷原子含有____个质子,一个NH4+含有_____个电子。
16.(2020·乐山)元素周期表是学习和研究化学的重要工具。请根据下图(元素周期表的部分内容)回答有关问题:
(1)请从上图中查出关于氟元素的一条信息:______________
_____________________________________________。
(2)写出该结构简图的微粒符号________。
(3)第13号元素与第17号元素组成的化合物的化学式是_____。
(4)在元素周期表中,同一族(纵行)的元素一般具有相似的化学性质。则下列各组元素具有相似化学性质的是______(填字母序号)。
A.Be和Mg B.C和Ne
C.Al和Si D.F和Cl
参考答案
一 选择题
DBAB BDBAD
二 非选择题
1.元素 离子 分子 原子 元素 原子 离子
2. 离子 分子 ④⑤ ②③⑦ ①⑥ 质子数(或核电荷数) 不改变 不一定
3. Al 2Si 氮元素,一个氮原子 3Cl- 3个锰原子
4.分子在不停地运动 分子的构成不同 H、O 分解反应 化学反应前后,分子的种类改变,原子的种类不变(或原子是化学变化中的最小粒子,其他答案合理亦可) Mg
①Na+ ②O2-。
5.Be 电子层数 不相似 Ne 15 10
6. 氟元素相对原子质量为19.00(合理即可) Mg2+ AlCl3 A、D
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
