2021-2022学年高一下学期化学苏教版(2020)必修第二册8.2.1乙醇教案
文档属性
| 名称 | 2021-2022学年高一下学期化学苏教版(2020)必修第二册8.2.1乙醇教案 |
|
|
| 格式 | zip | ||
| 文件大小 | 73.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-22 19:31:17 | ||
图片预览


文档简介
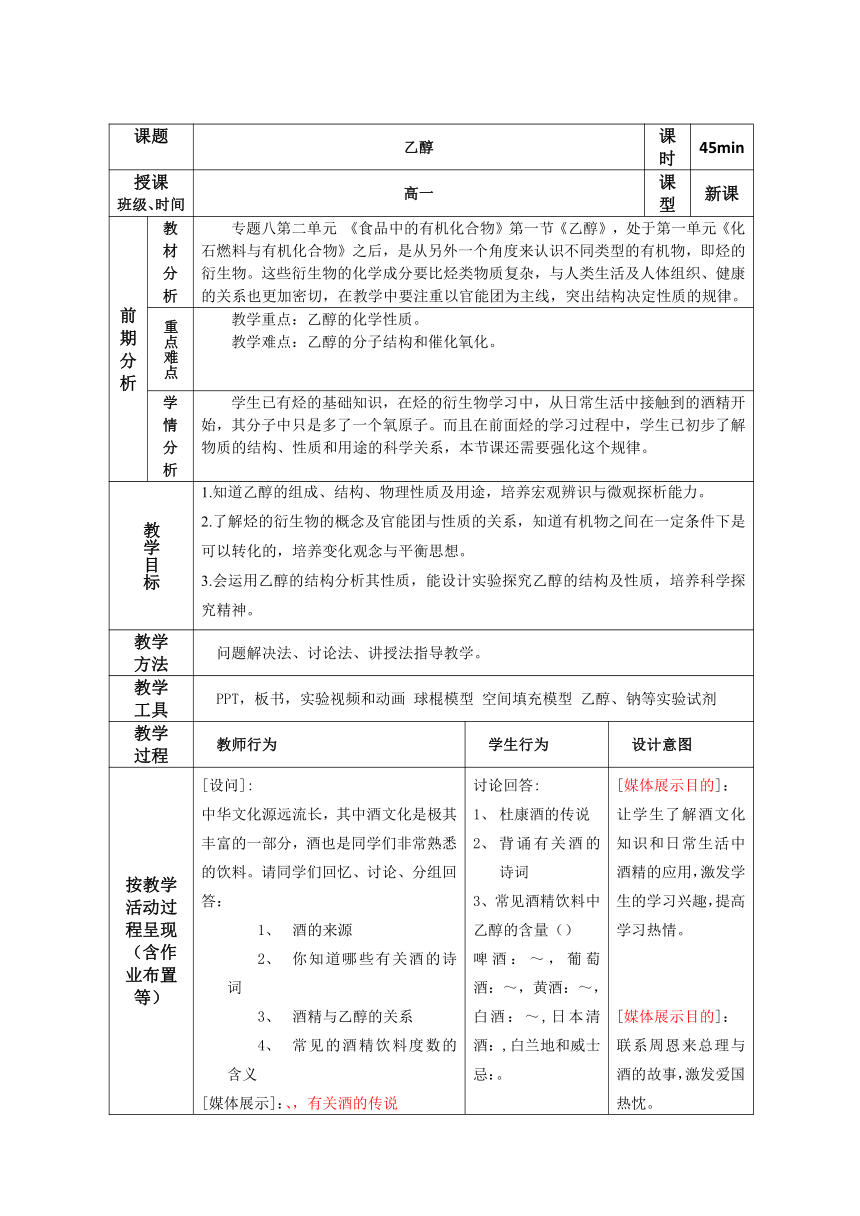
课题 乙醇 课时 45min
授课 班级、时间 高一 课型 新课
前期分析 教材分析 专题八第二单元 《食品中的有机化合物》第一节《乙醇》,处于第一单元《化石燃料与有机化合物》之后,是从另外一个角度来认识不同类型的有机物,即烃的衍生物。这些衍生物的化学成分要比烃类物质复杂,与人类生活及人体组织、健康的关系也更加密切,在教学中要注重以官能团为主线,突出结构决定性质的规律。
重点难点 教学重点:乙醇的化学性质。 教学难点:乙醇的分子结构和催化氧化。
学情分析 学生已有烃的基础知识,在烃的衍生物学习中,从日常生活中接触到的酒精开始,其分子中只是多了一个氧原子。而且在前面烃的学习过程中,学生已初步了解物质的结构、性质和用途的科学关系,本节课还需要强化这个规律。
教学目标 1.知道乙醇的组成、结构、物理性质及用途,培养宏观辨识与微观探析能力。 2.了解烃的衍生物的概念及官能团与性质的关系,知道有机物之间在一定条件下是可以转化的,培养变化观念与平衡思想。 3.会运用乙醇的结构分析其性质,能设计实验探究乙醇的结构及性质,培养科学探究精神。
教学 方法 问题解决法、讨论法、讲授法指导教学。
教学 工具 PPT,板书,实验视频和动画 球棍模型 空间填充模型 乙醇、钠等实验试剂
教学 过程 教师行为 学生行为 设计意图
按教学活动过程呈现(含作业布置等) [设问]: 中华文化源远流长,其中酒文化是极其丰富的一部分,酒也是同学们非常熟悉的饮料。请同学们回忆、讨论、分组回答: 酒的来源 你知道哪些有关酒的诗词 酒精与乙醇的关系 常见的酒精饮料度数的含义 [媒体展示]:、,有关酒的传说 [媒体展示]:,周恩来与酒的几则故事 [展示]:实物——乙醇和碘酒, 推断乙醇的物理性质。 乙醇物理性质 [小结]: 引导学生归纳乙醇的物理性质。 [媒体展示]:,乙醇重要的物理性质 [板书]: 乙 醇 一、乙醇的物理性质 色液体、气味、沸点、 挥发、密度比水、能溶解多种和,能与水。 [设问]: 怎样检验酒精是否含有水? 怎样除去酒精中的少量水份? 乙醇分子结构推断 [提问]: 根据第一单元的知识与经验,我们如何推断乙醇的分子结构? [指导]: 请完成学案题: [媒体展示]:、,乙醇可能的结构式 [板书]: 二、乙醇的分子结构 分子式: 可能结构式:(略) 可能结构简式:(); 或 [提问]: ()这两个结构(简)式区别何在? ()如何验证乙醇是哪一种结构? [提示]: 学过的哪些物质分子中含有原子团?它们有什么共性? 怎样验证乙醇结构? [提示]: 实验室中,金属钠是如何保存的?煤油的成分是什么?钠保存其中,说明什么问题? [指示]: 将钠分别加入乙醇和水中,比较现象。 再根据钠能保存在煤油中的事实,能否推测乙醇的结构式? [媒体展示]:、,水、乙醇分别与钠反应过程 [确定]: 乙醇的结构简式为:或 [媒体展示]:、,乙醇分子的空间结构 [媒体展示]:乙醇分子模型 [媒体展示]:,乙醇结构小结 羟基,写作-; 官能团的概念; 烃的衍生物的概念。 乙醇与金属钠反应 [过渡]: 根据乙醇的分子结构,你能推理出乙醇的化学性质吗? [分析实验]: 钠与乙醇 钠与水 [板书]: 三、乙醇的化学性质 1、与活泼金属反应 [媒体展示]:、,乙醇和水分别与钠反应的实验对比 乙醇的燃烧反应 [展示实物]: 酒精灯、固体酒精、乙醇汽油 [提出问题]:乙醇完全燃烧可观察到什么现象?产物是什么?乙醇为什么可用做燃料?写出乙醇燃烧的化学反应方程式,判断其反应类型。 [板书]:、氧化反应 乙醇的催化氧化 [指导实验]: 取一支大试管,倒入约无水乙醇,闻一下气味;将一端弯成螺旋状的铜丝在酒精灯的外焰部分灼烧至红热,迅速插入无水乙醇中,稍后取出,反复几次后,闻试管中液体的气味。 [媒体展示]:,乙醇催化氧化实验 [设问]: 1、铜丝灼烧前后有什么变化? 2、伸入无水乙醇中有什么现象? 3、铜在反应中起到什么作用呢 4、闻一闻液体的气味。 [媒体展示]:,乙醇脱氢氧化的反应机理 [板书]: ()乙醇的催化氧化(脱氢) 整理、小结 [设问] 通过本节课的学习,你学到了什么? 讨论回答: 杜康酒的传说 背诵有关酒的诗词 3、常见酒精饮料中乙醇的含量() 啤酒:~,葡萄酒:~,黄酒:~,白酒:~,日本清酒:,白兰地和威士忌:。 学生观察,讨论、修正答案 观察得出物理性质; 填写学案题。 观察、对比 填写学案题 .硫酸铜 .生石灰 必须知道乙醇的组成元素、分子式、结构式 完成习题, 学生上黑板板演 对比答案,特别观察原子的排列顺序。 讨论、回答: 前者有一个氢原子与氧原子相连接,而后者的氢原子全部连接在碳原子上。 水分子、含氧酸分子中都含有,它们能与活泼金属反应生成氢气。可验证乙醇能否与金属钠反应产生氢气。 回答: 煤油属于烃类,钠不能与之反应产后氢气,说明钠不能置换连在碳原子上的氢原子。 做实验,回答现象: 盛有乙醇的试管内钠粒沉于底部,有无色气泡产生,最终钠粒消失,液体仍为无色透明。 钠与水反应比钠与乙醇反应要剧烈得多。 讨论、得出结论: 与碳原子直接相连的氢原子不能被金属钠置换,而乙醇可以与钠反应,所以乙醇分子中氧原子上应该连有氢原子,结构式为: 了解羟基和官能团的概念 思考,联想 回答: 因含有-,能与钠等活泼金属反应。 回忆实验现象。 填写学案题、、、 思考,回答 对比乙醇、水与金属钠反应的异同。 观察、分析 书写方程式 反应类型:氧化反应。 实验 观察 思考 回答: 由红色变黑色 由黑色变红色 催化剂 有刺激性气味 思考 回答 [媒体展示目的]: 让学生了解酒文化知识和日常生活中酒精的应用,激发学生的学习兴趣,提高学习热情。 [媒体展示目的]: 联系周恩来总理与酒的故事,激发爱国热忱。 引导学生观察乙醇,激活学生已有经验,激发学生探究乙醇性质的欲望。 培养学生分析、观察和归纳的能力。 [媒体展示目的]: 强化乙醇能与水混溶的特性及其应用,扩展知识面。 掌握对有机化合物结构推断的一般方法 [媒体展示目的]: 清晰、直观地表现出乙醇分子中各原子的连接方式 增强观察分析能力,提高探究意识,培养逻辑思维能力。 锻炼实验操作能力,提高对实验现象的观察、表述能力。 回忆已有知识,弥补实验不足,增强实验效果。 [媒体展示目的]: 回放以前实验,对比本课实验,温故知新,又节约时间 [媒体展示目的] 展示图片和模型,形象直观地反映出乙醇的分子结构,清晰呈现出原子连接顺序,加深学生对乙醇分子空间结构的认识。 [媒体展示目的] 及时归纳,并引出新知识 通过引导,使学生认识到对化学反应的重要影响。形成官能团决定物质性质的观点。 [媒体展示目的]: 对比二个实验现象,初步了解基团对官能团的影响 与学生已有知识衔接,从氧气参与的角度,分析有机反应中重要的反应类型。 理解乙醇催化氧化的本质,同时加深对催化剂概念的认识;培养学生的观察能力。 [媒体展示目的]: 强化实验细节 弥补了实验的不足。 [媒体展示目的]: 形象反映脱去氢原子的方式,容易理解反应机理。 培养学生总结问题的能力
板书 设计 一、乙醇物理性质 二、乙醇分子结构 分子式: 结构式: 结构简式: 或 ; 三、乙醇化学性质 1、与金属钠反应 2、氧化反应 (1)点燃: (2)催化氧化:
课后 反思 《化学课程标准》是在选修模块中才开始系统地学习有机化学的基础知识,对官能团的学习没有强化,在选修模块《有机化学基础》中对有机物知识的系统性则要求很高。所以我们并不需要去追求知识的系统性,亦不需要过多的知识迁移,不需要强化有机物的衍生转化关系。但是在实际的教学中,我们还是先学习物质的结构,再根据结构去推出性质,也就是在无形之中强化了官能团的学习,这样的教学学生的反馈也比较好。其中 对分子结构、反应产物通过实验探究、合作学习获得,这样有利于知识的掌握;从乙醇与乙烷的物理、化学性质的比较入手,得出官能团是决定化合物具有其特殊性质的基团,有助于学生对官能团的概念的理解。
授课 班级、时间 高一 课型 新课
前期分析 教材分析 专题八第二单元 《食品中的有机化合物》第一节《乙醇》,处于第一单元《化石燃料与有机化合物》之后,是从另外一个角度来认识不同类型的有机物,即烃的衍生物。这些衍生物的化学成分要比烃类物质复杂,与人类生活及人体组织、健康的关系也更加密切,在教学中要注重以官能团为主线,突出结构决定性质的规律。
重点难点 教学重点:乙醇的化学性质。 教学难点:乙醇的分子结构和催化氧化。
学情分析 学生已有烃的基础知识,在烃的衍生物学习中,从日常生活中接触到的酒精开始,其分子中只是多了一个氧原子。而且在前面烃的学习过程中,学生已初步了解物质的结构、性质和用途的科学关系,本节课还需要强化这个规律。
教学目标 1.知道乙醇的组成、结构、物理性质及用途,培养宏观辨识与微观探析能力。 2.了解烃的衍生物的概念及官能团与性质的关系,知道有机物之间在一定条件下是可以转化的,培养变化观念与平衡思想。 3.会运用乙醇的结构分析其性质,能设计实验探究乙醇的结构及性质,培养科学探究精神。
教学 方法 问题解决法、讨论法、讲授法指导教学。
教学 工具 PPT,板书,实验视频和动画 球棍模型 空间填充模型 乙醇、钠等实验试剂
教学 过程 教师行为 学生行为 设计意图
按教学活动过程呈现(含作业布置等) [设问]: 中华文化源远流长,其中酒文化是极其丰富的一部分,酒也是同学们非常熟悉的饮料。请同学们回忆、讨论、分组回答: 酒的来源 你知道哪些有关酒的诗词 酒精与乙醇的关系 常见的酒精饮料度数的含义 [媒体展示]:、,有关酒的传说 [媒体展示]:,周恩来与酒的几则故事 [展示]:实物——乙醇和碘酒, 推断乙醇的物理性质。 乙醇物理性质 [小结]: 引导学生归纳乙醇的物理性质。 [媒体展示]:,乙醇重要的物理性质 [板书]: 乙 醇 一、乙醇的物理性质 色液体、气味、沸点、 挥发、密度比水、能溶解多种和,能与水。 [设问]: 怎样检验酒精是否含有水? 怎样除去酒精中的少量水份? 乙醇分子结构推断 [提问]: 根据第一单元的知识与经验,我们如何推断乙醇的分子结构? [指导]: 请完成学案题: [媒体展示]:、,乙醇可能的结构式 [板书]: 二、乙醇的分子结构 分子式: 可能结构式:(略) 可能结构简式:(); 或 [提问]: ()这两个结构(简)式区别何在? ()如何验证乙醇是哪一种结构? [提示]: 学过的哪些物质分子中含有原子团?它们有什么共性? 怎样验证乙醇结构? [提示]: 实验室中,金属钠是如何保存的?煤油的成分是什么?钠保存其中,说明什么问题? [指示]: 将钠分别加入乙醇和水中,比较现象。 再根据钠能保存在煤油中的事实,能否推测乙醇的结构式? [媒体展示]:、,水、乙醇分别与钠反应过程 [确定]: 乙醇的结构简式为:或 [媒体展示]:、,乙醇分子的空间结构 [媒体展示]:乙醇分子模型 [媒体展示]:,乙醇结构小结 羟基,写作-; 官能团的概念; 烃的衍生物的概念。 乙醇与金属钠反应 [过渡]: 根据乙醇的分子结构,你能推理出乙醇的化学性质吗? [分析实验]: 钠与乙醇 钠与水 [板书]: 三、乙醇的化学性质 1、与活泼金属反应 [媒体展示]:、,乙醇和水分别与钠反应的实验对比 乙醇的燃烧反应 [展示实物]: 酒精灯、固体酒精、乙醇汽油 [提出问题]:乙醇完全燃烧可观察到什么现象?产物是什么?乙醇为什么可用做燃料?写出乙醇燃烧的化学反应方程式,判断其反应类型。 [板书]:、氧化反应 乙醇的催化氧化 [指导实验]: 取一支大试管,倒入约无水乙醇,闻一下气味;将一端弯成螺旋状的铜丝在酒精灯的外焰部分灼烧至红热,迅速插入无水乙醇中,稍后取出,反复几次后,闻试管中液体的气味。 [媒体展示]:,乙醇催化氧化实验 [设问]: 1、铜丝灼烧前后有什么变化? 2、伸入无水乙醇中有什么现象? 3、铜在反应中起到什么作用呢 4、闻一闻液体的气味。 [媒体展示]:,乙醇脱氢氧化的反应机理 [板书]: ()乙醇的催化氧化(脱氢) 整理、小结 [设问] 通过本节课的学习,你学到了什么? 讨论回答: 杜康酒的传说 背诵有关酒的诗词 3、常见酒精饮料中乙醇的含量() 啤酒:~,葡萄酒:~,黄酒:~,白酒:~,日本清酒:,白兰地和威士忌:。 学生观察,讨论、修正答案 观察得出物理性质; 填写学案题。 观察、对比 填写学案题 .硫酸铜 .生石灰 必须知道乙醇的组成元素、分子式、结构式 完成习题, 学生上黑板板演 对比答案,特别观察原子的排列顺序。 讨论、回答: 前者有一个氢原子与氧原子相连接,而后者的氢原子全部连接在碳原子上。 水分子、含氧酸分子中都含有,它们能与活泼金属反应生成氢气。可验证乙醇能否与金属钠反应产生氢气。 回答: 煤油属于烃类,钠不能与之反应产后氢气,说明钠不能置换连在碳原子上的氢原子。 做实验,回答现象: 盛有乙醇的试管内钠粒沉于底部,有无色气泡产生,最终钠粒消失,液体仍为无色透明。 钠与水反应比钠与乙醇反应要剧烈得多。 讨论、得出结论: 与碳原子直接相连的氢原子不能被金属钠置换,而乙醇可以与钠反应,所以乙醇分子中氧原子上应该连有氢原子,结构式为: 了解羟基和官能团的概念 思考,联想 回答: 因含有-,能与钠等活泼金属反应。 回忆实验现象。 填写学案题、、、 思考,回答 对比乙醇、水与金属钠反应的异同。 观察、分析 书写方程式 反应类型:氧化反应。 实验 观察 思考 回答: 由红色变黑色 由黑色变红色 催化剂 有刺激性气味 思考 回答 [媒体展示目的]: 让学生了解酒文化知识和日常生活中酒精的应用,激发学生的学习兴趣,提高学习热情。 [媒体展示目的]: 联系周恩来总理与酒的故事,激发爱国热忱。 引导学生观察乙醇,激活学生已有经验,激发学生探究乙醇性质的欲望。 培养学生分析、观察和归纳的能力。 [媒体展示目的]: 强化乙醇能与水混溶的特性及其应用,扩展知识面。 掌握对有机化合物结构推断的一般方法 [媒体展示目的]: 清晰、直观地表现出乙醇分子中各原子的连接方式 增强观察分析能力,提高探究意识,培养逻辑思维能力。 锻炼实验操作能力,提高对实验现象的观察、表述能力。 回忆已有知识,弥补实验不足,增强实验效果。 [媒体展示目的]: 回放以前实验,对比本课实验,温故知新,又节约时间 [媒体展示目的] 展示图片和模型,形象直观地反映出乙醇的分子结构,清晰呈现出原子连接顺序,加深学生对乙醇分子空间结构的认识。 [媒体展示目的] 及时归纳,并引出新知识 通过引导,使学生认识到对化学反应的重要影响。形成官能团决定物质性质的观点。 [媒体展示目的]: 对比二个实验现象,初步了解基团对官能团的影响 与学生已有知识衔接,从氧气参与的角度,分析有机反应中重要的反应类型。 理解乙醇催化氧化的本质,同时加深对催化剂概念的认识;培养学生的观察能力。 [媒体展示目的]: 强化实验细节 弥补了实验的不足。 [媒体展示目的]: 形象反映脱去氢原子的方式,容易理解反应机理。 培养学生总结问题的能力
板书 设计 一、乙醇物理性质 二、乙醇分子结构 分子式: 结构式: 结构简式: 或 ; 三、乙醇化学性质 1、与金属钠反应 2、氧化反应 (1)点燃: (2)催化氧化:
课后 反思 《化学课程标准》是在选修模块中才开始系统地学习有机化学的基础知识,对官能团的学习没有强化,在选修模块《有机化学基础》中对有机物知识的系统性则要求很高。所以我们并不需要去追求知识的系统性,亦不需要过多的知识迁移,不需要强化有机物的衍生转化关系。但是在实际的教学中,我们还是先学习物质的结构,再根据结构去推出性质,也就是在无形之中强化了官能团的学习,这样的教学学生的反馈也比较好。其中 对分子结构、反应产物通过实验探究、合作学习获得,这样有利于知识的掌握;从乙醇与乙烷的物理、化学性质的比较入手,得出官能团是决定化合物具有其特殊性质的基团,有助于学生对官能团的概念的理解。
