第三单元 物质构成的奥秘测试卷—2021—2022学年九年级化学人教版上册(word版 含解析)
文档属性
| 名称 | 第三单元 物质构成的奥秘测试卷—2021—2022学年九年级化学人教版上册(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 105.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-22 00:00:00 | ||
图片预览



文档简介
第三单元 物质构成的奥秘 测试卷
一、单选题(共15小题)
1.以下物质由原子构成的是( )
A. 蒸馏水
B. 氯化钠
C. 金刚石
D. 干冰
2.下列关于四种粒子的结构示意图的说法中正确的是( )
A. ①③属于不同种元素
B. ④属于离子,离子符号为Mg+2
C. ②③的化学性质相似
D. ④表示的元素是金属元素
3.水结成冰是由于( )
A. 水分子的运动停止了
B. 水分子的化学性质发生了改变
C. 水分子变小了
D. 水分子间的间隔发生了变化
4.下列事实不能说明分子之间有间隔的是( )
A. 墙内开花墙外香
B. 空气受热体积膨胀
C. 氧气加压降温形成液氧
D. 1体积酒精和1体积水混合小于2体积
5.关于氧分子和氧原子的说法,错误的是( )
A. 在化学变化中,氧分子能再分,氧原子不能
B. 氧分子大,氧原子小
C. 氧气的化学性质由氧分子保持
D. 氧气由氧分子构成,也由氧原子构成
6.对下列现象或事实的解释错误的是( )
A. 选项A
B. 选项B
C. 选项C
D. 选项D
7.将用塑料袋密封良好的方便面从平原带到高原时,塑料袋鼓起,是因为袋内的气体分子( )
A. 质量增大
B. 个数增多
C. 间隔增大
D. 体积增大
8.2014年5月,德国亥姆霍兹重离子研究中心再次成功合成117号元素。该元素已获正式名称“Ununseptium”,元素符号为Uus。该原子的原子核内有ll7个质子,原子质量约是氢原子质量的291倍,是目前获得正式承认的最重的原子。该原子的原子核外电子数为( )
A. 117
B. 174
C. 291
D. 408
9.原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A. 中子数为145
B. 核外电子数为94
C. 质子数为94
D. 核电荷数为239
10.下列有关原子结构的说法中正确的是( )
A. 氢、碳、氧的原子核都由质子和中子构成
B. “毒大米”中含有金属铬(Cr),铬原子序数为24,则质子数和中子数都为24
C. 氯原子的结构示意图为,在反应中若得到一个电子即变成氯离子(Cl-)
D. 质子和中子的相对质量都约等于1,每个质子、中子都带1个单位正电荷
11.镉属于重金属,会危害人体健康。2013年5月16日,广州市食品药品监管公布的结果显示,抽检大米四成镉超标。这里的镉可理解为( )
A. 镉元素
B. 镉单质
C. 镉离子
D. 镉原子
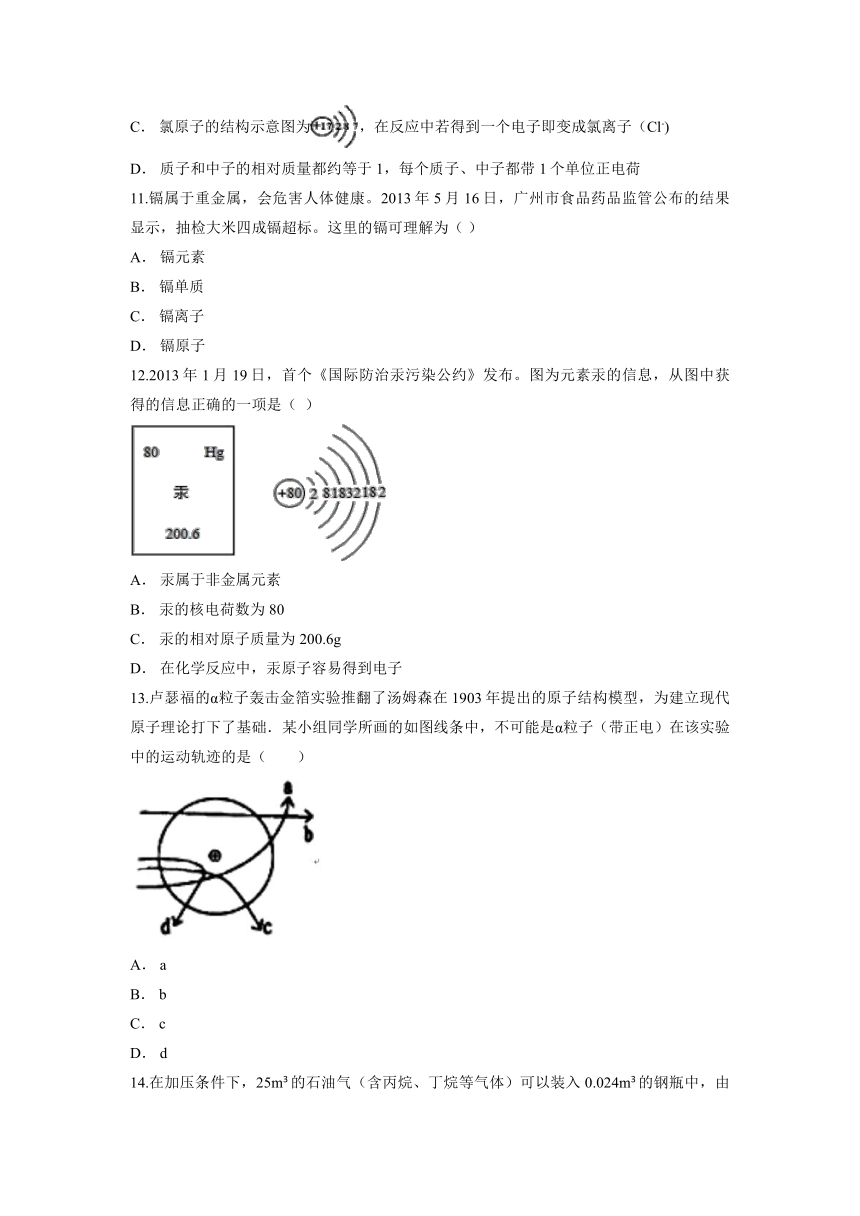
12.2013年1月19日,首个《国际防治汞污染公约》发布。图为元素汞的信息,从图中获得的信息正确的一项是( )
A. 汞属于非金属元素
B. 汞的核电荷数为80
C. 汞的相对原子质量为200.6g
D. 在化学反应中,汞原子容易得到电子
13.卢瑟福的α粒子轰击金箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础.某小组同学所画的如图线条中,不可能是α粒子(带正电)在该实验中的运动轨迹的是( )
A. a
B. b
C. c
D. d
14.在加压条件下,25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,由此可以说明的是( )
A. 分子的质量很小
B. 分子由原子构成
C. 分子之间有间隔
D. 分子在不断地运动
15.正在生产中的国产大型客机C919部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性。铝锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )
A. 元素符号不同
B. 原子质量不同
C. 原子的质子数不同
D. 原子的电子数不同
二、填空题(共3小题)
16.下图是某原子结构示意图,回答下列问题:
该原子最外层电子数为,由该数字你能获得的一条信息是。
17.如图是钠元素在元素周期表中的信息。
(1)上图方框的横线上填的是______。
(2)用化学符号和数字表示:3个氟原子________。
(3)钠元素属于___________(填“金属”或“非金属”)元素。
18.如图1是钠原子的结构示意图,结合图形回答下列问题:
(1)在化学反应中,钠原子一般易(填“得到”或“失去”)电子,形成(填“阳”或“阴”)离子。
(2)钠原子与图2哪种原子化学性质相似(填选项)。
三、实验与探究(共2小题)
19.实验探究
(1)实验方法:如图所示:在A烧杯中盛有浓氨水,在盛有20mL水的B烧杯中加入5~6滴酚酞溶液,从B烧杯中取少量溶液置于试管中,向其中滴加浓氨水,用一个大烧杯罩住AB两个小烧杯。
(2)实验现象:①过一会儿,观察到的现象:试管中的现象_________________________,
②AB烧杯中的现象__________________________________。
(3)你的猜想:_________________________________________________。
(4)讨论交流:与小组同学交流你的看法:往装有酚酞溶液的试管中加浓氨水这样操作的
目的_________________________________________________。
20.实验探究:某化学兴趣小组同学为了研究影响分子运动速率的因素,如下图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨水。浓氨水挥发出来的氨气(NH3)和浓盐酸挥发出来的氯化氢气体(HCl)能发生反应生成白色的氯化铵固体。两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,过一会,先在A处产生大量白烟,然后白烟逐渐充满整个试管。
根据现象回答问题:
(1)A处形成白烟是因为分子在___________________________;
(2)有同学认为先在A处产生白烟是因为氯化氢分子比氨气分子运动速度__________,已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成__________比。(填正或反)
答案解析
1.【答案】C
【解析】自然界中物质都是由微观的粒子构成的,微观的粒子有分子、原子、离子,学习中要能记住常见的由分子、原子、离子构成的物质,由分子构成的物质:常见的气体、水、有机物等;由原子构成的物质:金属、稀有气体、金刚石、晶体硅等;由离子构成的物质:氯化钠等。故选C。
2.【答案】D
【解析】A同种元素质子数一定相同,①③的质子数都是17,所以两者属于同种元素,故错误;B由于离子中质子数与核外电子数不等,④中质子数=12>电子数=10,是镁离子,符号为:Mg2+,故错误;C因为元素的性质和最外层电子数关系密切,所以最外层电子数相同则化学性质相似,②③的最外层电子数分别是1、7,故性质不会相似,故错误;D④表示的元素是镁元素,是金属元素,正确。故答案选D。
3.【答案】D
【解析】水结成冰的过程中,水分子的运动没有停止,只是减慢了,并且水分子的大小没有变化,水分子的化学性质也没有改变,这一过程中改变的是水分子之间的间隔。
4.【答案】A
【解析】墙内开花墙外香说明分子是不断运动的,而空气受热体积膨胀,氧气加压降温形成液氧,1体积酒精和体积水混合小于2体积都说明分子之间有间隔,所以答案选A。
5.【答案】D
【解析】氧气是由氧分子构成,不是由氧原子构成,而氧分子由氧原子构成,故选D。
6.【答案】C
【解析】温度升高,分子之间的间隔增大;温度降低,分子之间的间隔减少。气体热胀冷缩是因为气体分子之间的间隔随温度变化而变化,但是分子本身不会变大也不会变小。故选C。
7.【答案】C
【解析】从平原地区到高原地区,由于外界的气压变小,袋内的气体中的分子没有增多,本身也没有变化,变大的是分子间的间隔。所以应选C项。
8.【答案】A
【解析】元素为具有相同质子数即核电荷数的一类原子的总称,也就是说质子数决定元素种类,该元素的原子核内质子数等于原子核外的电子数,故选A。
9.【答案】D
【解析】在原子,中原子序数=质子数=核外电子数=核电荷数;质子数+中子数=相对原子质量,故选D
10.【答案】C
【解析】A.氢的原子核中没有中子,错误;B.“毒大米”中含有金属铬(Cr),铬原子序数为24,但质子数不等于中子数,它的中子数为28,错误;C.氯原子的最外层电子数为7,所以在反应中若得到一个电子即变成氯离子(Cl-),正确;D.质子和中子的相对质量都约等于1,每个质子都带1个单位正电荷,而中子不带电,错误。故答案应选C。
11.【答案】A
【解析】这里的镉是指镉元素,故选A
12.【答案】B
【解析】根据元素周期表中的一格中获取的信息,该元素的名称是汞,是唯一一种常温下是液态的金属元素,故A说法错误;根据元素周期表中的一格中获取的信息,汞的原子序数为80,根据原子序数=核电荷数可知,汞的核电荷数为80,故B说法正确;根据元素周期表中的一格中获取的信息,汞的相对原子质量为200.6,不是200.6g,因为相对原子质量是个比值,单位是1,故C说法错误;从汞原子的结构示意图可知,最外层有2个电子,在化学反应中易失去电子,故D说法错误。故选B。
13.【答案】A
【解析】卢瑟福所做的“α粒子轰击金箔实验”,可以探究出原子的构成。绝大多数α粒子通过金箔;一少部分α粒子方向发生了偏转,极少数的α粒子被反弹。所以答案选A
14.【答案】C
【解析】25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,说明分子之间有间隔。故选C。
15.【答案】C
【解析】元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,所以铝(Al)元素和锂(Li)元素的本质区别是质子数(即核电荷数)不同。故选C。
16.【答案】6 该元素是非金属元素;或该原子在化学反应中易得电子
【解析】观察原子结构示意图可知,该原子的最外层电子数为6;因为6大于4小于8,故该元素是非金属元素;或该原子在化学反应中易得电子。
17.【答案】(1)Na(2)3F(3)金属
【解析】上图方框的横线上填的是钠元素的元素符号Na,3 个氟原子表示为3F,钠元素属于金属元素。
18.【答案】(1)失去,阳; (2)A
【解析】(1)钠原子最外层电子数小于4个,易失去最外层电子,形成阳离子;(2)原子的化学性质主要由最外层电子数决定。A粒子最外层上有1个电子,故A与钠原子的化学性质相似。
19.【答案】(2)①液体变为红色 ;②A无明显变化,B烧杯中酚酞变红;
(3)分子在不断地运动;
(4)说明浓氨水能使酚酞变红
【解析】浓氨水显碱性能够使无色酚酞变红色,A烧杯中浓氨水中的氨气分子是不断运动着的,氨气分子运动到B烧杯中,能够使B烧杯中的无色酚酞变红,所以可以观察到B烧杯中酚酞变红,这一现象从而也证明了分子是不断运动的。往装有酚酞溶液的试管中加浓氨水这样操作的目的正是说明浓氨水能使酚酞变红。
20.【答案】(1)不停地运动(2)慢 反
【解析】由于浓盐酸中的氯化氢分子和浓氨水中的氨气分子都在不停地运动,所以会在A处形成白烟。形成的白烟在A处,离浓盐酸较近,离浓氨水较远,这是因为氯化氢分子运动速度比氨气分子运动速度慢。已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成反比。
一、单选题(共15小题)
1.以下物质由原子构成的是( )
A. 蒸馏水
B. 氯化钠
C. 金刚石
D. 干冰
2.下列关于四种粒子的结构示意图的说法中正确的是( )
A. ①③属于不同种元素
B. ④属于离子,离子符号为Mg+2
C. ②③的化学性质相似
D. ④表示的元素是金属元素
3.水结成冰是由于( )
A. 水分子的运动停止了
B. 水分子的化学性质发生了改变
C. 水分子变小了
D. 水分子间的间隔发生了变化
4.下列事实不能说明分子之间有间隔的是( )
A. 墙内开花墙外香
B. 空气受热体积膨胀
C. 氧气加压降温形成液氧
D. 1体积酒精和1体积水混合小于2体积
5.关于氧分子和氧原子的说法,错误的是( )
A. 在化学变化中,氧分子能再分,氧原子不能
B. 氧分子大,氧原子小
C. 氧气的化学性质由氧分子保持
D. 氧气由氧分子构成,也由氧原子构成
6.对下列现象或事实的解释错误的是( )
A. 选项A
B. 选项B
C. 选项C
D. 选项D
7.将用塑料袋密封良好的方便面从平原带到高原时,塑料袋鼓起,是因为袋内的气体分子( )
A. 质量增大
B. 个数增多
C. 间隔增大
D. 体积增大
8.2014年5月,德国亥姆霍兹重离子研究中心再次成功合成117号元素。该元素已获正式名称“Ununseptium”,元素符号为Uus。该原子的原子核内有ll7个质子,原子质量约是氢原子质量的291倍,是目前获得正式承认的最重的原子。该原子的原子核外电子数为( )
A. 117
B. 174
C. 291
D. 408
9.原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A. 中子数为145
B. 核外电子数为94
C. 质子数为94
D. 核电荷数为239
10.下列有关原子结构的说法中正确的是( )
A. 氢、碳、氧的原子核都由质子和中子构成
B. “毒大米”中含有金属铬(Cr),铬原子序数为24,则质子数和中子数都为24
C. 氯原子的结构示意图为,在反应中若得到一个电子即变成氯离子(Cl-)
D. 质子和中子的相对质量都约等于1,每个质子、中子都带1个单位正电荷
11.镉属于重金属,会危害人体健康。2013年5月16日,广州市食品药品监管公布的结果显示,抽检大米四成镉超标。这里的镉可理解为( )
A. 镉元素
B. 镉单质
C. 镉离子
D. 镉原子
12.2013年1月19日,首个《国际防治汞污染公约》发布。图为元素汞的信息,从图中获得的信息正确的一项是( )
A. 汞属于非金属元素
B. 汞的核电荷数为80
C. 汞的相对原子质量为200.6g
D. 在化学反应中,汞原子容易得到电子
13.卢瑟福的α粒子轰击金箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础.某小组同学所画的如图线条中,不可能是α粒子(带正电)在该实验中的运动轨迹的是( )
A. a
B. b
C. c
D. d
14.在加压条件下,25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,由此可以说明的是( )
A. 分子的质量很小
B. 分子由原子构成
C. 分子之间有间隔
D. 分子在不断地运动
15.正在生产中的国产大型客机C919部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性。铝锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )
A. 元素符号不同
B. 原子质量不同
C. 原子的质子数不同
D. 原子的电子数不同
二、填空题(共3小题)
16.下图是某原子结构示意图,回答下列问题:
该原子最外层电子数为,由该数字你能获得的一条信息是。
17.如图是钠元素在元素周期表中的信息。
(1)上图方框的横线上填的是______。
(2)用化学符号和数字表示:3个氟原子________。
(3)钠元素属于___________(填“金属”或“非金属”)元素。
18.如图1是钠原子的结构示意图,结合图形回答下列问题:
(1)在化学反应中,钠原子一般易(填“得到”或“失去”)电子,形成(填“阳”或“阴”)离子。
(2)钠原子与图2哪种原子化学性质相似(填选项)。
三、实验与探究(共2小题)
19.实验探究
(1)实验方法:如图所示:在A烧杯中盛有浓氨水,在盛有20mL水的B烧杯中加入5~6滴酚酞溶液,从B烧杯中取少量溶液置于试管中,向其中滴加浓氨水,用一个大烧杯罩住AB两个小烧杯。
(2)实验现象:①过一会儿,观察到的现象:试管中的现象_________________________,
②AB烧杯中的现象__________________________________。
(3)你的猜想:_________________________________________________。
(4)讨论交流:与小组同学交流你的看法:往装有酚酞溶液的试管中加浓氨水这样操作的
目的_________________________________________________。
20.实验探究:某化学兴趣小组同学为了研究影响分子运动速率的因素,如下图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨水。浓氨水挥发出来的氨气(NH3)和浓盐酸挥发出来的氯化氢气体(HCl)能发生反应生成白色的氯化铵固体。两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,过一会,先在A处产生大量白烟,然后白烟逐渐充满整个试管。
根据现象回答问题:
(1)A处形成白烟是因为分子在___________________________;
(2)有同学认为先在A处产生白烟是因为氯化氢分子比氨气分子运动速度__________,已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成__________比。(填正或反)
答案解析
1.【答案】C
【解析】自然界中物质都是由微观的粒子构成的,微观的粒子有分子、原子、离子,学习中要能记住常见的由分子、原子、离子构成的物质,由分子构成的物质:常见的气体、水、有机物等;由原子构成的物质:金属、稀有气体、金刚石、晶体硅等;由离子构成的物质:氯化钠等。故选C。
2.【答案】D
【解析】A同种元素质子数一定相同,①③的质子数都是17,所以两者属于同种元素,故错误;B由于离子中质子数与核外电子数不等,④中质子数=12>电子数=10,是镁离子,符号为:Mg2+,故错误;C因为元素的性质和最外层电子数关系密切,所以最外层电子数相同则化学性质相似,②③的最外层电子数分别是1、7,故性质不会相似,故错误;D④表示的元素是镁元素,是金属元素,正确。故答案选D。
3.【答案】D
【解析】水结成冰的过程中,水分子的运动没有停止,只是减慢了,并且水分子的大小没有变化,水分子的化学性质也没有改变,这一过程中改变的是水分子之间的间隔。
4.【答案】A
【解析】墙内开花墙外香说明分子是不断运动的,而空气受热体积膨胀,氧气加压降温形成液氧,1体积酒精和体积水混合小于2体积都说明分子之间有间隔,所以答案选A。
5.【答案】D
【解析】氧气是由氧分子构成,不是由氧原子构成,而氧分子由氧原子构成,故选D。
6.【答案】C
【解析】温度升高,分子之间的间隔增大;温度降低,分子之间的间隔减少。气体热胀冷缩是因为气体分子之间的间隔随温度变化而变化,但是分子本身不会变大也不会变小。故选C。
7.【答案】C
【解析】从平原地区到高原地区,由于外界的气压变小,袋内的气体中的分子没有增多,本身也没有变化,变大的是分子间的间隔。所以应选C项。
8.【答案】A
【解析】元素为具有相同质子数即核电荷数的一类原子的总称,也就是说质子数决定元素种类,该元素的原子核内质子数等于原子核外的电子数,故选A。
9.【答案】D
【解析】在原子,中原子序数=质子数=核外电子数=核电荷数;质子数+中子数=相对原子质量,故选D
10.【答案】C
【解析】A.氢的原子核中没有中子,错误;B.“毒大米”中含有金属铬(Cr),铬原子序数为24,但质子数不等于中子数,它的中子数为28,错误;C.氯原子的最外层电子数为7,所以在反应中若得到一个电子即变成氯离子(Cl-),正确;D.质子和中子的相对质量都约等于1,每个质子都带1个单位正电荷,而中子不带电,错误。故答案应选C。
11.【答案】A
【解析】这里的镉是指镉元素,故选A
12.【答案】B
【解析】根据元素周期表中的一格中获取的信息,该元素的名称是汞,是唯一一种常温下是液态的金属元素,故A说法错误;根据元素周期表中的一格中获取的信息,汞的原子序数为80,根据原子序数=核电荷数可知,汞的核电荷数为80,故B说法正确;根据元素周期表中的一格中获取的信息,汞的相对原子质量为200.6,不是200.6g,因为相对原子质量是个比值,单位是1,故C说法错误;从汞原子的结构示意图可知,最外层有2个电子,在化学反应中易失去电子,故D说法错误。故选B。
13.【答案】A
【解析】卢瑟福所做的“α粒子轰击金箔实验”,可以探究出原子的构成。绝大多数α粒子通过金箔;一少部分α粒子方向发生了偏转,极少数的α粒子被反弹。所以答案选A
14.【答案】C
【解析】25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,说明分子之间有间隔。故选C。
15.【答案】C
【解析】元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,所以铝(Al)元素和锂(Li)元素的本质区别是质子数(即核电荷数)不同。故选C。
16.【答案】6 该元素是非金属元素;或该原子在化学反应中易得电子
【解析】观察原子结构示意图可知,该原子的最外层电子数为6;因为6大于4小于8,故该元素是非金属元素;或该原子在化学反应中易得电子。
17.【答案】(1)Na(2)3F(3)金属
【解析】上图方框的横线上填的是钠元素的元素符号Na,3 个氟原子表示为3F,钠元素属于金属元素。
18.【答案】(1)失去,阳; (2)A
【解析】(1)钠原子最外层电子数小于4个,易失去最外层电子,形成阳离子;(2)原子的化学性质主要由最外层电子数决定。A粒子最外层上有1个电子,故A与钠原子的化学性质相似。
19.【答案】(2)①液体变为红色 ;②A无明显变化,B烧杯中酚酞变红;
(3)分子在不断地运动;
(4)说明浓氨水能使酚酞变红
【解析】浓氨水显碱性能够使无色酚酞变红色,A烧杯中浓氨水中的氨气分子是不断运动着的,氨气分子运动到B烧杯中,能够使B烧杯中的无色酚酞变红,所以可以观察到B烧杯中酚酞变红,这一现象从而也证明了分子是不断运动的。往装有酚酞溶液的试管中加浓氨水这样操作的目的正是说明浓氨水能使酚酞变红。
20.【答案】(1)不停地运动(2)慢 反
【解析】由于浓盐酸中的氯化氢分子和浓氨水中的氨气分子都在不停地运动,所以会在A处形成白烟。形成的白烟在A处,离浓盐酸较近,离浓氨水较远,这是因为氯化氢分子运动速度比氨气分子运动速度慢。已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成反比。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
