人教版九年级下册化学 第九单元 溶液 练习题(含答案)
文档属性
| 名称 | 人教版九年级下册化学 第九单元 溶液 练习题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 104.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-22 21:56:20 | ||
图片预览


文档简介
(
…………○…………外…………○…………装…………○…………订…………○…………线…………○…………
) (
※※请※※不※※要※※在※※装※※订※※线※※内※※答※※题※※
) (
…………○…………内…………○…………装…………○…………订…………○…………线…………○…………
)
人教版九年级下册化学 第九单元 溶液
一、单选题
1.某混合物其组成特点是“各成分彼此完全混合,处处相同”,这种混合物不可能是()
A. 食盐水 B. 黄泥水 C. 空气 D. 盐酸
2.下列溶液中,溶剂不是水的是( )
A. 蔗糖溶液 B. 生理盐水 C. 碘的酒精溶液 D. 稀盐酸
3.下列所示约图象与实验相符合的是( )
A. 饱和Ca(OH)2溶液升温
B. 镁在空气中燃烧
C. 向含少量氢氧化钠的碳酸钠溶液中逐渐加入稀盐酸过量
D. 等质量的镁片,锌片分别和足量的稀硫酸反应
4.推理是学习化学的一种重要方法,但不合理的推理会得到不符合题意结论。以下推理正确的是()
A. 分子可以构成物质——物质一定由分子构成
B. 溶液具有均一性和稳定性——具有均一性、稳定性的液体一定是溶液
C. 单质中只含有一种元素,含有一种元素的纯净物一定是单质
D. 离子是带电荷的微粒,带电荷的微粒一定是离子
5.在“停课不停学”期间,小兰同学通过网课学习了溶液的形成后,将少量下列物质分别放入水中并充分搅拌,其中不能形成溶液的是( )
A. 白砂糖 B. 食盐 C. 纯碱 D. 植物油
6.如图为甲、乙两种固体(不含结晶水)在水中的溶解度曲线,下列说法正确的是( )
A. 除去甲中少量的乙,用蒸发结晶的方法
B. t1℃甲的饱和溶液中溶质和溶剂的质量比为1:5
C. t2℃时,将等质量的甲和乙配成饱和溶液,所得溶液质量甲<乙
D. 将t2℃时甲和乙的饱和溶液降温至t1℃,溶质质量分数甲=乙
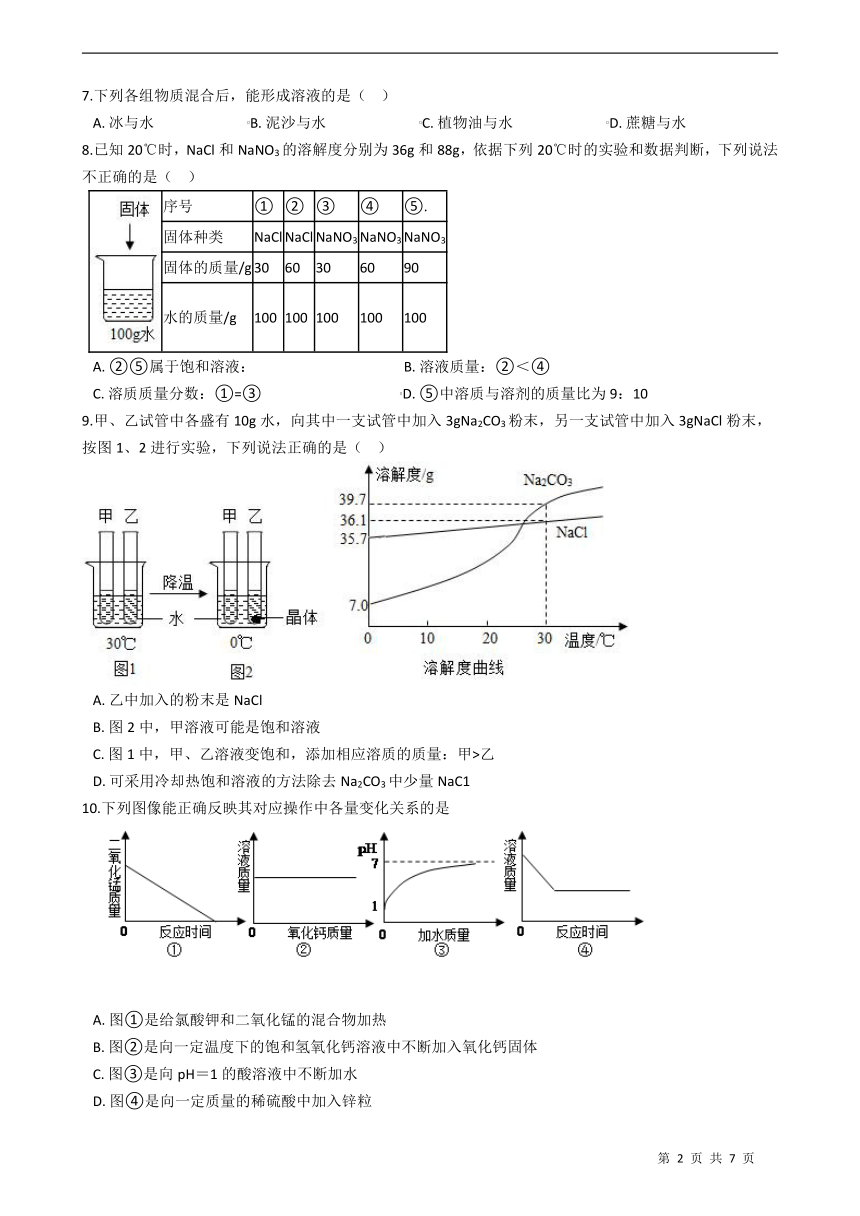
7.下列各组物质混合后,能形成溶液的是( )
A. 冰与水 B. 泥沙与水 C. 植物油与水 D. 蔗糖与水
8.已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g,依据下列20℃时的实验和数据判断,下列说法不正确的是( )
序号 ① ② ③ ④ ⑤.
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
A. ②⑤属于饱和溶液: B. 溶液质量:②<④
C. 溶质质量分数:①=③ D. ⑤中溶质与溶剂的质量比为9:10
9.甲、乙试管中各盛有10g水,向其中一支试管中加入3gNa2CO3粉末,另一支试管中加入3gNaCl粉末,按图1、2进行实验,下列说法正确的是( )
A. 乙中加入的粉末是NaCl
B. 图2中,甲溶液可能是饱和溶液
C. 图1中,甲、乙溶液变饱和,添加相应溶质的质量:甲>乙
D. 可采用冷却热饱和溶液的方法除去Na2CO3中少量NaC1
10.下列图像能正确反映其对应操作中各量变化关系的是
A. 图①是给氯酸钾和二氧化锰的混合物加热
B. 图②是向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
C. 图③是向pH=1的酸溶液中不断加水
D. 图④是向一定质量的稀硫酸中加入锌粒
11.甲、乙两种不含结晶水的固体的溶解度曲线如图所示.下列说法中正确的是( )
A. t3℃时,甲的饱和溶液溶质与溶液的质量比为1:2
B. t1℃时,甲的溶解度大于乙的溶解度
C. t2℃时,甲、乙溶液的溶质质量分数都为30%
D. t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙的质量
12.下图所示为甲、乙两物质的溶解度曲线。20℃时,取甲、乙两种物质(均不含结晶水)各30g,分别加入到100g水中,使之充分溶解,得到相应的混合物。下列有关说法不正确的是( )
A. 20℃时,所得甲、乙两种溶液的质量相等
B. 将混合物分别冷却到0℃时,溶液中溶质的质量分数甲小于乙
C. 将混合物分别升高到50℃时,分别得到甲和乙的不饱和溶液
D. 若将20℃时的两种混合物降温至0℃,得到晶体的质量相等
二、填空题
13.如图甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
(1)20℃时,三种物质的溶解度由大到小的顺序是 ;
(2)当乙中混有少量的甲时,可采用 结晶的方法提纯乙;
(3)50℃时,配制一定量甲物质的饱和溶液,将溶液降温到10℃时,该溶液的溶质质量分数一定减小,该说法是 (填“正确”或“错误”).
(4)20℃时,向盛有20g乙物质的烧杯中加入50g水,充分溶解后形成的是 (填“饱和”或“不饱和”)溶液;
再将烧杯内的物质升温到50℃,此时溶液中溶质与溶剂的质量之比为 .
14.铁和稀硫酸恰好完全反应后的溶液中,溶质的名称是 . 氢气在氯气中燃烧生成的氯化氢气体溶于水得到盐酸,盐酸中的溶质名称是 .
15.水是人类最宝贵的资源,也是一种常用的溶剂.用你学过的化学知识回答下列问题:
(1)自然界中的水都不是纯水,欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是 .
(2)某同学在完成电解水实验时,发现正极产生4mL气体,则负极产生的气体体积是 mL.
(3)如图所示是硝酸钾和氯化钾的溶解度曲线.
① ℃时,两种物质的溶解度相等.
②60℃时,将硝酸钾的饱和溶液转化为不饱和溶液的方法有 (填一种).
16. 一定条件下,某物质溶解于水的实验数据如下表,请回答有关问题。
实验序号 温度/℃ 水的质量/g 所加物质质量/g 溶液质量/g
① 20 10 2 12
② 20 15 2.5 a
③ 20 20 7 26
④ 30 20 7 27
(1)表中a= 。
(2)20℃时,该物质的溶解度为 。
(3)右图中,能表示该物质溶解度的曲线是 (填字母)。
(4)所得溶液一定为饱和溶液的是 (填实验序号,下同); 所得溶液中溶质质量分数最大的是 。
(5)温度不变,将①、②所得溶液混合后,向其中再加入 g该物质,能使溶液恰好达到饱和。
17.在实验室配制溶液时,常涉及以下过程:①称量、量取;②过滤;③蒸发结晶、干燥;④计算;⑤溶解.请按要求回答下列问题:
(1)甲同学用氯化钠和蒸馏水配制50g5%的氯化钠溶液.现实验室中有10mL、50mL、100mL等不同规格的量筒,配制上述溶液时最好选用 mL的量筒.
(2)乙同学用10g含杂质10%的食盐(杂质不溶于水)和蒸馏水配制50g溶质质量分数一定的氯化钠溶液,正确的操作顺序是(操作步骤可重复使用) (用以上序号填空).若乙同学将所得精盐完全用于配制该溶液,则所得溶液的溶质质量分数为 .
三、综合题
18.下图是a、b、c三种物质的溶解度曲线,根据图像回答下列问题
(1)t2℃时30ga物质加入到50g水中不断搅拌,能形成 g溶液,溶质质量分数为
(2)t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是 (填写物质序号)。
(3)相同质量的a、b、c三种物t2℃时的饱和溶液降温到t1℃时,析出晶体较多的是 , 没有晶体析出的是
(4)将t1℃时a、b、c三种物成饱和溶液的溫度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是 (填写物质序号)
19.碳酸钾广泛应用于玻璃、纺织印染和肥皂生产等领域,制取碳酸钾的工艺流程示意图如下:
温度/°C 0 10 20 30 40 60 80 100
K2CO3的溶解度/g 107.0 109.0 111.0 114.0 117.0 126.0 139.0 156.0
根据以上图表信息,回答下列问题:
(1)生成碳酸钾的化学方程式为________。
(2)上述流程中可循环使用的物质是________,NH4Cl在农业上可用作________。
(3)得到K2CO3晶浆的结晶方法是________。
(4)上述流程中洗涤K2CO3晶体应选用________(填序号)。
①NH4Cl溶液
②热水
③饱和K2CO3溶液
答案部分
一、单选题
1.【答案】 B
2.【答案】 C
3.【答案】 C
4.【答案】 C
5.【答案】 D
6.【答案】 C
7.【答案】 D
8.【答案】 D
9.【答案】 D
10.【答案】 C
11.【答案】 D
12.【答案】 D
二、填空题
13.【答案】 乙>甲>丙;蒸发溶剂;正确;饱和;2:5
14.【答案】 硫酸亚铁;氯化氢
15.【答案】 引流;8;t;升高温度
16.【答案】 17.5;30 g;A;③;④;3
17.【答案】 50;⑤②③④①⑤;18%
三、综合题
18.【答案】 (1)75;33.3%
(2)abc
(3)a;c
(4)b>a>c
19.【答案】 (1)
(2)有机萃剂;氮肥
(3)蒸发结晶
(4)③
(
第
一
页 共
1
页
)
…………○…………外…………○…………装…………○…………订…………○…………线…………○…………
) (
※※请※※不※※要※※在※※装※※订※※线※※内※※答※※题※※
) (
…………○…………内…………○…………装…………○…………订…………○…………线…………○…………
)
人教版九年级下册化学 第九单元 溶液
一、单选题
1.某混合物其组成特点是“各成分彼此完全混合,处处相同”,这种混合物不可能是()
A. 食盐水 B. 黄泥水 C. 空气 D. 盐酸
2.下列溶液中,溶剂不是水的是( )
A. 蔗糖溶液 B. 生理盐水 C. 碘的酒精溶液 D. 稀盐酸
3.下列所示约图象与实验相符合的是( )
A. 饱和Ca(OH)2溶液升温
B. 镁在空气中燃烧
C. 向含少量氢氧化钠的碳酸钠溶液中逐渐加入稀盐酸过量
D. 等质量的镁片,锌片分别和足量的稀硫酸反应
4.推理是学习化学的一种重要方法,但不合理的推理会得到不符合题意结论。以下推理正确的是()
A. 分子可以构成物质——物质一定由分子构成
B. 溶液具有均一性和稳定性——具有均一性、稳定性的液体一定是溶液
C. 单质中只含有一种元素,含有一种元素的纯净物一定是单质
D. 离子是带电荷的微粒,带电荷的微粒一定是离子
5.在“停课不停学”期间,小兰同学通过网课学习了溶液的形成后,将少量下列物质分别放入水中并充分搅拌,其中不能形成溶液的是( )
A. 白砂糖 B. 食盐 C. 纯碱 D. 植物油
6.如图为甲、乙两种固体(不含结晶水)在水中的溶解度曲线,下列说法正确的是( )
A. 除去甲中少量的乙,用蒸发结晶的方法
B. t1℃甲的饱和溶液中溶质和溶剂的质量比为1:5
C. t2℃时,将等质量的甲和乙配成饱和溶液,所得溶液质量甲<乙
D. 将t2℃时甲和乙的饱和溶液降温至t1℃,溶质质量分数甲=乙
7.下列各组物质混合后,能形成溶液的是( )
A. 冰与水 B. 泥沙与水 C. 植物油与水 D. 蔗糖与水
8.已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g,依据下列20℃时的实验和数据判断,下列说法不正确的是( )
序号 ① ② ③ ④ ⑤.
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
A. ②⑤属于饱和溶液: B. 溶液质量:②<④
C. 溶质质量分数:①=③ D. ⑤中溶质与溶剂的质量比为9:10
9.甲、乙试管中各盛有10g水,向其中一支试管中加入3gNa2CO3粉末,另一支试管中加入3gNaCl粉末,按图1、2进行实验,下列说法正确的是( )
A. 乙中加入的粉末是NaCl
B. 图2中,甲溶液可能是饱和溶液
C. 图1中,甲、乙溶液变饱和,添加相应溶质的质量:甲>乙
D. 可采用冷却热饱和溶液的方法除去Na2CO3中少量NaC1
10.下列图像能正确反映其对应操作中各量变化关系的是
A. 图①是给氯酸钾和二氧化锰的混合物加热
B. 图②是向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
C. 图③是向pH=1的酸溶液中不断加水
D. 图④是向一定质量的稀硫酸中加入锌粒
11.甲、乙两种不含结晶水的固体的溶解度曲线如图所示.下列说法中正确的是( )
A. t3℃时,甲的饱和溶液溶质与溶液的质量比为1:2
B. t1℃时,甲的溶解度大于乙的溶解度
C. t2℃时,甲、乙溶液的溶质质量分数都为30%
D. t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙的质量
12.下图所示为甲、乙两物质的溶解度曲线。20℃时,取甲、乙两种物质(均不含结晶水)各30g,分别加入到100g水中,使之充分溶解,得到相应的混合物。下列有关说法不正确的是( )
A. 20℃时,所得甲、乙两种溶液的质量相等
B. 将混合物分别冷却到0℃时,溶液中溶质的质量分数甲小于乙
C. 将混合物分别升高到50℃时,分别得到甲和乙的不饱和溶液
D. 若将20℃时的两种混合物降温至0℃,得到晶体的质量相等
二、填空题
13.如图甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
(1)20℃时,三种物质的溶解度由大到小的顺序是 ;
(2)当乙中混有少量的甲时,可采用 结晶的方法提纯乙;
(3)50℃时,配制一定量甲物质的饱和溶液,将溶液降温到10℃时,该溶液的溶质质量分数一定减小,该说法是 (填“正确”或“错误”).
(4)20℃时,向盛有20g乙物质的烧杯中加入50g水,充分溶解后形成的是 (填“饱和”或“不饱和”)溶液;
再将烧杯内的物质升温到50℃,此时溶液中溶质与溶剂的质量之比为 .
14.铁和稀硫酸恰好完全反应后的溶液中,溶质的名称是 . 氢气在氯气中燃烧生成的氯化氢气体溶于水得到盐酸,盐酸中的溶质名称是 .
15.水是人类最宝贵的资源,也是一种常用的溶剂.用你学过的化学知识回答下列问题:
(1)自然界中的水都不是纯水,欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是 .
(2)某同学在完成电解水实验时,发现正极产生4mL气体,则负极产生的气体体积是 mL.
(3)如图所示是硝酸钾和氯化钾的溶解度曲线.
① ℃时,两种物质的溶解度相等.
②60℃时,将硝酸钾的饱和溶液转化为不饱和溶液的方法有 (填一种).
16. 一定条件下,某物质溶解于水的实验数据如下表,请回答有关问题。
实验序号 温度/℃ 水的质量/g 所加物质质量/g 溶液质量/g
① 20 10 2 12
② 20 15 2.5 a
③ 20 20 7 26
④ 30 20 7 27
(1)表中a= 。
(2)20℃时,该物质的溶解度为 。
(3)右图中,能表示该物质溶解度的曲线是 (填字母)。
(4)所得溶液一定为饱和溶液的是 (填实验序号,下同); 所得溶液中溶质质量分数最大的是 。
(5)温度不变,将①、②所得溶液混合后,向其中再加入 g该物质,能使溶液恰好达到饱和。
17.在实验室配制溶液时,常涉及以下过程:①称量、量取;②过滤;③蒸发结晶、干燥;④计算;⑤溶解.请按要求回答下列问题:
(1)甲同学用氯化钠和蒸馏水配制50g5%的氯化钠溶液.现实验室中有10mL、50mL、100mL等不同规格的量筒,配制上述溶液时最好选用 mL的量筒.
(2)乙同学用10g含杂质10%的食盐(杂质不溶于水)和蒸馏水配制50g溶质质量分数一定的氯化钠溶液,正确的操作顺序是(操作步骤可重复使用) (用以上序号填空).若乙同学将所得精盐完全用于配制该溶液,则所得溶液的溶质质量分数为 .
三、综合题
18.下图是a、b、c三种物质的溶解度曲线,根据图像回答下列问题
(1)t2℃时30ga物质加入到50g水中不断搅拌,能形成 g溶液,溶质质量分数为
(2)t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是 (填写物质序号)。
(3)相同质量的a、b、c三种物t2℃时的饱和溶液降温到t1℃时,析出晶体较多的是 , 没有晶体析出的是
(4)将t1℃时a、b、c三种物成饱和溶液的溫度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是 (填写物质序号)
19.碳酸钾广泛应用于玻璃、纺织印染和肥皂生产等领域,制取碳酸钾的工艺流程示意图如下:
温度/°C 0 10 20 30 40 60 80 100
K2CO3的溶解度/g 107.0 109.0 111.0 114.0 117.0 126.0 139.0 156.0
根据以上图表信息,回答下列问题:
(1)生成碳酸钾的化学方程式为________。
(2)上述流程中可循环使用的物质是________,NH4Cl在农业上可用作________。
(3)得到K2CO3晶浆的结晶方法是________。
(4)上述流程中洗涤K2CO3晶体应选用________(填序号)。
①NH4Cl溶液
②热水
③饱和K2CO3溶液
答案部分
一、单选题
1.【答案】 B
2.【答案】 C
3.【答案】 C
4.【答案】 C
5.【答案】 D
6.【答案】 C
7.【答案】 D
8.【答案】 D
9.【答案】 D
10.【答案】 C
11.【答案】 D
12.【答案】 D
二、填空题
13.【答案】 乙>甲>丙;蒸发溶剂;正确;饱和;2:5
14.【答案】 硫酸亚铁;氯化氢
15.【答案】 引流;8;t;升高温度
16.【答案】 17.5;30 g;A;③;④;3
17.【答案】 50;⑤②③④①⑤;18%
三、综合题
18.【答案】 (1)75;33.3%
(2)abc
(3)a;c
(4)b>a>c
19.【答案】 (1)
(2)有机萃剂;氮肥
(3)蒸发结晶
(4)③
(
第
一
页 共
1
页
)
同课章节目录
