平衡的图像
图片预览





文档简介
课件39张PPT。化学平衡中的常见图像
速率-时间图
浓度-时间图
转化率(或百分含量)-时间-温度(或压强)图
转化率(或百分含量)-温度-压强图⒈五看图像
⑴面:即明确横纵坐标的意义;
⑵线:了解线的走向和变化趋势;
⑶点:即起点、交点、终点、拐点与极值点等
⑷辅助线:如等温线、等压线、平衡线等;
⑸量的变化:如浓度、温度、压强的变化等。 图像题是化学平衡中的常见题型,这类题目是考查自变量(如时间、温度、压强等)与因变量(如物质的量、浓度、百分含量、转化率)之间的定量或定性关系。⒉分析判断
⑴根据到达平衡的时间长短,结合化学反应速率理论判断温度的高低或压强的大小;
⑵根据图像中量的变化判断平衡移动的方向,结合平衡移动原理,分析可逆反应的特点(是气体分子数增大还是减小的反应;或是吸热还是放热反应);
⑶定一议二:若图像中有三个量,要先固定一个自变量,再讨论另外两个量之间的关系;思维要全面,要注意变换定量与变量,最后下综合结论。 可用于:
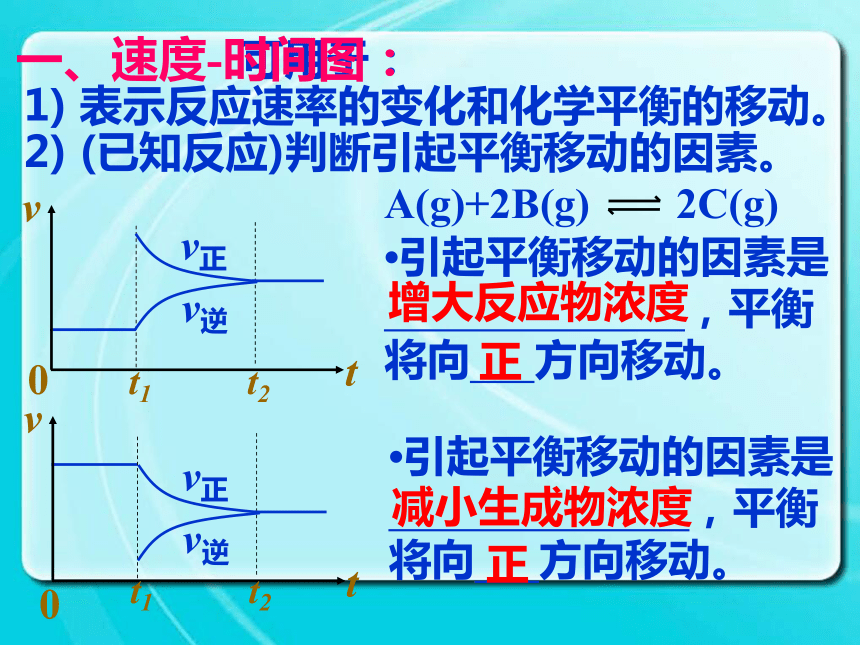
1) 表示反应速率的变化和化学平衡的移动。
2) (已知反应)判断引起平衡移动的因素。一、速度-时间图:增大反应物浓度正?引起平衡移动的因素是
,平衡
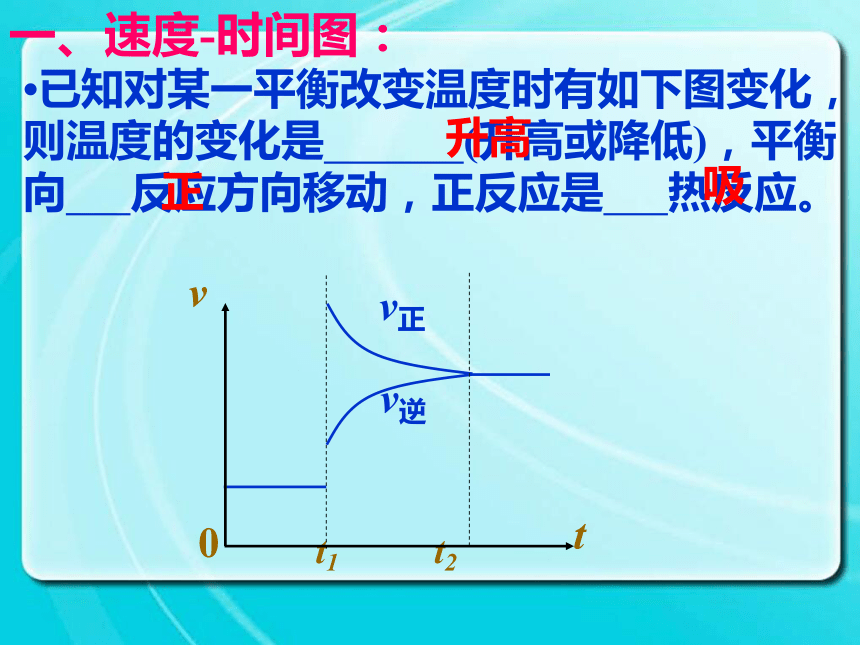
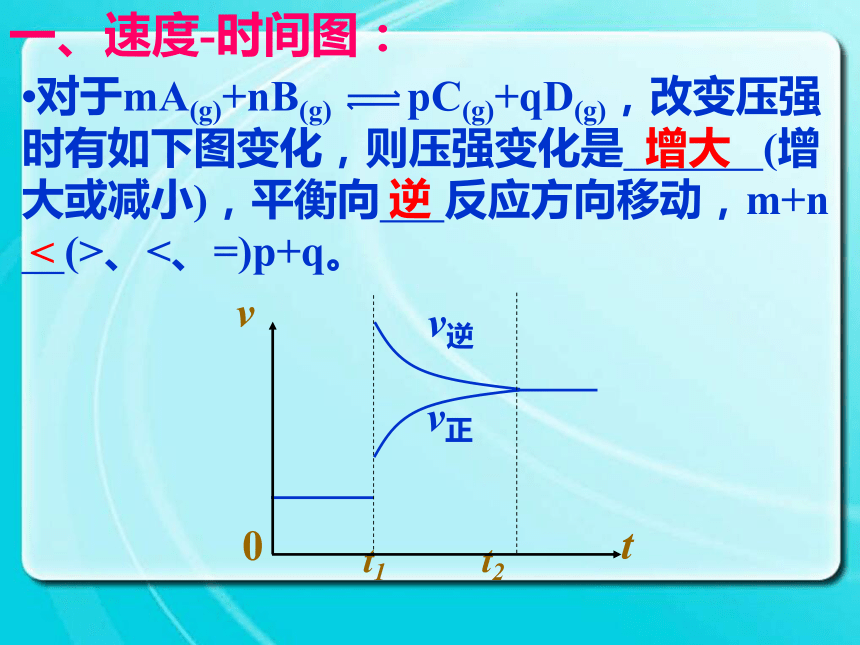
将向 方向移动。减小生成物浓度正一、速度-时间图:?已知对某一平衡改变温度时有如下图变化,则温度的变化是 (升高或降低),平衡向 反应方向移动,正反应是 热反应。升高正吸一、速度-时间图:?对于mA(g)+nB(g) pC(g)+qD(g),改变压强时有如下图变化,则压强变化是 (增大或减小),平衡向 反应方向移动,m+n
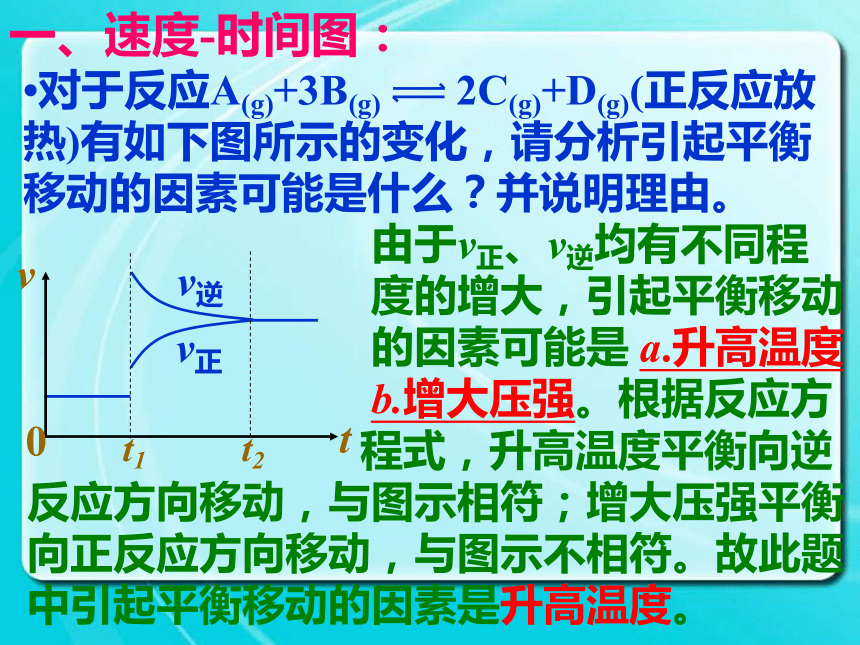
(>、<、=)p+q。增大逆<一、速度-时间图:?对于反应A(g)+3B(g) 2C(g)+D(g)(正反应放热)有如下图所示的变化,请分析引起平衡移动的因素可能是什么?并说明理由。 由于v正、v逆均有不同程
度的增大,引起平衡移动
的因素可能是 a.升高温度
b.增大压强。根据反应方
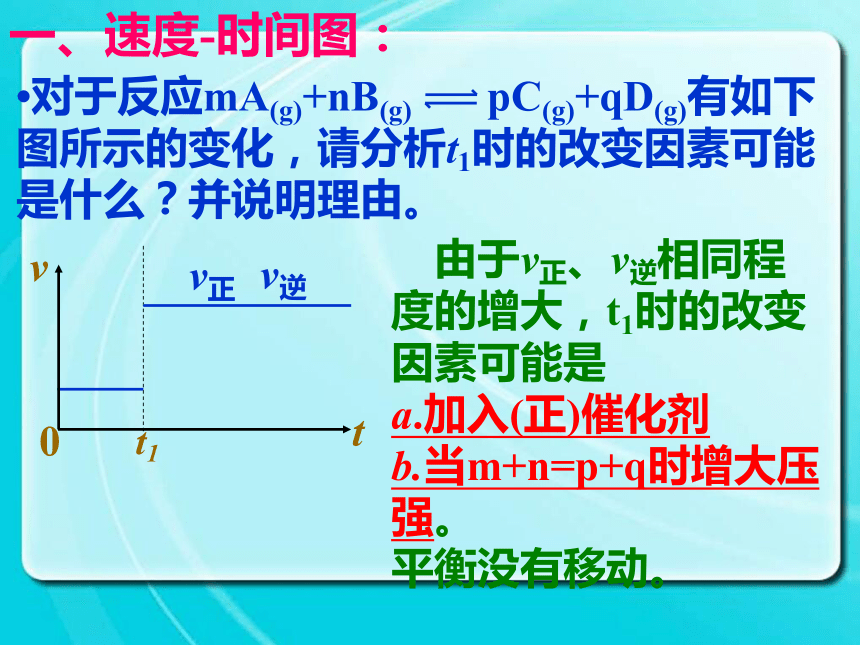
程式,升高温度平衡向逆反应方向移动,与图示相符;增大压强平衡向正反应方向移动,与图示不相符。故此题中引起平衡移动的因素是升高温度。?对于反应mA(g)+nB(g) pC(g)+qD(g)有如下图所示的变化,请分析t1时的改变因素可能是什么?并说明理由。一、速度-时间图: 由于v正、v逆相同程 度的增大,t1时的改变因素可能是
a.加入(正)催化剂
b.当m+n=p+q时增大压强。
平衡没有移动。速率 - 时间图的关键:
①看出反应速率的变化,是增大还是减小。
②根据正逆反应速率的相对大小,判断化学平衡的移动方向
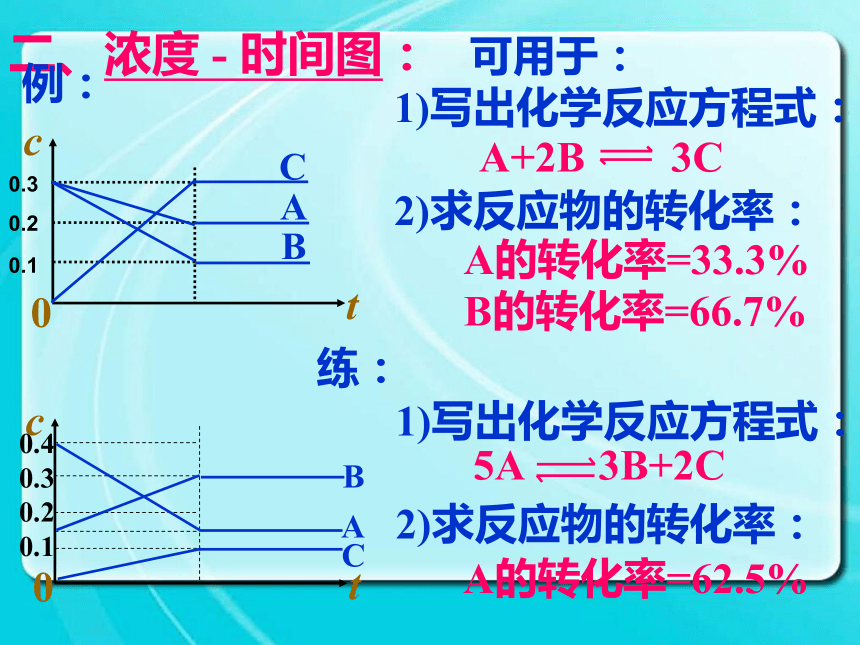
③结合勒夏特列原理分析判断影响化学平衡移动的因素。二、浓度 - 时间图: 可用于:
1)写出化学反应方程式:
2)求反应物的转化率:A+2B 3CA的转化率=33.3%
B的转化率=66.7%1)写出化学反应方程式:
2)求反应物的转化率:例:练:5A 3B+2CA的转化率=62.5%
0.2
0.10.3浓度 - 时间图的关键:
①写出反应方程式
A、何为反应物、生成物
B、反应物、生成物计量数关系
C、是否为可逆反应
②计算反应物的转化率
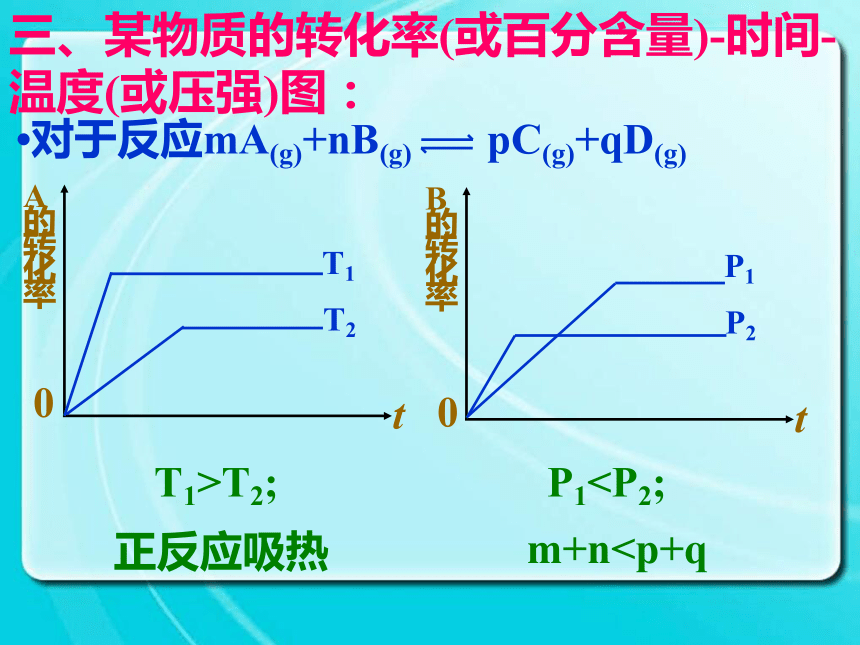
③计算某物质的化学反应速率三、某物质的转化率(或百分含量)-时间-温度(或压强)图:?对于反应mA(g)+nB(g) pC(g)+qD(g)T1>T2;P1P2m+n=p+q三、某物质的转化率(或百分含量)-时间-温度(或压强)图:?对于反应mA(g)+nB(g) pC(g)+qD(g)P1T2;m+n①判断温度(或压强)的大小
(先拐相平,数值大)
②学会“定一议二”法。四、某物质的转化率(或百分含量)-温度-压强图: (恒压线/恒温线)?对于反应mA(g)+nB(g) pC(g)+qD(g)?正反应放热?正反应吸热m+n>p+qm+n>p+q四、某物质的转化率(或百分含量)-温度-压强图:在以密闭容器中进行的反应mA(g)+nB(g) pC(g)+qD(g)?m+n=p+q正反应吸热?对于2A(g)+B(g) C(g)+3D(g)(正反应吸热)有如下图所示的变化,图中Y轴可能表示:
A、B物质的转化率
B、正反应的速率
C、平衡体系中的A%
D、平衡体系中的C%A、D四、某物质的转化率(或百分含量)-温度-压强图:某物质的转化率(或百分含量)-温度-压强图的关键:
学会“定一议二”法,找出条件改变对平衡的影响。在一固定体积的容器中,在一定条件下发生反应A(s)+2B(g) 2C(?)。且达到化学平衡。当升高温度时,容器内气体的密度随温度的变化如图所示A.若C是气体,正反应是放热反应
B.若C是气体,正反应是吸热反应
C.若C是非气体,正反应是放热反应
D.若C是非气体,正反应是吸热反应√√五、其它:?正反应吸热?正反应吸热?正反应放热?m+n
下列判断一定错误的是
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 A B例1. mA(s)+nB(g) qC(g)正反应为吸热反应)的可逆反应中,在恒温条件下,B的体积分数(B%)与压强(p)的关系如图6所示,有关叙述正确的是( )。 A.n<q B.n>q
C.X点,v正>v逆;Y点,v正<v逆
D.X点比Y点反应速率快
[分析]X、Y点则未达平衡状态,反应要向“趋向于平衡状态方向”进行,以此判断某点v正、v逆的
大小关系。比较X、Y两点的速率快慢则依据压强的高低(或温度的高低)。A、C根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500 ℃,从反应开始到平衡,氢气的平均反应速率v (H2)= 。 减小 mol·(L·min)-1 根据题意完成下列各题:(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快 c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大 bc 根据题意完成下列各题:(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:_______________________________________(用化学方程式表示)。在一定条件下,反应A(气)+B(气) C(气)+Q达到平衡后,根据下列图象判断 (1)升温,达到新的平衡的是( )
(2)降压,达到新的平衡的是( )
(3)减少C的量,移向新平衡的是( )
(4)增加A的量,移向新平衡的是( )
(5)使用催化剂,达到平衡的是( ) A. B. C. D. E.BCEAD练1练2 现有可逆反应A(气)+B(气) 3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则___曲线是表示有催化剂时的情况。
(2)若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是_____热反应。
(3)若丙图中两条曲线分别表示不同压强下的情况,则____曲线是表示压强较大的情况。a吸b练3 密闭容器中mA(g)+nB(g) pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
(1)增大压强,A的转化率____,平衡向____移动,达到平衡后,混合物中C的质量分数________。
(2)上述化学方程式中的系数m、n、p的正确关系是____,向上述平衡体系中加入B,则平衡________。
(3)当降低温度时,C的质量分数增大,则A的转化率____,正反应是____热反应。降低左减少m+n (A)4NH3(气)+5O2(气) 4NO(气)+6H2O(气) △H=- 808.7kJ
(B)N2O3(气) NO2(气)+NO(气) △H=41.8kJ
(C)3NO2(气)+H2O(液) 2HNO3(液)+NO(气) △H=-261.3kJ
(D)CO2(气)+C(固) 2CO(气) △H=+ 171.4kJ A练5对于mA(固)+nB(气) pC(气) △H>0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )
(A)m+n<p (B)n>p
(C)x点的状态是v正>v逆
(D)x点比y点的反应速度慢 CD练6 在密闭容器中进行下列反应:
M(气)+N(气) R(气)+2L
此反应符合下面图像,下列叙述是正确的是( )
(A) 正反应吸热,L是气体
(B) 正反应吸热,L是固体
(C) 正反应放热,L是气体
(D) 正反应放热,L是固体或液体 C练7 可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是( )。
(A)达平衡后,加入催化剂
则C%增大
(B)达平衡后,若升温,平衡左移
(C)化学方程式中n>e+f
(D)达平衡后,增加A的量有利于平衡向右移动 B C练8在可逆反应mA(g)+nB(g) pC(g)+Q中m、n、p为系数,且m+n>p △H<0。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是( ) B练9图中表示外界条件(t、p)的变化对下列反应的影响:L(固)+G(气) 2R(气)△H>0 ,y 轴表示的是( )
(A) 平衡时,混合气中R的百分含量
(B) 平衡时,混合气中G的百分含量
(C) G的转化率
(D) L的转化率 B练10某可逆反应L(s)+G(g) 3R(g) △H>0 ,本图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )
(A)平衡混合气中R的质量分数
(B)达到平衡时G的转化率
(C)平衡混合气中G的质量分数
(D)达到平衡时L的转化率 C练11在一个固定容积的密闭容器中,可发生以下反应:符合下图(a)所示的关系,由此推断关于图(b)的说法正确的是( )A.P3>P4,y轴表示A的转化率
B.P3C.P3>P4,y轴表示混合气体的平均相对分子质量
D.P3>P4,y轴表示混合气体的密度AC练1211.在密闭容器中能入A、B两种气体,在一定条件下反应:2A(g)+B(g) 2C(g) △H<0
达到平衡后,改变一个条件,下列量(Y)的变化一定符合图中曲线的是( )
AC练13某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g) ΔH<0上图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
A.t2时加入了催化剂 B.t3时降低了温度
C.t5时增大了压强 D.t4~t5时间内转化率最低A
速率-时间图
浓度-时间图
转化率(或百分含量)-时间-温度(或压强)图
转化率(或百分含量)-温度-压强图⒈五看图像
⑴面:即明确横纵坐标的意义;
⑵线:了解线的走向和变化趋势;
⑶点:即起点、交点、终点、拐点与极值点等
⑷辅助线:如等温线、等压线、平衡线等;
⑸量的变化:如浓度、温度、压强的变化等。 图像题是化学平衡中的常见题型,这类题目是考查自变量(如时间、温度、压强等)与因变量(如物质的量、浓度、百分含量、转化率)之间的定量或定性关系。⒉分析判断
⑴根据到达平衡的时间长短,结合化学反应速率理论判断温度的高低或压强的大小;
⑵根据图像中量的变化判断平衡移动的方向,结合平衡移动原理,分析可逆反应的特点(是气体分子数增大还是减小的反应;或是吸热还是放热反应);
⑶定一议二:若图像中有三个量,要先固定一个自变量,再讨论另外两个量之间的关系;思维要全面,要注意变换定量与变量,最后下综合结论。 可用于:
1) 表示反应速率的变化和化学平衡的移动。
2) (已知反应)判断引起平衡移动的因素。一、速度-时间图:增大反应物浓度正?引起平衡移动的因素是
,平衡
将向 方向移动。减小生成物浓度正一、速度-时间图:?已知对某一平衡改变温度时有如下图变化,则温度的变化是 (升高或降低),平衡向 反应方向移动,正反应是 热反应。升高正吸一、速度-时间图:?对于mA(g)+nB(g) pC(g)+qD(g),改变压强时有如下图变化,则压强变化是 (增大或减小),平衡向 反应方向移动,m+n
(>、<、=)p+q。增大逆<一、速度-时间图:?对于反应A(g)+3B(g) 2C(g)+D(g)(正反应放热)有如下图所示的变化,请分析引起平衡移动的因素可能是什么?并说明理由。 由于v正、v逆均有不同程
度的增大,引起平衡移动
的因素可能是 a.升高温度
b.增大压强。根据反应方
程式,升高温度平衡向逆反应方向移动,与图示相符;增大压强平衡向正反应方向移动,与图示不相符。故此题中引起平衡移动的因素是升高温度。?对于反应mA(g)+nB(g) pC(g)+qD(g)有如下图所示的变化,请分析t1时的改变因素可能是什么?并说明理由。一、速度-时间图: 由于v正、v逆相同程 度的增大,t1时的改变因素可能是
a.加入(正)催化剂
b.当m+n=p+q时增大压强。
平衡没有移动。速率 - 时间图的关键:
①看出反应速率的变化,是增大还是减小。
②根据正逆反应速率的相对大小,判断化学平衡的移动方向
③结合勒夏特列原理分析判断影响化学平衡移动的因素。二、浓度 - 时间图: 可用于:
1)写出化学反应方程式:
2)求反应物的转化率:A+2B 3CA的转化率=33.3%
B的转化率=66.7%1)写出化学反应方程式:
2)求反应物的转化率:例:练:5A 3B+2CA的转化率=62.5%
0.2
0.10.3浓度 - 时间图的关键:
①写出反应方程式
A、何为反应物、生成物
B、反应物、生成物计量数关系
C、是否为可逆反应
②计算反应物的转化率
③计算某物质的化学反应速率三、某物质的转化率(或百分含量)-时间-温度(或压强)图:?对于反应mA(g)+nB(g) pC(g)+qD(g)T1>T2;P1
(先拐相平,数值大)
②学会“定一议二”法。四、某物质的转化率(或百分含量)-温度-压强图: (恒压线/恒温线)?对于反应mA(g)+nB(g) pC(g)+qD(g)?正反应放热?正反应吸热m+n>p+qm+n>p+q四、某物质的转化率(或百分含量)-温度-压强图:在以密闭容器中进行的反应mA(g)+nB(g) pC(g)+qD(g)?m+n=p+q正反应吸热?对于2A(g)+B(g) C(g)+3D(g)(正反应吸热)有如下图所示的变化,图中Y轴可能表示:
A、B物质的转化率
B、正反应的速率
C、平衡体系中的A%
D、平衡体系中的C%A、D四、某物质的转化率(或百分含量)-温度-压强图:某物质的转化率(或百分含量)-温度-压强图的关键:
学会“定一议二”法,找出条件改变对平衡的影响。在一固定体积的容器中,在一定条件下发生反应A(s)+2B(g) 2C(?)。且达到化学平衡。当升高温度时,容器内气体的密度随温度的变化如图所示A.若C是气体,正反应是放热反应
B.若C是气体,正反应是吸热反应
C.若C是非气体,正反应是放热反应
D.若C是非气体,正反应是吸热反应√√五、其它:?正反应吸热?正反应吸热?正反应放热?m+n
下列判断一定错误的是
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 A B例1. mA(s)+nB(g) qC(g)正反应为吸热反应)的可逆反应中,在恒温条件下,B的体积分数(B%)与压强(p)的关系如图6所示,有关叙述正确的是( )。 A.n<q B.n>q
C.X点,v正>v逆;Y点,v正<v逆
D.X点比Y点反应速率快
[分析]X、Y点则未达平衡状态,反应要向“趋向于平衡状态方向”进行,以此判断某点v正、v逆的
大小关系。比较X、Y两点的速率快慢则依据压强的高低(或温度的高低)。A、C根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500 ℃,从反应开始到平衡,氢气的平均反应速率v (H2)= 。 减小 mol·(L·min)-1 根据题意完成下列各题:(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快 c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大 bc 根据题意完成下列各题:(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:_______________________________________(用化学方程式表示)。在一定条件下,反应A(气)+B(气) C(气)+Q达到平衡后,根据下列图象判断 (1)升温,达到新的平衡的是( )
(2)降压,达到新的平衡的是( )
(3)减少C的量,移向新平衡的是( )
(4)增加A的量,移向新平衡的是( )
(5)使用催化剂,达到平衡的是( ) A. B. C. D. E.BCEAD练1练2 现有可逆反应A(气)+B(气) 3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则___曲线是表示有催化剂时的情况。
(2)若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是_____热反应。
(3)若丙图中两条曲线分别表示不同压强下的情况,则____曲线是表示压强较大的情况。a吸b练3 密闭容器中mA(g)+nB(g) pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
(1)增大压强,A的转化率____,平衡向____移动,达到平衡后,混合物中C的质量分数________。
(2)上述化学方程式中的系数m、n、p的正确关系是____,向上述平衡体系中加入B,则平衡________。
(3)当降低温度时,C的质量分数增大,则A的转化率____,正反应是____热反应。降低左减少m+n
(B)N2O3(气) NO2(气)+NO(气) △H=41.8kJ
(C)3NO2(气)+H2O(液) 2HNO3(液)+NO(气) △H=-261.3kJ
(D)CO2(气)+C(固) 2CO(气) △H=+ 171.4kJ A练5对于mA(固)+nB(气) pC(气) △H>0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )
(A)m+n<p (B)n>p
(C)x点的状态是v正>v逆
(D)x点比y点的反应速度慢 CD练6 在密闭容器中进行下列反应:
M(气)+N(气) R(气)+2L
此反应符合下面图像,下列叙述是正确的是( )
(A) 正反应吸热,L是气体
(B) 正反应吸热,L是固体
(C) 正反应放热,L是气体
(D) 正反应放热,L是固体或液体 C练7 可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是( )。
(A)达平衡后,加入催化剂
则C%增大
(B)达平衡后,若升温,平衡左移
(C)化学方程式中n>e+f
(D)达平衡后,增加A的量有利于平衡向右移动 B C练8在可逆反应mA(g)+nB(g) pC(g)+Q中m、n、p为系数,且m+n>p △H<0。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是( ) B练9图中表示外界条件(t、p)的变化对下列反应的影响:L(固)+G(气) 2R(气)△H>0 ,y 轴表示的是( )
(A) 平衡时,混合气中R的百分含量
(B) 平衡时,混合气中G的百分含量
(C) G的转化率
(D) L的转化率 B练10某可逆反应L(s)+G(g) 3R(g) △H>0 ,本图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )
(A)平衡混合气中R的质量分数
(B)达到平衡时G的转化率
(C)平衡混合气中G的质量分数
(D)达到平衡时L的转化率 C练11在一个固定容积的密闭容器中,可发生以下反应:符合下图(a)所示的关系,由此推断关于图(b)的说法正确的是( )A.P3>P4,y轴表示A的转化率
B.P3
D.P3>P4,y轴表示混合气体的密度AC练1211.在密闭容器中能入A、B两种气体,在一定条件下反应:2A(g)+B(g) 2C(g) △H<0
达到平衡后,改变一个条件,下列量(Y)的变化一定符合图中曲线的是( )
AC练13某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g) ΔH<0上图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
A.t2时加入了催化剂 B.t3时降低了温度
C.t5时增大了压强 D.t4~t5时间内转化率最低A
