6.1金刚石、石墨和c60同步分层作业(培优篇)—2021-2022学年九年级化学人教版上册(word版 含解析)
文档属性
| 名称 | 6.1金刚石、石墨和c60同步分层作业(培优篇)—2021-2022学年九年级化学人教版上册(word版 含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 272.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-25 00:00:00 | ||
图片预览



文档简介
(培优篇)2021-2022学年上学期初中化学人教新版九年级同步分层作业6.1金刚石、石墨和C60
一.选择题(共5小题)
1.某同学用如图所示的装置进行碳还原氧化铜的实验。实验前他先向试管内通入一段时间的氮气,实验过程中他观察到澄清石灰水变浑浊,但却没有看到有红色物质出现。下列原因分析合理的是( )
A.反应没有发生 B.反应前没有预热
C.氧化铜的量过少 D.酒精灯火焰的温度不足
2.下列说法不正确的是( )
A.石墨具有优良的导电性能
B.C60是由碳原子直接构成的
C.金刚石是天然存在最坚硬的物质
D.C60可能广泛应用于超导、催化、材料、医学及生物等领域
3.2019年10月,清华大学科研团队实现一步法制备99.9999%半导体碳纳米管阵列。下列说法正确的是( )
A.阵列中的碳原子在不断运动
B.碳元素只能组成一种物质
C.阵列中的碳原子间没有间隔
D.该物质与金刚石的化学性质不同
4.芯片是电脑、“智能”家电的核心部件,它是用高纯度硅制成的,目前广泛用石英砂(主要成分是SiO2)为原料制取,其中有一步反应为:SiO2+2CSi+2CO↑,下列关于该反应说法正确的是( )
A.碳发生了还原反应
B.碳的失电子能力比硅强
C.硅元素的化合价由+4价变为+2价
D.12g碳与足量二氧化硅充分反应生成56g一氧化碳
5.物质的性质在很大程度上决定了物质的用途。下列关于碳单质的描述中正确的是( )
选项 性质 用途
A 石墨能导电 石墨可用作电极
B 金刚石密度大 金刚石可用来切割玻璃
C 活性炭具有很强的吸附性 活性炭可用作净化硬水
D 碳具有氧化性 焦炭可用于冶金工业
A.A B.B C.C D.D
二.填空题(共3小题)
6.对比、分析、归纳是学习化学的重要方法。
(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuOCu+H2O
3CO+Fe2O32Fe+3CO2
C+O2CO2
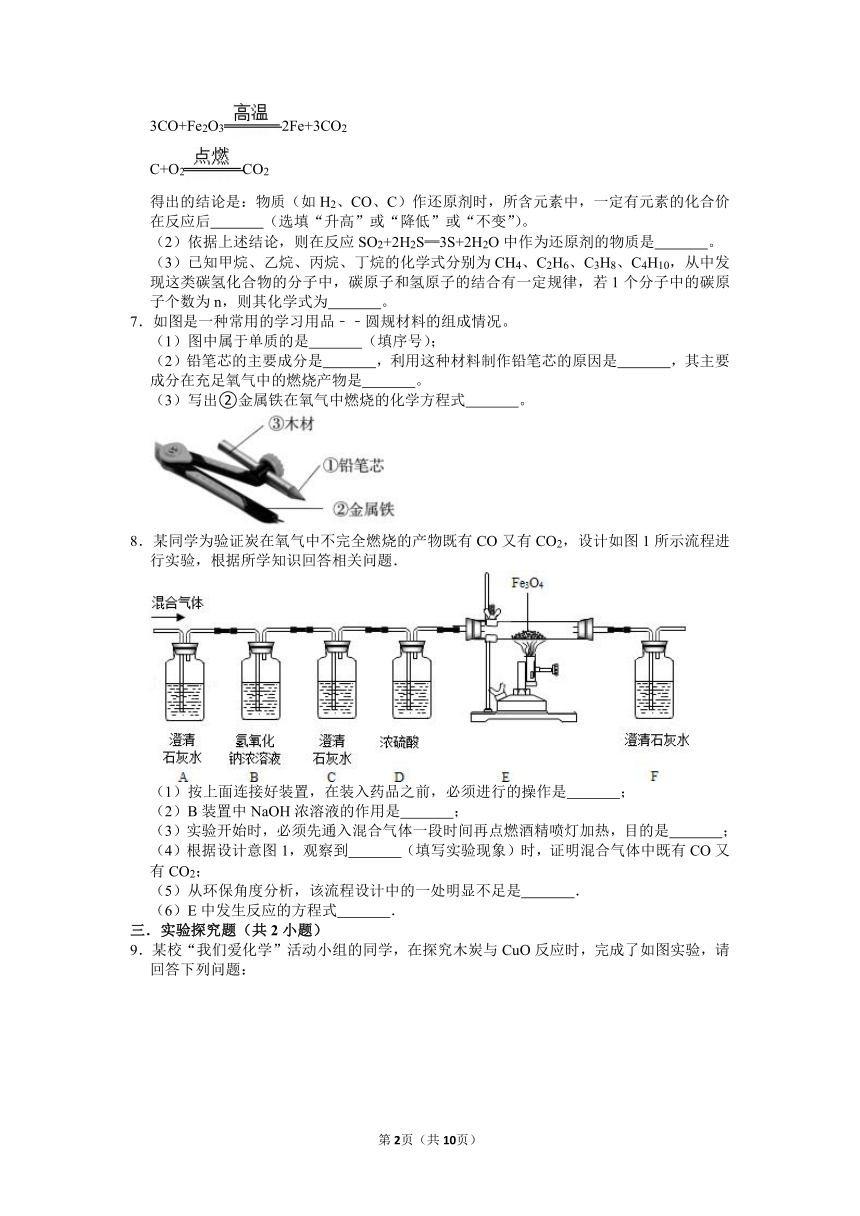
得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后 (选填“升高”或“降低”或“不变”)。
(2)依据上述结论,则在反应SO2+2H2S═3S+2H2O中作为还原剂的物质是 。
(3)已知甲烷、乙烷、丙烷、丁烷的化学式分别为CH4、C2H6、C3H8、C4H10,从中发现这类碳氢化合物的分子中,碳原子和氢原子的结合有一定规律,若1个分子中的碳原子个数为n,则其化学式为 。
7.如图是一种常用的学习用品﹣﹣圆规材料的组成情况。
(1)图中属于单质的是 (填序号);
(2)铅笔芯的主要成分是 ,利用这种材料制作铅笔芯的原因是 ,其主要成分在充足氧气中的燃烧产物是 。
(3)写出②金属铁在氧气中燃烧的化学方程式 。
8.某同学为验证炭在氧气中不完全燃烧的产物既有CO又有CO2,设计如图1所示流程进行实验,根据所学知识回答相关问题.
(1)按上面连接好装置,在装入药品之前,必须进行的操作是 ;
(2)B装置中NaOH浓溶液的作用是 ;
(3)实验开始时,必须先通入混合气体一段时间再点燃酒精喷灯加热,目的是 ;
(4)根据设计意图1,观察到 (填写实验现象)时,证明混合气体中既有CO又有CO2;
(5)从环保角度分析,该流程设计中的一处明显不足是 .
(6)E中发生反应的方程式 .
三.实验探究题(共2小题)
9.某校“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如图实验,请回答下列问题:
Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
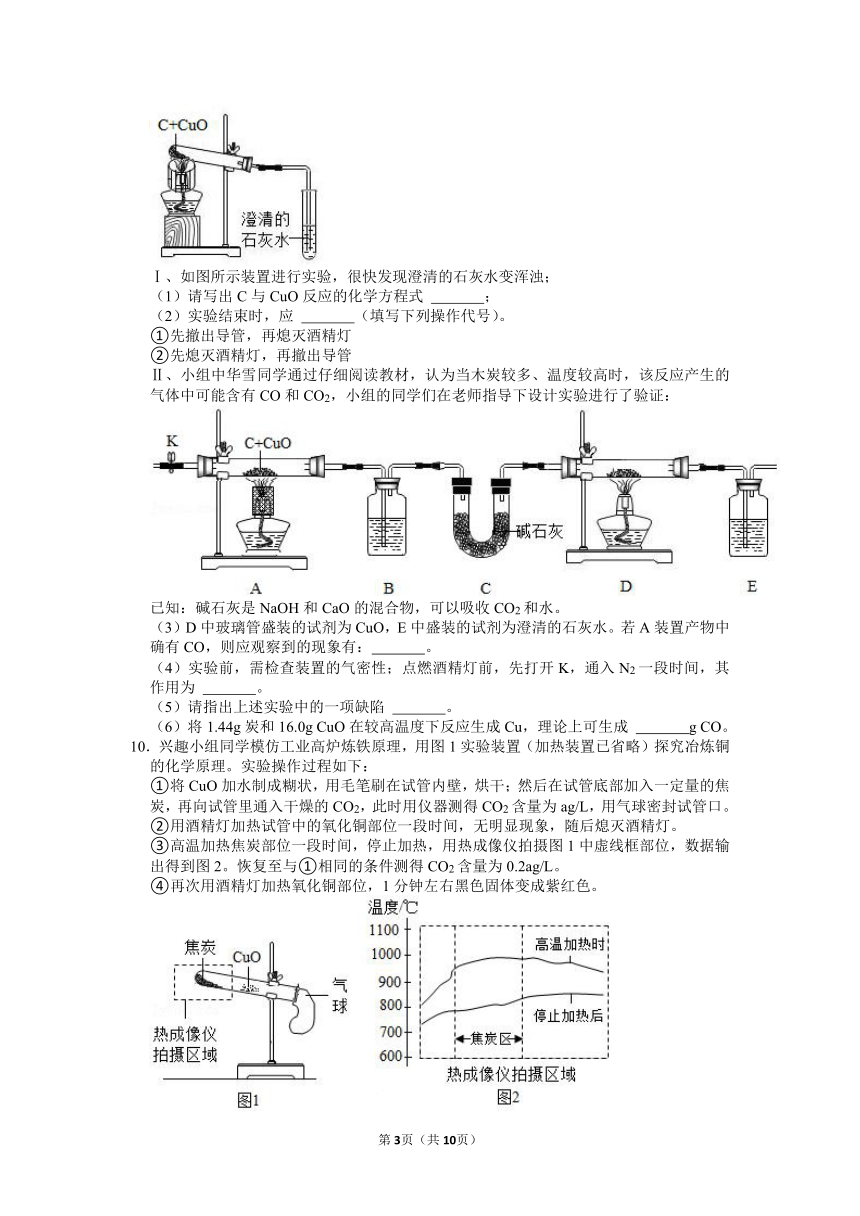
(1)请写出C与CuO反应的化学方程式 ;
(2)实验结束时,应 (填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:
已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
(3)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有: 。
(4)实验前,需检查装置的气密性;点燃酒精灯前,先打开K,通入N2一段时间,其作用为 。
(5)请指出上述实验中的一项缺陷 。
(6)将1.44g炭和16.0g CuO在较高温度下反应生成Cu,理论上可生成 g CO。
10.兴趣小组同学模仿工业高炉炼铁原理,用图1实验装置(加热装置已省略)探究冶炼铜的化学原理。实验操作过程如下:
①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2,此时用仪器测得CO2含量为ag/L,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图2。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右黑色固体变成紫红色。
(1)操作②中实验现象说明CO2 (选填“能”或“不能”)与CuO反应。
(2)操作③中CO2含量减小的原因是 。
(3)操作④中的化学反应方程式为 。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是 。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是 。
(培优篇)2021-2022学年上学期初中化学人教新版九年级同步分层作业6.1金刚石、石墨和C60
参考答案与试题解析
一.选择题(共5小题)
1.某同学用如图所示的装置进行碳还原氧化铜的实验。实验前他先向试管内通入一段时间的氮气,实验过程中他观察到澄清石灰水变浑浊,但却没有看到有红色物质出现。下列原因分析合理的是( )
A.反应没有发生 B.反应前没有预热
C.氧化铜的量过少 D.酒精灯火焰的温度不足
【解答】解:A、实验过程中他观察到澄清石灰水变浑浊,说明生成了二氧化碳,说明发生了反应,故选项错误。
B、反应前没有预热,不会造成没有看到有红色物质出现,故选项错误。
C、碳是黑色的,氧化铜的量过少,可能会造成没有看到有红色物质出现,故选项正确。
D、由于实验前他先向试管内通入一段时间的氮气,排尽了装置中的空气,酒精灯火焰的温度不足,会导致反应不能发生,不会造成没有看到有红色物质出现,故选项错误。
故选:C。
2.下列说法不正确的是( )
A.石墨具有优良的导电性能
B.C60是由碳原子直接构成的
C.金刚石是天然存在最坚硬的物质
D.C60可能广泛应用于超导、催化、材料、医学及生物等领域
【解答】解:A、石墨具有优良的导电性能,可作电极,说法正确;
B、C60是由C60分子构成的,说法错误;
C、金刚石是天然存在的最硬的物质,说法正确;
D、C60可能广泛应用于超导、催化、材料、医学及生物等领域,说法正确;
故选:B。
3.2019年10月,清华大学科研团队实现一步法制备99.9999%半导体碳纳米管阵列。下列说法正确的是( )
A.阵列中的碳原子在不断运动
B.碳元素只能组成一种物质
C.阵列中的碳原子间没有间隔
D.该物质与金刚石的化学性质不同
【解答】解:A、原子在不断运动的,所以阵列中的碳原子也在不断运动,故A正确;
B、碳元素可以组成金刚石、石墨等物质,故B错误;
C、半导体碳纳米管阵列中的原子间有间隔,故C错误;
D、半导体碳纳米管阵列与金刚石都是由碳元素组成的不同物质,化学性质相同,故D错误。
故选:A。
4.芯片是电脑、“智能”家电的核心部件,它是用高纯度硅制成的,目前广泛用石英砂(主要成分是SiO2)为原料制取,其中有一步反应为:SiO2+2CSi+2CO↑,下列关于该反应说法正确的是( )
A.碳发生了还原反应
B.碳的失电子能力比硅强
C.硅元素的化合价由+4价变为+2价
D.12g碳与足量二氧化硅充分反应生成56g一氧化碳
【解答】解:A、碳夺取了二氧化硅中的氧,具有还原性,发生了氧化反应,故选项说法错误。
B、该反应中,碳元素的化合价升高,硅元素的化合价降低,则碳的失电子能力比硅强,故选项说法正确。
C、硅元素的化合价由+4价转化为0价,故选项说法错误。
D、由反应的化学方程式SiO2+2CSi+2CO↑,碳与一氧化碳的质量为12:28,则12g碳与足量二氧化硅充分反应生成28g一氧化碳,故选项说法错误。
故选:B。
5.物质的性质在很大程度上决定了物质的用途。下列关于碳单质的描述中正确的是( )
选项 性质 用途
A 石墨能导电 石墨可用作电极
B 金刚石密度大 金刚石可用来切割玻璃
C 活性炭具有很强的吸附性 活性炭可用作净化硬水
D 碳具有氧化性 焦炭可用于冶金工业
A.A B.B C.C D.D
【解答】解:A、石墨具有导电性,可以用石墨来制电极,故正确;
B、金刚石是自然界中硬度最大的矿物,所以可用金刚石来刻画玻璃,故错误;
C、活性炭具有很强的吸附性,可用来吸附水中的色素、异味的物质,但是不能使硬水软化,故错误;
D、碳具有还原性,可用焦炭来冶炼金属,故错误。
故选:A。
二.填空题(共3小题)
6.对比、分析、归纳是学习化学的重要方法。
(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuOCu+H2O
3CO+Fe2O32Fe+3CO2
C+O2CO2
得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后 升高 (选填“升高”或“降低”或“不变”)。
(2)依据上述结论,则在反应SO2+2H2S═3S+2H2O中作为还原剂的物质是 H2S 。
(3)已知甲烷、乙烷、丙烷、丁烷的化学式分别为CH4、C2H6、C3H8、C4H10,从中发现这类碳氢化合物的分子中,碳原子和氢原子的结合有一定规律,若1个分子中的碳原子个数为n,则其化学式为 CnH(2n+2) 。
【解答】解:(1)在H2+CuOCu+H2O; Fe2O3+3CO2Fe+3CO2; C+O2CO2中,H2、C属于单质,其中氢元素和碳元素的化合价为0;CO中氧元素显﹣2价,碳元素显+2价;生成物水、二氧化碳中,水中氢元素显+1价,二氧化碳中碳元素显+4价,则物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后升高.故填:升高;
(2)根据反应可以看出,二氧化硫中硫元素的化合价反应后降低,氧元素的化合价不变,故不是还原剂;硫化氢中氢元素的化合计反应前后不变,硫元素的化合价由反应前的﹣2价变为0价,故化合价升高,作的是还原剂;H2S;故填:H2S;
(3)甲烷(CH4)、丙烷(C3H8)、丁烷(C4H10),碳原子的个数分别是1、3、4时,氢原子个数是4、8、10,所以分子中的碳原子数为n,则其化学式为CnH(2n+2);故填:CnH(2n+2)。
7.如图是一种常用的学习用品﹣﹣圆规材料的组成情况。
(1)图中属于单质的是 ② (填序号);
(2)铅笔芯的主要成分是 石墨 ,利用这种材料制作铅笔芯的原因是 石墨的硬度小 ,其主要成分在充足氧气中的燃烧产物是 CO2 。
(3)写出②金属铁在氧气中燃烧的化学方程式 3Fe+2O2 Fe3O4 。
【解答】解:(1)铁是由一种元素组成的纯净物,是单质,故填 ②;
(2)铅笔芯的主要成分是石墨,石墨的硬度小,在纸上划能留下痕迹,利用石墨可制作铅笔芯,石墨在充足氧气中的燃烧生成CO2。
(3)铁在氧气中燃烧生成四氧化三铁,化学方程式 3Fe+2O2 Fe3O4;
故答案为:(1)②;
(2)石墨; 石墨的硬度小; CO2。
(3)3Fe+2O2 Fe3O4;
8.某同学为验证炭在氧气中不完全燃烧的产物既有CO又有CO2,设计如图1所示流程进行实验,根据所学知识回答相关问题.
(1)按上面连接好装置,在装入药品之前,必须进行的操作是 检查装置的气密性 ;
(2)B装置中NaOH浓溶液的作用是 除去混合气体中的二氧化碳 ;
(3)实验开始时,必须先通入混合气体一段时间再点燃酒精喷灯加热,目的是 排净试管中的空气以防止爆炸事故 ;
(4)根据设计意图1,观察到 A、F中的石灰水变浑浊,C中的石灰水无明显现象 (填写实验现象)时,证明混合气体中既有CO又有CO2;
(5)从环保角度分析,该流程设计中的一处明显不足是 没有尾气处理(吸收)装置 .
(6)E中发生反应的方程式 Fe3O4+4CO3Fe+4CO2 .
【解答】解:(1)装置连接好之后,装药品之前必须检查装置的气密性;故填:检查装置的气密性;
(2)氢氧化钠能吸收空气中的二氧化碳气体.故作用是:除去空气中的二氧化碳;故填:除去混合气体中的二氧化碳;
(3)一氧化碳具有可燃性,所以加热四氧化三铁之前需先通一氧化碳,目的是排净试管中的空气以防止爆炸事故.故填:排净试管中的空气以防止爆炸事故;
(4)因二氧化碳遇澄清石灰水变浑浊,一氧化碳可以还原四氧化三铁,所以确认混合气体中存在CO、CO2实验结论的实验现象是A、F中的石灰水变浑浊,C中的石灰水无明显现象.故填:A、F中的石灰水变浑浊,C中的石灰水无明显现象.
(5)因为一氧化碳有毒,不能直接排放到空气中,要对尾气进行点燃处理.故填:没有尾气处理(吸收)装置.
(5)E中一氧化碳能与四氧化三铁高温反应生成铁和二氧化碳,故其化学方程式为Fe3O4+4CO3Fe+4CO2;
故答案为:
(1)检查装置的气密性;
(2)除去混合气体中的二氧化碳;
(3)排净试管中的空气以防止爆炸事故;
(4)A、F中的石灰水变浑浊,C中的石灰水无明显现象.
(5)没有尾气处理(吸收)装置.
(5)Fe3O4+4CO3Fe+4CO2;
三.实验探究题(共2小题)
9.某校“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如图实验,请回答下列问题:
Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)请写出C与CuO反应的化学方程式 C+2CuO2Cu+CO2↑ ;
(2)实验结束时,应 ① (填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:
已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
(3)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有: D 中黑色固体变红色,E中澄清石灰水变浑浊 。
(4)实验前,需检查装置的气密性;点燃酒精灯前,先打开K,通入N2一段时间,其作用为 排出装置中的空气,防止空气中氧气和木炭发生反应 。
(5)请指出上述实验中的一项缺陷 没有处理尾气 。
(6)将1.44g炭和16.0g CuO在较高温度下反应生成Cu,理论上可生成 1.12 g CO。
【解答】解:Ⅰ:(1)高温条件下,C与CuO反应生成铜和二氧化碳,反应的化学方程式:C+2CuO2Cu+CO2↑;故答案为:C+2CuO2Cu+CO2↑;
(2)实验结束时,应先撤出导管,再熄灭酒精灯,以防止液体倒流炸裂试管;故答案为:①;
Ⅱ:(3)若A装置产物中确有CO,则应观察到的现象有:D 中黑色固体变红色,E中澄清石灰水变浑浊;故答案为:D中黑色固体变红色,E中澄清石灰水变浑浊;
(4)实验前,需检查装置气密性;点燃酒精灯前,先打开K,通入N2段时间,其作用为排出装置中的空气,防止空气中的二氧化碳影响实验结果;故答案为:排出装置中的空气,防止空气中的二氧化碳影响实验结果;
(5)一氧化碳有毒,扩散到空气中污染环所以要对尾气进行处理;故答案为:没有处理尾气;
(6)反应的化学方程式及其质量关系:C+2CuO2Cu+CO2↑
12 160 44
1.2g 16.0g 4.4g
CO2+C2CO
12 56
1.44g﹣1.2g 1.12g
由以上质量关系可知,将1.44g炭和16.0g CuO在较高温度下反应生成C,理论上可生成1.12gCO;故答案为:1.12。
10.兴趣小组同学模仿工业高炉炼铁原理,用图1实验装置(加热装置已省略)探究冶炼铜的化学原理。实验操作过程如下:
①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2,此时用仪器测得CO2含量为ag/L,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图2。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右黑色固体变成紫红色。
(1)操作②中实验现象说明CO2 不能 (选填“能”或“不能”)与CuO反应。
(2)操作③中CO2含量减小的原因是 高温条件下二氧化碳和碳发生反应 。
(3)操作④中的化学反应方程式为 CO+CuOCu+CO2 。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是 防止一氧化碳污染环境 。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是 焦炭和二氧化碳的反应为吸热反应 。
【解答】解:(1)操作②中实验现象说明CO2不能与CuO反应。
故填:不能。
(2)操作③中CO2含量减小的原因是高温条件下二氧化碳和碳发生反应。
故填:高温条件下二氧化碳和碳发生反应。
(3)操作④中加热时氧化铜和一氧化碳反应生成铜和二氧化碳,化学反应方程式为:CO+CuOCu+CO2。
故填:CO+CuOCu+CO2。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是防止一氧化碳污染环境。
故填:防止一氧化碳污染环境。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是焦炭和二氧化碳的反应为吸热反应。
故填:焦炭和二氧化碳的反应为吸热反应。
第1页(共1页)
一.选择题(共5小题)
1.某同学用如图所示的装置进行碳还原氧化铜的实验。实验前他先向试管内通入一段时间的氮气,实验过程中他观察到澄清石灰水变浑浊,但却没有看到有红色物质出现。下列原因分析合理的是( )
A.反应没有发生 B.反应前没有预热
C.氧化铜的量过少 D.酒精灯火焰的温度不足
2.下列说法不正确的是( )
A.石墨具有优良的导电性能
B.C60是由碳原子直接构成的
C.金刚石是天然存在最坚硬的物质
D.C60可能广泛应用于超导、催化、材料、医学及生物等领域
3.2019年10月,清华大学科研团队实现一步法制备99.9999%半导体碳纳米管阵列。下列说法正确的是( )
A.阵列中的碳原子在不断运动
B.碳元素只能组成一种物质
C.阵列中的碳原子间没有间隔
D.该物质与金刚石的化学性质不同
4.芯片是电脑、“智能”家电的核心部件,它是用高纯度硅制成的,目前广泛用石英砂(主要成分是SiO2)为原料制取,其中有一步反应为:SiO2+2CSi+2CO↑,下列关于该反应说法正确的是( )
A.碳发生了还原反应
B.碳的失电子能力比硅强
C.硅元素的化合价由+4价变为+2价
D.12g碳与足量二氧化硅充分反应生成56g一氧化碳
5.物质的性质在很大程度上决定了物质的用途。下列关于碳单质的描述中正确的是( )
选项 性质 用途
A 石墨能导电 石墨可用作电极
B 金刚石密度大 金刚石可用来切割玻璃
C 活性炭具有很强的吸附性 活性炭可用作净化硬水
D 碳具有氧化性 焦炭可用于冶金工业
A.A B.B C.C D.D
二.填空题(共3小题)
6.对比、分析、归纳是学习化学的重要方法。
(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuOCu+H2O
3CO+Fe2O32Fe+3CO2
C+O2CO2
得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后 (选填“升高”或“降低”或“不变”)。
(2)依据上述结论,则在反应SO2+2H2S═3S+2H2O中作为还原剂的物质是 。
(3)已知甲烷、乙烷、丙烷、丁烷的化学式分别为CH4、C2H6、C3H8、C4H10,从中发现这类碳氢化合物的分子中,碳原子和氢原子的结合有一定规律,若1个分子中的碳原子个数为n,则其化学式为 。
7.如图是一种常用的学习用品﹣﹣圆规材料的组成情况。
(1)图中属于单质的是 (填序号);
(2)铅笔芯的主要成分是 ,利用这种材料制作铅笔芯的原因是 ,其主要成分在充足氧气中的燃烧产物是 。
(3)写出②金属铁在氧气中燃烧的化学方程式 。
8.某同学为验证炭在氧气中不完全燃烧的产物既有CO又有CO2,设计如图1所示流程进行实验,根据所学知识回答相关问题.
(1)按上面连接好装置,在装入药品之前,必须进行的操作是 ;
(2)B装置中NaOH浓溶液的作用是 ;
(3)实验开始时,必须先通入混合气体一段时间再点燃酒精喷灯加热,目的是 ;
(4)根据设计意图1,观察到 (填写实验现象)时,证明混合气体中既有CO又有CO2;
(5)从环保角度分析,该流程设计中的一处明显不足是 .
(6)E中发生反应的方程式 .
三.实验探究题(共2小题)
9.某校“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如图实验,请回答下列问题:
Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)请写出C与CuO反应的化学方程式 ;
(2)实验结束时,应 (填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:
已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
(3)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有: 。
(4)实验前,需检查装置的气密性;点燃酒精灯前,先打开K,通入N2一段时间,其作用为 。
(5)请指出上述实验中的一项缺陷 。
(6)将1.44g炭和16.0g CuO在较高温度下反应生成Cu,理论上可生成 g CO。
10.兴趣小组同学模仿工业高炉炼铁原理,用图1实验装置(加热装置已省略)探究冶炼铜的化学原理。实验操作过程如下:
①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2,此时用仪器测得CO2含量为ag/L,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图2。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右黑色固体变成紫红色。
(1)操作②中实验现象说明CO2 (选填“能”或“不能”)与CuO反应。
(2)操作③中CO2含量减小的原因是 。
(3)操作④中的化学反应方程式为 。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是 。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是 。
(培优篇)2021-2022学年上学期初中化学人教新版九年级同步分层作业6.1金刚石、石墨和C60
参考答案与试题解析
一.选择题(共5小题)
1.某同学用如图所示的装置进行碳还原氧化铜的实验。实验前他先向试管内通入一段时间的氮气,实验过程中他观察到澄清石灰水变浑浊,但却没有看到有红色物质出现。下列原因分析合理的是( )
A.反应没有发生 B.反应前没有预热
C.氧化铜的量过少 D.酒精灯火焰的温度不足
【解答】解:A、实验过程中他观察到澄清石灰水变浑浊,说明生成了二氧化碳,说明发生了反应,故选项错误。
B、反应前没有预热,不会造成没有看到有红色物质出现,故选项错误。
C、碳是黑色的,氧化铜的量过少,可能会造成没有看到有红色物质出现,故选项正确。
D、由于实验前他先向试管内通入一段时间的氮气,排尽了装置中的空气,酒精灯火焰的温度不足,会导致反应不能发生,不会造成没有看到有红色物质出现,故选项错误。
故选:C。
2.下列说法不正确的是( )
A.石墨具有优良的导电性能
B.C60是由碳原子直接构成的
C.金刚石是天然存在最坚硬的物质
D.C60可能广泛应用于超导、催化、材料、医学及生物等领域
【解答】解:A、石墨具有优良的导电性能,可作电极,说法正确;
B、C60是由C60分子构成的,说法错误;
C、金刚石是天然存在的最硬的物质,说法正确;
D、C60可能广泛应用于超导、催化、材料、医学及生物等领域,说法正确;
故选:B。
3.2019年10月,清华大学科研团队实现一步法制备99.9999%半导体碳纳米管阵列。下列说法正确的是( )
A.阵列中的碳原子在不断运动
B.碳元素只能组成一种物质
C.阵列中的碳原子间没有间隔
D.该物质与金刚石的化学性质不同
【解答】解:A、原子在不断运动的,所以阵列中的碳原子也在不断运动,故A正确;
B、碳元素可以组成金刚石、石墨等物质,故B错误;
C、半导体碳纳米管阵列中的原子间有间隔,故C错误;
D、半导体碳纳米管阵列与金刚石都是由碳元素组成的不同物质,化学性质相同,故D错误。
故选:A。
4.芯片是电脑、“智能”家电的核心部件,它是用高纯度硅制成的,目前广泛用石英砂(主要成分是SiO2)为原料制取,其中有一步反应为:SiO2+2CSi+2CO↑,下列关于该反应说法正确的是( )
A.碳发生了还原反应
B.碳的失电子能力比硅强
C.硅元素的化合价由+4价变为+2价
D.12g碳与足量二氧化硅充分反应生成56g一氧化碳
【解答】解:A、碳夺取了二氧化硅中的氧,具有还原性,发生了氧化反应,故选项说法错误。
B、该反应中,碳元素的化合价升高,硅元素的化合价降低,则碳的失电子能力比硅强,故选项说法正确。
C、硅元素的化合价由+4价转化为0价,故选项说法错误。
D、由反应的化学方程式SiO2+2CSi+2CO↑,碳与一氧化碳的质量为12:28,则12g碳与足量二氧化硅充分反应生成28g一氧化碳,故选项说法错误。
故选:B。
5.物质的性质在很大程度上决定了物质的用途。下列关于碳单质的描述中正确的是( )
选项 性质 用途
A 石墨能导电 石墨可用作电极
B 金刚石密度大 金刚石可用来切割玻璃
C 活性炭具有很强的吸附性 活性炭可用作净化硬水
D 碳具有氧化性 焦炭可用于冶金工业
A.A B.B C.C D.D
【解答】解:A、石墨具有导电性,可以用石墨来制电极,故正确;
B、金刚石是自然界中硬度最大的矿物,所以可用金刚石来刻画玻璃,故错误;
C、活性炭具有很强的吸附性,可用来吸附水中的色素、异味的物质,但是不能使硬水软化,故错误;
D、碳具有还原性,可用焦炭来冶炼金属,故错误。
故选:A。
二.填空题(共3小题)
6.对比、分析、归纳是学习化学的重要方法。
(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuOCu+H2O
3CO+Fe2O32Fe+3CO2
C+O2CO2
得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后 升高 (选填“升高”或“降低”或“不变”)。
(2)依据上述结论,则在反应SO2+2H2S═3S+2H2O中作为还原剂的物质是 H2S 。
(3)已知甲烷、乙烷、丙烷、丁烷的化学式分别为CH4、C2H6、C3H8、C4H10,从中发现这类碳氢化合物的分子中,碳原子和氢原子的结合有一定规律,若1个分子中的碳原子个数为n,则其化学式为 CnH(2n+2) 。
【解答】解:(1)在H2+CuOCu+H2O; Fe2O3+3CO2Fe+3CO2; C+O2CO2中,H2、C属于单质,其中氢元素和碳元素的化合价为0;CO中氧元素显﹣2价,碳元素显+2价;生成物水、二氧化碳中,水中氢元素显+1价,二氧化碳中碳元素显+4价,则物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后升高.故填:升高;
(2)根据反应可以看出,二氧化硫中硫元素的化合价反应后降低,氧元素的化合价不变,故不是还原剂;硫化氢中氢元素的化合计反应前后不变,硫元素的化合价由反应前的﹣2价变为0价,故化合价升高,作的是还原剂;H2S;故填:H2S;
(3)甲烷(CH4)、丙烷(C3H8)、丁烷(C4H10),碳原子的个数分别是1、3、4时,氢原子个数是4、8、10,所以分子中的碳原子数为n,则其化学式为CnH(2n+2);故填:CnH(2n+2)。
7.如图是一种常用的学习用品﹣﹣圆规材料的组成情况。
(1)图中属于单质的是 ② (填序号);
(2)铅笔芯的主要成分是 石墨 ,利用这种材料制作铅笔芯的原因是 石墨的硬度小 ,其主要成分在充足氧气中的燃烧产物是 CO2 。
(3)写出②金属铁在氧气中燃烧的化学方程式 3Fe+2O2 Fe3O4 。
【解答】解:(1)铁是由一种元素组成的纯净物,是单质,故填 ②;
(2)铅笔芯的主要成分是石墨,石墨的硬度小,在纸上划能留下痕迹,利用石墨可制作铅笔芯,石墨在充足氧气中的燃烧生成CO2。
(3)铁在氧气中燃烧生成四氧化三铁,化学方程式 3Fe+2O2 Fe3O4;
故答案为:(1)②;
(2)石墨; 石墨的硬度小; CO2。
(3)3Fe+2O2 Fe3O4;
8.某同学为验证炭在氧气中不完全燃烧的产物既有CO又有CO2,设计如图1所示流程进行实验,根据所学知识回答相关问题.
(1)按上面连接好装置,在装入药品之前,必须进行的操作是 检查装置的气密性 ;
(2)B装置中NaOH浓溶液的作用是 除去混合气体中的二氧化碳 ;
(3)实验开始时,必须先通入混合气体一段时间再点燃酒精喷灯加热,目的是 排净试管中的空气以防止爆炸事故 ;
(4)根据设计意图1,观察到 A、F中的石灰水变浑浊,C中的石灰水无明显现象 (填写实验现象)时,证明混合气体中既有CO又有CO2;
(5)从环保角度分析,该流程设计中的一处明显不足是 没有尾气处理(吸收)装置 .
(6)E中发生反应的方程式 Fe3O4+4CO3Fe+4CO2 .
【解答】解:(1)装置连接好之后,装药品之前必须检查装置的气密性;故填:检查装置的气密性;
(2)氢氧化钠能吸收空气中的二氧化碳气体.故作用是:除去空气中的二氧化碳;故填:除去混合气体中的二氧化碳;
(3)一氧化碳具有可燃性,所以加热四氧化三铁之前需先通一氧化碳,目的是排净试管中的空气以防止爆炸事故.故填:排净试管中的空气以防止爆炸事故;
(4)因二氧化碳遇澄清石灰水变浑浊,一氧化碳可以还原四氧化三铁,所以确认混合气体中存在CO、CO2实验结论的实验现象是A、F中的石灰水变浑浊,C中的石灰水无明显现象.故填:A、F中的石灰水变浑浊,C中的石灰水无明显现象.
(5)因为一氧化碳有毒,不能直接排放到空气中,要对尾气进行点燃处理.故填:没有尾气处理(吸收)装置.
(5)E中一氧化碳能与四氧化三铁高温反应生成铁和二氧化碳,故其化学方程式为Fe3O4+4CO3Fe+4CO2;
故答案为:
(1)检查装置的气密性;
(2)除去混合气体中的二氧化碳;
(3)排净试管中的空气以防止爆炸事故;
(4)A、F中的石灰水变浑浊,C中的石灰水无明显现象.
(5)没有尾气处理(吸收)装置.
(5)Fe3O4+4CO3Fe+4CO2;
三.实验探究题(共2小题)
9.某校“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如图实验,请回答下列问题:
Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)请写出C与CuO反应的化学方程式 C+2CuO2Cu+CO2↑ ;
(2)实验结束时,应 ① (填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:
已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
(3)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有: D 中黑色固体变红色,E中澄清石灰水变浑浊 。
(4)实验前,需检查装置的气密性;点燃酒精灯前,先打开K,通入N2一段时间,其作用为 排出装置中的空气,防止空气中氧气和木炭发生反应 。
(5)请指出上述实验中的一项缺陷 没有处理尾气 。
(6)将1.44g炭和16.0g CuO在较高温度下反应生成Cu,理论上可生成 1.12 g CO。
【解答】解:Ⅰ:(1)高温条件下,C与CuO反应生成铜和二氧化碳,反应的化学方程式:C+2CuO2Cu+CO2↑;故答案为:C+2CuO2Cu+CO2↑;
(2)实验结束时,应先撤出导管,再熄灭酒精灯,以防止液体倒流炸裂试管;故答案为:①;
Ⅱ:(3)若A装置产物中确有CO,则应观察到的现象有:D 中黑色固体变红色,E中澄清石灰水变浑浊;故答案为:D中黑色固体变红色,E中澄清石灰水变浑浊;
(4)实验前,需检查装置气密性;点燃酒精灯前,先打开K,通入N2段时间,其作用为排出装置中的空气,防止空气中的二氧化碳影响实验结果;故答案为:排出装置中的空气,防止空气中的二氧化碳影响实验结果;
(5)一氧化碳有毒,扩散到空气中污染环所以要对尾气进行处理;故答案为:没有处理尾气;
(6)反应的化学方程式及其质量关系:C+2CuO2Cu+CO2↑
12 160 44
1.2g 16.0g 4.4g
CO2+C2CO
12 56
1.44g﹣1.2g 1.12g
由以上质量关系可知,将1.44g炭和16.0g CuO在较高温度下反应生成C,理论上可生成1.12gCO;故答案为:1.12。
10.兴趣小组同学模仿工业高炉炼铁原理,用图1实验装置(加热装置已省略)探究冶炼铜的化学原理。实验操作过程如下:
①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2,此时用仪器测得CO2含量为ag/L,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图2。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右黑色固体变成紫红色。
(1)操作②中实验现象说明CO2 不能 (选填“能”或“不能”)与CuO反应。
(2)操作③中CO2含量减小的原因是 高温条件下二氧化碳和碳发生反应 。
(3)操作④中的化学反应方程式为 CO+CuOCu+CO2 。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是 防止一氧化碳污染环境 。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是 焦炭和二氧化碳的反应为吸热反应 。
【解答】解:(1)操作②中实验现象说明CO2不能与CuO反应。
故填:不能。
(2)操作③中CO2含量减小的原因是高温条件下二氧化碳和碳发生反应。
故填:高温条件下二氧化碳和碳发生反应。
(3)操作④中加热时氧化铜和一氧化碳反应生成铜和二氧化碳,化学反应方程式为:CO+CuOCu+CO2。
故填:CO+CuOCu+CO2。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是防止一氧化碳污染环境。
故填:防止一氧化碳污染环境。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是焦炭和二氧化碳的反应为吸热反应。
故填:焦炭和二氧化碳的反应为吸热反应。
第1页(共1页)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
