4.1 空气的成分 同步训练— 2021-2022学年九年级鲁教版上册(word版含答案)
文档属性
| 名称 | 4.1 空气的成分 同步训练— 2021-2022学年九年级鲁教版上册(word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 155.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-25 00:00:00 | ||
图片预览



文档简介
4.1 空气的成分
一、单选题
1.如下图为空气成分示意图 (按体积分数计算),其中“Y”代表的是
A.氧气 B.二氧化碳 C.氮气 D.稀有气体
2.空气是一种宝贵的自然资源,下列有关空气的说法不正确的是
A.二氧化碳是植物光合作用的原料 B.空气中氧气的质量分数约为21%
C.氮气充入食品包装袋防腐 D.氦气可用来填充探空气球
3.下列实验方案,不能达到实验目的的是
选项 实验目的 实验方案
A 鉴别软水和硬水 用肥皂水
B 鉴别氧气和二氧化碳 分别加入澄清石灰水
C 鉴别水和白醋 闻气味
D 鉴别空气和氮气 用带火星的木条
A.A B.B C.C D.D
4.利用图甲装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度随时间的变化趋势如图乙所示。
关于以上实验,有如下说法其中正确的说法是
①反应结束后容器内的氧气已全部被消耗
②AB段气体压强变化的原因是由燃烧放热造成的
③红磷有剩余的原因是容器内氧气的体积分数小于一定值时,红磷无法继续燃烧
④t2后氧气浓度略微上升的原因之一是因为止水夹右侧导管中的空气进入了集气瓶中
⑤从红磷燃烧到熄灭的整个过程中,集气瓶中的液面一直升高
⑥实验中红磷可用铁丝来代替
A.①②④ B.②③④ C.②③⑥ D.②④⑤
5.如果煤燃烧后大量尾气直接排放到空气中,不会对空气造成污染的是
A.CO2 B.NO2 C.SO2 D.可吸入颗粒物
6.小兰同学用如图所示的装置测定空气中氧气的体积分数,实验后发现测定氧气的体积分数低于1/5,针对这一事实,你认为下列做法或想法不可取的是
A.查看实验装置是否漏气
B.实验中可能红磷的量不足,没有将瓶内氧气消耗尽
C.将红磷改为木炭再重做实验
D.实验中可能未冷却至室温就打开止水夹,使进入瓶内的水的体积减少
7.引起酸雨的是
A.二氧化碳 B.一氧化碳 C.二氧化硫 D.PM2.5
8.空气中含量较多且化学性质比较活泼的气体是
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
二、填空题
9.唐诗《风》中有这样两句“过江千尺浪,入竹万竿斜”。诗人观察到的这种自然现象证明了___________的存在。
10.人体中含量最多的元素是_______;约占空气体积的21%的气体是_______。
11.下图是元素周期表中部分元素位置关系示意图。
用相应的化学符号填空:
(1)与碳元素化学性质相似的是________。
(2)由X与Y形成的一种空气污染物为_________。
(3)列举由X元素组成的单质在生产生活中的一种用途:________。
12.空气是一种宝贵的资源,请回答下列问题。
(1)按体积计算:氮气占78%,氧气占21%,稀有气体占______;空气是______(填“纯净物”或“混合物”)。
(2)下列表示某些气体的主要用途,这些气体依次是______
A.食品包装时充入某气体以防腐 B.填充霓虹灯
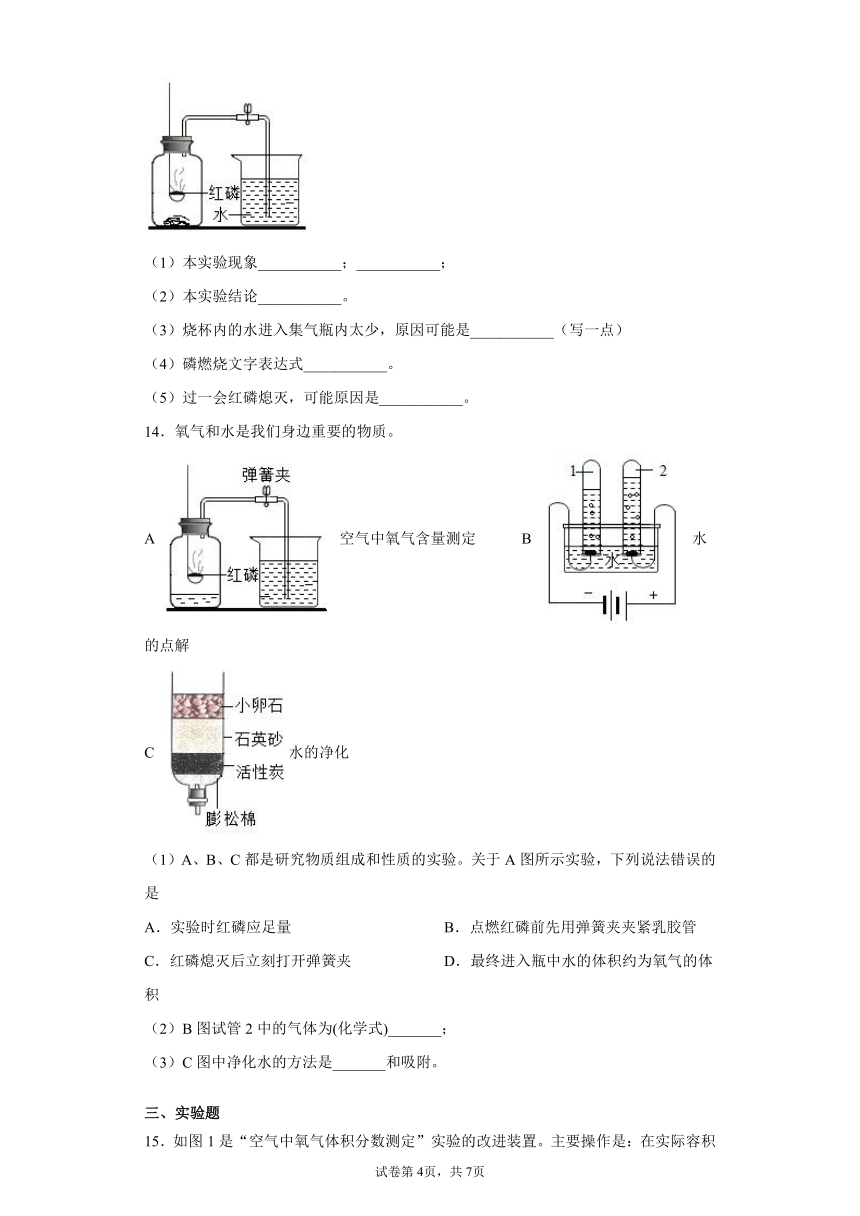
13.如图,是测定空气中氧气含量的实验装置图。回答下列问题:
(1)本实验现象___________;___________;
(2)本实验结论___________。
(3)烧杯内的水进入集气瓶内太少,原因可能是___________(写一点)
(4)磷燃烧文字表达式___________。
(5)过一会红磷熄灭,可能原因是___________。
14.氧气和水是我们身边重要的物质。
A 空气中氧气含量测定 B 水的点解
C 水的净化
(1)A、B、C都是研究物质组成和性质的实验。关于A图所示实验,下列说法错误的是
A.实验时红磷应足量 B.点燃红磷前先用弹簧夹夹紧乳胶管
C.红磷熄灭后立刻打开弹簧夹 D.最终进入瓶中水的体积约为氧气的体积
(2)B图试管2中的气体为(化学式)_______;
(3)C图中净化水的方法是_______和吸附。
三、实验题
15.如图1是“空气中氧气体积分数测定”实验的改进装置。主要操作是:在实际容积为150 mL的集气瓶里,先装进50 mL的水,再按图1连好仪器,按下热的玻璃棒,白磷立即被点燃。(白磷40℃即燃烧,燃烧产物与红磷相同)
(1)白磷燃烧的符号表达式______,白磷燃烧的现象是:______;若实验成功,最终集气瓶中水的体积约为______ mL。
(2)该实验可推论出氮气的物理性质为______化学性质为______。
(3)若将白磷换成炭粉,该实验能否获得成功______原因是______。
(4)集气瓶里预先装进的50 mL水,在实验过程的作用是______。
(5)图2是另一实验小组对测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。(已知铜和氧气在加热的条件下反应生成氧化铜固体)
①根据下表提供的实验数据,完成如表
硬质玻璃管中空气的体积 反应前注射器中空气体积 反应后注射器中气体体积 实验测得空气中氧气的体积分数
25mL 15 mL 9 mL ______
②装置一和装置二中气球的位置不同,______(填“装置一”或“装置二”)更合理,理由是______。
③若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?______(列举两条)。
16.某同学设计了测定空气中氧气含量的实验,实验装置如图1该同学的实验步骤如下:
①将图中的集气瓶分为5等份,并做好标记。
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞。
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
(1)该实验中红磷需稍过量,目的是_________。
(2)红磷燃烧的符号表达式为_________,步骤②集气瓶中的现象是_________。
(3)根据步骤③中打开止水夹后观察到的现象可得出空气中氧气的体积约占_______。
(4)实验完毕后,若进入集气瓶中水的体积偏小,则可能的原因有哪些(答出一点即可)?____________。
(5)用来测定空气成分的方法很多,某同学对实验进行反思后,提出了改进方法,如图2所示,你认为改进后的优点是__________。
四、计算题
17.如果用分离1000L液态空气的方法来制取液态氧气,实际可制取168L液态氧气,请计算氧气的制取率(制取率=)
18.在标准状况下,氧气的密度为1.43g/L、空气的密度为1.29 g/L,一般情况下,正常成年人每分钟吸入8L氧气。问正常成年人每分钟需要吸入空气多少升___________?在标准状况下,每分钟吸入氧气的质量是多少克___________?(提示:氧气约占空气体积的1/5)
试卷第4页,共7页
试卷第5页,共7页
参考答案
1.A
2.B
3.D
4.B
5.A
6.C
7.C
8.B
9.空气
10.氧元素 氧气2
11.
(1)Si
(2)NO2
(3)作保护气(合理即可)
12.0.94% 混合物 氮气、稀有气体
13.
(1) 红磷燃烧生成大量白烟 烧杯内的水通过导管进入集气瓶,约占空气总体积的1/5
(2)氧气约占空气总体积的1/5
(3)红磷的量不足(或装置漏气)
(4)
(5)集气瓶内的氧气被消耗完了
14.
(1)C
(2)O2
(3)过滤
15.
(1)
产生大量白烟,放出热量 70
(2) 难溶于水 不燃烧、不支持燃烧
(3) 否
炭粉在空气中燃烧生成二氧化碳,二氧化碳是气体,化学反应前后,压强变化不大
(4)加快集气瓶内气体冷却、液封导气管末端以防气体逸出、吸收五氧化二磷
(5) 15% 装置二 装置二中的气球在玻璃管的后部,更易让空气流通,使氧气与铜能充分反应 铜粉的量不足或装置漏气或未冷却至室温就读数
16.
(1)使集气瓶中的氧气完全消耗,减少误差
(2) P+O2P2O5 红磷燃烧,放出大量的热量,冒出大量的白烟
(3)1/5五分之一
(4)红磷量不足(装置漏气或未冷却到室温就打开止水夹)
(5)实验结果更准确,更环保。
17.80%
18.氧气约占空气体积的1/5,一般情况下,正常成年人每分钟吸入8L氧气,正常成年人每分钟需要吸入空气8L×5=40L;
在标准状况下,氧气的密度为1.43g/L每分钟吸入氧气的质量8L×1.43g/L=11.44g。答案第2页,共2页
答案第1页,共1页
一、单选题
1.如下图为空气成分示意图 (按体积分数计算),其中“Y”代表的是
A.氧气 B.二氧化碳 C.氮气 D.稀有气体
2.空气是一种宝贵的自然资源,下列有关空气的说法不正确的是
A.二氧化碳是植物光合作用的原料 B.空气中氧气的质量分数约为21%
C.氮气充入食品包装袋防腐 D.氦气可用来填充探空气球
3.下列实验方案,不能达到实验目的的是
选项 实验目的 实验方案
A 鉴别软水和硬水 用肥皂水
B 鉴别氧气和二氧化碳 分别加入澄清石灰水
C 鉴别水和白醋 闻气味
D 鉴别空气和氮气 用带火星的木条
A.A B.B C.C D.D
4.利用图甲装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度随时间的变化趋势如图乙所示。
关于以上实验,有如下说法其中正确的说法是
①反应结束后容器内的氧气已全部被消耗
②AB段气体压强变化的原因是由燃烧放热造成的
③红磷有剩余的原因是容器内氧气的体积分数小于一定值时,红磷无法继续燃烧
④t2后氧气浓度略微上升的原因之一是因为止水夹右侧导管中的空气进入了集气瓶中
⑤从红磷燃烧到熄灭的整个过程中,集气瓶中的液面一直升高
⑥实验中红磷可用铁丝来代替
A.①②④ B.②③④ C.②③⑥ D.②④⑤
5.如果煤燃烧后大量尾气直接排放到空气中,不会对空气造成污染的是
A.CO2 B.NO2 C.SO2 D.可吸入颗粒物
6.小兰同学用如图所示的装置测定空气中氧气的体积分数,实验后发现测定氧气的体积分数低于1/5,针对这一事实,你认为下列做法或想法不可取的是
A.查看实验装置是否漏气
B.实验中可能红磷的量不足,没有将瓶内氧气消耗尽
C.将红磷改为木炭再重做实验
D.实验中可能未冷却至室温就打开止水夹,使进入瓶内的水的体积减少
7.引起酸雨的是
A.二氧化碳 B.一氧化碳 C.二氧化硫 D.PM2.5
8.空气中含量较多且化学性质比较活泼的气体是
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
二、填空题
9.唐诗《风》中有这样两句“过江千尺浪,入竹万竿斜”。诗人观察到的这种自然现象证明了___________的存在。
10.人体中含量最多的元素是_______;约占空气体积的21%的气体是_______。
11.下图是元素周期表中部分元素位置关系示意图。
用相应的化学符号填空:
(1)与碳元素化学性质相似的是________。
(2)由X与Y形成的一种空气污染物为_________。
(3)列举由X元素组成的单质在生产生活中的一种用途:________。
12.空气是一种宝贵的资源,请回答下列问题。
(1)按体积计算:氮气占78%,氧气占21%,稀有气体占______;空气是______(填“纯净物”或“混合物”)。
(2)下列表示某些气体的主要用途,这些气体依次是______
A.食品包装时充入某气体以防腐 B.填充霓虹灯
13.如图,是测定空气中氧气含量的实验装置图。回答下列问题:
(1)本实验现象___________;___________;
(2)本实验结论___________。
(3)烧杯内的水进入集气瓶内太少,原因可能是___________(写一点)
(4)磷燃烧文字表达式___________。
(5)过一会红磷熄灭,可能原因是___________。
14.氧气和水是我们身边重要的物质。
A 空气中氧气含量测定 B 水的点解
C 水的净化
(1)A、B、C都是研究物质组成和性质的实验。关于A图所示实验,下列说法错误的是
A.实验时红磷应足量 B.点燃红磷前先用弹簧夹夹紧乳胶管
C.红磷熄灭后立刻打开弹簧夹 D.最终进入瓶中水的体积约为氧气的体积
(2)B图试管2中的气体为(化学式)_______;
(3)C图中净化水的方法是_______和吸附。
三、实验题
15.如图1是“空气中氧气体积分数测定”实验的改进装置。主要操作是:在实际容积为150 mL的集气瓶里,先装进50 mL的水,再按图1连好仪器,按下热的玻璃棒,白磷立即被点燃。(白磷40℃即燃烧,燃烧产物与红磷相同)
(1)白磷燃烧的符号表达式______,白磷燃烧的现象是:______;若实验成功,最终集气瓶中水的体积约为______ mL。
(2)该实验可推论出氮气的物理性质为______化学性质为______。
(3)若将白磷换成炭粉,该实验能否获得成功______原因是______。
(4)集气瓶里预先装进的50 mL水,在实验过程的作用是______。
(5)图2是另一实验小组对测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。(已知铜和氧气在加热的条件下反应生成氧化铜固体)
①根据下表提供的实验数据,完成如表
硬质玻璃管中空气的体积 反应前注射器中空气体积 反应后注射器中气体体积 实验测得空气中氧气的体积分数
25mL 15 mL 9 mL ______
②装置一和装置二中气球的位置不同,______(填“装置一”或“装置二”)更合理,理由是______。
③若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?______(列举两条)。
16.某同学设计了测定空气中氧气含量的实验,实验装置如图1该同学的实验步骤如下:
①将图中的集气瓶分为5等份,并做好标记。
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞。
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
(1)该实验中红磷需稍过量,目的是_________。
(2)红磷燃烧的符号表达式为_________,步骤②集气瓶中的现象是_________。
(3)根据步骤③中打开止水夹后观察到的现象可得出空气中氧气的体积约占_______。
(4)实验完毕后,若进入集气瓶中水的体积偏小,则可能的原因有哪些(答出一点即可)?____________。
(5)用来测定空气成分的方法很多,某同学对实验进行反思后,提出了改进方法,如图2所示,你认为改进后的优点是__________。
四、计算题
17.如果用分离1000L液态空气的方法来制取液态氧气,实际可制取168L液态氧气,请计算氧气的制取率(制取率=)
18.在标准状况下,氧气的密度为1.43g/L、空气的密度为1.29 g/L,一般情况下,正常成年人每分钟吸入8L氧气。问正常成年人每分钟需要吸入空气多少升___________?在标准状况下,每分钟吸入氧气的质量是多少克___________?(提示:氧气约占空气体积的1/5)
试卷第4页,共7页
试卷第5页,共7页
参考答案
1.A
2.B
3.D
4.B
5.A
6.C
7.C
8.B
9.空气
10.氧元素 氧气2
11.
(1)Si
(2)NO2
(3)作保护气(合理即可)
12.0.94% 混合物 氮气、稀有气体
13.
(1) 红磷燃烧生成大量白烟 烧杯内的水通过导管进入集气瓶,约占空气总体积的1/5
(2)氧气约占空气总体积的1/5
(3)红磷的量不足(或装置漏气)
(4)
(5)集气瓶内的氧气被消耗完了
14.
(1)C
(2)O2
(3)过滤
15.
(1)
产生大量白烟,放出热量 70
(2) 难溶于水 不燃烧、不支持燃烧
(3) 否
炭粉在空气中燃烧生成二氧化碳,二氧化碳是气体,化学反应前后,压强变化不大
(4)加快集气瓶内气体冷却、液封导气管末端以防气体逸出、吸收五氧化二磷
(5) 15% 装置二 装置二中的气球在玻璃管的后部,更易让空气流通,使氧气与铜能充分反应 铜粉的量不足或装置漏气或未冷却至室温就读数
16.
(1)使集气瓶中的氧气完全消耗,减少误差
(2) P+O2P2O5 红磷燃烧,放出大量的热量,冒出大量的白烟
(3)1/5五分之一
(4)红磷量不足(装置漏气或未冷却到室温就打开止水夹)
(5)实验结果更准确,更环保。
17.80%
18.氧气约占空气体积的1/5,一般情况下,正常成年人每分钟吸入8L氧气,正常成年人每分钟需要吸入空气8L×5=40L;
在标准状况下,氧气的密度为1.43g/L每分钟吸入氧气的质量8L×1.43g/L=11.44g。答案第2页,共2页
答案第1页,共1页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
