3.2 溶液组成的定量表示 同步训练-鲁教版 九年级上册(word版 含答案)
文档属性
| 名称 | 3.2 溶液组成的定量表示 同步训练-鲁教版 九年级上册(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 112.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-26 00:00:00 | ||
图片预览



文档简介
3.2 溶液组成的定量表示
一、单选题
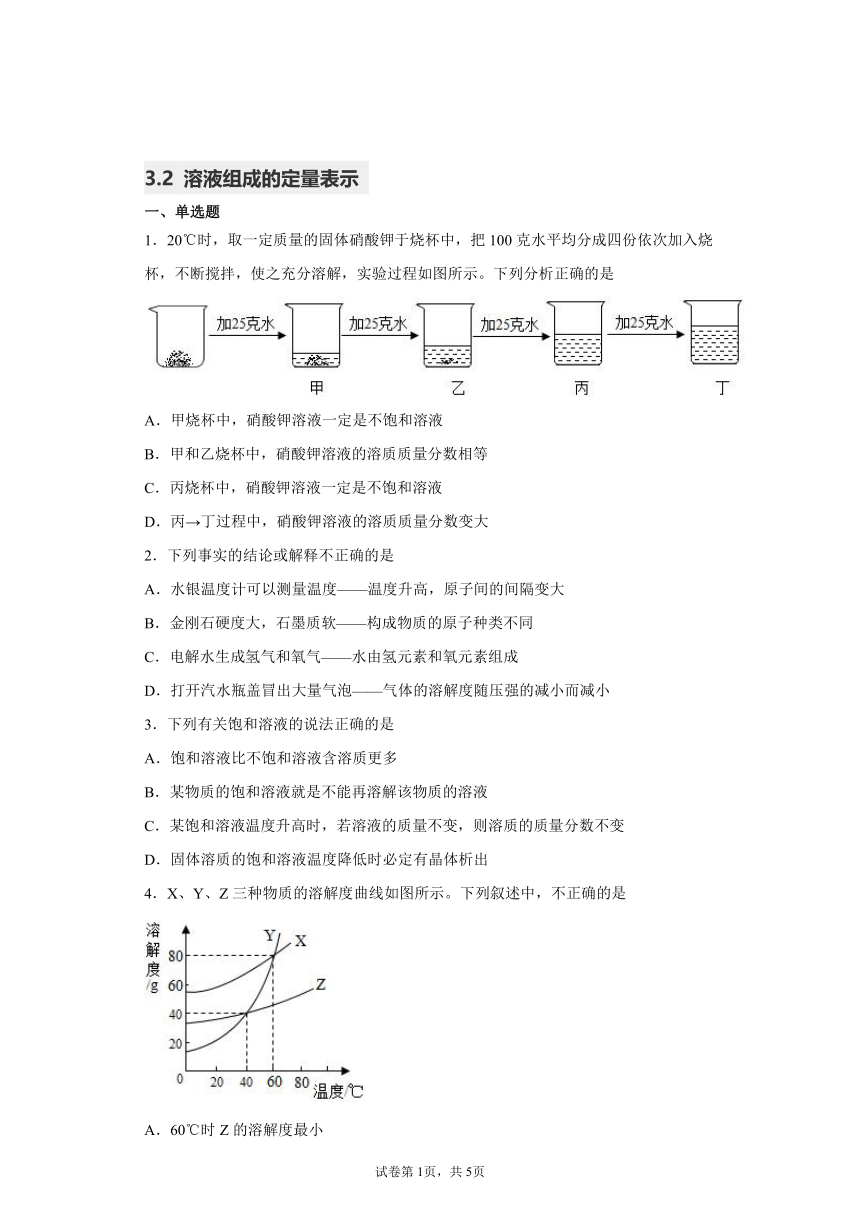
1.20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分溶解,实验过程如图所示。下列分析正确的是
A.甲烧杯中,硝酸钾溶液一定是不饱和溶液
B.甲和乙烧杯中,硝酸钾溶液的溶质质量分数相等
C.丙烧杯中,硝酸钾溶液一定是不饱和溶液
D.丙→丁过程中,硝酸钾溶液的溶质质量分数变大
2.下列事实的结论或解释不正确的是
A.水银温度计可以测量温度——温度升高,原子间的间隔变大
B.金刚石硬度大,石墨质软——构成物质的原子种类不同
C.电解水生成氢气和氧气——水由氢元素和氧元素组成
D.打开汽水瓶盖冒出大量气泡——气体的溶解度随压强的减小而减小
3.下列有关饱和溶液的说法正确的是
A.饱和溶液比不饱和溶液含溶质更多
B.某物质的饱和溶液就是不能再溶解该物质的溶液
C.某饱和溶液温度升高时,若溶液的质量不变,则溶质的质量分数不变
D.固体溶质的饱和溶液温度降低时必定有晶体析出
4.X、Y、Z三种物质的溶解度曲线如图所示。下列叙述中,不正确的是
A.60℃时Z的溶解度最小
B.等质量的三种饱和溶液温度由80℃降至40℃时,Y析出的晶体最多
C.40℃时,Y和Z的饱和溶液的溶质质量分数相同
D.40℃时,X、Y、Z的饱和溶液升温至60℃,所得溶液溶质质量分数X=Y>Z
5.下列关于溶液的说法正确的是
A.一瓶合格的生理盐水密封一段时间,不会出现浑浊
B.饱和溶液的浓度一定大于不饱和溶液的浓度
C.长期放置后不会分层的液体一定是溶液
D.饱和溶液析出晶体后,其溶质的质量分数不变
6.一定温度下,将氯化钠溶于水中,再向溶液中加入硝酸钾,完全溶解后所得溶液的质量为
A. B. C. D.
7.将100克20%的某溶液要使其溶质质量分数增大一倍,可采用的方法是
A.蒸发掉50克水 B.蒸发掉一半溶剂
C.加入20克溶质 D.加入100克20%的该溶液
8.预防“地方性甲状腺肿”最经济、有效的措施是“食盐加碘”,通常是在氯化钠中加入碘酸钾。下图是氯化钠和碘酸钾的溶解度曲线图,下列说法中正确的是
A.碘酸钾属于易溶于水的物质
B.可用过滤的方法分离溶液中的氯化钠和碘酸钾
C.20℃时两者的饱和溶液,氯化钠的溶质质量分数大
D.20℃时不可能制得相同溶质质量分数的碘酸钾溶液和氯化钠溶液
二、填空题
9.根据如图甲、乙、丙三种固体的溶解度曲线回答:
(1)50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为______。
(2)20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数______(填“变大”、“变小”或“不变”)。
(3)分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为______。
10.在100克水中加入2克NaCl和3克KCl,完全溶解后,溶液的质量是_____;现有一杯接近饱和的氢氧化钙溶液欲变成饱和溶液,可采用_____、_____、_____三种方法。
11.将a克食盐粉末放入b克水中,搅拌充分溶解所得溶液的质量___________________(a+b)克(填“>”、“<”、“=”、“≤”)。
12.现有一定温度下底部有少量未溶解固体的硝酸钾溶液,均分为两份进行如下变化:
(1)A、B、C、D四杯溶液中,一定属于不饱和溶液的是________________。
(2)A、B、C、D四杯溶液中,溶质质量分数由大到小的顺序是________________。
(3)同一温度下,同一种物质的饱和(水)溶液________________(填“一定”或“不一定”)比它的不饱和(水)溶液溶质的质量分数大。
13.图为A、B两种固体物质的溶解度曲线。
(1)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是_____。
(2)t2℃时,A物质饱和溶液中溶质的质量分数为_____。若要把100g该饱和溶液稀释成质量分数为5%的溶液,应再加入水_____g。
14.如图是A、B、C三种物质的溶解度曲线。
(1) N点表示的意义是____________。
(2)大量的A中含有少量的B,提纯A的方法是____________。
(3)将t3°C时A、B、C三种物质的饱和溶液降温到t1°C,所得三种溶液的溶质质量分数从大到小的顺序是____________。
三、实验题
15.下图是配制50g质量分数为5% 的氯化钠溶液的操作过程示意图:试回答:
(1)B操作中应称量氯化钠的质量是 _____ g 。放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是 _______________ 。
(2)D操作应选用 ______ 量筒(从50 mL、100 mL中选择);量水时,量筒必须平放,视线要跟量筒 ____________________ 保持水平。若仰视读数,配得溶液的质量分数会 _____ (“偏大”或“偏小”)。
(3)E操作的作用是 ______________ 。
16.现有三支试管,分别加入不同温度和体积的水,试管编号及相关数据如下表.
试管编号 A B C
水的体积/mL 5 10 10
水的温度/℃ 20 20 50
(1)向三支试管中各加入0.5 g硫酸铜粉末,完全溶解.溶液颜色最深的是________.
(2)再向B、C两支试管中加硫酸铜粉末至饱和,则B中溶液的颜色较C中的________.
(3)由此实验可得出:①溶质的质量分数越大,有色溶液的颜色越________;②________.
四、计算题
17.某课外实验小组在进行实验时,发现一瓶无标签的盐酸,为测定该盐酸的溶质质量分数,课外实验小组取足量石灰石与73g该盐酸反应(杂质不溶于水,也不参与反应),生成气体的质量与反应时间的关系如图所示:(假设生成的气体全部逸出)。
请计算:该盐酸的溶质质量分数________。
18.为了防止流感的传播,每天用0.5%的过氧乙酸消毒液消毒。要配制600g溶质质量分数为0.5%的过氧乙酸溶液,需要15%的过氧乙酸溶液多少克______?
试卷第4页,共4页
试卷第1页,共5页
参考答案
1.B
2.B
3.C
4.D
5.A
6.D
7.A
8.C
9.2:5 不变 丙>乙>甲
10.105g 升高温度 增加溶质 蒸发溶剂
11.≤
12.A B>A>C>D 一定
13.B 20% 300
14.在t1°C时,A和C的溶解度相等 降温结晶 B>A>C
15.2.5 取出适量的氯化钠,使天平平衡 50 mL 中凹液面最低处 偏小 加快溶质的溶解速率
16. A 浅 深 温度越高,硫酸铜的溶解度越大(或温度不同,硫酸铜的溶解度不同)
17.10%
18.20g
答案第1页,共2页
答案第1页,共1页
一、单选题
1.20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分溶解,实验过程如图所示。下列分析正确的是
A.甲烧杯中,硝酸钾溶液一定是不饱和溶液
B.甲和乙烧杯中,硝酸钾溶液的溶质质量分数相等
C.丙烧杯中,硝酸钾溶液一定是不饱和溶液
D.丙→丁过程中,硝酸钾溶液的溶质质量分数变大
2.下列事实的结论或解释不正确的是
A.水银温度计可以测量温度——温度升高,原子间的间隔变大
B.金刚石硬度大,石墨质软——构成物质的原子种类不同
C.电解水生成氢气和氧气——水由氢元素和氧元素组成
D.打开汽水瓶盖冒出大量气泡——气体的溶解度随压强的减小而减小
3.下列有关饱和溶液的说法正确的是
A.饱和溶液比不饱和溶液含溶质更多
B.某物质的饱和溶液就是不能再溶解该物质的溶液
C.某饱和溶液温度升高时,若溶液的质量不变,则溶质的质量分数不变
D.固体溶质的饱和溶液温度降低时必定有晶体析出
4.X、Y、Z三种物质的溶解度曲线如图所示。下列叙述中,不正确的是
A.60℃时Z的溶解度最小
B.等质量的三种饱和溶液温度由80℃降至40℃时,Y析出的晶体最多
C.40℃时,Y和Z的饱和溶液的溶质质量分数相同
D.40℃时,X、Y、Z的饱和溶液升温至60℃,所得溶液溶质质量分数X=Y>Z
5.下列关于溶液的说法正确的是
A.一瓶合格的生理盐水密封一段时间,不会出现浑浊
B.饱和溶液的浓度一定大于不饱和溶液的浓度
C.长期放置后不会分层的液体一定是溶液
D.饱和溶液析出晶体后,其溶质的质量分数不变
6.一定温度下,将氯化钠溶于水中,再向溶液中加入硝酸钾,完全溶解后所得溶液的质量为
A. B. C. D.
7.将100克20%的某溶液要使其溶质质量分数增大一倍,可采用的方法是
A.蒸发掉50克水 B.蒸发掉一半溶剂
C.加入20克溶质 D.加入100克20%的该溶液
8.预防“地方性甲状腺肿”最经济、有效的措施是“食盐加碘”,通常是在氯化钠中加入碘酸钾。下图是氯化钠和碘酸钾的溶解度曲线图,下列说法中正确的是
A.碘酸钾属于易溶于水的物质
B.可用过滤的方法分离溶液中的氯化钠和碘酸钾
C.20℃时两者的饱和溶液,氯化钠的溶质质量分数大
D.20℃时不可能制得相同溶质质量分数的碘酸钾溶液和氯化钠溶液
二、填空题
9.根据如图甲、乙、丙三种固体的溶解度曲线回答:
(1)50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为______。
(2)20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数______(填“变大”、“变小”或“不变”)。
(3)分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为______。
10.在100克水中加入2克NaCl和3克KCl,完全溶解后,溶液的质量是_____;现有一杯接近饱和的氢氧化钙溶液欲变成饱和溶液,可采用_____、_____、_____三种方法。
11.将a克食盐粉末放入b克水中,搅拌充分溶解所得溶液的质量___________________(a+b)克(填“>”、“<”、“=”、“≤”)。
12.现有一定温度下底部有少量未溶解固体的硝酸钾溶液,均分为两份进行如下变化:
(1)A、B、C、D四杯溶液中,一定属于不饱和溶液的是________________。
(2)A、B、C、D四杯溶液中,溶质质量分数由大到小的顺序是________________。
(3)同一温度下,同一种物质的饱和(水)溶液________________(填“一定”或“不一定”)比它的不饱和(水)溶液溶质的质量分数大。
13.图为A、B两种固体物质的溶解度曲线。
(1)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是_____。
(2)t2℃时,A物质饱和溶液中溶质的质量分数为_____。若要把100g该饱和溶液稀释成质量分数为5%的溶液,应再加入水_____g。
14.如图是A、B、C三种物质的溶解度曲线。
(1) N点表示的意义是____________。
(2)大量的A中含有少量的B,提纯A的方法是____________。
(3)将t3°C时A、B、C三种物质的饱和溶液降温到t1°C,所得三种溶液的溶质质量分数从大到小的顺序是____________。
三、实验题
15.下图是配制50g质量分数为5% 的氯化钠溶液的操作过程示意图:试回答:
(1)B操作中应称量氯化钠的质量是 _____ g 。放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是 _______________ 。
(2)D操作应选用 ______ 量筒(从50 mL、100 mL中选择);量水时,量筒必须平放,视线要跟量筒 ____________________ 保持水平。若仰视读数,配得溶液的质量分数会 _____ (“偏大”或“偏小”)。
(3)E操作的作用是 ______________ 。
16.现有三支试管,分别加入不同温度和体积的水,试管编号及相关数据如下表.
试管编号 A B C
水的体积/mL 5 10 10
水的温度/℃ 20 20 50
(1)向三支试管中各加入0.5 g硫酸铜粉末,完全溶解.溶液颜色最深的是________.
(2)再向B、C两支试管中加硫酸铜粉末至饱和,则B中溶液的颜色较C中的________.
(3)由此实验可得出:①溶质的质量分数越大,有色溶液的颜色越________;②________.
四、计算题
17.某课外实验小组在进行实验时,发现一瓶无标签的盐酸,为测定该盐酸的溶质质量分数,课外实验小组取足量石灰石与73g该盐酸反应(杂质不溶于水,也不参与反应),生成气体的质量与反应时间的关系如图所示:(假设生成的气体全部逸出)。
请计算:该盐酸的溶质质量分数________。
18.为了防止流感的传播,每天用0.5%的过氧乙酸消毒液消毒。要配制600g溶质质量分数为0.5%的过氧乙酸溶液,需要15%的过氧乙酸溶液多少克______?
试卷第4页,共4页
试卷第1页,共5页
参考答案
1.B
2.B
3.C
4.D
5.A
6.D
7.A
8.C
9.2:5 不变 丙>乙>甲
10.105g 升高温度 增加溶质 蒸发溶剂
11.≤
12.A B>A>C>D 一定
13.B 20% 300
14.在t1°C时,A和C的溶解度相等 降温结晶 B>A>C
15.2.5 取出适量的氯化钠,使天平平衡 50 mL 中凹液面最低处 偏小 加快溶质的溶解速率
16. A 浅 深 温度越高,硫酸铜的溶解度越大(或温度不同,硫酸铜的溶解度不同)
17.10%
18.20g
答案第1页,共2页
答案第1页,共1页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
