备战2022 浙教版科学 中考一轮 基础知识 第29课时 物质的分类(课件 20张ppt)
文档属性
| 名称 | 备战2022 浙教版科学 中考一轮 基础知识 第29课时 物质的分类(课件 20张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-12-27 00:00:00 | ||
图片预览

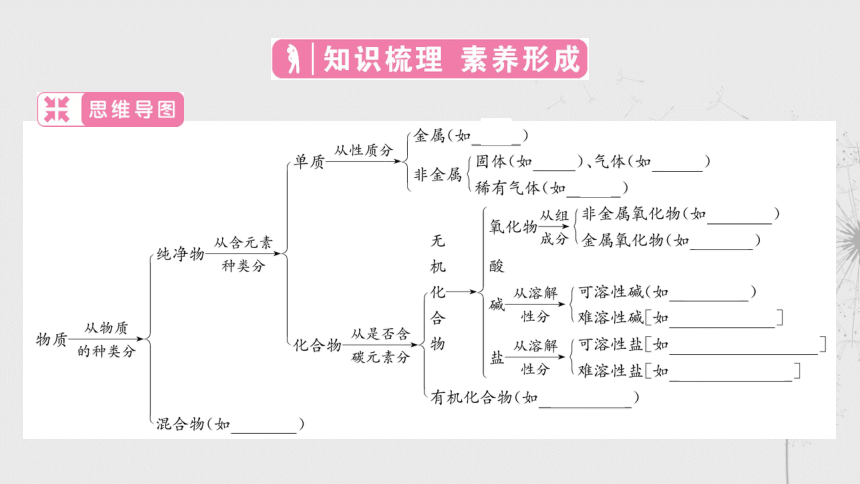







文档简介
(共20张PPT)
第29课时 物质的分类
§分类一 纯净物和混合物
纯净物与混合物
纯净物 混合物
宏观 由 _____物质组成,
_____固定的组成 由_______物质组成,
_____固定组成
微观 由_____种分子构成
(由分子构成) 由_____种分子构成
(由分子构成)
特征 一定条件下,有固定的熔点、沸点及密度 无固定的熔点、沸点
表示 可用化学式表示 不能用化学式表示
一种
有
多种
无
同
不同
§分类二 单质和化合物
单质、化合物的概念及单质和化合物的异同点
单质 化合物
区别 由 _____元素组成 由 _______元素组成
相同点 都属于 _______
同种
不同种
纯净物
§分类三 氧化物、酸、碱、盐
氧化物、酸、碱、盐的概念
1.氧化物:由_____种元素组成,其中有一种元素是_____元素
的化合物。
2.酸:解离时产生的阳离子全部是 ___________的化合物。
3.碱:解离时产生的阴离子全部是 ________________的化合
物。
4.盐:由 ___________________与酸根离子组成的化合物。
两
氧
氢离子(H+)
氢氧根离子(OH-)
金属离子或铵根离子
§分类四 无机物和有机物
无机物和有机物的区别
有机物:含有_____元素的化合物叫做有机化合物(简称有机物);把除有机物以外的其他化合物统称为无机化合物(简称无机物)。
注:不是所有的含碳化合物都是有机物,碳的氧化物、碳酸、碳酸盐等,因其结构和性质与无机物更相似,故通常认为它们是无机物。
碳
常见的有机物
1.甲烷:化学式是 ___,无色、无味、气体,密度比空气小,
极难溶于水,具有 _____性。
燃烧的化学方程式: ______________________。
2.丁烷C4H10——易燃、易液化,是打火机中的燃料。
3.乙炔(C2H2)——易燃,用于焊接和切割金属,氧炔焰的温度可达3000℃以上。
====
点燃
CH4
可燃
CH4+2O2 CO2+2H2O
4.乙酸——俗名醋酸,具有酸的性质。日常生活里 _____中含
少量醋酸。
5.乙醇——俗名_____,酒精灯中的燃料。燃烧的化学方程式:
________________________。
====
点燃
食醋
酒精
C2H5OH+3O2 2CO2+3H2O
对生命活动具有重大意义的有机物
1.糖类:人体消耗能量的主要来源,是合成人体中许多重要化合
物的原料。人体供能的主要物质 _______、蔗糖、植物光合作用
合成的 _____、植物细胞壁中的 _______都是糖类。
2.蛋白质:构成生物体的基本物质。蛋白质是细胞结构里最复杂
多变的一类大分子。遇酸、碱、重金属盐或加热时会变性,如酶
的活性就明显受上述因素影响。
3.脂肪:摄入的脂肪,一部分通过氧化释放出生命活动所需的能
量,另一部分以贮存能量的形式存在于体内。
葡萄糖
淀粉
纤维素
§分类五 矿物能源
重要的矿物能源
1.天然气:主要成分是_______,是常见的气体燃料。
2.石油:“工业的血液”,是古代动植物遗体在地层下经过非常复杂的变化形成的。
3.煤:“工业的粮食”,是古代植物遗体在地层下经过复杂的变化形成的。
甲烷
练习1:“共享单车”是指在公共场所提供共享服务的自行车,由于符合“低碳出行”的理念,颇受年轻人的喜爱。
(1)“低碳出行”中“低碳”指的是较低的_________气体排放。
二氧化碳
(2)上图所示自行车中的材料属于金属材料的是_________(选填
一个序号,下同),属于有机合成材料的是 _________。
(3)采用实体轮胎的“共享单车”可有效防止爆胎。而普通自行
车夏天易爆胎,请用分子的观点解释“夏天易爆胎”的原因:
___________________________。
(4)扫描二维码可以租用“共享单车”,二维码的制作材料一般
是PVC不干胶贴纸。PVC[化学式(C2H3Cl)n]中碳元素和氢元素的质
量比为 _____。
②(或③)
①(或④)
温度升高,分子间间隔增大
8∶1
练习2:如图所示,甲、乙两集气瓶充满氧气,瓶底分别装有澄清石灰水与无水CuSO4。
(1)点燃集气瓶甲中的蜡烛,观察到蜡烛燃烧的产物使澄清石灰水
变浑浊。其中使澄清石灰水变浑浊反应的化学方程式是 _______
____________________。
(2)点燃集气瓶乙中的蜡烛,发现蜡烛燃烧产物使无水CuSO4变蓝
色。其中使无水CuSO4变蓝色反应的化学方程式是 ___________
______________。
(3)由上述2个实验可推断出组成蜡烛的物质中一定含有 _______
元素。
Ca(OH)2
+CO2===CaCO3↓+H2O
CuSO4+5H2O
===CuSO4·5H2O
碳、氢
练习3:实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子构成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按图所示装置进行实验,每步均充分反应,回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是_______
________________________________________________。
(2)以上装置中需要加热的仪器有A和D两处,操作时应先点燃
____处的酒精灯。
(3)实验测得B、C装置分别增重m1克和m2克,则该物质化学式中
x、y比值为____。
(4)将B和C装置互换,则测得的氢元素的含量会 _____(填“偏大”“偏小”或“不变”)。
排尽装
置中的N2、CO2和H2O(或空气),防止对本实验产生干扰
D
偏大
练习4:日常生活中使用的塑料袋,有的是用聚乙烯制成的,也有的是用聚氯乙烯制成的。小凤对包装食品的塑料袋进行探究,以验证其成分。
【作出猜想】
①该塑料袋是用聚乙烯制成的;
②该塑料袋是用聚氯乙烯制成的。
【查阅资料】
聚乙烯燃烧生成二氧化碳和水,聚氯乙烯燃烧生成二氧化碳、水和氯化氢。无水硫酸铜是白色粉末,遇水变成蓝色。
【实验探究】
小凤将装置按A、B、C、D顺序连接好后,进行实验。在实验过程
中,B、D产生明显现象,C无明显现象,说明塑料袋燃烧没有____
(填化学式)气体生成。B装置的作用 _________________,D瓶中
发生反应的化学方程式是___________________________。
【实验结论】通过实验证明,猜想_____是正确的。
HCl
验证是否有水生成
CO2+Ca(OH)2 ===CaCO3↓+H2O
①
【交流反思】
(1)从化学角度分析,大量使用塑料制品会导致_________。
(2)进行实验时, _____(填“能”或“不能”)将B、C位置进行
交换,理由是 _____________________。
白色污染
不能
无法验证是否有水生成
第29课时 物质的分类
§分类一 纯净物和混合物
纯净物与混合物
纯净物 混合物
宏观 由 _____物质组成,
_____固定的组成 由_______物质组成,
_____固定组成
微观 由_____种分子构成
(由分子构成) 由_____种分子构成
(由分子构成)
特征 一定条件下,有固定的熔点、沸点及密度 无固定的熔点、沸点
表示 可用化学式表示 不能用化学式表示
一种
有
多种
无
同
不同
§分类二 单质和化合物
单质、化合物的概念及单质和化合物的异同点
单质 化合物
区别 由 _____元素组成 由 _______元素组成
相同点 都属于 _______
同种
不同种
纯净物
§分类三 氧化物、酸、碱、盐
氧化物、酸、碱、盐的概念
1.氧化物:由_____种元素组成,其中有一种元素是_____元素
的化合物。
2.酸:解离时产生的阳离子全部是 ___________的化合物。
3.碱:解离时产生的阴离子全部是 ________________的化合
物。
4.盐:由 ___________________与酸根离子组成的化合物。
两
氧
氢离子(H+)
氢氧根离子(OH-)
金属离子或铵根离子
§分类四 无机物和有机物
无机物和有机物的区别
有机物:含有_____元素的化合物叫做有机化合物(简称有机物);把除有机物以外的其他化合物统称为无机化合物(简称无机物)。
注:不是所有的含碳化合物都是有机物,碳的氧化物、碳酸、碳酸盐等,因其结构和性质与无机物更相似,故通常认为它们是无机物。
碳
常见的有机物
1.甲烷:化学式是 ___,无色、无味、气体,密度比空气小,
极难溶于水,具有 _____性。
燃烧的化学方程式: ______________________。
2.丁烷C4H10——易燃、易液化,是打火机中的燃料。
3.乙炔(C2H2)——易燃,用于焊接和切割金属,氧炔焰的温度可达3000℃以上。
====
点燃
CH4
可燃
CH4+2O2 CO2+2H2O
4.乙酸——俗名醋酸,具有酸的性质。日常生活里 _____中含
少量醋酸。
5.乙醇——俗名_____,酒精灯中的燃料。燃烧的化学方程式:
________________________。
====
点燃
食醋
酒精
C2H5OH+3O2 2CO2+3H2O
对生命活动具有重大意义的有机物
1.糖类:人体消耗能量的主要来源,是合成人体中许多重要化合
物的原料。人体供能的主要物质 _______、蔗糖、植物光合作用
合成的 _____、植物细胞壁中的 _______都是糖类。
2.蛋白质:构成生物体的基本物质。蛋白质是细胞结构里最复杂
多变的一类大分子。遇酸、碱、重金属盐或加热时会变性,如酶
的活性就明显受上述因素影响。
3.脂肪:摄入的脂肪,一部分通过氧化释放出生命活动所需的能
量,另一部分以贮存能量的形式存在于体内。
葡萄糖
淀粉
纤维素
§分类五 矿物能源
重要的矿物能源
1.天然气:主要成分是_______,是常见的气体燃料。
2.石油:“工业的血液”,是古代动植物遗体在地层下经过非常复杂的变化形成的。
3.煤:“工业的粮食”,是古代植物遗体在地层下经过复杂的变化形成的。
甲烷
练习1:“共享单车”是指在公共场所提供共享服务的自行车,由于符合“低碳出行”的理念,颇受年轻人的喜爱。
(1)“低碳出行”中“低碳”指的是较低的_________气体排放。
二氧化碳
(2)上图所示自行车中的材料属于金属材料的是_________(选填
一个序号,下同),属于有机合成材料的是 _________。
(3)采用实体轮胎的“共享单车”可有效防止爆胎。而普通自行
车夏天易爆胎,请用分子的观点解释“夏天易爆胎”的原因:
___________________________。
(4)扫描二维码可以租用“共享单车”,二维码的制作材料一般
是PVC不干胶贴纸。PVC[化学式(C2H3Cl)n]中碳元素和氢元素的质
量比为 _____。
②(或③)
①(或④)
温度升高,分子间间隔增大
8∶1
练习2:如图所示,甲、乙两集气瓶充满氧气,瓶底分别装有澄清石灰水与无水CuSO4。
(1)点燃集气瓶甲中的蜡烛,观察到蜡烛燃烧的产物使澄清石灰水
变浑浊。其中使澄清石灰水变浑浊反应的化学方程式是 _______
____________________。
(2)点燃集气瓶乙中的蜡烛,发现蜡烛燃烧产物使无水CuSO4变蓝
色。其中使无水CuSO4变蓝色反应的化学方程式是 ___________
______________。
(3)由上述2个实验可推断出组成蜡烛的物质中一定含有 _______
元素。
Ca(OH)2
+CO2===CaCO3↓+H2O
CuSO4+5H2O
===CuSO4·5H2O
碳、氢
练习3:实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子构成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按图所示装置进行实验,每步均充分反应,回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是_______
________________________________________________。
(2)以上装置中需要加热的仪器有A和D两处,操作时应先点燃
____处的酒精灯。
(3)实验测得B、C装置分别增重m1克和m2克,则该物质化学式中
x、y比值为____。
(4)将B和C装置互换,则测得的氢元素的含量会 _____(填“偏大”“偏小”或“不变”)。
排尽装
置中的N2、CO2和H2O(或空气),防止对本实验产生干扰
D
偏大
练习4:日常生活中使用的塑料袋,有的是用聚乙烯制成的,也有的是用聚氯乙烯制成的。小凤对包装食品的塑料袋进行探究,以验证其成分。
【作出猜想】
①该塑料袋是用聚乙烯制成的;
②该塑料袋是用聚氯乙烯制成的。
【查阅资料】
聚乙烯燃烧生成二氧化碳和水,聚氯乙烯燃烧生成二氧化碳、水和氯化氢。无水硫酸铜是白色粉末,遇水变成蓝色。
【实验探究】
小凤将装置按A、B、C、D顺序连接好后,进行实验。在实验过程
中,B、D产生明显现象,C无明显现象,说明塑料袋燃烧没有____
(填化学式)气体生成。B装置的作用 _________________,D瓶中
发生反应的化学方程式是___________________________。
【实验结论】通过实验证明,猜想_____是正确的。
HCl
验证是否有水生成
CO2+Ca(OH)2 ===CaCO3↓+H2O
①
【交流反思】
(1)从化学角度分析,大量使用塑料制品会导致_________。
(2)进行实验时, _____(填“能”或“不能”)将B、C位置进行
交换,理由是 _____________________。
白色污染
不能
无法验证是否有水生成
同课章节目录
