高一化学《物质的分类》课件
图片预览








文档简介
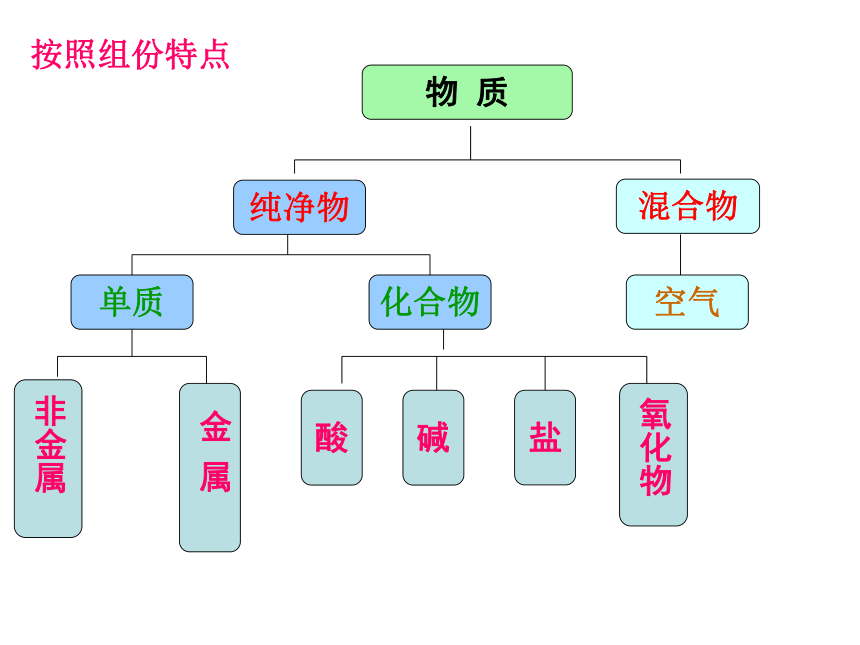
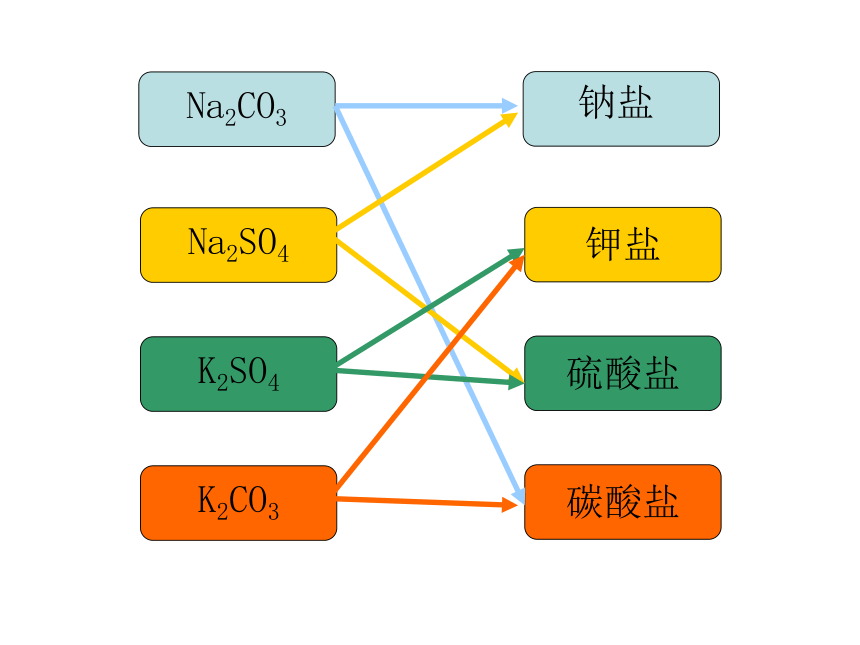
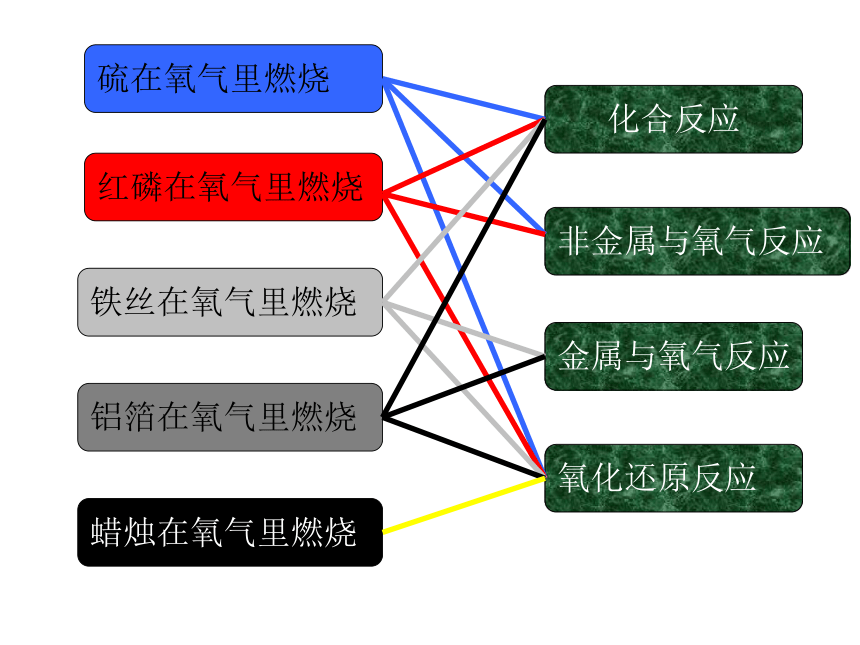
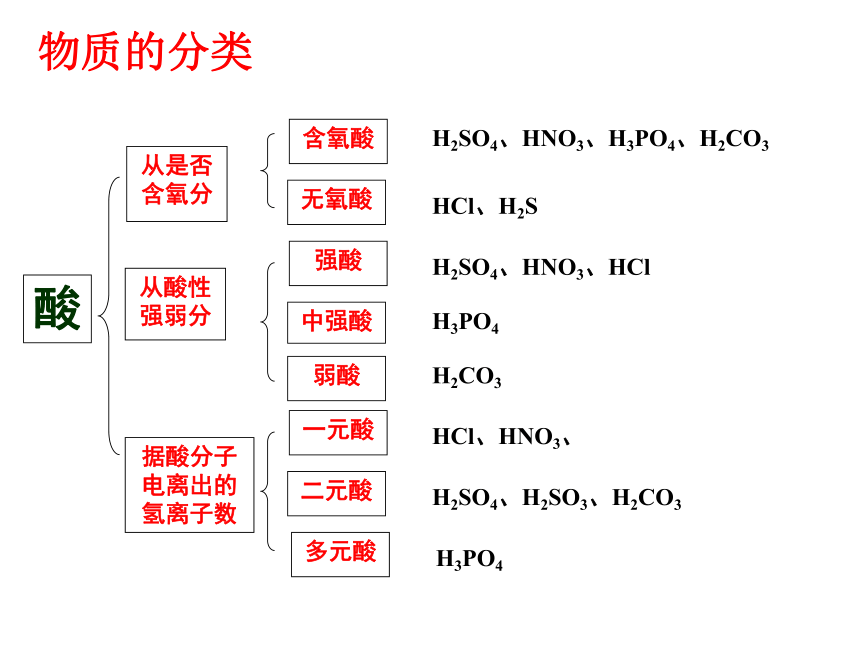
课件40张PPT。第二章 化学物质及其分类第一节 物质的分类化学是人类文明、进步的关键牙膏氢能轿车液晶记忆合金普钙味精第一节 物质的分类? 图书馆里有许许多多的书籍,为什么你很快就能找到你需要的书呢你身边的分类 超市里有成千上万种商品,为什么你能够迅速挑出你所需要的东西? 简单分类法及应用第一节 物质的分类 分类是学习和研究化学物质及其变化的一种常用的科学方法。运用分类的方法不仅能使有关化学物质及其变化的知识系统化,还可以通过分门别类的研究,发现物质及其变化规律。物 质纯净物混合物空气化合物单质盐碱酸按照组份特点Na2SO4K2SO4K2CO3碳酸盐硫酸盐钾盐Na2CO3钠盐硫在氧气里燃烧红磷在氧气里燃烧铁丝在氧气里燃烧铝箔在氧气里燃烧蜡烛在氧气里燃烧非金属与氧气反应化合反应金属与氧气反应氧化还原反应一、简单分类及其应用2、交叉分类法:对同一事物按照不同的标准进行分类1、树状分类法:对同类事物按照某种属性进行分类的方法.酸从酸性强弱分无氧酸中强酸弱酸H2SO4、HNO3、H3PO4、H2CO3HCl、H2SH2SO4、HNO3、HClH3PO4H2CO3物质的分类据酸分子电离出的氢离子数多元酸二元酸HCl、HNO3、H2SO4、H2SO3、H2CO3H3PO4碱从碱性强弱分难溶碱弱碱NaOH、KOH、Ca(OH) 2、Ba(OH)2、NH3·H2ONaOH、KOH、Ca(OH) 2、Ba(OH)2Cu(OH)2、Mg(OH)2、Fe(OH) 3NH3·H2O 、Cu(OH)2、Mg(OH)2、Fe(OH) 3物质的分类据碱分子电离出的氢氧根离子数多元碱二元碱NH3·H2O 、 NaOH、KOH、Cu(OH)2、Mg(OH)2、Fe(OH) 2
Ca(OH) 2、Ba(OH)2、Fe(OH) 3盐按阴阳离子分无氧酸盐按酸根是否含氧分难溶盐K+ Na+ NH4+ NO3- CL- SO42-CaCO3、BaSO4、AgclKNO3、KMnO4、FeSO4NaCl、ZnS、CaCl2物质的分类据组成分
**碱式盐酸式盐Cu2(OH)2CO3NaHCO3、NH4HCO3、NaHSO4KNO3、KMnO4、FeSO4 、 NaCl、ZnS、CaCl2氧化物酸性氧化物
碱性氧化物
不成盐氧化物CuO、Fe2O3、Na2OCO、P2O5、H2OCO2、P2O5、SO3CaO、CuO、K2OCO、非金属氧化物金属氧化物物质的分类两性氧化物Al2O3、化学反应按反应物和生成物的类别以及反应前后物质的多少化合反应分解反应置换反应复分解反应按反应中是否有离子参加离子反应非离子反应按反应中是否有氧得失氧化还原反应非氧化还原反应H2O + CO2 === H2CO3H2CO3=== H2O+CO2↑
H2 + CuO === H2O + CuHCl + AgNO3 === HNO3 + AgCl ↓
CO + CuO === CO2 + Cu 1.在豆浆里加了白糖,豆浆依然像牛奶一样——纯白甜蜜。可若在豆浆里加进少量酱油或红糖,却很快凝成白花花的叫做豆花的东西。你知道这是为什么吗?
2.阳光灿烂的清晨,在茂密的树林里,你会看到有什么景象?
3.你知道烟、云、雾是怎么形成的吗?
你能解释这些生活中的现象吗??一、分散系及其分类分散质:分散剂:1、分散系:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。被分散的物质起容纳分散质作用的物质2、分散系的组成:3、分散系的分类: 从分散质和分散剂的状态考虑,可以组成几种分散系?为什么
继续回忆分散系的分类?空气云、雾烟、尘泡沫乳浊液:牛奶悬浊液:泡沫塑料珍珠有色玻璃、合金分散系胶体浊液溶液悬浊液乳浊液据微粒大小不同胶体分散质粒子的直径一种特殊的分散系——胶体胶体的概念 常见的胶体【知识拓展】浓烟雾 【活动与探究】 胶体与溶液、浊液的性质有何不同? 将盛有硫酸铜溶液和氢氧化铁胶体的两只烧杯置于暗处,用聚光手电筒(或激光笔)照射(如下图),从垂直于光线的方向观察实验现象。胶体的性质实验一丁达尔现象 当一束强光透过胶体时,可以看到一条光亮的通路,这种现象叫做丁达尔现象。溶液胶体三、胶体的性质(1)丁达尔现象
胶体微粒对光线散射而形成一条光亮的通路。(应用:区分胶体和溶液)树林中的丁达尔效应 海洋中的丁达尔效应 电影放映时的丁达尔效应 胶体的性质(1)丁达尔现象—
(2)电泳—
胶体微粒对光线散射而形成
一条光亮的通路。(应用:鉴别胶体和溶液)*** 在外加电场的作用下,胶体分散质
微粒在分散剂里向阴极(阳极)作定向运动的现象。
胶体发生电泳现象说明 [Fe(OH)3]胶体颗粒带电荷应用:1、提纯和精制胶体
2、胶体稳定存在的原因** ③升温—— 增加碰撞机会
②加入电性相反的胶粒
——破坏胶粒的带电结构(3)胶体的聚沉方法胶体的性质①加入电解质等方法能使胶体凝聚。
利用半透膜把胶体中混有的离子或分子从胶体溶液里分离的操作,叫做渗析。
其原理为胶体微粒不能透过半透膜,而溶液中的分子和离子能透过半透膜。 溶液、胶体的粒子大小比较应用:
胶体净化、提纯使胶体和溶液分离胶体的制备当粒子直径达到1nm~100nm1、分散法2、聚集法氢氧化铁胶体的制备:向沸水中滴加饱和氯化铁溶液5~6滴,继续煮沸至溶液呈红褐色,停止加热。 1、人们喝豆浆,常加入白糖,而不加入食盐。
2、喷墨打印机由于混用了几种不同品牌的墨水,而导致喷头堵塞,影响使用。
3、某些胶体,只需涂在伤口表面,就能有效止血。
4、在医学上,许多血液病的诊断和治疗都利用了胶体的性质。
5、国防工业上有些火药、炸药必须制成胶体。
6、在金属、陶瓷等材料中加入某些固态胶体粒子,可以使材料更耐冲击、不易断裂。都与我有关我是胶体胶体及其应用
7 静电除尘
8 土壤的保肥
9 石膏或卤水点豆腐、制造果冻和皮冻
10 明矾净水原理
11 江河入海处形成沙洲
1、胶体的最本质的特征是( )
A、属于一种分散系
B、有丁达尔效应
C、可以通过滤纸
D、分散质粒子的直径在
1nm ~100nm之间D 随堂练习2、用特殊方法把固体物质加 工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同数量级的是 ( )
A、溶液 B、悬浊液
C、胶体 D、乳浊液
C随堂练习
3、下列各组物质中,常用渗析法分离
的是 ( )
A、CaCO3和Na2CO3固体
B、I2和K2CO3固体
C、CCl4和水
D、Fe(OH)3胶体和FeCl3溶液DA.加水溶解后过滤 B.升华
C.分液 D.渗析随堂练习 4、用你学的知识来分离混合液中的NaCl溶液、AgCl沉淀、淀粉胶体溶液。 随堂练习
Ca(OH) 2、Ba(OH)2、Fe(OH) 3盐按阴阳离子分无氧酸盐按酸根是否含氧分难溶盐K+ Na+ NH4+ NO3- CL- SO42-CaCO3、BaSO4、AgclKNO3、KMnO4、FeSO4NaCl、ZnS、CaCl2物质的分类据组成分
**碱式盐酸式盐Cu2(OH)2CO3NaHCO3、NH4HCO3、NaHSO4KNO3、KMnO4、FeSO4 、 NaCl、ZnS、CaCl2氧化物酸性氧化物
碱性氧化物
不成盐氧化物CuO、Fe2O3、Na2OCO、P2O5、H2OCO2、P2O5、SO3CaO、CuO、K2OCO、非金属氧化物金属氧化物物质的分类两性氧化物Al2O3、化学反应按反应物和生成物的类别以及反应前后物质的多少化合反应分解反应置换反应复分解反应按反应中是否有离子参加离子反应非离子反应按反应中是否有氧得失氧化还原反应非氧化还原反应H2O + CO2 === H2CO3H2CO3=== H2O+CO2↑
H2 + CuO === H2O + CuHCl + AgNO3 === HNO3 + AgCl ↓
CO + CuO === CO2 + Cu 1.在豆浆里加了白糖,豆浆依然像牛奶一样——纯白甜蜜。可若在豆浆里加进少量酱油或红糖,却很快凝成白花花的叫做豆花的东西。你知道这是为什么吗?
2.阳光灿烂的清晨,在茂密的树林里,你会看到有什么景象?
3.你知道烟、云、雾是怎么形成的吗?
你能解释这些生活中的现象吗??一、分散系及其分类分散质:分散剂:1、分散系:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。被分散的物质起容纳分散质作用的物质2、分散系的组成:3、分散系的分类: 从分散质和分散剂的状态考虑,可以组成几种分散系?为什么
继续回忆分散系的分类?空气云、雾烟、尘泡沫乳浊液:牛奶悬浊液:泡沫塑料珍珠有色玻璃、合金分散系胶体浊液溶液悬浊液乳浊液据微粒大小不同胶体分散质粒子的直径一种特殊的分散系——胶体胶体的概念 常见的胶体【知识拓展】浓烟雾 【活动与探究】 胶体与溶液、浊液的性质有何不同? 将盛有硫酸铜溶液和氢氧化铁胶体的两只烧杯置于暗处,用聚光手电筒(或激光笔)照射(如下图),从垂直于光线的方向观察实验现象。胶体的性质实验一丁达尔现象 当一束强光透过胶体时,可以看到一条光亮的通路,这种现象叫做丁达尔现象。溶液胶体三、胶体的性质(1)丁达尔现象
胶体微粒对光线散射而形成一条光亮的通路。(应用:区分胶体和溶液)树林中的丁达尔效应 海洋中的丁达尔效应 电影放映时的丁达尔效应 胶体的性质(1)丁达尔现象—
(2)电泳—
胶体微粒对光线散射而形成
一条光亮的通路。(应用:鉴别胶体和溶液)*** 在外加电场的作用下,胶体分散质
微粒在分散剂里向阴极(阳极)作定向运动的现象。
胶体发生电泳现象说明 [Fe(OH)3]胶体颗粒带电荷应用:1、提纯和精制胶体
2、胶体稳定存在的原因** ③升温—— 增加碰撞机会
②加入电性相反的胶粒
——破坏胶粒的带电结构(3)胶体的聚沉方法胶体的性质①加入电解质等方法能使胶体凝聚。
利用半透膜把胶体中混有的离子或分子从胶体溶液里分离的操作,叫做渗析。
其原理为胶体微粒不能透过半透膜,而溶液中的分子和离子能透过半透膜。 溶液、胶体的粒子大小比较应用:
胶体净化、提纯使胶体和溶液分离胶体的制备当粒子直径达到1nm~100nm1、分散法2、聚集法氢氧化铁胶体的制备:向沸水中滴加饱和氯化铁溶液5~6滴,继续煮沸至溶液呈红褐色,停止加热。 1、人们喝豆浆,常加入白糖,而不加入食盐。
2、喷墨打印机由于混用了几种不同品牌的墨水,而导致喷头堵塞,影响使用。
3、某些胶体,只需涂在伤口表面,就能有效止血。
4、在医学上,许多血液病的诊断和治疗都利用了胶体的性质。
5、国防工业上有些火药、炸药必须制成胶体。
6、在金属、陶瓷等材料中加入某些固态胶体粒子,可以使材料更耐冲击、不易断裂。都与我有关我是胶体胶体及其应用
7 静电除尘
8 土壤的保肥
9 石膏或卤水点豆腐、制造果冻和皮冻
10 明矾净水原理
11 江河入海处形成沙洲
1、胶体的最本质的特征是( )
A、属于一种分散系
B、有丁达尔效应
C、可以通过滤纸
D、分散质粒子的直径在
1nm ~100nm之间D 随堂练习2、用特殊方法把固体物质加 工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同数量级的是 ( )
A、溶液 B、悬浊液
C、胶体 D、乳浊液
C随堂练习
3、下列各组物质中,常用渗析法分离
的是 ( )
A、CaCO3和Na2CO3固体
B、I2和K2CO3固体
C、CCl4和水
D、Fe(OH)3胶体和FeCl3溶液DA.加水溶解后过滤 B.升华
C.分液 D.渗析随堂练习 4、用你学的知识来分离混合液中的NaCl溶液、AgCl沉淀、淀粉胶体溶液。 随堂练习
