高一化学《化学计量在化学实验中的应用》课件
文档属性
| 名称 | 高一化学《化学计量在化学实验中的应用》课件 |  | |
| 格式 | zip | ||
| 文件大小 | 163.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-10-30 14:48:07 | ||
图片预览





文档简介
课件18张PPT。摩尔质量复习上节内容在0.5 mol O2中含有的氧分子数目是多少?解:N(O2)= n(O2) × NA =0.5 mol× 6.02 ×1023mol-1
= 3.01 × 1023 答:O2的氧分子数为3.01 × 1023个。[例题1]注意解题格式在0.5 mol O2中含有的氧原子数目是多少?解:每个O2分子中含有两个氧原子,氧原子数为N(O)= n(O2)×2 × NA =0.5 mol×2× 6.02 ×1023mol-1
= 6.02 × 1023 答:O2的氧原子数为6.02 × 1023个。[例题2]在0.5molO2中含有的电子数目是多少?
解:O2的电子数为8X2=16N = n ×16 × NA = 4.816 × 1024 答:0.5molO2的电子数为4.816 × 1024个。[例题三]=0.5 mol×16× 6.02 ×1023mol-1 N ———— n————m
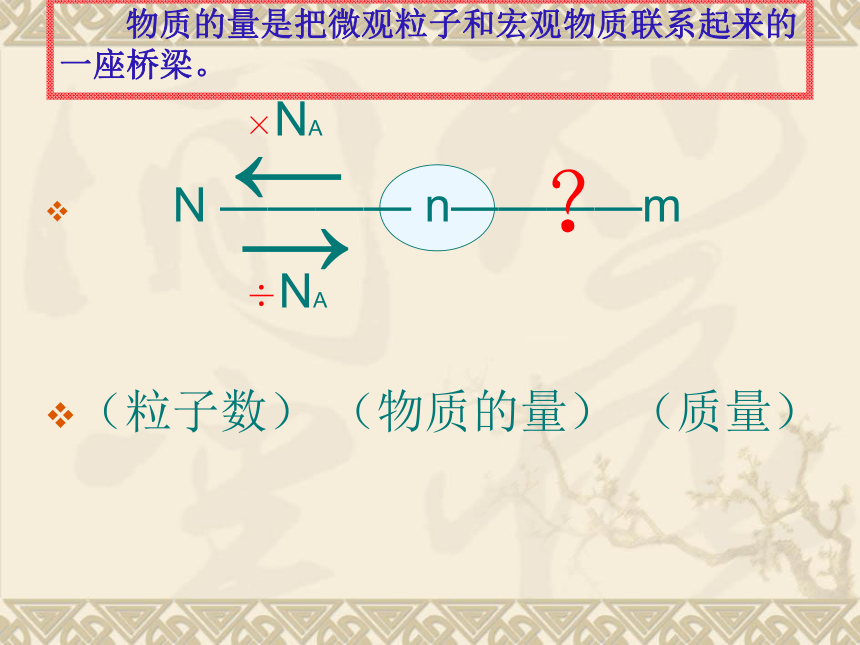
(粒子数) (物质的量) (质量)←×NA→÷NA
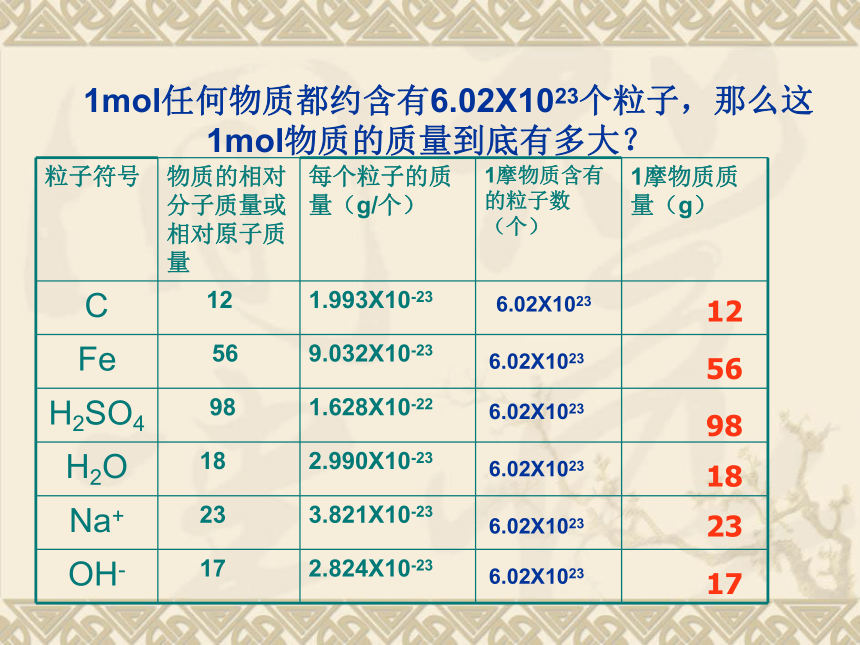
? 物质的量是把微观粒子和宏观物质联系起来的 一座桥梁。 1mol任何物质都约含有6.02X1023个粒子,那么这1mol物质的质量到底有多大?6.02X10236.02X10236.02X10236.02X10236.02X10236.02X1023125698182317分析以上计算结果可得出什么规律?(1)1mol任何原子的质量(以克为单位)在数值上等于这种原子的相对原子质量。
(2) 1mol任何分子的质量(以克为单位)在数值上等于这种分子的相对分子质量。
(3) 1mol任何离子的质量(以克为单位)在数值上等于这种离子的式量。二、摩尔质量1、1mol物质的质量:
1mol任何微粒或物质的质量在以克为单位时,数值上等于该微粒的相对原子质量或相对分子质量。课堂练习:1、填空:
(1)1molCu质量是 克
(2)1molO2质量是 克
(3) 1molCO2质量是 克
(4) 1molCl-质量是 克
(5) 1molNa+质量是 克
(6) 1molNaCl质量是 克64324435.52358.52、摩尔质量
(1)定义:单位物质的量的物质所具有的质量叫做摩尔质量。
(2)符号:M
(3)单位:g/mol(或kg/mol)
(4)数值: (当单位为 g/mol )等于物质或粒子的相对分子质量或相对原子质量
(5)物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系:
n(mol)=m(g)M(g/mol)例1 24.5克H2SO4的物质的量是多少?课堂练习:(1)、O2的摩尔质量是多少?
(2)、H2SO4的摩尔质量是多少?
(3)、100molH2O的质量是多少克?
(4)、0.1molOH-的质量是多少克?
(5)、34gNH3的物质的量是多少?32g.mol-198g.mol-11800g1.7g2mol摩尔质量、1mol物质的质量以及相对分子(原子)质量的区别注意NA重要关系式N=n·n=NNAn1n2N1=N2粒子数阿伏加德罗常数物质的量即:粒子数与物质的量成正比M=mMm=n·n注意:利用上述关系式进行计算时,要统一单位即M÷m× Mn质量摩尔质量物质的量同种物质的质量(m)、物质的量(n)和微粒数(N)三者之间的换算方法N×NANA÷分析反应 C + O2 == CO2表达的含义1个CC + O2 == CO21个O21个CO2扩大 NA倍扩大 NA倍扩大 NA倍1molC1molO21molCO2结论方程式的系数比==物质的量之比==微粒数之比微粒数物质的量系数111摩尔质量的计算方法:(1)M=m/n(2)M=Mr(3)M=m(粒子数)XNA今天你学到了什么?
= 3.01 × 1023 答:O2的氧分子数为3.01 × 1023个。[例题1]注意解题格式在0.5 mol O2中含有的氧原子数目是多少?解:每个O2分子中含有两个氧原子,氧原子数为N(O)= n(O2)×2 × NA =0.5 mol×2× 6.02 ×1023mol-1
= 6.02 × 1023 答:O2的氧原子数为6.02 × 1023个。[例题2]在0.5molO2中含有的电子数目是多少?
解:O2的电子数为8X2=16N = n ×16 × NA = 4.816 × 1024 答:0.5molO2的电子数为4.816 × 1024个。[例题三]=0.5 mol×16× 6.02 ×1023mol-1 N ———— n————m
(粒子数) (物质的量) (质量)←×NA→÷NA
? 物质的量是把微观粒子和宏观物质联系起来的 一座桥梁。 1mol任何物质都约含有6.02X1023个粒子,那么这1mol物质的质量到底有多大?6.02X10236.02X10236.02X10236.02X10236.02X10236.02X1023125698182317分析以上计算结果可得出什么规律?(1)1mol任何原子的质量(以克为单位)在数值上等于这种原子的相对原子质量。
(2) 1mol任何分子的质量(以克为单位)在数值上等于这种分子的相对分子质量。
(3) 1mol任何离子的质量(以克为单位)在数值上等于这种离子的式量。二、摩尔质量1、1mol物质的质量:
1mol任何微粒或物质的质量在以克为单位时,数值上等于该微粒的相对原子质量或相对分子质量。课堂练习:1、填空:
(1)1molCu质量是 克
(2)1molO2质量是 克
(3) 1molCO2质量是 克
(4) 1molCl-质量是 克
(5) 1molNa+质量是 克
(6) 1molNaCl质量是 克64324435.52358.52、摩尔质量
(1)定义:单位物质的量的物质所具有的质量叫做摩尔质量。
(2)符号:M
(3)单位:g/mol(或kg/mol)
(4)数值: (当单位为 g/mol )等于物质或粒子的相对分子质量或相对原子质量
(5)物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系:
n(mol)=m(g)M(g/mol)例1 24.5克H2SO4的物质的量是多少?课堂练习:(1)、O2的摩尔质量是多少?
(2)、H2SO4的摩尔质量是多少?
(3)、100molH2O的质量是多少克?
(4)、0.1molOH-的质量是多少克?
(5)、34gNH3的物质的量是多少?32g.mol-198g.mol-11800g1.7g2mol摩尔质量、1mol物质的质量以及相对分子(原子)质量的区别注意NA重要关系式N=n·n=NNAn1n2N1=N2粒子数阿伏加德罗常数物质的量即:粒子数与物质的量成正比M=mMm=n·n注意:利用上述关系式进行计算时,要统一单位即M÷m× Mn质量摩尔质量物质的量同种物质的质量(m)、物质的量(n)和微粒数(N)三者之间的换算方法N×NANA÷分析反应 C + O2 == CO2表达的含义1个CC + O2 == CO21个O21个CO2扩大 NA倍扩大 NA倍扩大 NA倍1molC1molO21molCO2结论方程式的系数比==物质的量之比==微粒数之比微粒数物质的量系数111摩尔质量的计算方法:(1)M=m/n(2)M=Mr(3)M=m(粒子数)XNA今天你学到了什么?
