备战2022 浙教版科学 中考一轮 第31课时 空气、氧气、二氧化碳(二) 知识梳理(课件 22张PPT)
文档属性
| 名称 | 备战2022 浙教版科学 中考一轮 第31课时 空气、氧气、二氧化碳(二) 知识梳理(课件 22张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-12-29 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
第31课时 空气、氧气、二氧化碳(二)
§分类一 二氧化碳
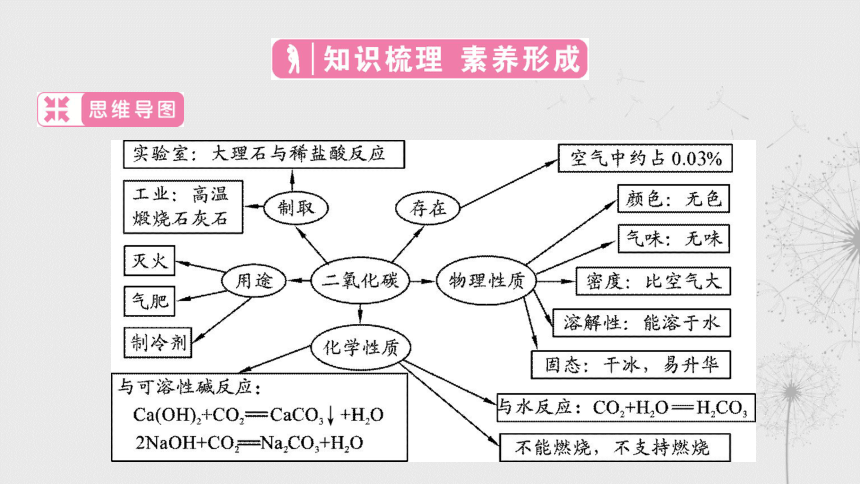
二氧化碳的主要物理性质
无色、无味、密度比空气___,所以可用___________法收集;
___溶于水,所以不能用_____法收集;固体CO2叫_____,易
_____,这个过程要 _____大量热,所以可用固体CO2作制冷剂。
大
向上排空气
能
排水
干冰
升华
吸收
二氧化碳的主要化学性质
1.CO2与水反应,反应的化学方程式为:_______________。碳酸
不稳定,易分解,反应的化学方程式为:_________________。
2.CO2与石灰水反应,能使澄清石灰水变_______,该反应常用于
检验CO2。化学方程式为: __________________________。
CO2+H2O===H2CO3
H2CO3===CO2↑+H2O
浑浊
CO2+Ca(OH)2===CaCO3↓+H2O
3.CO2与NaOH反应,一般用 _________吸收CO2,化学方程式为:
_______________________。
4.CO2参与光合作用,维持空气中CO2和O2平衡,化学方程式为:
______________________________。
光
叶绿体
NaOH溶液
CO2+2NaOH===Na2CO3+H2O
6CO2+6H2O C6H12O6+6O2
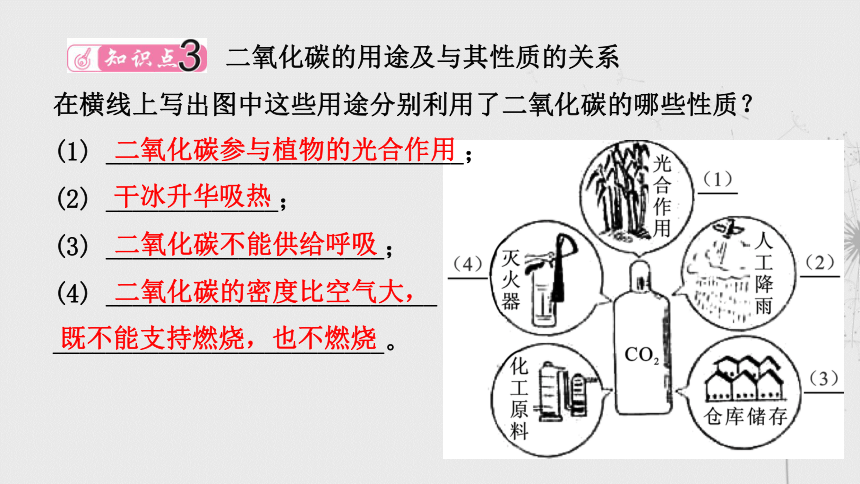
二氧化碳的用途及与其性质的关系
在横线上写出图中这些用途分别利用了二氧化碳的哪些性质?
(1) ___________________________;
(2) _____________;
(3) _____________________;
(4) _________________________
_________________________。
二氧化碳参与植物的光合作用
干冰升华吸热
二氧化碳不能供给呼吸
二氧化碳的密度比空气大,
既不能支持燃烧,也不燃烧
二氧化碳的实验室制备及检验方法
1.二氧化碳的实验室制法
(1)反应原理
_________________________________。
CaCO3+2HCl===CaCl2+H2O+CO2↑
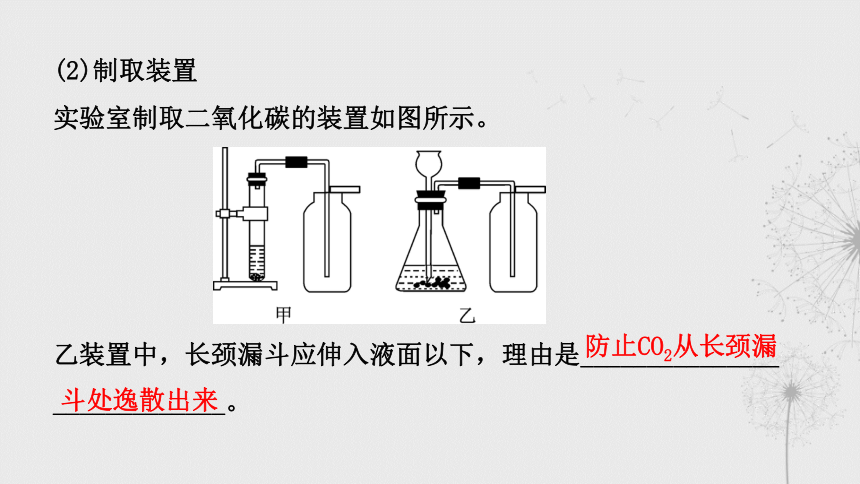
(2)制取装置
实验室制取二氧化碳的装置如图所示。
乙装置中,长颈漏斗应伸入液面以下,理由是_______________
_____________。
防止CO2从长颈漏
斗处逸散出来
(3)收集及验满
用 ___________法收集;将燃烧的木条放在 _________,若木
条_______,证明CO2已收集满;收集满后盖上玻璃片,_____放
在桌面上。
2.二氧化碳的工业制法
高温煅烧石灰石,反应的化学方程式为:___________________。
====
高温
向上排空气
集气瓶口
熄灭
正
CaCO3 CaO+CO2↑
空气中污染物的主要来源及防治空气污染的方法
1.空气污染物
(1)固体:可吸入颗粒物,如_______。
(2)气体:如 _______________________________。
【注意】二氧化碳不是大气污染物,属于大气的正常成分。
PM2.5
二氧化硫、氮氧化物、一氧化碳等
2.全球性大气环境问题有酸雨、温室效应(加剧)、臭氧空洞。
原因 对策
温室效应 大量使用_________、植被被破坏 减少_________的使用、开发新能源、植树造林等
酸雨 二氧化硫、氮氧化物的排放 燃料_____、工业废气_____ 处理等
臭氧空洞 含_______物质的使用 禁止生产和使用含_______的物质
化石燃料
化石燃料
脱硫
净化
氯氟烃
氯氟烃
3.如何防治空气污染
(1)减少污染物的排放;
(2)合理规划工业区与非工业区;
(3)植树造林。
森林对大气的净化作用:吸收 _________等有毒气体;吸收大
量 ___________;分泌抑杀某些微生物的物质。
二氧化硫
烟尘与粉尘
4.CO2对环境的影响
(1)温室效应:大气中的CO2气体能像温室的玻璃或塑料薄膜那
样,使地面吸收的太阳光的热量不易散失,从而使_________。
适度的“温室效应”能保证地球上的气温恒定,适于动植物生
存。
(2)其他能产生温室效应的气体有:水蒸气(H2O)、臭氧(O3)、氧
化亚氮(N2O)、甲烷(CH4)、氢氟氯碳化物、全氟碳化物及六氟化
硫等。
全球变暖
(3)温室效应加剧的危害:导致两极的_________,使_________
___,淹没部分沿海城市,使土地沙漠化、农业减产等。
(4)缓解措施:①减少CO2的排放,如减少使用_______________
___等化石燃料,更多地利用_________、风能、地热能等清洁能
源;②增加CO2的消耗,如大力 _________,严禁乱砍滥伐等。
冰川融化
海平面上
升
煤、石油、天然
气
太阳能
植树造林
练习1:目前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡。如图是碳循环和碳中和策略的示意图。
(1)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏
的主要原因之一,对此可采取的碳中和策略②有_______________
___________。
节能减排,改善
能源结构等
(2)要实现我国政府提出的目标,除图中策略外,还可用化学方法
人工减排,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写
出用氢氧化钾捕获CO2的化学方程式 _____________________。
(3)2020年12月下旬,我国部分地区出现多年未遇的极寒天气,因
此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这
样的质疑,你是否认同?并说明理由。
参考答案:不认同。2020年12月我国部分地区出现的极端低温天气,在空间与时间上都属于个例,事实上温室气体的增加,导致全球极端天气频发;这种空间与时间上的极端天气作为个例不能否定全球气温整体上升这一事实。
2KOH+CO2===K2CO3+H2O
练习2:三位同学分别用相同质量分数的稀盐酸,测定某石灰石样
品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶
于水)。
(1)小敏的方法可用如下流程表示,测得的碳酸钙的质量分数为
____;在过滤操作中,需要用到的玻璃仪器有____(填字母)。
A.酒精灯、漏斗、玻璃棒
B.漏斗、玻璃棒、烧杯
C.酒精灯、试管、玻璃棒
79%
B
(2)小华取10克样品,用如图甲实验装置进行实验,反应结束
后,测得B装置质量增加了4.6克,根据上述数据,算得碳酸钙
的质量分数,发现与事实严重不符,造成这种情况的可能原因
是 ____________________________________。
B中碱石灰吸收了CO2带出的H2O或HCl气体
(3)小军用如图乙的实验装置进行实验,将20克稀盐酸加入到1.25克样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8克/升,求该石灰石样品中CaCO3的质量分数。
(4)求实验所用的稀盐酸溶质质量分数。
第31课时 空气、氧气、二氧化碳(二)
§分类一 二氧化碳
二氧化碳的主要物理性质
无色、无味、密度比空气___,所以可用___________法收集;
___溶于水,所以不能用_____法收集;固体CO2叫_____,易
_____,这个过程要 _____大量热,所以可用固体CO2作制冷剂。
大
向上排空气
能
排水
干冰
升华
吸收
二氧化碳的主要化学性质
1.CO2与水反应,反应的化学方程式为:_______________。碳酸
不稳定,易分解,反应的化学方程式为:_________________。
2.CO2与石灰水反应,能使澄清石灰水变_______,该反应常用于
检验CO2。化学方程式为: __________________________。
CO2+H2O===H2CO3
H2CO3===CO2↑+H2O
浑浊
CO2+Ca(OH)2===CaCO3↓+H2O
3.CO2与NaOH反应,一般用 _________吸收CO2,化学方程式为:
_______________________。
4.CO2参与光合作用,维持空气中CO2和O2平衡,化学方程式为:
______________________________。
光
叶绿体
NaOH溶液
CO2+2NaOH===Na2CO3+H2O
6CO2+6H2O C6H12O6+6O2
二氧化碳的用途及与其性质的关系
在横线上写出图中这些用途分别利用了二氧化碳的哪些性质?
(1) ___________________________;
(2) _____________;
(3) _____________________;
(4) _________________________
_________________________。
二氧化碳参与植物的光合作用
干冰升华吸热
二氧化碳不能供给呼吸
二氧化碳的密度比空气大,
既不能支持燃烧,也不燃烧
二氧化碳的实验室制备及检验方法
1.二氧化碳的实验室制法
(1)反应原理
_________________________________。
CaCO3+2HCl===CaCl2+H2O+CO2↑
(2)制取装置
实验室制取二氧化碳的装置如图所示。
乙装置中,长颈漏斗应伸入液面以下,理由是_______________
_____________。
防止CO2从长颈漏
斗处逸散出来
(3)收集及验满
用 ___________法收集;将燃烧的木条放在 _________,若木
条_______,证明CO2已收集满;收集满后盖上玻璃片,_____放
在桌面上。
2.二氧化碳的工业制法
高温煅烧石灰石,反应的化学方程式为:___________________。
====
高温
向上排空气
集气瓶口
熄灭
正
CaCO3 CaO+CO2↑
空气中污染物的主要来源及防治空气污染的方法
1.空气污染物
(1)固体:可吸入颗粒物,如_______。
(2)气体:如 _______________________________。
【注意】二氧化碳不是大气污染物,属于大气的正常成分。
PM2.5
二氧化硫、氮氧化物、一氧化碳等
2.全球性大气环境问题有酸雨、温室效应(加剧)、臭氧空洞。
原因 对策
温室效应 大量使用_________、植被被破坏 减少_________的使用、开发新能源、植树造林等
酸雨 二氧化硫、氮氧化物的排放 燃料_____、工业废气_____ 处理等
臭氧空洞 含_______物质的使用 禁止生产和使用含_______的物质
化石燃料
化石燃料
脱硫
净化
氯氟烃
氯氟烃
3.如何防治空气污染
(1)减少污染物的排放;
(2)合理规划工业区与非工业区;
(3)植树造林。
森林对大气的净化作用:吸收 _________等有毒气体;吸收大
量 ___________;分泌抑杀某些微生物的物质。
二氧化硫
烟尘与粉尘
4.CO2对环境的影响
(1)温室效应:大气中的CO2气体能像温室的玻璃或塑料薄膜那
样,使地面吸收的太阳光的热量不易散失,从而使_________。
适度的“温室效应”能保证地球上的气温恒定,适于动植物生
存。
(2)其他能产生温室效应的气体有:水蒸气(H2O)、臭氧(O3)、氧
化亚氮(N2O)、甲烷(CH4)、氢氟氯碳化物、全氟碳化物及六氟化
硫等。
全球变暖
(3)温室效应加剧的危害:导致两极的_________,使_________
___,淹没部分沿海城市,使土地沙漠化、农业减产等。
(4)缓解措施:①减少CO2的排放,如减少使用_______________
___等化石燃料,更多地利用_________、风能、地热能等清洁能
源;②增加CO2的消耗,如大力 _________,严禁乱砍滥伐等。
冰川融化
海平面上
升
煤、石油、天然
气
太阳能
植树造林
练习1:目前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡。如图是碳循环和碳中和策略的示意图。
(1)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏
的主要原因之一,对此可采取的碳中和策略②有_______________
___________。
节能减排,改善
能源结构等
(2)要实现我国政府提出的目标,除图中策略外,还可用化学方法
人工减排,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写
出用氢氧化钾捕获CO2的化学方程式 _____________________。
(3)2020年12月下旬,我国部分地区出现多年未遇的极寒天气,因
此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这
样的质疑,你是否认同?并说明理由。
参考答案:不认同。2020年12月我国部分地区出现的极端低温天气,在空间与时间上都属于个例,事实上温室气体的增加,导致全球极端天气频发;这种空间与时间上的极端天气作为个例不能否定全球气温整体上升这一事实。
2KOH+CO2===K2CO3+H2O
练习2:三位同学分别用相同质量分数的稀盐酸,测定某石灰石样
品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶
于水)。
(1)小敏的方法可用如下流程表示,测得的碳酸钙的质量分数为
____;在过滤操作中,需要用到的玻璃仪器有____(填字母)。
A.酒精灯、漏斗、玻璃棒
B.漏斗、玻璃棒、烧杯
C.酒精灯、试管、玻璃棒
79%
B
(2)小华取10克样品,用如图甲实验装置进行实验,反应结束
后,测得B装置质量增加了4.6克,根据上述数据,算得碳酸钙
的质量分数,发现与事实严重不符,造成这种情况的可能原因
是 ____________________________________。
B中碱石灰吸收了CO2带出的H2O或HCl气体
(3)小军用如图乙的实验装置进行实验,将20克稀盐酸加入到1.25克样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8克/升,求该石灰石样品中CaCO3的质量分数。
(4)求实验所用的稀盐酸溶质质量分数。
同课章节目录
