吉林省油田第11高级中学2021-2022学年高二上学期期中考试化学试题(Word版含答案)
文档属性
| 名称 | 吉林省油田第11高级中学2021-2022学年高二上学期期中考试化学试题(Word版含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 620.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-30 00:00:00 | ||
图片预览



文档简介
油田第11高级中学2021-2022学年高二上学期期中考试
化学试卷
一、单项选择题(本部分共30题,每小题2分,共60分。)
1.适度饮水有益于健康,但过量饮水使体内电解质浓度过低,导致生理紊乱而引起“水中毒”,下列属于人体内常见电解质的是( )
A.二氧化碳 B.氯化钠 C.硫酸钡 D.葡萄糖
2.要使工业废水中的重金属离子Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,已知Pb2+与这些离子形成的化合物的溶解度如下:
化合物 PbSO4 PbCO3 PbS
溶解度/g 1.03×10 4 1.81×10 7 1.84×10 14
由上述数据可知,选用的沉淀剂最好为 ( )
A.硫酸盐 B. 碳酸盐 C.硫化物 D.以上沉淀剂均可
3.下列水解的离子方程式正确的是( )
A.Br-+H2OHBr+OH- B.NH+H2ONH3·H2O+H+
C.CO+2H2OH2CO3+2OH- D.Fe3++3H2OFe(OH)3↓+3H+
4.在醋酸溶液中存在电离平衡:CH3COOHCH3COO-+H+,要使电离平衡左移且c(H+)减小,应采取的措施是( )
A.加入NaOH(s) B.加入盐酸 C.加蒸馏水 D.降低温度
5. 50 ℃时水的离子积Kw=5.5×10-14,则在此温度下,c(H+)=1×10-7mol·L-1的溶液
A.呈酸性 B.呈碱性 C.呈中性 D.无法判断
6.对于碳酸溶液中的电离平衡,下列电离常数的表达式正确的是( )
A. B.
C. D.
7.常温下,0.01mol/L HCl溶液的pH为( )
A.1 B.12 C.2 D.13
8.下列措施抑制水的电离的是( )
A.加热 B.加入NaOH溶液 C.加入CuSO4固体 D.加入Na2CO3固体
9.下列关于溶液的酸碱性,说法正确的是( )
A.pH=7的溶液呈中性 B.中性溶液中一定有:c(H+)=1.0×10-7mol·L-1
C.c(H+)=c(OH-)的溶液呈中性 D.在100°C时,纯水的pH<7,因此显酸性
10.酸碱中和滴定中常用如图所给仪器,其中为酸式滴定管的是
A. B. C. D.
11.下列物质的水溶液因水解而呈碱性的是
A.Na2CO3 B.AlCl3 C.Ca(OH)2 D.NaNO3
12.常温下,将PH=4的盐酸溶液加水稀释1000倍后,溶液的PH是( )
A.8 B.7 C.接近于7但小于7 D.大于7而小于8
13.下列表述中,与盐类水解无关的是( )
A.明矾和FeCl3可作净水剂 B.盛放NaOH溶液的试剂瓶不能用玻璃塞
C.热的纯碱溶液去污能力增强 D.NH4Cl与ZnCl2溶液可作焊接中的除锈剂
14.室温下,将碳酸钠溶液加热至70℃,其结果是 ( )
A.溶液中c(CO)增大 B.水的电离程度不变
C.KW(水的离子积)将变小 D.溶液的碱性增强
15.相同物质的量浓度的下列铵盐中,c(NH)最大的是( )
A. NH4HCO3 B. NH4HSO4 C.NH4NO3 D.CH3COONH4
16.下列溶液:①CH3COOH ②HCl ③NaOH ④CH3COONa ⑤KCl ⑥NH4Cl其物质的量浓度均为0.1mol/L,其pH由大到小排列顺序为( )
A.③④⑤⑥①② B.④⑤⑥①③②
C.②①⑥⑤④③ D.②③①⑥⑤④
17.常温下在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
A.滴加石蕊试液显红色的溶液:Fe3+、NH、Cl-、I-
B.pH值为1的溶液:Fe2+、Na+、Mg2+、NO
C.水电离出来的c(H+)=10-13 mol/L的溶液:K+、HCO、Br-、Ba2+
D.能与Al反应产生H2的溶液:K+、Na+、Cl-、NO
18.下表是常温下某些一元弱酸的电离常数:
弱酸 HCN HF CH3COOH HNO2
电离常数 6.2×10-10 6.8×10-4 1.8×10-5 6.4×10-6
则0.1 mol/L的下列溶液中,c(H+)最大的是( )
A.HCN B.HF C.CH3COOH D.HNO2
19.向三份0.1mol/LCH3COONa溶液中分别加入少量硫酸铵、碳酸钠、硫酸铝固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
A.减小、增大、增大 B.增大、减小、减小
C.减小、增大、减小 D.增大、增大、减小
20.关于溶液的叙述正确的是( )
A.加入盐酸,抑制水解 B.升温,抑制水解
C.浓度越大,水解程度越大 D.将溶液蒸干可得固体
21.采取下列措施后,溶液颜色变深的是( )
A.加热明矾溶液(滴有酚酞试液) B.加热溶液(滴有酚酞试液)
C.氨水(滴有酚酞试液)中加入少量固体 D.小苏打溶液(滴有酚酞试液)中加入少量固体
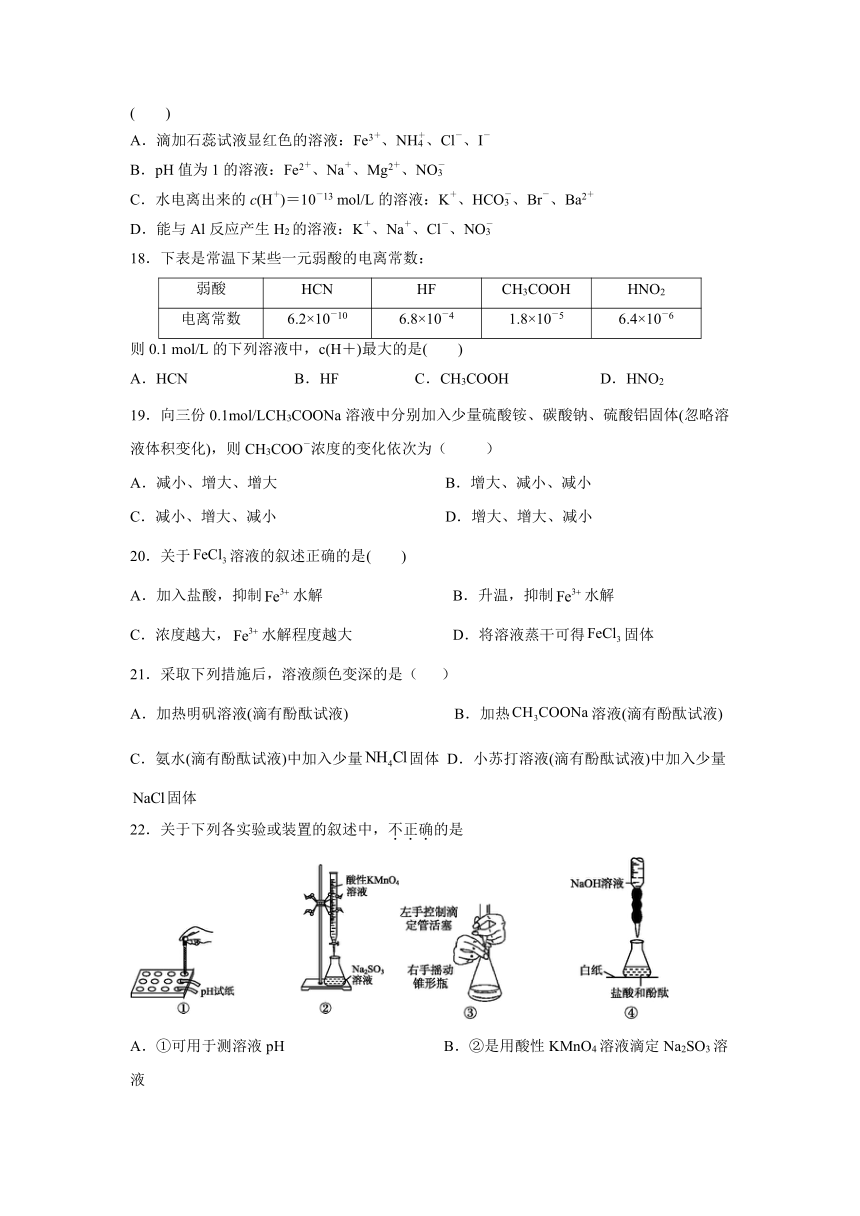
22.关于下列各实验或装置的叙述中,不正确的是
A.①可用于测溶液pH B.②是用酸性KMnO4溶液滴定Na2SO3溶液
C.③是滴定操作时手的操作
D.④中滴入一滴NaOH标准液使溶液由无色变为红色,即达到滴定终点
23.某温度时测得纯水中的,则为( )
A. B.
C. D.无法确定
24. 下列四种肥料可以与草木灰(主要成分是K2CO3)混合施用的是 ( )
A. 硫酸铵 B.氯化铵 C.硝酸钾 D.硝酸铵
25.常温下,PH均为5的NH4Cl溶液和盐酸中,由水电离出的H+浓度( )
A.一样大 B.前者大 C.后者大 D.无法判断
26.一定温度下,氯化银在水中的沉淀溶解平衡曲线如图,下列说法不正确的是( )
A.向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp不变
B.向c点的溶液中加入0.1molAgNO3,则c(Cl-)减小
C.图中a点对应的是不饱和溶液
D.升高温度可以实现c点到b点的转化
27.在25℃时,用0.125 mol·L-1的标准盐酸溶液滴定25.00 mL未知浓度的NaOH溶液所得滴定曲线如图所示,图中K点代表的pH为( )
A.13
B.12
C.10
D.11
28.常温下 ,向氨水中加水稀释的过程中,NH3 H2O的电离平衡常数、电离度、溶液导电性的变化正确的是( )
A.增大、增大、减小 B.不变、增大、减小
C.不变、减小、减小 D.减小、减小、增大
29.在室温下,等体积的酸和碱的溶液混合后,pH一定少于7的是( )
A.pH=3的HNO3跟pH=11的KOH溶液 B.pH=3的盐酸跟pH=11的氨水
C.pH=3硫酸跟pH=11的氢氧化钠溶液 D.pH=3的醋酸跟pH=11的氢氧化钡溶液
30.五育并举,劳动先行。下列劳动项目与所述化学知识相符的是( )
选项 劳动项目 化学知识
A 社区服务:宣传推广使用免洗手酒精消毒液 酒精具有氧化性
B 家务劳动:使用热的纯碱溶液去除餐具油污 Na2CO3能直接与油脂反应
C 农业劳动:用植物秸秆生产酒精 秸秆中含有乙醇
D 职业劳动:用明矾溶液擦拭铜镜去除铜锈 明矾中的Al3+水解产生H+,与铜锈发生反应
A.A B.B C.C D.
2、非选择题(本部分共4题,共40分)
31.某温度下纯水的,按要求回答下列问题(8分):
(1)的溶液呈_______(填“酸性”“中性”或“碱性”)。
(2)该温度下某溶液中由水电离出的C(OH-)=10-9mol/L的_______。
(3)pH=3的H2SO4溶液与pH=6的HCl溶液的等体积混合,溶液的pH=_ 。
(4)将pH=2的盐酸和pH=11的氢氧化钠溶液,以体积比1∶9混合后,溶液的pH= 。
32.在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题(6分):
(1)“O”点导电能力为0,原因是______________________________________________________。
(2)a、b、c三点处,溶液中c(H+)由小到大的顺序为____________________。
(3)a、b、c三点处,电离程度最大的是________。
33.用盐类水解的相关知识回答下列问题(14分):
(1)Cu(NO3)2的水溶液呈______(填“酸”、“中”、“碱”)性,常温时的pH _____7(填“>”、“=”、“<”), 原因是(用离子方程式表示):_______________________________。
(2)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是________,把Al2(SO4)3溶液蒸干得到的固体产物是___________ 。
(3)在NaHCO3溶液中存在的电荷守恒式为 。
物料守恒式为 。
(4)泡沫灭火器的原理(药品:Al2(SO4)3溶液、NaHCO3溶液)原理为 。(用离子方程式解释)
34.酸碱中和滴定是一种重要的实验方法,用溶液滴定未知浓度的盐酸,其操作可分为如下几步:
A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.用待测的溶液润洗酸式滴定管
D.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
E.取下碱式滴定管用NaOH标准溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0”刻度以下
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作2~3次
完成以下填空(12分):
(1)排除碱式滴定管中气泡的方法应采用如图所示操作中的___________(填“甲”“乙”或“丙”),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
(2)判断滴定终点的现象:锥形瓶中溶液从___________色变为___________色,且半分钟内不变色。
(3)如图是第一次滴定时的滴定管中的液面,其读数为X=___________mL。
(4)根据下列数据,请计算待测盐酸的浓度:___________mol/L。
滴定次数 待测液体积(mL) 标准液体积(mL)
滴定前读数 滴定后读数
第一次 20.00 0.60 X
第二次 20.00 2.00 24.10
第三次' 20.00 4.00 24.00
(5)在上述实验过程中,出现了以下操作(其他操作正确),其中会造成测定结果(待测液浓度值)偏高的有___________(填序号,下同)。
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前碱式滴定管尖嘴部分有气泡,滴定后气泡消失
(6)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处,现把管内液体全部放出,用量筒接收,得到溶液的体积是___________。
A.不能确定 B.为40mL
C.为10mL D.大于40mL
化学试卷参考答案
一、选择题答案:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
B C B D B C C B C B A C B D B
16 17 18 19 20 21 22 23 24 25 26 27 28 29 30
A D B C A B D A C B D A B D D
2、非选择题答案:
31.(1)中性 (2)5或9 (3)3.3 (4)4
32.(1)在O点处冰醋酸未电离,以分子形式存在,无自由移动的离子存在
(2) c(3) c
33.(1)酸 (1分) <(1分) Cu2++H2OCu(OH)2+2H+
(2)Al2O3(或三氧化二铝) Al2(SO4)3(或硫酸铝)
(3) c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
c(Na+) =c(HCO3-)+c(H2CO3)+c(CO32-)
(4) 3HCO3-+Al3+=Al(OH)3↓+3CO2↑
34.(1)丙
(2) 无 粉红(浅红)
(3)20.60
(4)0.1000
(5)AE
(6)D
化学试卷
一、单项选择题(本部分共30题,每小题2分,共60分。)
1.适度饮水有益于健康,但过量饮水使体内电解质浓度过低,导致生理紊乱而引起“水中毒”,下列属于人体内常见电解质的是( )
A.二氧化碳 B.氯化钠 C.硫酸钡 D.葡萄糖
2.要使工业废水中的重金属离子Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,已知Pb2+与这些离子形成的化合物的溶解度如下:
化合物 PbSO4 PbCO3 PbS
溶解度/g 1.03×10 4 1.81×10 7 1.84×10 14
由上述数据可知,选用的沉淀剂最好为 ( )
A.硫酸盐 B. 碳酸盐 C.硫化物 D.以上沉淀剂均可
3.下列水解的离子方程式正确的是( )
A.Br-+H2OHBr+OH- B.NH+H2ONH3·H2O+H+
C.CO+2H2OH2CO3+2OH- D.Fe3++3H2OFe(OH)3↓+3H+
4.在醋酸溶液中存在电离平衡:CH3COOHCH3COO-+H+,要使电离平衡左移且c(H+)减小,应采取的措施是( )
A.加入NaOH(s) B.加入盐酸 C.加蒸馏水 D.降低温度
5. 50 ℃时水的离子积Kw=5.5×10-14,则在此温度下,c(H+)=1×10-7mol·L-1的溶液
A.呈酸性 B.呈碱性 C.呈中性 D.无法判断
6.对于碳酸溶液中的电离平衡,下列电离常数的表达式正确的是( )
A. B.
C. D.
7.常温下,0.01mol/L HCl溶液的pH为( )
A.1 B.12 C.2 D.13
8.下列措施抑制水的电离的是( )
A.加热 B.加入NaOH溶液 C.加入CuSO4固体 D.加入Na2CO3固体
9.下列关于溶液的酸碱性,说法正确的是( )
A.pH=7的溶液呈中性 B.中性溶液中一定有:c(H+)=1.0×10-7mol·L-1
C.c(H+)=c(OH-)的溶液呈中性 D.在100°C时,纯水的pH<7,因此显酸性
10.酸碱中和滴定中常用如图所给仪器,其中为酸式滴定管的是
A. B. C. D.
11.下列物质的水溶液因水解而呈碱性的是
A.Na2CO3 B.AlCl3 C.Ca(OH)2 D.NaNO3
12.常温下,将PH=4的盐酸溶液加水稀释1000倍后,溶液的PH是( )
A.8 B.7 C.接近于7但小于7 D.大于7而小于8
13.下列表述中,与盐类水解无关的是( )
A.明矾和FeCl3可作净水剂 B.盛放NaOH溶液的试剂瓶不能用玻璃塞
C.热的纯碱溶液去污能力增强 D.NH4Cl与ZnCl2溶液可作焊接中的除锈剂
14.室温下,将碳酸钠溶液加热至70℃,其结果是 ( )
A.溶液中c(CO)增大 B.水的电离程度不变
C.KW(水的离子积)将变小 D.溶液的碱性增强
15.相同物质的量浓度的下列铵盐中,c(NH)最大的是( )
A. NH4HCO3 B. NH4HSO4 C.NH4NO3 D.CH3COONH4
16.下列溶液:①CH3COOH ②HCl ③NaOH ④CH3COONa ⑤KCl ⑥NH4Cl其物质的量浓度均为0.1mol/L,其pH由大到小排列顺序为( )
A.③④⑤⑥①② B.④⑤⑥①③②
C.②①⑥⑤④③ D.②③①⑥⑤④
17.常温下在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
A.滴加石蕊试液显红色的溶液:Fe3+、NH、Cl-、I-
B.pH值为1的溶液:Fe2+、Na+、Mg2+、NO
C.水电离出来的c(H+)=10-13 mol/L的溶液:K+、HCO、Br-、Ba2+
D.能与Al反应产生H2的溶液:K+、Na+、Cl-、NO
18.下表是常温下某些一元弱酸的电离常数:
弱酸 HCN HF CH3COOH HNO2
电离常数 6.2×10-10 6.8×10-4 1.8×10-5 6.4×10-6
则0.1 mol/L的下列溶液中,c(H+)最大的是( )
A.HCN B.HF C.CH3COOH D.HNO2
19.向三份0.1mol/LCH3COONa溶液中分别加入少量硫酸铵、碳酸钠、硫酸铝固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
A.减小、增大、增大 B.增大、减小、减小
C.减小、增大、减小 D.增大、增大、减小
20.关于溶液的叙述正确的是( )
A.加入盐酸,抑制水解 B.升温,抑制水解
C.浓度越大,水解程度越大 D.将溶液蒸干可得固体
21.采取下列措施后,溶液颜色变深的是( )
A.加热明矾溶液(滴有酚酞试液) B.加热溶液(滴有酚酞试液)
C.氨水(滴有酚酞试液)中加入少量固体 D.小苏打溶液(滴有酚酞试液)中加入少量固体
22.关于下列各实验或装置的叙述中,不正确的是
A.①可用于测溶液pH B.②是用酸性KMnO4溶液滴定Na2SO3溶液
C.③是滴定操作时手的操作
D.④中滴入一滴NaOH标准液使溶液由无色变为红色,即达到滴定终点
23.某温度时测得纯水中的,则为( )
A. B.
C. D.无法确定
24. 下列四种肥料可以与草木灰(主要成分是K2CO3)混合施用的是 ( )
A. 硫酸铵 B.氯化铵 C.硝酸钾 D.硝酸铵
25.常温下,PH均为5的NH4Cl溶液和盐酸中,由水电离出的H+浓度( )
A.一样大 B.前者大 C.后者大 D.无法判断
26.一定温度下,氯化银在水中的沉淀溶解平衡曲线如图,下列说法不正确的是( )
A.向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp不变
B.向c点的溶液中加入0.1molAgNO3,则c(Cl-)减小
C.图中a点对应的是不饱和溶液
D.升高温度可以实现c点到b点的转化
27.在25℃时,用0.125 mol·L-1的标准盐酸溶液滴定25.00 mL未知浓度的NaOH溶液所得滴定曲线如图所示,图中K点代表的pH为( )
A.13
B.12
C.10
D.11
28.常温下 ,向氨水中加水稀释的过程中,NH3 H2O的电离平衡常数、电离度、溶液导电性的变化正确的是( )
A.增大、增大、减小 B.不变、增大、减小
C.不变、减小、减小 D.减小、减小、增大
29.在室温下,等体积的酸和碱的溶液混合后,pH一定少于7的是( )
A.pH=3的HNO3跟pH=11的KOH溶液 B.pH=3的盐酸跟pH=11的氨水
C.pH=3硫酸跟pH=11的氢氧化钠溶液 D.pH=3的醋酸跟pH=11的氢氧化钡溶液
30.五育并举,劳动先行。下列劳动项目与所述化学知识相符的是( )
选项 劳动项目 化学知识
A 社区服务:宣传推广使用免洗手酒精消毒液 酒精具有氧化性
B 家务劳动:使用热的纯碱溶液去除餐具油污 Na2CO3能直接与油脂反应
C 农业劳动:用植物秸秆生产酒精 秸秆中含有乙醇
D 职业劳动:用明矾溶液擦拭铜镜去除铜锈 明矾中的Al3+水解产生H+,与铜锈发生反应
A.A B.B C.C D.
2、非选择题(本部分共4题,共40分)
31.某温度下纯水的,按要求回答下列问题(8分):
(1)的溶液呈_______(填“酸性”“中性”或“碱性”)。
(2)该温度下某溶液中由水电离出的C(OH-)=10-9mol/L的_______。
(3)pH=3的H2SO4溶液与pH=6的HCl溶液的等体积混合,溶液的pH=_ 。
(4)将pH=2的盐酸和pH=11的氢氧化钠溶液,以体积比1∶9混合后,溶液的pH= 。
32.在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题(6分):
(1)“O”点导电能力为0,原因是______________________________________________________。
(2)a、b、c三点处,溶液中c(H+)由小到大的顺序为____________________。
(3)a、b、c三点处,电离程度最大的是________。
33.用盐类水解的相关知识回答下列问题(14分):
(1)Cu(NO3)2的水溶液呈______(填“酸”、“中”、“碱”)性,常温时的pH _____7(填“>”、“=”、“<”), 原因是(用离子方程式表示):_______________________________。
(2)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是________,把Al2(SO4)3溶液蒸干得到的固体产物是___________ 。
(3)在NaHCO3溶液中存在的电荷守恒式为 。
物料守恒式为 。
(4)泡沫灭火器的原理(药品:Al2(SO4)3溶液、NaHCO3溶液)原理为 。(用离子方程式解释)
34.酸碱中和滴定是一种重要的实验方法,用溶液滴定未知浓度的盐酸,其操作可分为如下几步:
A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.用待测的溶液润洗酸式滴定管
D.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
E.取下碱式滴定管用NaOH标准溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0”刻度以下
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作2~3次
完成以下填空(12分):
(1)排除碱式滴定管中气泡的方法应采用如图所示操作中的___________(填“甲”“乙”或“丙”),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
(2)判断滴定终点的现象:锥形瓶中溶液从___________色变为___________色,且半分钟内不变色。
(3)如图是第一次滴定时的滴定管中的液面,其读数为X=___________mL。
(4)根据下列数据,请计算待测盐酸的浓度:___________mol/L。
滴定次数 待测液体积(mL) 标准液体积(mL)
滴定前读数 滴定后读数
第一次 20.00 0.60 X
第二次 20.00 2.00 24.10
第三次' 20.00 4.00 24.00
(5)在上述实验过程中,出现了以下操作(其他操作正确),其中会造成测定结果(待测液浓度值)偏高的有___________(填序号,下同)。
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前碱式滴定管尖嘴部分有气泡,滴定后气泡消失
(6)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处,现把管内液体全部放出,用量筒接收,得到溶液的体积是___________。
A.不能确定 B.为40mL
C.为10mL D.大于40mL
化学试卷参考答案
一、选择题答案:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
B C B D B C C B C B A C B D B
16 17 18 19 20 21 22 23 24 25 26 27 28 29 30
A D B C A B D A C B D A B D D
2、非选择题答案:
31.(1)中性 (2)5或9 (3)3.3 (4)4
32.(1)在O点处冰醋酸未电离,以分子形式存在,无自由移动的离子存在
(2) c
33.(1)酸 (1分) <(1分) Cu2++H2OCu(OH)2+2H+
(2)Al2O3(或三氧化二铝) Al2(SO4)3(或硫酸铝)
(3) c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
c(Na+) =c(HCO3-)+c(H2CO3)+c(CO32-)
(4) 3HCO3-+Al3+=Al(OH)3↓+3CO2↑
34.(1)丙
(2) 无 粉红(浅红)
(3)20.60
(4)0.1000
(5)AE
(6)D
同课章节目录
