第二单元课题2氧气教学课件-2021-2022学年九年级化学人教版上册(32张PPT)
文档属性
| 名称 | 第二单元课题2氧气教学课件-2021-2022学年九年级化学人教版上册(32张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 926.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-30 00:00:00 | ||
图片预览











文档简介
(共32张PPT)
第二单元 我们周围的空气
课题2 氧 气
学习目标
1.记住氧气的主要物理性质。
2.掌握氧气的检验方法
3. 会描述木炭、硫、铁,在氧气中燃烧的现象,从中归纳出氧气的化学性质。
4.说出化合反应、氧化反应、缓慢氧化的基本含义,并能判断常见生活现象是否属于缓慢氧化。能够写出这些反应的文字表达式
5.比较分析化合反应、氧化反应,认清化合反应、氧化反应的本质特点。会判断化学反应
一物无色又无味,
加压降温变液体;
它在水中微溶解,
足够鱼儿来呼吸;
它有一副热心肠,
支持燃烧创奇迹;
生来活泼又好动,
氧化反应有魅力。
它与木炭能化合,
生成二氧化碳气;
铁丝遇它来点燃,
火星四射多美丽;
硫在其中能燃烧,
蓝紫火焰好神气;
它的用途多又广,
气焊气割堪称奇;
液体炸药威力大,
劈山采矿开沟渠;
运载火箭需要它,
推动飞船快如飞;
它是人类好朋友,
造福人类建功绩。
【新课引入】猜一猜:它是谁?
【思考】观察一瓶氧气,并阅读课本第33页第一段内容,说说氧气有哪些物理性质?
一、氧气的性质
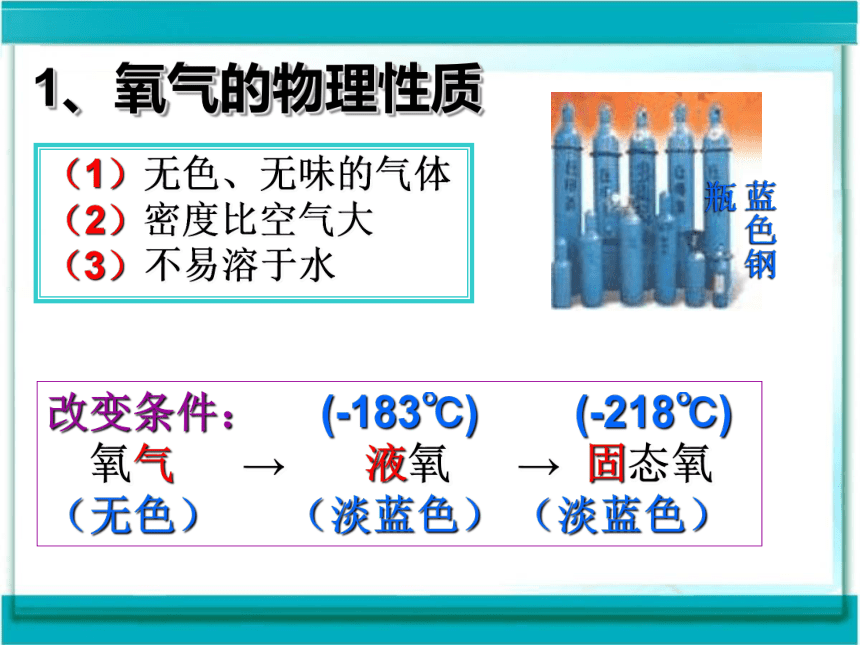
(1)无色、无味的气体
(2)密度比空气大
(3)不易溶于水
1、氧气的物理性质
改变条件: (-183℃) (-218℃)
氧气 → 液氧 → 固态氧
(无色) (淡蓝色) (淡蓝色)
蓝色钢瓶
⑴支持燃烧:氧气可使带火星的木条复燃。
注意:
带火星的木条在空气中不能复燃,而在氧气中能复燃。
2. 氧气的化学性质
怎样检验氧气一瓶气体是氧气?
互助探究
演示实验:硫磺燃烧
要求:
① 请同学们观察硫在空气中和在氧气中燃烧的现象
有什么不同?
② 根据现象正确书写反应的文字表达式。
③ 观察时要按反应前、反应中、反应后的顺序进行。
用心观察
【现象】 ①产生微弱的淡蓝色火焰;②放热;③生成有刺激性气味的气体。
【现象】 ①产生明亮的蓝紫色火焰;②放热;③生成有刺激性气味的气体。
硫 + 氧气 二氧化硫
点燃
文字表达式:
比较:硫在氧气中燃烧比在空气中燃烧剧烈。
⑵硫与氧气反应
硫在空气中燃烧:
硫在氧气中燃烧:
——溶解吸收生成的二氧化硫,
防止二氧化硫逸出污染环境。
硫在氧气里燃烧,为什么集气瓶底要留少量水?
硫 + 氧气 → 二氧化硫
点燃
烟花、爆竹中的火药是由木炭、硫磺等物质组成的,为什么很多城市禁止燃放烟花爆竹?
防止硫燃烧后生成的二氧化硫污染空气
木炭燃烧实验现象:
在空气中:木炭红热
在氧气中:木炭燃烧得更旺,发出白光,
放出热量,燃烧后生成的气体
能使澄清石灰水变浑浊。
课本P34讨论:
可燃物在氧气里燃烧比在空气里燃烧要剧烈。
为什么木炭、硫分别在空气里和氧气里 燃烧的现象不同 它说明了什么
——氧气的含量越高,燃烧越剧烈。
铁丝在空气中能燃烧吗?
演示实验:铁丝燃烧
要求:
① 请同学们观察铁丝在空气中和在氧气中燃烧的现象
有什么不同?
② 根据现象正确书写反应的文字表达式。
③ 观察时要按反应前、反应中、反应后的顺序进行。
用心观察
铁丝燃烧实验现象:
在氧气中:铁丝剧烈燃烧,火星四射,
放出大量热,生成黑色固体。
在空气中:铁丝不能燃烧,发生红热
现象。
【实验2-4】
操作注意事项:
①火柴的作用:
②将铁丝绕成螺旋状:
③待火柴即将燃尽时再将铁丝伸入氧气瓶中:
④预先在集气瓶中装少量水或在瓶底铺一薄层 细沙:
引燃铁丝
增大铁丝与氧气接触面积
防止火柴燃烧消耗过多氧气而使铁丝不能顺利燃烧
防止生成物物溅落炸裂集气瓶底
合作释疑
如果实验没有成功,可能原因是什么?
1、未用火柴引燃
2、铁丝未打磨(生锈或上面有油漆)
3、铁丝未达到一定温度
4、氧气含量太低或浓度太低
【讨论】 物质在空气中燃烧与在氧气中燃烧现象一样吗?这说明了什么?
物质在空气中燃烧主要是与空气中的氧气反应,反应的剧烈程度取决于氧气的含量,氧气含量越高,燃烧越剧烈。
实验编号 反应前的物质 反应后生成的物质 反应的文字表达式
实验2-1
实验2-3
实验2-4
磷+氧气 五氧化二磷
点燃
硫+氧气 二氧化硫
点燃
铁+氧气 四氧化三铁
点燃
【思考】上述几个变化中,有什么共同的特征?
红磷、
氧气
硫、
氧气
铁、
氧气
五氧化二磷
二氧化硫
四氧化三铁
上述反应的共同点
(1)反应物中都是两种物质参加反应。
(2)反应物中都有氧气参加反应。
(3)反应条件都是点燃。
(4)生成物都只有一种物质。
(5)都是固体和气体的反应。
(6)反应都放出热量。
化合反应与氧化反应
化合反应:由两种或两种以上的物 质生成一种物质的反应。
氧化反应:物质跟氧发生的反应。
氧化反应
燃烧:
发光、放热的剧烈的氧化反应
缓慢氧化:
进行得很缓慢,甚至不容易察觉的氧化反应。
如:动植物的呼吸、食物的腐烂、酒和醋的酿造、农家肥的腐熟、铁的生锈等
它们的共同点:都是氧化反应,都放热
总结提升
提示:
① 氧化反应中的“氧”不能说成“氧气”,以后还会学到没有氧气参加的氧化反应。
在有氧气参加的氧化反应中,氧气提供了氧,是氧化剂。
氧化反应不是反应的基本类型,和化合反应之间没有必然的联系。
判断下列反应是否为化合反应?是否氧化反应?
硫 + 氧气 二氧化硫
点燃
锌 + 盐酸 氯化锌+氢气
石蜡 + 氧气 二氧化碳+水
点燃
镁 + 氧气 氧化镁
点燃
讨论:在什么情况下,一个反应既是化合反应又是氧化反应?
氧气的化学性质
氧气是一种化学性质比较活泼的气体,可以支持燃烧(助燃性),可以跟很多物质发生反应。
它在氧化反应中提供氧,具有氧化性,是一种常用的氧化剂。
氧气含量越高,燃烧越剧烈。
【小结】
本节课你学到了哪些知识?
小组讨论交流,然后每组派代表发言.
盘点收获
知识回顾
课题2 氧气
1、氧气的物理性质(通常状况下)?
(1)无色、无味的气体 (液态和固态时变为淡蓝色)
(2)密度比空气大
(3)不易溶于水
2、氧气的化学性质
(1)带火星的木条在氧气中复燃(可检验氧气)
(2)硫+氧气 二氧化硫
(3)碳+氧气 二氧化碳
(4)铁+氧气 四氧化三铁
3、化合反应:由两种或两种以上的物质生成另一种物质的反应,叫做化 合反应
4、氧化反应:物质跟氧发生的化学反应叫做氧化反应
5、氧气是一种化学性质比较活泼的气体,具有氧化性,可以支持燃烧,可以跟很多物质发生反应。
1、对氧气物理性质的叙述正确的是( )
A、极易溶于水
B、在标准状况下,密度比空气略大
C、在-183℃时变成无色液体
D、在-218℃时变成白色固体
2、要除去密闭容器内空气的氧气,并不使混入其他气体,在其中燃烧的可燃物可以是( )
A、硫粉 B、木炭
C、铁丝 D、红磷
练习
B
D
1、对氧气物理性质的叙述正确的是( )
A、极易溶于水
B、在标准状况下,密度比空气略大
C、在-183℃时变成无色液体
D、在-218℃时变成白色固体
2、要除去密闭容器内空气的氧气,并不使混入其他气体,在其中燃烧的可燃物可以是( )
A、硫粉 B、木炭
C、铁丝 D、红磷
练习
B
D
4、下列反应属于化合反应的是( ),
属于氧化反应的是( )
A、酒精+氧气 水+二氧化碳
B、锌 + 盐酸 氯化锌+氢气
C、磷 + 氧气 五氧化二磷
D、碱式碳酸铜 水+氧化铜+二氧化碳
C
AC
5、判断下列说法正确的是( )
A、由两种物质生成一种物质的反应叫做化合反应
B、氧化反应是指物质跟氧气发生的化学反应
C、凡是在空气中不能燃烧的物质,在氧气中
也不能燃烧
D、蜡烛的燃烧过程既有物理变化,又有化学变化
D
本节课结束
同学们,再见!
第二单元 我们周围的空气
课题2 氧 气
学习目标
1.记住氧气的主要物理性质。
2.掌握氧气的检验方法
3. 会描述木炭、硫、铁,在氧气中燃烧的现象,从中归纳出氧气的化学性质。
4.说出化合反应、氧化反应、缓慢氧化的基本含义,并能判断常见生活现象是否属于缓慢氧化。能够写出这些反应的文字表达式
5.比较分析化合反应、氧化反应,认清化合反应、氧化反应的本质特点。会判断化学反应
一物无色又无味,
加压降温变液体;
它在水中微溶解,
足够鱼儿来呼吸;
它有一副热心肠,
支持燃烧创奇迹;
生来活泼又好动,
氧化反应有魅力。
它与木炭能化合,
生成二氧化碳气;
铁丝遇它来点燃,
火星四射多美丽;
硫在其中能燃烧,
蓝紫火焰好神气;
它的用途多又广,
气焊气割堪称奇;
液体炸药威力大,
劈山采矿开沟渠;
运载火箭需要它,
推动飞船快如飞;
它是人类好朋友,
造福人类建功绩。
【新课引入】猜一猜:它是谁?
【思考】观察一瓶氧气,并阅读课本第33页第一段内容,说说氧气有哪些物理性质?
一、氧气的性质
(1)无色、无味的气体
(2)密度比空气大
(3)不易溶于水
1、氧气的物理性质
改变条件: (-183℃) (-218℃)
氧气 → 液氧 → 固态氧
(无色) (淡蓝色) (淡蓝色)
蓝色钢瓶
⑴支持燃烧:氧气可使带火星的木条复燃。
注意:
带火星的木条在空气中不能复燃,而在氧气中能复燃。
2. 氧气的化学性质
怎样检验氧气一瓶气体是氧气?
互助探究
演示实验:硫磺燃烧
要求:
① 请同学们观察硫在空气中和在氧气中燃烧的现象
有什么不同?
② 根据现象正确书写反应的文字表达式。
③ 观察时要按反应前、反应中、反应后的顺序进行。
用心观察
【现象】 ①产生微弱的淡蓝色火焰;②放热;③生成有刺激性气味的气体。
【现象】 ①产生明亮的蓝紫色火焰;②放热;③生成有刺激性气味的气体。
硫 + 氧气 二氧化硫
点燃
文字表达式:
比较:硫在氧气中燃烧比在空气中燃烧剧烈。
⑵硫与氧气反应
硫在空气中燃烧:
硫在氧气中燃烧:
——溶解吸收生成的二氧化硫,
防止二氧化硫逸出污染环境。
硫在氧气里燃烧,为什么集气瓶底要留少量水?
硫 + 氧气 → 二氧化硫
点燃
烟花、爆竹中的火药是由木炭、硫磺等物质组成的,为什么很多城市禁止燃放烟花爆竹?
防止硫燃烧后生成的二氧化硫污染空气
木炭燃烧实验现象:
在空气中:木炭红热
在氧气中:木炭燃烧得更旺,发出白光,
放出热量,燃烧后生成的气体
能使澄清石灰水变浑浊。
课本P34讨论:
可燃物在氧气里燃烧比在空气里燃烧要剧烈。
为什么木炭、硫分别在空气里和氧气里 燃烧的现象不同 它说明了什么
——氧气的含量越高,燃烧越剧烈。
铁丝在空气中能燃烧吗?
演示实验:铁丝燃烧
要求:
① 请同学们观察铁丝在空气中和在氧气中燃烧的现象
有什么不同?
② 根据现象正确书写反应的文字表达式。
③ 观察时要按反应前、反应中、反应后的顺序进行。
用心观察
铁丝燃烧实验现象:
在氧气中:铁丝剧烈燃烧,火星四射,
放出大量热,生成黑色固体。
在空气中:铁丝不能燃烧,发生红热
现象。
【实验2-4】
操作注意事项:
①火柴的作用:
②将铁丝绕成螺旋状:
③待火柴即将燃尽时再将铁丝伸入氧气瓶中:
④预先在集气瓶中装少量水或在瓶底铺一薄层 细沙:
引燃铁丝
增大铁丝与氧气接触面积
防止火柴燃烧消耗过多氧气而使铁丝不能顺利燃烧
防止生成物物溅落炸裂集气瓶底
合作释疑
如果实验没有成功,可能原因是什么?
1、未用火柴引燃
2、铁丝未打磨(生锈或上面有油漆)
3、铁丝未达到一定温度
4、氧气含量太低或浓度太低
【讨论】 物质在空气中燃烧与在氧气中燃烧现象一样吗?这说明了什么?
物质在空气中燃烧主要是与空气中的氧气反应,反应的剧烈程度取决于氧气的含量,氧气含量越高,燃烧越剧烈。
实验编号 反应前的物质 反应后生成的物质 反应的文字表达式
实验2-1
实验2-3
实验2-4
磷+氧气 五氧化二磷
点燃
硫+氧气 二氧化硫
点燃
铁+氧气 四氧化三铁
点燃
【思考】上述几个变化中,有什么共同的特征?
红磷、
氧气
硫、
氧气
铁、
氧气
五氧化二磷
二氧化硫
四氧化三铁
上述反应的共同点
(1)反应物中都是两种物质参加反应。
(2)反应物中都有氧气参加反应。
(3)反应条件都是点燃。
(4)生成物都只有一种物质。
(5)都是固体和气体的反应。
(6)反应都放出热量。
化合反应与氧化反应
化合反应:由两种或两种以上的物 质生成一种物质的反应。
氧化反应:物质跟氧发生的反应。
氧化反应
燃烧:
发光、放热的剧烈的氧化反应
缓慢氧化:
进行得很缓慢,甚至不容易察觉的氧化反应。
如:动植物的呼吸、食物的腐烂、酒和醋的酿造、农家肥的腐熟、铁的生锈等
它们的共同点:都是氧化反应,都放热
总结提升
提示:
① 氧化反应中的“氧”不能说成“氧气”,以后还会学到没有氧气参加的氧化反应。
在有氧气参加的氧化反应中,氧气提供了氧,是氧化剂。
氧化反应不是反应的基本类型,和化合反应之间没有必然的联系。
判断下列反应是否为化合反应?是否氧化反应?
硫 + 氧气 二氧化硫
点燃
锌 + 盐酸 氯化锌+氢气
石蜡 + 氧气 二氧化碳+水
点燃
镁 + 氧气 氧化镁
点燃
讨论:在什么情况下,一个反应既是化合反应又是氧化反应?
氧气的化学性质
氧气是一种化学性质比较活泼的气体,可以支持燃烧(助燃性),可以跟很多物质发生反应。
它在氧化反应中提供氧,具有氧化性,是一种常用的氧化剂。
氧气含量越高,燃烧越剧烈。
【小结】
本节课你学到了哪些知识?
小组讨论交流,然后每组派代表发言.
盘点收获
知识回顾
课题2 氧气
1、氧气的物理性质(通常状况下)?
(1)无色、无味的气体 (液态和固态时变为淡蓝色)
(2)密度比空气大
(3)不易溶于水
2、氧气的化学性质
(1)带火星的木条在氧气中复燃(可检验氧气)
(2)硫+氧气 二氧化硫
(3)碳+氧气 二氧化碳
(4)铁+氧气 四氧化三铁
3、化合反应:由两种或两种以上的物质生成另一种物质的反应,叫做化 合反应
4、氧化反应:物质跟氧发生的化学反应叫做氧化反应
5、氧气是一种化学性质比较活泼的气体,具有氧化性,可以支持燃烧,可以跟很多物质发生反应。
1、对氧气物理性质的叙述正确的是( )
A、极易溶于水
B、在标准状况下,密度比空气略大
C、在-183℃时变成无色液体
D、在-218℃时变成白色固体
2、要除去密闭容器内空气的氧气,并不使混入其他气体,在其中燃烧的可燃物可以是( )
A、硫粉 B、木炭
C、铁丝 D、红磷
练习
B
D
1、对氧气物理性质的叙述正确的是( )
A、极易溶于水
B、在标准状况下,密度比空气略大
C、在-183℃时变成无色液体
D、在-218℃时变成白色固体
2、要除去密闭容器内空气的氧气,并不使混入其他气体,在其中燃烧的可燃物可以是( )
A、硫粉 B、木炭
C、铁丝 D、红磷
练习
B
D
4、下列反应属于化合反应的是( ),
属于氧化反应的是( )
A、酒精+氧气 水+二氧化碳
B、锌 + 盐酸 氯化锌+氢气
C、磷 + 氧气 五氧化二磷
D、碱式碳酸铜 水+氧化铜+二氧化碳
C
AC
5、判断下列说法正确的是( )
A、由两种物质生成一种物质的反应叫做化合反应
B、氧化反应是指物质跟氧气发生的化学反应
C、凡是在空气中不能燃烧的物质,在氧气中
也不能燃烧
D、蜡烛的燃烧过程既有物理变化,又有化学变化
D
本节课结束
同学们,再见!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
