铁的化合物
图片预览






文档简介
课件18张PPT。铁的化合物 一、铁盐和亚铁盐 1、Fe3+的检验 向FeCl3和FeSO4溶液中分别加入KSCN溶液 溶液呈血红色溶液颜色无变化 含Fe3+的盐溶液中加入KSCN溶液,溶液呈血红色 Fe3+ Fe2+ Fe 氧化性 还原性 Fe3+ ? Fe2、Fe3+、 Fe2+的相互转化氧化性还原性(1)Fe3+的氧化性实验1:在滴有KSCN的FeCl3溶液中加入Fe粉,振荡。现象:结论:2FeCl3 + Fe == 3FeCl2 反应方程式:(氧化剂)(还原剂)离子方程式:2FeCl3 + Cu == 2FeCl2+CuCl2(氧化剂)(还原剂)溶液血红色褪去溶液中不含Fe3+2Fe3+ + Fe == 3Fe2+金属铜也能将Fe3+还原: Fe3+ ? Fe Fe2+实验2:在FeSO4和KSCN的混合溶液中,滴加氯水(Cl2)现象:溶液变成血红色结论:化学方程式:2FeCl2 + Cl2 == 2FeCl3氧化剂还原剂总结:还原剂+氧化剂(Cl2)+还原剂(Fe)氧化剂离子方程式:2Fe2+ + Cl2 == 2Fe3+ +2Cl-(2)Fe2+的还原性 Fe2+ Cl2 Fe3+交流和讨论:
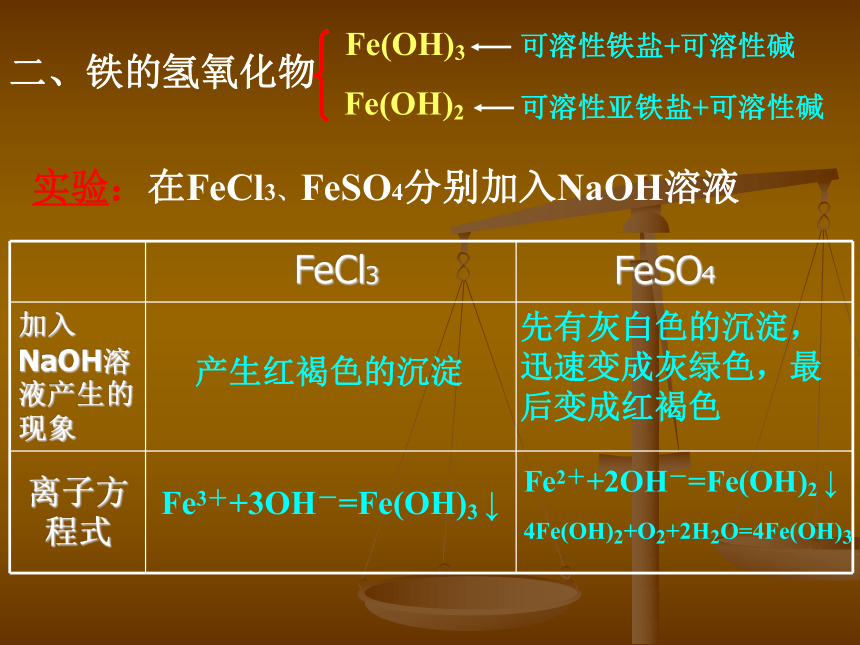
有哪些方法可以鉴别Fe3+溶液和Fe2+溶液?滴入KSCN溶液溶液呈血红色溶液颜色无变化观察颜色溶液为黄色溶液为浅绿色加碱?二、铁的氢氧化物产生红褐色的沉淀先有灰白色的沉淀,迅速变成灰绿色,最后变成红褐色Fe3++3OH-=Fe(OH)3 ↓4Fe(OH)2+O2+2H2O=4Fe(OH)3Fe(OH)3 Fe(OH)2实验:在FeCl3、FeSO4分别加入NaOH溶液Fe2++2OH-=Fe(OH)2 ↓?你觉得该方案合理吗?为什么?实验目的:制备Fe(OH)2
所用试剂: FeSO4溶液、NaOH溶液
操作步骤:用长滴管吸取NaOH溶液,插入FeSO4溶液液面下,慢慢挤出NaOH溶液,观察最初生成的沉淀的颜色,不要振荡。试一试吧小结:
要制得Fe(OH)2 ,可采取什么措施?用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。(1)除去蒸馏水中溶解的O2常采用煮沸的方法
(2)生成白色Fe(OH)2沉淀的操作可采用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。
(3)用植物油将反应体系与空气隔离.交流和讨论:
有哪些方法可以鉴别Fe3+溶液和Fe2+溶液?滴入KSCN溶液溶液呈血红色溶液颜色无变化观察颜色溶液为黄色溶液为浅绿色加碱?(1)颜色:Fe 2+ Fe3+ .Fe2+ 和Fe3+的鉴别方法浅绿色黄色(2)KSCN法:滴入KSCN溶液,呈 色的是Fe 3+血红(3)碱液法:分别加入碱液(或氨水),生成 色沉淀是Fe3+溶液,先生成
色沉淀,又迅速转变为 色,最后变
为 的是Fe2+溶液红褐白灰绿红褐色氢氧化物的通性 思考和交流 1、氢氧化物可由 与 反应制得;可溶性盐碱2、不溶性碱受热分解。一、铁盐和亚铁盐 白色沉淀迅速变成灰绿色,最后变成红褐色红褐色沉淀 溶液变血红色 无明显现象主要表现为还原性只有氧化性总 结二、铁的氢氧化物 Fe2++2OH-=Fe(OH)2↓(隔绝空气) Fe3++3OH-=Fe(OH)3↓ 白色固体 红褐色固体 难溶于水 难溶于水 受热易分解极易被空气中氧气氧化成氢氧化铁 4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe(OH)2+ 2HCl=FeCl2 +2H2OFe(OH)3+ 3HCl=FeCl3 +3H2O4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3 Fe2O3+3H2O可溶性铁盐、碱溶液可溶性亚铁盐、碱溶液红褐色沉淀白色→灰绿色→红褐色沉淀1、要除去FeCl2溶液中少量的FeCl3,下列方法可行的是 ( )
A、滴入KSCN溶液 B、加入铁粉
C、通入氯气 D、加入铜粉B练一练:练一练:2、下列4种铁的化合物溶于稀盐酸后,滴加KSCN溶液没有颜色变化,再加氯水呈红色的是 ( )
A.FeO B.Fe2O3 C.FeCl3 D.FeSO4A、D3、为了防止试剂变质,配制FeSO4的溶液在试剂瓶中除加入少量H2SO4外,还要加入 ( )
A.加入Cu B.通入Cl2 C.加入Fe D.加入KSCNC3、硫酸亚铁是一种可用于治疗缺铁性贫血的药剂。硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的氧气氧化成硫酸铁(硫酸铁无治疗贫血的药效)。试设计一个实验方案,验证某硫酸亚铁药片是否被氧化。写出主要实验步骤、现象。如图装置中用 NaOH溶液、铁屑、稀H2SO4等制备Fe(OH)2。 (1) 在试管A和B中加入试剂,打开止水夹,塞紧塞子,实验中的B管中观察到的现象为 ,目的是 。
(2)A管反应一段时间后夹紧止水夹,实验中的B管中观察到的现象为 , B管中发生反应的离子方程式是
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,
其理由 。
有哪些方法可以鉴别Fe3+溶液和Fe2+溶液?滴入KSCN溶液溶液呈血红色溶液颜色无变化观察颜色溶液为黄色溶液为浅绿色加碱?二、铁的氢氧化物产生红褐色的沉淀先有灰白色的沉淀,迅速变成灰绿色,最后变成红褐色Fe3++3OH-=Fe(OH)3 ↓4Fe(OH)2+O2+2H2O=4Fe(OH)3Fe(OH)3 Fe(OH)2实验:在FeCl3、FeSO4分别加入NaOH溶液Fe2++2OH-=Fe(OH)2 ↓?你觉得该方案合理吗?为什么?实验目的:制备Fe(OH)2
所用试剂: FeSO4溶液、NaOH溶液
操作步骤:用长滴管吸取NaOH溶液,插入FeSO4溶液液面下,慢慢挤出NaOH溶液,观察最初生成的沉淀的颜色,不要振荡。试一试吧小结:
要制得Fe(OH)2 ,可采取什么措施?用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。(1)除去蒸馏水中溶解的O2常采用煮沸的方法
(2)生成白色Fe(OH)2沉淀的操作可采用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。
(3)用植物油将反应体系与空气隔离.交流和讨论:
有哪些方法可以鉴别Fe3+溶液和Fe2+溶液?滴入KSCN溶液溶液呈血红色溶液颜色无变化观察颜色溶液为黄色溶液为浅绿色加碱?(1)颜色:Fe 2+ Fe3+ .Fe2+ 和Fe3+的鉴别方法浅绿色黄色(2)KSCN法:滴入KSCN溶液,呈 色的是Fe 3+血红(3)碱液法:分别加入碱液(或氨水),生成 色沉淀是Fe3+溶液,先生成
色沉淀,又迅速转变为 色,最后变
为 的是Fe2+溶液红褐白灰绿红褐色氢氧化物的通性 思考和交流 1、氢氧化物可由 与 反应制得;可溶性盐碱2、不溶性碱受热分解。一、铁盐和亚铁盐 白色沉淀迅速变成灰绿色,最后变成红褐色红褐色沉淀 溶液变血红色 无明显现象主要表现为还原性只有氧化性总 结二、铁的氢氧化物 Fe2++2OH-=Fe(OH)2↓(隔绝空气) Fe3++3OH-=Fe(OH)3↓ 白色固体 红褐色固体 难溶于水 难溶于水 受热易分解极易被空气中氧气氧化成氢氧化铁 4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe(OH)2+ 2HCl=FeCl2 +2H2OFe(OH)3+ 3HCl=FeCl3 +3H2O4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3 Fe2O3+3H2O可溶性铁盐、碱溶液可溶性亚铁盐、碱溶液红褐色沉淀白色→灰绿色→红褐色沉淀1、要除去FeCl2溶液中少量的FeCl3,下列方法可行的是 ( )
A、滴入KSCN溶液 B、加入铁粉
C、通入氯气 D、加入铜粉B练一练:练一练:2、下列4种铁的化合物溶于稀盐酸后,滴加KSCN溶液没有颜色变化,再加氯水呈红色的是 ( )
A.FeO B.Fe2O3 C.FeCl3 D.FeSO4A、D3、为了防止试剂变质,配制FeSO4的溶液在试剂瓶中除加入少量H2SO4外,还要加入 ( )
A.加入Cu B.通入Cl2 C.加入Fe D.加入KSCNC3、硫酸亚铁是一种可用于治疗缺铁性贫血的药剂。硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的氧气氧化成硫酸铁(硫酸铁无治疗贫血的药效)。试设计一个实验方案,验证某硫酸亚铁药片是否被氧化。写出主要实验步骤、现象。如图装置中用 NaOH溶液、铁屑、稀H2SO4等制备Fe(OH)2。 (1) 在试管A和B中加入试剂,打开止水夹,塞紧塞子,实验中的B管中观察到的现象为 ,目的是 。
(2)A管反应一段时间后夹紧止水夹,实验中的B管中观察到的现象为 , B管中发生反应的离子方程式是
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,
其理由 。
