10.2酸和碱的中和反应专项训练C—2021-2022学年九年级化学人教版下册(word版有答案)
文档属性
| 名称 | 10.2酸和碱的中和反应专项训练C—2021-2022学年九年级化学人教版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 124.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-01 00:00:00 | ||
图片预览




文档简介
人教版九年级化学下册第十单元 10.2酸和碱的中和反应 专项训练C
姓名:___________班级:___________
一、单选题
1.(2021·江苏高邮·一模)物质的性质决定物质的用途。下列相关物质的性质与其用途不匹配的是
A.石墨质软—用作电池的电极材料 B.不锈钢耐腐蚀—制造医疗器械
C.熟石灰显碱性—用来改良酸性土壤 D.N2不可燃—用粮食瓜果的保护气
2.(2021·江苏·苏州市工业园区第一中学九年级阶段练习)酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展下列有关酸、碱、盐的生产或应用的说法不合理的是( )
A.用氢氧化钠治疗酸过多 B.氢氧化钙可用于改良酸性土壤
C.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 D.实验室用浓硫酸干燥氧气、氢气
3.(2021·江苏·星海实验中学九年级阶段练习)下列反应中属于中和反应的是( )
A. B.
C. D.
4.(2021·陕西·九年级专题练习)下列应用利用了中和反应原理的是
A.用稀盐酸除去铁钉表面的铁锈 B.用纯碱除去面团发酵时产生的酸
C.用硫酸处理工业废水中的碱 D.用石灰乳与硫酸铜配制波尔多液
5.(2021·全国·九年级课时练习)下列有关中和反应的理解正确的是( )
A.反应的实质是氢离子与氢氧根离子反应生成水分子 B.有盐和水生成的反应都是中和反应
C.用碳酸氢钠治疗胃酸过多是中和反应 D.中和反应的现象很明显
6.(2021·山东周村·九年级期末)中和反应在生产和生活中有着广泛的应用。下列应用与中和反应原理无直接关系的是
A.服用含氢氧化铝的药物治疗胃酸过多症 B.用稀硫酸处理印染厂的碱性废水
C.在工业上,用盐酸来除铁锈 D.在蚊虫叮咬处涂抹稀碱液减轻痛痒
7.(2021·山东岱岳·九年级期中)如图是盐酸与氢氧化钠溶液反应的示意图,下列关于酸碱反应说法正确的是
A.酸碱中和反应的实质是H++OH-=H2O B.生成盐和水的反应,都是中和反应
C.当酸碱完全中和时,两者所用质量一定相等 D.当酸碱完全中和时,所得盐溶液pH等于0
8.(2021·湖南·武冈市第二中学九年级开学考试)下列没有运用中和反应原理的是
A.用熟石灰改良酸性土壤 B.服用含氢氧化镁的药物,可以治疗胃酸过多症
C.用生石灰做干燥剂 D.蚊虫叮咬处涂上肥皂水,可减轻痛痒
9.(2021·重庆·西南大学附中九年级阶段练习)下列对生活中的现象或做法的解释错误的是
现象或做法 解 释
A 格致楼下樱花飘香 分子在不断运动
B 打开可乐瓶盖有气泡冒出 压强增大,气体溶解度减小
C 用含氢氧化铝的药物治疗胃酸过多 酸碱发生中和反应
D 用碳素墨水书写档案 碳常温下化学性质稳定
A.A B.B C.C D.D
10.(2021·山东高青·一模)下列物质性质和用途的关系描述不一致的是
A.氢气具有可燃性,用作高能燃料
B.液氮通常情况下化学性质稳定,用作制冷剂
C.稀有气体通电时发出不同颜色的光,用作多种用途的电光源
D.氢氧化铝显碱性,用作治疗胃酸过多
11.(2021·湖北·石首市文峰初级中学九年级阶段练习)推理是一种重要的思维方法。下列推理合理的是
A.化合物是由不同元素组成的纯净物,所以只含一种元素的物质一定不是化合物
B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
C.碱的溶液显碱性,所以显碱性的物质都是碱
D.氧化物含有氧元素,所以含有氧元素的物质一定是氧化物
12.(2021·江苏·如皋初级中学一模)归纳和推理是学习化学的重要方法,下列说法正确的是( )
A.H+和OH-能结合成,故H2O由H+和OH-构成
B.可用于吸附色素和异味的物质有活性炭、明矾等物质
C.碳、一氧化碳都具有还原性,故二者均能还原氧化铁
D.某物质燃烧生成二氧化碳,该物质中一定含有碳单质
13.(2021·宁夏·吴忠市第四中学一模)化学帮助人类认识和探索物质世界。下列对化学规律运用的描述中,不正确的是
A.利用中和反应改良酸性土壤 B.利用分解反应分离液态空气
C.利用置换反应湿法炼铜 D.利用化学反应获得能量
14.(2021·江苏连云港·一模)下列有关物质的性质与用途对应关系不成立的是
A.氮气的化学性质不活泼,可用来作保护气 B.石墨有滑腻感,可用来作电极
C.熟石灰具有碱性,可用来改良酸性土壤 D.活性炭具有吸附性,可用来去除色素和异味
15.(2021·广西·南宁外国语学校三模)下列对实验现象的描述正确的是
A.木炭在氧气中燃烧,发出白光,生成二氧化碳气体
B.在滴有酚酞的氢氧化钠溶液中逐滴加入稀盐酸,溶液颜色由无色逐渐变成红色
C.打开浓盐酸的试剂瓶,瓶口出现白烟
D.将黄铜片和铜片相互刻画,铜片上会出现划痕
16.(2021·湖北枣阳·一模)下列物质的用途和性质对应关系错误的是
A.氮气——保护气——化学性质不活泼 B.炭黑——制碳素墨水——常温下碳的化学性质不活泼
C.二氧化碳——灭火——密度比空气大,不能燃烧也不能支持燃烧
D.氢氧化钠——治疗胃酸过多——与酸发生中和反应
17.(2021·宁夏中宁·模拟预测)类推是化学学习中常用的思维方法。现有以下类推结果:①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;④金属元素在化合物中显正价,故非金属元素在化合物中一定显负价。其中错误的是
A.只有① B.只有①②③ C.只有②③④ D.全部
18.(2021·广东·深圳外国语学校九年级阶段练习)“归纳推理”是化学学习过程中常用的思维方法,下列推理合理的是
A.稀有气体可作保护气,则作保护气的气体一定是稀有气体
B.碱性溶液的pH>7,则pH>7的溶液一定是碱性溶液
C.铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀
D.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
19.(2021·广东黄埔·一模)除去下列物质中的杂质,所选用的方法正确的是
物质(括号内为杂质) 操作方法
A CO2(HCl) 先通过过量氢氧化钠溶液,再通过浓硫酸
B NaCl溶液(Na2CO3) 加稀硫酸至恰好不再产生气泡为止
C CuSO4溶液(H2SO4) 加过量氧化铜粉末充分反应后过滤
D CaCl2溶液(HCl) 加过量生石灰充分反应后过滤
A.A B.B C.C D.D
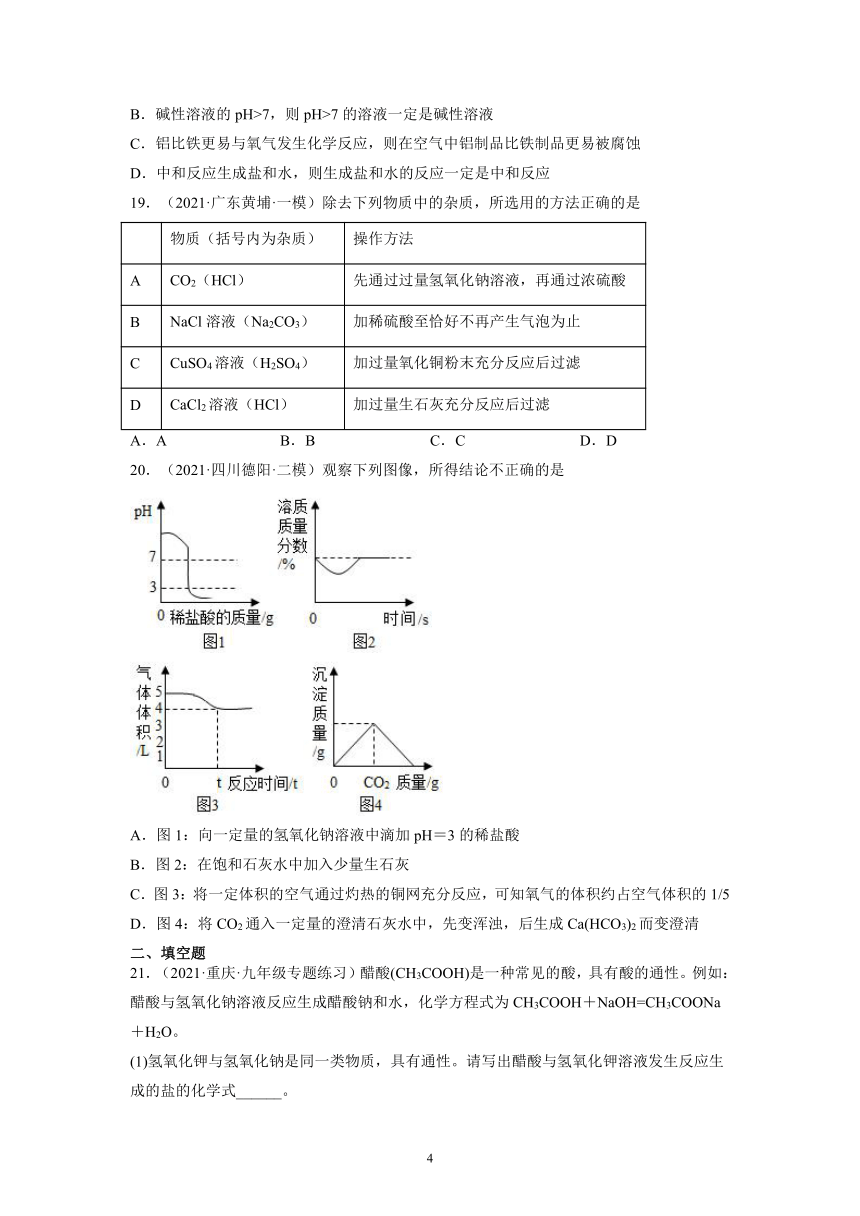
20.(2021·四川德阳·二模)观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
二、填空题
21.(2021·重庆·九年级专题练习)醋酸(CH3COOH)是一种常见的酸,具有酸的通性。例如:醋酸与氢氧化钠溶液反应生成醋酸钠和水,化学方程式为CH3COOH+NaOH=CH3COONa+H2O。
(1)氢氧化钾与氢氧化钠是同一类物质,具有通性。请写出醋酸与氢氧化钾溶液发生反应生成的盐的化学式______。
(2)醋酸与盐酸一样,能与活泼金属反应生成氢气。请写出醋酸与金属锌反应的化学方程式:___________________________________________________。
22.(2021·河南卫辉·二模)如图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是将______(填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液。
②相同质量、相同质量分数的两种溶液充分反应后,所得溶液的pH______7。
23.(2021·山东临沭·二模)酸碱盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出_______(填符号)。
(2)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如下图,当滴入溶液为V2mL时,所得溶液中溶质的化学式为_______,所得溶液能使紫色石蕊溶液变成_______色。
24.(2021·吉林船营·一模)某同学在做中和反应实验时,用pH传感器测得溶液的pH变化如图所示,回答下列问题。
(1)曲线上___________点表示酸和碱恰好完全反应。
(2)C点溶液中含有的阴离子中一定有___________离子。
25.(2021·山东禹城·一模)实验小组用pH传感器探究稀硫酸和氢氧化钠溶液的反应,实验中溶液pH的变化如图所示。
(1)该实验是将______滴加到另一种溶液中,反应的化学方程式是______。
(2)a点时溶液中的溶质是______(用化学式表示),该溶液中滴加紫色石蕊试液,溶液变______色。
26.(2021·河南平顶山·一模)生活中若将84消毒液(主要成分是NaClO)和洁厕灵(主要成分是盐酸)混合使用,会产生有毒气体。反应的化学方程式为。
(1)上述反应中,含氯元素化合价为+1价的物质是______(填字母)。
A、 HCl B、 Cl2 C、 NaClO D、 NaCl
(2)人的胃液中有胃酸(主要成分盐酸),胃酸过多常用含Al (OH)3的药物治疗,其治疗原理用化学方程式可表示为______。
27.(2021·河南鹤壁·一模)如图是某化学小组向一定量稀盐酸中滴入氢氧化钠溶液时用pH传感器测得的pH变化图像。
(1)b点溶液中溶质的化学式为___________。
(2)若保持原稀盐酸的量不变,改用与ng原氢氧化钠溶液中溶质质量相等的熟石灰与其反应,则反应后的溶液的pH___________(填“>”“<”或“=”)。
(3)用实际参加化学反应的离子符号表示化学反应的式子叫离子方程式。请写出氢氧化钠和稀盐酸反应的离子方程式___________。
28.(2021·河南·武陟中学三模)化学小组在探究稀硫酸与氢氧化钠溶液的反应时,利用数字化实验技术测得溶液pH变化曲线如图所示。c点时溶液中溶质的化学式为______;若改用与稀硫酸溶质质量分数相同的盐酸进行实验,则当氢氧化钠恰好完全反应时,pH曲线可能经过______(填“a”或“b”)点。
29.(2021·湖南·长沙市开福区青竹湖湘一外国语学校二模)写出下列变化的化学方程式:
(1)铁丝在氧气中燃烧:_______。
(2)小苏打(碳酸氢钠)治疗胃酸过多:_______。
30.(2021·山东高青·二模)如图是氢氧化钠溶液和稀盐酸反应过程中溶液pH的变化图。写出反应的化学方程式_____,该反应的实质是_______。b点处溶液中溶质是_______。向d点处的溶液中滴加紫色石蕊试液,溶液呈_______色。
三、实验题
31.(2021·四川锦江·二模)归纳总结是学习化学的重要方法,某同学整理复习以下四个教材实验,请与他一起完成下面相关整理。
(1)图1实验的目的是______,该实验的化学方程式为______。
(2)图2实验说明水由氢、氧元素组成,b 试管收集到的气体能______。
(3)图3实验中观察到乒乓球碎片先燃着,说明______。
(4)图4实验中,当观察到______时,说明两种溶液恰好完全反应。
32.(2021·四川岳池·三模)在学习了酸的化学性质之后,某实验小组选用稀盐酸做了如下图所示实验。
请回答下列问题:
(1)A烧杯中,铜不与稀盐酸发生反应的原因是___________。
(2)能产生气泡且反应是置换反应的是___________(填字母序号)。
(3)写出E烧杯中反应的化学方程式___________。
(4)向D烧杯逐渐加入盐酸至过量,溶液由红色变为___________色,说明盐酸与氢氧化钠发生了中和反应。
(5)小组另外的同学选用稀硫酸代替稀盐酸重复实验,证明了硫酸与盐酸具有相似的化学性质。酸有一些相似的化学性质,是因为在不同的酸溶液中都含有相同的___________(填离子符号)。
四、计算题
33.(2021·内蒙古新城·二模)将40g稀盐酸逐滴加入20g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐酸的滴入,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中的热量损失)。试回答:
(1)图二中B点时溶液中溶质为______。
(2)计算稀盐酸中溶质的质量分数。
34.(2021·贵州织金·三模)实验室有一瓶标签破损的稀H2SO4溶液,为测定该硫酸溶的溶质质量分数,现取40g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如图所示。试回答:
(1)a点溶液中所含有的阳离子是 (填离子符号)。
(2)当pH=7时,所得溶液中溶质质量分数为多少?(写出计算过程)
参考答案
1.A 2.A 3.B 4.C 5.A 6.C 7.A 8.C
9.B 10.B 11.A 12.C 13.B 14.B 15.D 16.D
17.D 18.B 19.C 20.A
21.CH3COOK 2CH3COOH+Zn=(CH3COO)2Zn+H2↑
22.硫酸 大于
23.H+ NaCl、HCl 红
24.B 氢氧根
25.稀硫酸 H2SO4+2NaOH=Na2SO4+2H2O NaOH、Na2SO4 蓝
26.C
27.NaCl NaOH >
28.H2SO4、Na2SO4 a
29.
30.NaOH+HCl=NaCl+H2O 氢离子和氢氧根离子反应生成水 氯化钠和氢氧化钠 红
31.测定空气中氧气的含量 使带火星的木条复燃 乒乓球碎片着火点更低 红色恰好褪去
32.在金属活动性顺序表中铜排在氢的后面 B NaHCO3+HCl=NaCl+H2O+CO2↑ 无 H+
33.
(1)NaCl
(2)解:设稀盐酸中溶质的质量分数为x
x=3.65%
答:稀盐酸中溶质的质量分数为3.65%。
34.(1)Na+、H+
(2)由图象看出,当pH=7时,消耗的氢氧化钠的质量为160g×5%=8g
生成的硫酸钠的质量为x
x=14.2g
所得溶液的溶质质量分数为;
答:所得溶液中溶质质量分数为7.1%。
姓名:___________班级:___________
一、单选题
1.(2021·江苏高邮·一模)物质的性质决定物质的用途。下列相关物质的性质与其用途不匹配的是
A.石墨质软—用作电池的电极材料 B.不锈钢耐腐蚀—制造医疗器械
C.熟石灰显碱性—用来改良酸性土壤 D.N2不可燃—用粮食瓜果的保护气
2.(2021·江苏·苏州市工业园区第一中学九年级阶段练习)酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展下列有关酸、碱、盐的生产或应用的说法不合理的是( )
A.用氢氧化钠治疗酸过多 B.氢氧化钙可用于改良酸性土壤
C.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 D.实验室用浓硫酸干燥氧气、氢气
3.(2021·江苏·星海实验中学九年级阶段练习)下列反应中属于中和反应的是( )
A. B.
C. D.
4.(2021·陕西·九年级专题练习)下列应用利用了中和反应原理的是
A.用稀盐酸除去铁钉表面的铁锈 B.用纯碱除去面团发酵时产生的酸
C.用硫酸处理工业废水中的碱 D.用石灰乳与硫酸铜配制波尔多液
5.(2021·全国·九年级课时练习)下列有关中和反应的理解正确的是( )
A.反应的实质是氢离子与氢氧根离子反应生成水分子 B.有盐和水生成的反应都是中和反应
C.用碳酸氢钠治疗胃酸过多是中和反应 D.中和反应的现象很明显
6.(2021·山东周村·九年级期末)中和反应在生产和生活中有着广泛的应用。下列应用与中和反应原理无直接关系的是
A.服用含氢氧化铝的药物治疗胃酸过多症 B.用稀硫酸处理印染厂的碱性废水
C.在工业上,用盐酸来除铁锈 D.在蚊虫叮咬处涂抹稀碱液减轻痛痒
7.(2021·山东岱岳·九年级期中)如图是盐酸与氢氧化钠溶液反应的示意图,下列关于酸碱反应说法正确的是
A.酸碱中和反应的实质是H++OH-=H2O B.生成盐和水的反应,都是中和反应
C.当酸碱完全中和时,两者所用质量一定相等 D.当酸碱完全中和时,所得盐溶液pH等于0
8.(2021·湖南·武冈市第二中学九年级开学考试)下列没有运用中和反应原理的是
A.用熟石灰改良酸性土壤 B.服用含氢氧化镁的药物,可以治疗胃酸过多症
C.用生石灰做干燥剂 D.蚊虫叮咬处涂上肥皂水,可减轻痛痒
9.(2021·重庆·西南大学附中九年级阶段练习)下列对生活中的现象或做法的解释错误的是
现象或做法 解 释
A 格致楼下樱花飘香 分子在不断运动
B 打开可乐瓶盖有气泡冒出 压强增大,气体溶解度减小
C 用含氢氧化铝的药物治疗胃酸过多 酸碱发生中和反应
D 用碳素墨水书写档案 碳常温下化学性质稳定
A.A B.B C.C D.D
10.(2021·山东高青·一模)下列物质性质和用途的关系描述不一致的是
A.氢气具有可燃性,用作高能燃料
B.液氮通常情况下化学性质稳定,用作制冷剂
C.稀有气体通电时发出不同颜色的光,用作多种用途的电光源
D.氢氧化铝显碱性,用作治疗胃酸过多
11.(2021·湖北·石首市文峰初级中学九年级阶段练习)推理是一种重要的思维方法。下列推理合理的是
A.化合物是由不同元素组成的纯净物,所以只含一种元素的物质一定不是化合物
B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
C.碱的溶液显碱性,所以显碱性的物质都是碱
D.氧化物含有氧元素,所以含有氧元素的物质一定是氧化物
12.(2021·江苏·如皋初级中学一模)归纳和推理是学习化学的重要方法,下列说法正确的是( )
A.H+和OH-能结合成,故H2O由H+和OH-构成
B.可用于吸附色素和异味的物质有活性炭、明矾等物质
C.碳、一氧化碳都具有还原性,故二者均能还原氧化铁
D.某物质燃烧生成二氧化碳,该物质中一定含有碳单质
13.(2021·宁夏·吴忠市第四中学一模)化学帮助人类认识和探索物质世界。下列对化学规律运用的描述中,不正确的是
A.利用中和反应改良酸性土壤 B.利用分解反应分离液态空气
C.利用置换反应湿法炼铜 D.利用化学反应获得能量
14.(2021·江苏连云港·一模)下列有关物质的性质与用途对应关系不成立的是
A.氮气的化学性质不活泼,可用来作保护气 B.石墨有滑腻感,可用来作电极
C.熟石灰具有碱性,可用来改良酸性土壤 D.活性炭具有吸附性,可用来去除色素和异味
15.(2021·广西·南宁外国语学校三模)下列对实验现象的描述正确的是
A.木炭在氧气中燃烧,发出白光,生成二氧化碳气体
B.在滴有酚酞的氢氧化钠溶液中逐滴加入稀盐酸,溶液颜色由无色逐渐变成红色
C.打开浓盐酸的试剂瓶,瓶口出现白烟
D.将黄铜片和铜片相互刻画,铜片上会出现划痕
16.(2021·湖北枣阳·一模)下列物质的用途和性质对应关系错误的是
A.氮气——保护气——化学性质不活泼 B.炭黑——制碳素墨水——常温下碳的化学性质不活泼
C.二氧化碳——灭火——密度比空气大,不能燃烧也不能支持燃烧
D.氢氧化钠——治疗胃酸过多——与酸发生中和反应
17.(2021·宁夏中宁·模拟预测)类推是化学学习中常用的思维方法。现有以下类推结果:①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;④金属元素在化合物中显正价,故非金属元素在化合物中一定显负价。其中错误的是
A.只有① B.只有①②③ C.只有②③④ D.全部
18.(2021·广东·深圳外国语学校九年级阶段练习)“归纳推理”是化学学习过程中常用的思维方法,下列推理合理的是
A.稀有气体可作保护气,则作保护气的气体一定是稀有气体
B.碱性溶液的pH>7,则pH>7的溶液一定是碱性溶液
C.铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀
D.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
19.(2021·广东黄埔·一模)除去下列物质中的杂质,所选用的方法正确的是
物质(括号内为杂质) 操作方法
A CO2(HCl) 先通过过量氢氧化钠溶液,再通过浓硫酸
B NaCl溶液(Na2CO3) 加稀硫酸至恰好不再产生气泡为止
C CuSO4溶液(H2SO4) 加过量氧化铜粉末充分反应后过滤
D CaCl2溶液(HCl) 加过量生石灰充分反应后过滤
A.A B.B C.C D.D
20.(2021·四川德阳·二模)观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
二、填空题
21.(2021·重庆·九年级专题练习)醋酸(CH3COOH)是一种常见的酸,具有酸的通性。例如:醋酸与氢氧化钠溶液反应生成醋酸钠和水,化学方程式为CH3COOH+NaOH=CH3COONa+H2O。
(1)氢氧化钾与氢氧化钠是同一类物质,具有通性。请写出醋酸与氢氧化钾溶液发生反应生成的盐的化学式______。
(2)醋酸与盐酸一样,能与活泼金属反应生成氢气。请写出醋酸与金属锌反应的化学方程式:___________________________________________________。
22.(2021·河南卫辉·二模)如图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是将______(填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液。
②相同质量、相同质量分数的两种溶液充分反应后,所得溶液的pH______7。
23.(2021·山东临沭·二模)酸碱盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出_______(填符号)。
(2)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如下图,当滴入溶液为V2mL时,所得溶液中溶质的化学式为_______,所得溶液能使紫色石蕊溶液变成_______色。
24.(2021·吉林船营·一模)某同学在做中和反应实验时,用pH传感器测得溶液的pH变化如图所示,回答下列问题。
(1)曲线上___________点表示酸和碱恰好完全反应。
(2)C点溶液中含有的阴离子中一定有___________离子。
25.(2021·山东禹城·一模)实验小组用pH传感器探究稀硫酸和氢氧化钠溶液的反应,实验中溶液pH的变化如图所示。
(1)该实验是将______滴加到另一种溶液中,反应的化学方程式是______。
(2)a点时溶液中的溶质是______(用化学式表示),该溶液中滴加紫色石蕊试液,溶液变______色。
26.(2021·河南平顶山·一模)生活中若将84消毒液(主要成分是NaClO)和洁厕灵(主要成分是盐酸)混合使用,会产生有毒气体。反应的化学方程式为。
(1)上述反应中,含氯元素化合价为+1价的物质是______(填字母)。
A、 HCl B、 Cl2 C、 NaClO D、 NaCl
(2)人的胃液中有胃酸(主要成分盐酸),胃酸过多常用含Al (OH)3的药物治疗,其治疗原理用化学方程式可表示为______。
27.(2021·河南鹤壁·一模)如图是某化学小组向一定量稀盐酸中滴入氢氧化钠溶液时用pH传感器测得的pH变化图像。
(1)b点溶液中溶质的化学式为___________。
(2)若保持原稀盐酸的量不变,改用与ng原氢氧化钠溶液中溶质质量相等的熟石灰与其反应,则反应后的溶液的pH___________(填“>”“<”或“=”)。
(3)用实际参加化学反应的离子符号表示化学反应的式子叫离子方程式。请写出氢氧化钠和稀盐酸反应的离子方程式___________。
28.(2021·河南·武陟中学三模)化学小组在探究稀硫酸与氢氧化钠溶液的反应时,利用数字化实验技术测得溶液pH变化曲线如图所示。c点时溶液中溶质的化学式为______;若改用与稀硫酸溶质质量分数相同的盐酸进行实验,则当氢氧化钠恰好完全反应时,pH曲线可能经过______(填“a”或“b”)点。
29.(2021·湖南·长沙市开福区青竹湖湘一外国语学校二模)写出下列变化的化学方程式:
(1)铁丝在氧气中燃烧:_______。
(2)小苏打(碳酸氢钠)治疗胃酸过多:_______。
30.(2021·山东高青·二模)如图是氢氧化钠溶液和稀盐酸反应过程中溶液pH的变化图。写出反应的化学方程式_____,该反应的实质是_______。b点处溶液中溶质是_______。向d点处的溶液中滴加紫色石蕊试液,溶液呈_______色。
三、实验题
31.(2021·四川锦江·二模)归纳总结是学习化学的重要方法,某同学整理复习以下四个教材实验,请与他一起完成下面相关整理。
(1)图1实验的目的是______,该实验的化学方程式为______。
(2)图2实验说明水由氢、氧元素组成,b 试管收集到的气体能______。
(3)图3实验中观察到乒乓球碎片先燃着,说明______。
(4)图4实验中,当观察到______时,说明两种溶液恰好完全反应。
32.(2021·四川岳池·三模)在学习了酸的化学性质之后,某实验小组选用稀盐酸做了如下图所示实验。
请回答下列问题:
(1)A烧杯中,铜不与稀盐酸发生反应的原因是___________。
(2)能产生气泡且反应是置换反应的是___________(填字母序号)。
(3)写出E烧杯中反应的化学方程式___________。
(4)向D烧杯逐渐加入盐酸至过量,溶液由红色变为___________色,说明盐酸与氢氧化钠发生了中和反应。
(5)小组另外的同学选用稀硫酸代替稀盐酸重复实验,证明了硫酸与盐酸具有相似的化学性质。酸有一些相似的化学性质,是因为在不同的酸溶液中都含有相同的___________(填离子符号)。
四、计算题
33.(2021·内蒙古新城·二模)将40g稀盐酸逐滴加入20g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐酸的滴入,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中的热量损失)。试回答:
(1)图二中B点时溶液中溶质为______。
(2)计算稀盐酸中溶质的质量分数。
34.(2021·贵州织金·三模)实验室有一瓶标签破损的稀H2SO4溶液,为测定该硫酸溶的溶质质量分数,现取40g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如图所示。试回答:
(1)a点溶液中所含有的阳离子是 (填离子符号)。
(2)当pH=7时,所得溶液中溶质质量分数为多少?(写出计算过程)
参考答案
1.A 2.A 3.B 4.C 5.A 6.C 7.A 8.C
9.B 10.B 11.A 12.C 13.B 14.B 15.D 16.D
17.D 18.B 19.C 20.A
21.CH3COOK 2CH3COOH+Zn=(CH3COO)2Zn+H2↑
22.硫酸 大于
23.H+ NaCl、HCl 红
24.B 氢氧根
25.稀硫酸 H2SO4+2NaOH=Na2SO4+2H2O NaOH、Na2SO4 蓝
26.C
27.NaCl NaOH >
28.H2SO4、Na2SO4 a
29.
30.NaOH+HCl=NaCl+H2O 氢离子和氢氧根离子反应生成水 氯化钠和氢氧化钠 红
31.测定空气中氧气的含量 使带火星的木条复燃 乒乓球碎片着火点更低 红色恰好褪去
32.在金属活动性顺序表中铜排在氢的后面 B NaHCO3+HCl=NaCl+H2O+CO2↑ 无 H+
33.
(1)NaCl
(2)解:设稀盐酸中溶质的质量分数为x
x=3.65%
答:稀盐酸中溶质的质量分数为3.65%。
34.(1)Na+、H+
(2)由图象看出,当pH=7时,消耗的氢氧化钠的质量为160g×5%=8g
生成的硫酸钠的质量为x
x=14.2g
所得溶液的溶质质量分数为;
答:所得溶液中溶质质量分数为7.1%。
同课章节目录
