8.1金属材料同步练习-2021-2022学年九年级化学人教版下册(含解析)
文档属性
| 名称 | 8.1金属材料同步练习-2021-2022学年九年级化学人教版下册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 406.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-02 00:00:00 | ||
图片预览




文档简介
8.1、金属材料
一、选择题(共16题)
1.生活中的下列物品,其制作材料属于合金的是( )
A.金刚石钻头 B.钢化玻璃杯 C.不锈钢锅 D.瓷器
2..下列物质不属于合金的是( )
A.焊锡 B.硬铝 C.不锈钢 D.四氧化三铁
3.某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属丝,当玻璃被击碎时,产生电信号,与金属丝相连的警报系统就会立即报警,这是利用了金属的( )
A.延展性
B.导电性
C.导热性
D.可燃性
4.下列不属于金属材料的是( )
A.黄铜 B.不锈钢 C.四氧化三铁 D.黄金
5.下列关于合金的说法不正确的是( )
A.不锈钢在一定的条件下也会生锈 B.合金的熔点一般低于各成分金属
C.合金一定是由多种金属熔合而成 D.控制条件可制成性能不同的合金
6.下列区分物质的方法正确的是( )
A.用观察法区分木炭粉和氧化铜粉
B.用闻气味的方法区分氧气和二氧化碳气体
C.用相互刻画的方法区分纯铜和黄铜
D.用尝味道的方法区分实验室里的氯化钠和蔗糖
7.如图是中国人民抗日战争暨世界反法西斯战争胜利70周年发行的纪念币。该纪念币材质为多种贵金属包钢铸造,属于金属合金。下列相关说法不正确的是( )
A.从物质的材料角度看,该纪念币属于金属材料
B.从物质的导电性角度看,该纪念币属于导体
C.从物质的分类角度看,该纪念币属于金属单质
D.从金属的防锈角度看,该纪念币比铁抗腐蚀性能强
8.我省明代科学家宋应星所著的《天工开物》中,详细记述了金、铜、铁、锌等金属的开采和冶炼方法,记述的金属中金属活动性最强的是( )
A.金 B.钢 C.铁 D.锌
9.生活中的下列现象,属于化学变化的是( )
A.用石墨制金刚石 B.干冰升华 C.铁杵磨成针 D.铜和锌制成合金
10.下列有关金属材料的说法,不正确的是( )
A.合金不一定是金属和金属熔合而成
B.焊锡有很好的抗腐蚀性,常用做焊接金属
C.生铁的含碳量比钢高
D.钛合金与人体有很好的“相容性”,因此可用来制造人造骨骼
11.2019年4月15日傍晚,有着800多年历史的巴黎圣母院被熊熊大火吞噬,精美绝伦的木质塔尖在世人的叹息声中轰然坍塌,而大理石质地的左塔也损毁严重,下列有关说法中错误的是( )
A.火灾发生时,旅客应该赶紧乘电梯逃生
B.左塔的大理石受热分解而被损毁
C.木质塔尖属于可燃物
D.尖顶上的钢公鸡为铜合金制品,其硬度比纯铜大
12.下列实验得出的结论不合理的是( )
A.实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大
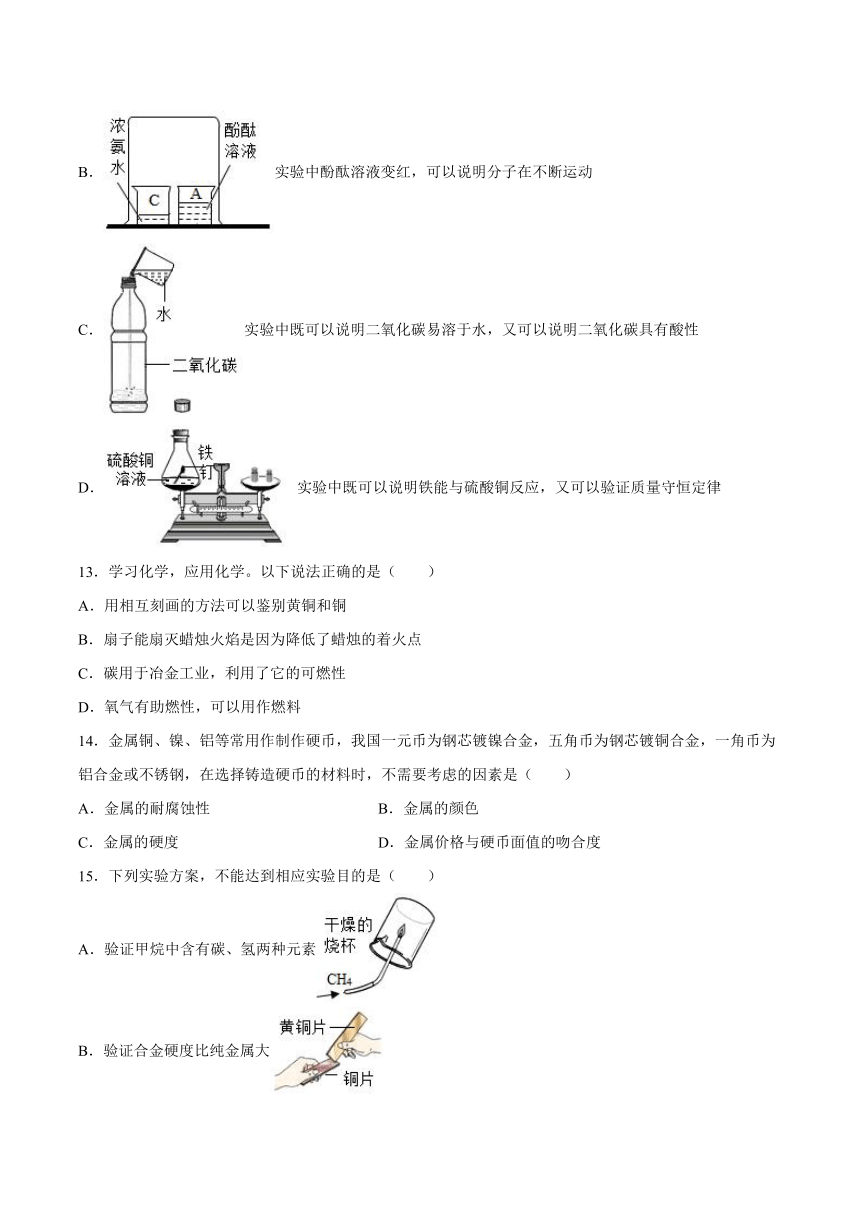
B.实验中酚酞溶液变红,可以说明分子在不断运动
C.实验中既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性
D.实验中既可以说明铁能与硫酸铜反应,又可以验证质量守恒定律
13.学习化学,应用化学。以下说法正确的是( )
A.用相互刻画的方法可以鉴别黄铜和铜
B.扇子能扇灭蜡烛火焰是因为降低了蜡烛的着火点
C.碳用于冶金工业,利用了它的可燃性
D.氧气有助燃性,可以用作燃料
14.金属铜、镍、铝等常用作制作硬币,我国一元币为钢芯镀镍合金,五角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时,不需要考虑的因素是( )
A.金属的耐腐蚀性 B.金属的颜色
C.金属的硬度 D.金属价格与硬币面值的吻合度
15.下列实验方案,不能达到相应实验目的是( )
A.验证甲烷中含有碳、氢两种元素
B.验证合金硬度比纯金属大
C.验证氯化氢分子发生了运动
D.验证质量守恒定律
16.铝锂合金是航空飞行器较理想的结构材料之一。铝锂合金具有的以下性质中,与该应用无关的是( )
A.硬度大 B.耐腐蚀 C.密度小 D.易导电
二、非选择题(共8题)
17.用化学符号填空:
(1)2个钠离子______;
(2)熔点最低的金属______;
(3)3个氯分子______;
(4)过氧化氢中氢元素的化合价为+1价______。
18.各种物质间存在着某种联系:
(1)含铁量:生铁_______钢(填“>”、“<”或“=”,下同);
(2)地壳中元素含量:硅元素________铁元素;
(3)空气中体积分数:二氧化碳_______稀有气体:
(4)碳元素的质量分数:甲醛(CH2O)_______醋酸(C2H4O2)。
19.从楚王陵中出土的铁器中发现了迄今世界上最早的炒钢技术,说明中国早在公元前2世纪就掌握了炒钢技术。炒钢是一种冶炼技术,冶炼时先将生铁加热到液态或半液态,然后靠鼓风 ,降低生铁的含碳量,使其成钢。由于在冶炼中要不断搅拌,好象炒菜一样,因而得名。
(1)生铁的含碳量为______,炼得的钢是_____(选填“纯净物”或“混合物”)。
(2)将生铁加热到液态或半液态并不断搅拌的原因是什么?____
(3)炒菜用的铁铲,一般要装上木柄,是因为铁具有______性,而电工用的钳子必须装上橡胶柄是因为铁有______性。
20.人类的生产、生活离不开金属。
(1)家用热水瓶内胆壁的银白色金属是________(填符号,下同);液体金属是__________;地壳中含量最高的金属元素是_______,人体中含量最多的金属元素是________。
(2)镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是_____(任写一个化学方程式)。该合金属于______(填“混合物”或“纯净物”),它是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于________(填“物理”或“化学”)变化。
(3)合金的很多性能与组成它们的纯金属不同。如图能表示锡铅合金的是________(填序号“a”“b”或“c”)。
(4)铝冶炼厂以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,其反应的化学方程式为________。
21.“见著知微,见微知著”是化学的思维方法。
(1)铜是生活中常见的一种金属
①铜可用以制作导线,体现了金属铜的_____性。
(2)固态的二氧化碳俗称“干冰”
①请写出干冰的一种用途_______;
②镁条在二氧化碳中燃烧生成氧化镁和一种黑色粉末,写出反应的化学方程式_____;
③通过这个反应,谈谈你对物质燃烧的新认识________。
(3)物质的性质决定用途,用途反映物质的性质。
①金刚石硬度很大、石墨硬度很小,两者物理性质有较大差异的原因_____。
②下列关于足球烯(C60)的说法正确的是______。
a 它的一个分子中含有60个碳原子
b 相对分子质量是720
c 它是一种化合物
22.开发利用氢能源是实现可持续发展的需要。根据图示分析,回答问题:
①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是_____(填序号)。
a.涤纶靠垫 b.橡胶轮胎 c.铜质导线 d.铝合金轮毂
②氢燃料电池的工作原理是:将氢气、氧气送到燃料电池中,经过催化剂的作用,发生反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式_____。
③氢气作燃料的优点是_____。
(2)工业上可通过下列工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。
主反应器中反应的化学方程式是_____。膜反应器中的基本反应类型是_____。该工艺流程中,能被循环利用的物质是_____。
(3)采用电解水的方式制备10Kg氢气,理论上需要水的质量是多少千克?____
23.随着我国深潜器“蛟龙”号考察任务(考察可燃冰的海底出口)顺利完成,我国的“蓝鲸1号”在南海首次试采俗称可燃冰的天然气水合物也获得圆满成功。
(1)蛟龙号的大部分材料由钛合金构成,这是因为它____;(多选)
A.抗腐蚀性优于不锈钢 B.密度小、机械性能好 C.导电性好、硬度大
(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是____;“蓝鲸1号”整体用钢达40000多吨,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,该反应的化学方程式为____,反应前后氮元素的化合价变化为____。
(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少______(至少填两种物质的化学式)等有害气体的排放,可极大限度地减少空气污染。
24.已知在不同的温度下,CO与铁的氧化物反应能生成另一种铁的氧化物(或铁单质)和CO2。现利用下图1的实验装置进行实验,反应过程中管内的固体质量随温度的变化曲线如图2。
注:图1中的仪器甲是一种加热仪器,图2中A、B点的固体组成分别是FeO、Fe3O4中的一种。
(1)查阅资料发现,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,仪器甲应选用的加热仪器是_____(填“酒精灯”或“酒精喷灯”);图1装置中的现象有____;________。
(2)利用图2显示的相关信息,回答如下问题:
①在0~400℃温度范围内,管内固体质量不变,其原因是________。
②图中x=__g。
计算过程:_____
③试据图计算并推断出A点固体的化学式是______。
参考答案
1.C
【详解】
A、 金刚石钻头,是由碳元素组成的,不属于合金,故选项错误;B、玻璃杯是硅酸盐产品,不属于合金,故选项错误;C、不锈钢是钢的一种,是铁的合金,故选项正确;D、陶瓷是用泥土烧制而成的,属于无机非金属材料,不属于合金,故选项错误。故选C。
2.D
【详解】
A、焊锡是锡和铅的合金,属于合金,故A正确;
B、硬铝是铝的一种合金,属于合金,故B正确;
C、不锈钢中含有铁、铬、碳,属于合金,属于合金,故C正确;
D、四氧化三铁是金属化合物,所以不是合金,不属合金,故D错误。故选D。
3.B
【详解】
与金属丝相连的警报系统就会立即报警,是利用了金属的导电性。故选B。
4.C
【分析】
金属材料包括纯金属和合金。
【详解】
A.黄铜是铜的合金,属于金属材料,不符合题意。
B.不锈钢是铁的合金,属于金属材料,不符合题意。
C.四氧化三铁是铁的化合物,不属于金属材料,符合题意。
D.黄金属于纯金属,属于金属材料,不符合题意。
故选:C。
5.C
【详解】
A、不锈钢在一定的条件下也会生锈,故选项正确;
B、合金的熔点一般比各成分金属低,故选项正确;
C、合金不一定是金属和金属熔合而成,合金可以是金属与非金属熔合而成的物质,故选项错误;
D、控制条件可制成性能不同的合金,例如控制铁的合金中的含碳量,可以制得性能不同的生铁和钢,故选项正确。
故选C。
6.C
【详解】
A、木炭粉和氧化铜粉都是黑色的,观察颜色无法区分,不符合题意;
B、氧气和二氧化碳都是无味的,闻气味无法区分,不符合题意;
C、黄铜是铜的合金,合金比组成它的纯金属的硬度大,可用相互刻画的方法区分,符合题意;
D、实验室禁止品尝药品的味道,防止发生危险,不符合题意。
故选C。
7.C
【解析】
A、该纪念币材质为多种贵金属包钢铸造,属于合金,是金属材料,正确;B、合金中含有金属,具有导电性,属于导体,正确;C、合金属于混合物,错误;D、该纪念币是包钢合金,抗腐蚀性能比铁强,正确。故选C。
8.D
【详解】
在金属活动性顺序表中四种金属的活动性顺序为锌、铁、铜、银。故活动性最强的是锌,选D。
9.A
【详解】
A、用石墨制金刚石,产生了新的物质,属于化学变化;
B、干冰升华是固态二氧化碳变为气态二氧化碳,没有产生新的物质,不属于化学变化;
C、铁杵磨成针只是铁的形状改变了,没有产生新的物质,不属于化学变化;
D、铜和锌制成合金是铜和锌按照一定方法制成的,没有产生新的物质,不属于化学变化。
故选A。
10.B
【详解】
解:A、合金是一种金属与其它金属或非金属熔合而成具有金属特性的物质,选项A正确;
B、焊锡的熔点较低,常用做焊接金属,选项B不正确;
C、生铁的含碳量高于钢的含碳量,所以其含铁量钢较高,选项C正确;
D、钛合金与人体有很好的“相容性”,使用后不产生排异反应,因此可用来制造人造骨骼,选项D正确;
故选B。
11.A
【分析】
碳酸钙高温生成氧化钙和二氧化碳。
【详解】
A、火灾发生时,电梯的供电系统在火灾发生时会随时断电,旅客不能乘电梯逃生,应该从安全通道逃生,故A不正确;
B、大理石的主要成分是碳酸钙,受热分解生成氧化钙和二氧化碳,左塔的大理石受热分解而被损毁,故B正确;
C、木材具有可燃性,木质塔尖属于可燃物,故C正确;
D、合金硬度比组成纯金属大,尖顶上的钢公鸡为铜合金制品,其硬度比纯铜大,故D正确。故选A。
12.C
【详解】
A、甲实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大,正确;
B、氨水和酚酞试液没有接触,酚酞变红,说明分子是运动的,正确;
C、丙实验既可以说明二氧化碳易溶于水,但不能说明二氧化碳具有酸性,错误;
D、铁能与硫酸铜反应生成红色的铜和硫酸亚铁,且反应前后烧杯中物质总质量不变,可以验证质量守恒定律,正确;
故选C。
13.A
【详解】
A、黄铜和铜的硬度不同,互相刻画的方法可以鉴别,相互刻画时,痕迹更明显的是铜,正确;
B、用扇子扇灭蜡烛,是因为降低了蜡烛的温度至其着火点以下,不是降低着火点,错误;
C、碳用于冶金工业,利用了它的还原性,错误;
D、氧气有助燃性,可以用作助燃剂,不能用作燃料,错误;
故选A。
14.B
【详解】
硬币作为货币的一种,使用环境复杂、使用范围较广、使用寿命不易过短,这就要求硬币应具有化学性质相对稳定不易被腐蚀、不易锈蚀的特点;同时不易变形、不易碎裂,因此所用金属还要有一定的硬度和强度;而作为货币,还要要求所使用的金属价格要与硬币面值相吻合,而与金属的颜色无太大关系。
故选B。
15.A
【详解】
A、将甲烷气体燃烧,在干燥的烧杯壁上有水珠产生,说明甲烷中含有氢元素,但是无法说明甲烷中含有碳元素,错误;
B、黄铜片能在铜片上能够有划痕产生,能够验证合金硬度比纯金属大,正确;
C、另一端的石蕊试液变红说明氯化氢分子发生了运动,正确;
D、图示是一个密闭系统能够验证质量守恒定律,正确;
故选A。
16.D
【分析】
合金的硬度大于其成分金属,熔点低于其成分金属,抗腐蚀性优于其成分金属,根据铝锂合金是航空飞行器较理想的结构材料之一来分析其所具备的特点。
【详解】
铝锂合金是航空飞行器较理想的结构材料之一,说明其耐腐蚀强、密度小、硬度大、强度高,和其易导电性无关。
故选:D。
17.2Na+ Hg 3Cl2
【详解】
(1)离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,在其离子符号前加上相应的数字,故2个钠离子可表示:2Na+;
(2)熔点最低的金属是汞,其化学式为:Hg;
(3)分子的表示方法是正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则三个氯分子可表示:3Cl2;
(4)化合价的表示方法是在该元素的上方用正负号和数字表示,正负号在前,数字在后,故过氧化氢中氢元素的化合价为+1价可表示为:。
18.< > < =
【详解】
(1)生铁和钢都是铁和碳的合金,含碳量生铁大于钢,含铁量生铁小于钢,故填:<;
(2)地壳中元素含量由多到少的顺序为:氧、硅、铝、铁等,故填:>;
(3)空气中二氧化碳的体积分数为0.03%,稀有气体的体积分数为0.94%,故填:<;
(4)甲醛中碳元素的质量分数为:=40%,醋酸中碳元素的质量分数为:=40%,故填:=。
19.2%~4.3% 混合物 利于铁水中的碳和空气中的氧气反应生成二氧化碳跑掉从而减少铁水中的含碳量 导热 导电
【详解】
(1)根据铁中含有的碳的质量分数的大小,把铁的合金分为生铁和钢;含碳量在2%~4.3%之间的属于生铁,含碳量在0.03%~2%之间的属于钢,故钢是混合物;
(2)将生铁加热到液态或半液态并不断搅拌可以增加反应物的接触面积,加快反应的进行,利于铁水中的碳和空气中的氧气反应生成二氧化碳跑掉从而减少铁水中的含碳量;
(3)装木柄,是因为铁具有良好的导热性;电工用的钳子必须装上橡胶柄是因为铁有导电性。
20.Ag Hg Al Ca 纯净物 化学 a
【详解】
(1).该银白色金属是银:Ag;
液体金属是汞:Hg;
地壳中含量最高的金属元素是铝:Al;
人体中含量最多的金属元素是钙:Ca。
(2).合金中的Mg会和氧气发生反应:;
该镁铝合金具有化学式,有固定的组成,属于纯净物;
储氢过程中生成了MgH2和Al,属于化学变化过程。
(3).合金的熔点比组成合金的纯金属的低,所以a能表示锡铅合金。
(4). 。
21.延展性和导电性 人工降雨 燃烧不一定需要氧气参加,一般情况下不支持燃烧的气体,在特殊情况下,也能参加燃烧 碳原子的排列方式不同 ab
【详解】
(1)①铜可用于制作导线,体现了金属铜的导电性和延展性;
(2)①干冰升华吸热,可用于人工降雨或做制冷剂;
②镁条在二氧化碳中燃烧生成氧化镁和一种黑色固体,根据质量守恒定律,化学反应前后,元素的种类、数量不变,故黑色固体为碳,反应的化学方程式是:;
③镁可以在二氧化碳中燃烧,说明燃烧不一定需要氧气参加,再者,二氧化碳一般情况下不支持燃烧,但在特殊情况下,也能参加燃烧;故填:燃烧不一定需要氧气参加,一般情况下不支持燃烧的气体,在特殊情况下,也能参加燃烧;
(3)①金刚石硬度很大、石墨硬度很小,是因为碳原子的排列方式不同,故物理性质有很大差异;
②a、C60由C60分子构成,1个C60分子由60个碳原子构成,符合题意;
b、C60的相对分子质量为:12×60=720,符合题意;
c、C60只由碳一种元素组成,属于单质,不符合题意。
故选ab。
22.CD 2H2+O22H2O 燃烧产物是水,对环境无污染 2H2O+SO2+I2=H2SO4+2HI 分解反应 I2 90kg
【详解】
(1)①涤纶和合成橡胶属于合成材料;铜和铝合金属于金属材料;故填:CD;
②氢气与氧气在催化剂的作用下生成水;故填:2H2+O22H2O;
③氢气的热值高,氢气燃烧生成水,对环境无污染;故填:燃烧产物是水,对环境无污染;
(2)主反应器中反应是水和二氧化硫以及碘反应生成硫酸和碘化氢,对应的化学方程式是 2H2O+SO2+I2=H2SO4+2HI.膜反应器中是碘化氢分解为氢气和碘,为一变多,符合分解反应特征,属于分解反应。该工艺流程中,开始碘作为反应物,后来是生成物,所以能被循环利用的物质是 I2.故填:2H2O+SO2+I2=H2SO4+2HI;分解反应; I2;
(3)解:设需要水的质量为x,则:
x=90kg
答:理论上需要水90kg。
23.AB 化学能转化为内能转化为机械能再转化为电能 6NH4Cl+4Fe2O3△6Fe +3N2↑+12H2O+2FeCl3 -3价变为0价 SO2、CO、NO2
【解析】
(1)蛟龙号的大部分材料由钛合金构成,这是因为它抗腐蚀性优于不锈钢,密度小、机械性能好;(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是化学能转化为内能转化为机械能再转化为电能,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,根据质量守恒定律可知:氯化铵和氧化铁在加热的条件下反应生成铁、氮气、水和氯化铁,该反应的化学方程式为6NH4Cl+4Fe2O3△6Fe +3N2↑+12H2O+2FeCl3,反应前后氮元素的化合价变化-3价变为0价;(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少SO2、CO、NO2等有害气体的排放,可极大限度地减少空气污染。
24.酒精喷灯 玻璃管内红棕色粉末逐渐变为黑色 澄清石灰水变浑浊 没有达到反应所需的温度 1.68g 解:设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。 Fe3O4
【详解】
(1)根据资料信息,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,反应条件是高温,因此仪器甲应选用的加热仪器是:酒精喷灯;因为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,氧化铁是红棕色,铁粉是黑色,二氧化碳能使澄清石灰水变浑浊,所以图1装置中的现象有:玻璃管内红棕色粉末逐渐变为黑色;澄清石灰水变浑浊。
(2)①因为一氧化碳和氧化铁反应必须达到一定的温度,在0~400℃温度范围内,管内固体质量不变,其原因是:没有达到反应所需的温度。
②图中x是氧化铁完全反应转变成铁的质量。设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。
③图中A点固体与氧化铁的质量差就是减少的氧元素质量,根据化学式Fe2O3,2.4g氧化铁中,铁元素质量= =1.68g,氧元素的质量=2.4g-1.68g=0.72g。到A点固体质量为2.32g,则A点固体中铁元素的质量仍为1.68g,氧元素的质量=0.72g-(2.40g-2.32g)=0.64g,假设A点固体中物质的化学式是FemOn, 则A点固体中物质的化学式是Fe3O4。
一、选择题(共16题)
1.生活中的下列物品,其制作材料属于合金的是( )
A.金刚石钻头 B.钢化玻璃杯 C.不锈钢锅 D.瓷器
2..下列物质不属于合金的是( )
A.焊锡 B.硬铝 C.不锈钢 D.四氧化三铁
3.某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属丝,当玻璃被击碎时,产生电信号,与金属丝相连的警报系统就会立即报警,这是利用了金属的( )
A.延展性
B.导电性
C.导热性
D.可燃性
4.下列不属于金属材料的是( )
A.黄铜 B.不锈钢 C.四氧化三铁 D.黄金
5.下列关于合金的说法不正确的是( )
A.不锈钢在一定的条件下也会生锈 B.合金的熔点一般低于各成分金属
C.合金一定是由多种金属熔合而成 D.控制条件可制成性能不同的合金
6.下列区分物质的方法正确的是( )
A.用观察法区分木炭粉和氧化铜粉
B.用闻气味的方法区分氧气和二氧化碳气体
C.用相互刻画的方法区分纯铜和黄铜
D.用尝味道的方法区分实验室里的氯化钠和蔗糖
7.如图是中国人民抗日战争暨世界反法西斯战争胜利70周年发行的纪念币。该纪念币材质为多种贵金属包钢铸造,属于金属合金。下列相关说法不正确的是( )
A.从物质的材料角度看,该纪念币属于金属材料
B.从物质的导电性角度看,该纪念币属于导体
C.从物质的分类角度看,该纪念币属于金属单质
D.从金属的防锈角度看,该纪念币比铁抗腐蚀性能强
8.我省明代科学家宋应星所著的《天工开物》中,详细记述了金、铜、铁、锌等金属的开采和冶炼方法,记述的金属中金属活动性最强的是( )
A.金 B.钢 C.铁 D.锌
9.生活中的下列现象,属于化学变化的是( )
A.用石墨制金刚石 B.干冰升华 C.铁杵磨成针 D.铜和锌制成合金
10.下列有关金属材料的说法,不正确的是( )
A.合金不一定是金属和金属熔合而成
B.焊锡有很好的抗腐蚀性,常用做焊接金属
C.生铁的含碳量比钢高
D.钛合金与人体有很好的“相容性”,因此可用来制造人造骨骼
11.2019年4月15日傍晚,有着800多年历史的巴黎圣母院被熊熊大火吞噬,精美绝伦的木质塔尖在世人的叹息声中轰然坍塌,而大理石质地的左塔也损毁严重,下列有关说法中错误的是( )
A.火灾发生时,旅客应该赶紧乘电梯逃生
B.左塔的大理石受热分解而被损毁
C.木质塔尖属于可燃物
D.尖顶上的钢公鸡为铜合金制品,其硬度比纯铜大
12.下列实验得出的结论不合理的是( )
A.实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大
B.实验中酚酞溶液变红,可以说明分子在不断运动
C.实验中既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性
D.实验中既可以说明铁能与硫酸铜反应,又可以验证质量守恒定律
13.学习化学,应用化学。以下说法正确的是( )
A.用相互刻画的方法可以鉴别黄铜和铜
B.扇子能扇灭蜡烛火焰是因为降低了蜡烛的着火点
C.碳用于冶金工业,利用了它的可燃性
D.氧气有助燃性,可以用作燃料
14.金属铜、镍、铝等常用作制作硬币,我国一元币为钢芯镀镍合金,五角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时,不需要考虑的因素是( )
A.金属的耐腐蚀性 B.金属的颜色
C.金属的硬度 D.金属价格与硬币面值的吻合度
15.下列实验方案,不能达到相应实验目的是( )
A.验证甲烷中含有碳、氢两种元素
B.验证合金硬度比纯金属大
C.验证氯化氢分子发生了运动
D.验证质量守恒定律
16.铝锂合金是航空飞行器较理想的结构材料之一。铝锂合金具有的以下性质中,与该应用无关的是( )
A.硬度大 B.耐腐蚀 C.密度小 D.易导电
二、非选择题(共8题)
17.用化学符号填空:
(1)2个钠离子______;
(2)熔点最低的金属______;
(3)3个氯分子______;
(4)过氧化氢中氢元素的化合价为+1价______。
18.各种物质间存在着某种联系:
(1)含铁量:生铁_______钢(填“>”、“<”或“=”,下同);
(2)地壳中元素含量:硅元素________铁元素;
(3)空气中体积分数:二氧化碳_______稀有气体:
(4)碳元素的质量分数:甲醛(CH2O)_______醋酸(C2H4O2)。
19.从楚王陵中出土的铁器中发现了迄今世界上最早的炒钢技术,说明中国早在公元前2世纪就掌握了炒钢技术。炒钢是一种冶炼技术,冶炼时先将生铁加热到液态或半液态,然后靠鼓风 ,降低生铁的含碳量,使其成钢。由于在冶炼中要不断搅拌,好象炒菜一样,因而得名。
(1)生铁的含碳量为______,炼得的钢是_____(选填“纯净物”或“混合物”)。
(2)将生铁加热到液态或半液态并不断搅拌的原因是什么?____
(3)炒菜用的铁铲,一般要装上木柄,是因为铁具有______性,而电工用的钳子必须装上橡胶柄是因为铁有______性。
20.人类的生产、生活离不开金属。
(1)家用热水瓶内胆壁的银白色金属是________(填符号,下同);液体金属是__________;地壳中含量最高的金属元素是_______,人体中含量最多的金属元素是________。
(2)镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是_____(任写一个化学方程式)。该合金属于______(填“混合物”或“纯净物”),它是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于________(填“物理”或“化学”)变化。
(3)合金的很多性能与组成它们的纯金属不同。如图能表示锡铅合金的是________(填序号“a”“b”或“c”)。
(4)铝冶炼厂以氧化铝为原料,在熔融状态下电解生成铝和一种常见的气体,其反应的化学方程式为________。
21.“见著知微,见微知著”是化学的思维方法。
(1)铜是生活中常见的一种金属
①铜可用以制作导线,体现了金属铜的_____性。
(2)固态的二氧化碳俗称“干冰”
①请写出干冰的一种用途_______;
②镁条在二氧化碳中燃烧生成氧化镁和一种黑色粉末,写出反应的化学方程式_____;
③通过这个反应,谈谈你对物质燃烧的新认识________。
(3)物质的性质决定用途,用途反映物质的性质。
①金刚石硬度很大、石墨硬度很小,两者物理性质有较大差异的原因_____。
②下列关于足球烯(C60)的说法正确的是______。
a 它的一个分子中含有60个碳原子
b 相对分子质量是720
c 它是一种化合物
22.开发利用氢能源是实现可持续发展的需要。根据图示分析,回答问题:
①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是_____(填序号)。
a.涤纶靠垫 b.橡胶轮胎 c.铜质导线 d.铝合金轮毂
②氢燃料电池的工作原理是:将氢气、氧气送到燃料电池中,经过催化剂的作用,发生反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式_____。
③氢气作燃料的优点是_____。
(2)工业上可通过下列工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。
主反应器中反应的化学方程式是_____。膜反应器中的基本反应类型是_____。该工艺流程中,能被循环利用的物质是_____。
(3)采用电解水的方式制备10Kg氢气,理论上需要水的质量是多少千克?____
23.随着我国深潜器“蛟龙”号考察任务(考察可燃冰的海底出口)顺利完成,我国的“蓝鲸1号”在南海首次试采俗称可燃冰的天然气水合物也获得圆满成功。
(1)蛟龙号的大部分材料由钛合金构成,这是因为它____;(多选)
A.抗腐蚀性优于不锈钢 B.密度小、机械性能好 C.导电性好、硬度大
(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是____;“蓝鲸1号”整体用钢达40000多吨,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,该反应的化学方程式为____,反应前后氮元素的化合价变化为____。
(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少______(至少填两种物质的化学式)等有害气体的排放,可极大限度地减少空气污染。
24.已知在不同的温度下,CO与铁的氧化物反应能生成另一种铁的氧化物(或铁单质)和CO2。现利用下图1的实验装置进行实验,反应过程中管内的固体质量随温度的变化曲线如图2。
注:图1中的仪器甲是一种加热仪器,图2中A、B点的固体组成分别是FeO、Fe3O4中的一种。
(1)查阅资料发现,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,仪器甲应选用的加热仪器是_____(填“酒精灯”或“酒精喷灯”);图1装置中的现象有____;________。
(2)利用图2显示的相关信息,回答如下问题:
①在0~400℃温度范围内,管内固体质量不变,其原因是________。
②图中x=__g。
计算过程:_____
③试据图计算并推断出A点固体的化学式是______。
参考答案
1.C
【详解】
A、 金刚石钻头,是由碳元素组成的,不属于合金,故选项错误;B、玻璃杯是硅酸盐产品,不属于合金,故选项错误;C、不锈钢是钢的一种,是铁的合金,故选项正确;D、陶瓷是用泥土烧制而成的,属于无机非金属材料,不属于合金,故选项错误。故选C。
2.D
【详解】
A、焊锡是锡和铅的合金,属于合金,故A正确;
B、硬铝是铝的一种合金,属于合金,故B正确;
C、不锈钢中含有铁、铬、碳,属于合金,属于合金,故C正确;
D、四氧化三铁是金属化合物,所以不是合金,不属合金,故D错误。故选D。
3.B
【详解】
与金属丝相连的警报系统就会立即报警,是利用了金属的导电性。故选B。
4.C
【分析】
金属材料包括纯金属和合金。
【详解】
A.黄铜是铜的合金,属于金属材料,不符合题意。
B.不锈钢是铁的合金,属于金属材料,不符合题意。
C.四氧化三铁是铁的化合物,不属于金属材料,符合题意。
D.黄金属于纯金属,属于金属材料,不符合题意。
故选:C。
5.C
【详解】
A、不锈钢在一定的条件下也会生锈,故选项正确;
B、合金的熔点一般比各成分金属低,故选项正确;
C、合金不一定是金属和金属熔合而成,合金可以是金属与非金属熔合而成的物质,故选项错误;
D、控制条件可制成性能不同的合金,例如控制铁的合金中的含碳量,可以制得性能不同的生铁和钢,故选项正确。
故选C。
6.C
【详解】
A、木炭粉和氧化铜粉都是黑色的,观察颜色无法区分,不符合题意;
B、氧气和二氧化碳都是无味的,闻气味无法区分,不符合题意;
C、黄铜是铜的合金,合金比组成它的纯金属的硬度大,可用相互刻画的方法区分,符合题意;
D、实验室禁止品尝药品的味道,防止发生危险,不符合题意。
故选C。
7.C
【解析】
A、该纪念币材质为多种贵金属包钢铸造,属于合金,是金属材料,正确;B、合金中含有金属,具有导电性,属于导体,正确;C、合金属于混合物,错误;D、该纪念币是包钢合金,抗腐蚀性能比铁强,正确。故选C。
8.D
【详解】
在金属活动性顺序表中四种金属的活动性顺序为锌、铁、铜、银。故活动性最强的是锌,选D。
9.A
【详解】
A、用石墨制金刚石,产生了新的物质,属于化学变化;
B、干冰升华是固态二氧化碳变为气态二氧化碳,没有产生新的物质,不属于化学变化;
C、铁杵磨成针只是铁的形状改变了,没有产生新的物质,不属于化学变化;
D、铜和锌制成合金是铜和锌按照一定方法制成的,没有产生新的物质,不属于化学变化。
故选A。
10.B
【详解】
解:A、合金是一种金属与其它金属或非金属熔合而成具有金属特性的物质,选项A正确;
B、焊锡的熔点较低,常用做焊接金属,选项B不正确;
C、生铁的含碳量高于钢的含碳量,所以其含铁量钢较高,选项C正确;
D、钛合金与人体有很好的“相容性”,使用后不产生排异反应,因此可用来制造人造骨骼,选项D正确;
故选B。
11.A
【分析】
碳酸钙高温生成氧化钙和二氧化碳。
【详解】
A、火灾发生时,电梯的供电系统在火灾发生时会随时断电,旅客不能乘电梯逃生,应该从安全通道逃生,故A不正确;
B、大理石的主要成分是碳酸钙,受热分解生成氧化钙和二氧化碳,左塔的大理石受热分解而被损毁,故B正确;
C、木材具有可燃性,木质塔尖属于可燃物,故C正确;
D、合金硬度比组成纯金属大,尖顶上的钢公鸡为铜合金制品,其硬度比纯铜大,故D正确。故选A。
12.C
【详解】
A、甲实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大,正确;
B、氨水和酚酞试液没有接触,酚酞变红,说明分子是运动的,正确;
C、丙实验既可以说明二氧化碳易溶于水,但不能说明二氧化碳具有酸性,错误;
D、铁能与硫酸铜反应生成红色的铜和硫酸亚铁,且反应前后烧杯中物质总质量不变,可以验证质量守恒定律,正确;
故选C。
13.A
【详解】
A、黄铜和铜的硬度不同,互相刻画的方法可以鉴别,相互刻画时,痕迹更明显的是铜,正确;
B、用扇子扇灭蜡烛,是因为降低了蜡烛的温度至其着火点以下,不是降低着火点,错误;
C、碳用于冶金工业,利用了它的还原性,错误;
D、氧气有助燃性,可以用作助燃剂,不能用作燃料,错误;
故选A。
14.B
【详解】
硬币作为货币的一种,使用环境复杂、使用范围较广、使用寿命不易过短,这就要求硬币应具有化学性质相对稳定不易被腐蚀、不易锈蚀的特点;同时不易变形、不易碎裂,因此所用金属还要有一定的硬度和强度;而作为货币,还要要求所使用的金属价格要与硬币面值相吻合,而与金属的颜色无太大关系。
故选B。
15.A
【详解】
A、将甲烷气体燃烧,在干燥的烧杯壁上有水珠产生,说明甲烷中含有氢元素,但是无法说明甲烷中含有碳元素,错误;
B、黄铜片能在铜片上能够有划痕产生,能够验证合金硬度比纯金属大,正确;
C、另一端的石蕊试液变红说明氯化氢分子发生了运动,正确;
D、图示是一个密闭系统能够验证质量守恒定律,正确;
故选A。
16.D
【分析】
合金的硬度大于其成分金属,熔点低于其成分金属,抗腐蚀性优于其成分金属,根据铝锂合金是航空飞行器较理想的结构材料之一来分析其所具备的特点。
【详解】
铝锂合金是航空飞行器较理想的结构材料之一,说明其耐腐蚀强、密度小、硬度大、强度高,和其易导电性无关。
故选:D。
17.2Na+ Hg 3Cl2
【详解】
(1)离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,在其离子符号前加上相应的数字,故2个钠离子可表示:2Na+;
(2)熔点最低的金属是汞,其化学式为:Hg;
(3)分子的表示方法是正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则三个氯分子可表示:3Cl2;
(4)化合价的表示方法是在该元素的上方用正负号和数字表示,正负号在前,数字在后,故过氧化氢中氢元素的化合价为+1价可表示为:。
18.< > < =
【详解】
(1)生铁和钢都是铁和碳的合金,含碳量生铁大于钢,含铁量生铁小于钢,故填:<;
(2)地壳中元素含量由多到少的顺序为:氧、硅、铝、铁等,故填:>;
(3)空气中二氧化碳的体积分数为0.03%,稀有气体的体积分数为0.94%,故填:<;
(4)甲醛中碳元素的质量分数为:=40%,醋酸中碳元素的质量分数为:=40%,故填:=。
19.2%~4.3% 混合物 利于铁水中的碳和空气中的氧气反应生成二氧化碳跑掉从而减少铁水中的含碳量 导热 导电
【详解】
(1)根据铁中含有的碳的质量分数的大小,把铁的合金分为生铁和钢;含碳量在2%~4.3%之间的属于生铁,含碳量在0.03%~2%之间的属于钢,故钢是混合物;
(2)将生铁加热到液态或半液态并不断搅拌可以增加反应物的接触面积,加快反应的进行,利于铁水中的碳和空气中的氧气反应生成二氧化碳跑掉从而减少铁水中的含碳量;
(3)装木柄,是因为铁具有良好的导热性;电工用的钳子必须装上橡胶柄是因为铁有导电性。
20.Ag Hg Al Ca 纯净物 化学 a
【详解】
(1).该银白色金属是银:Ag;
液体金属是汞:Hg;
地壳中含量最高的金属元素是铝:Al;
人体中含量最多的金属元素是钙:Ca。
(2).合金中的Mg会和氧气发生反应:;
该镁铝合金具有化学式,有固定的组成,属于纯净物;
储氢过程中生成了MgH2和Al,属于化学变化过程。
(3).合金的熔点比组成合金的纯金属的低,所以a能表示锡铅合金。
(4). 。
21.延展性和导电性 人工降雨 燃烧不一定需要氧气参加,一般情况下不支持燃烧的气体,在特殊情况下,也能参加燃烧 碳原子的排列方式不同 ab
【详解】
(1)①铜可用于制作导线,体现了金属铜的导电性和延展性;
(2)①干冰升华吸热,可用于人工降雨或做制冷剂;
②镁条在二氧化碳中燃烧生成氧化镁和一种黑色固体,根据质量守恒定律,化学反应前后,元素的种类、数量不变,故黑色固体为碳,反应的化学方程式是:;
③镁可以在二氧化碳中燃烧,说明燃烧不一定需要氧气参加,再者,二氧化碳一般情况下不支持燃烧,但在特殊情况下,也能参加燃烧;故填:燃烧不一定需要氧气参加,一般情况下不支持燃烧的气体,在特殊情况下,也能参加燃烧;
(3)①金刚石硬度很大、石墨硬度很小,是因为碳原子的排列方式不同,故物理性质有很大差异;
②a、C60由C60分子构成,1个C60分子由60个碳原子构成,符合题意;
b、C60的相对分子质量为:12×60=720,符合题意;
c、C60只由碳一种元素组成,属于单质,不符合题意。
故选ab。
22.CD 2H2+O22H2O 燃烧产物是水,对环境无污染 2H2O+SO2+I2=H2SO4+2HI 分解反应 I2 90kg
【详解】
(1)①涤纶和合成橡胶属于合成材料;铜和铝合金属于金属材料;故填:CD;
②氢气与氧气在催化剂的作用下生成水;故填:2H2+O22H2O;
③氢气的热值高,氢气燃烧生成水,对环境无污染;故填:燃烧产物是水,对环境无污染;
(2)主反应器中反应是水和二氧化硫以及碘反应生成硫酸和碘化氢,对应的化学方程式是 2H2O+SO2+I2=H2SO4+2HI.膜反应器中是碘化氢分解为氢气和碘,为一变多,符合分解反应特征,属于分解反应。该工艺流程中,开始碘作为反应物,后来是生成物,所以能被循环利用的物质是 I2.故填:2H2O+SO2+I2=H2SO4+2HI;分解反应; I2;
(3)解:设需要水的质量为x,则:
x=90kg
答:理论上需要水90kg。
23.AB 化学能转化为内能转化为机械能再转化为电能 6NH4Cl+4Fe2O3△6Fe +3N2↑+12H2O+2FeCl3 -3价变为0价 SO2、CO、NO2
【解析】
(1)蛟龙号的大部分材料由钛合金构成,这是因为它抗腐蚀性优于不锈钢,密度小、机械性能好;(2)“蓝鲸1号”钻井平台使用了燃油发电机,则其发电时的能量转化全过程是化学能转化为内能转化为机械能再转化为电能,在钢铁焊接时,常使用焊药(氯化铵)在加热时除去钢铁表面的氧化物(视为氧化铁),使焊接更加牢固,同时生成金属单质、空气中含量最多的气体、一种常见液体和氯化铁,根据质量守恒定律可知:氯化铵和氧化铁在加热的条件下反应生成铁、氮气、水和氯化铁,该反应的化学方程式为6NH4Cl+4Fe2O3△6Fe +3N2↑+12H2O+2FeCl3,反应前后氮元素的化合价变化-3价变为0价;(3)可燃冰被认为是比天然气还要清洁的能源,与煤、汽油、柴油等能源相比,可燃冰燃烧会减少SO2、CO、NO2等有害气体的排放,可极大限度地减少空气污染。
24.酒精喷灯 玻璃管内红棕色粉末逐渐变为黑色 澄清石灰水变浑浊 没有达到反应所需的温度 1.68g 解:设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。 Fe3O4
【详解】
(1)根据资料信息,酒精灯加热时玻璃管的受热温度是400~500℃,酒精喷灯加热时玻璃管的受热温度是800~1200℃。实验室要利用图1来制取金属铁,反应条件是高温,因此仪器甲应选用的加热仪器是:酒精喷灯;因为一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,氧化铁是红棕色,铁粉是黑色,二氧化碳能使澄清石灰水变浑浊,所以图1装置中的现象有:玻璃管内红棕色粉末逐渐变为黑色;澄清石灰水变浑浊。
(2)①因为一氧化碳和氧化铁反应必须达到一定的温度,在0~400℃温度范围内,管内固体质量不变,其原因是:没有达到反应所需的温度。
②图中x是氧化铁完全反应转变成铁的质量。设完全反应生成铁的质量为x.
解得x=1.68g
答:完全反应生成的铁质量为1.68g。
③图中A点固体与氧化铁的质量差就是减少的氧元素质量,根据化学式Fe2O3,2.4g氧化铁中,铁元素质量= =1.68g,氧元素的质量=2.4g-1.68g=0.72g。到A点固体质量为2.32g,则A点固体中铁元素的质量仍为1.68g,氧元素的质量=0.72g-(2.40g-2.32g)=0.64g,假设A点固体中物质的化学式是FemOn, 则A点固体中物质的化学式是Fe3O4。
同课章节目录
