9.1生命必需的营养物质基础练习-2021-2022学年九年级化学仁爱版下册(含解析)
文档属性
| 名称 | 9.1生命必需的营养物质基础练习-2021-2022学年九年级化学仁爱版下册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 398.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-02 00:00:00 | ||
图片预览



文档简介
9.1生命必需的营养物质
一、选择题(共16题)
1.下列说法正确的是( )
A.用洗洁精清洗油渍,目的是和油渍反应
B.称为糖类的有机物都有甜味
C.在积雪路面撒盐,目的是提高沸点
D.合金的熔点一般比组成金属低,如做保险丝的武德合金
2.下列食物中,富含蛋白质的是( )
A.馒头 B.苹果 C.鱼肉 D.白菜
3.下列说法正确的是
A.铁、钙、锰、碘等为常见微量元素
B.1mL水与1mL酒精混合后的总体积等于2mL
C.实验室用高锰酸钾制取氧气完毕,应该先熄灭酒精灯,再拿出导管
D.二氧化碳不供给呼吸,因此在人群密集的地方注意通风
4.下列河南特产中富含维生素的是( )
A.原阳大米
B.黄河鯉鱼
C.叶县岩盐
D.灵宝苹果
5.对于人体必需元素,我们也要注意合理摄入,摄入不足或过量均不利于人体健康。下列有关几种人体必需元素对人体健康的影响,说法正确的是( )
A.缺锌会引起佝偻病、骨质疏松 B.缺钙会引起贫血
C.缺氟会引起龋齿 D.缺铁会引起甲状腺肿大
6.下列做法不正确的是( )
A.高温煮沸,杀菌消毒 B.垃圾回收,资源再生
C.煤气泄漏,开灯检查 D.油锅着火,锅盖盖灭
7.归纳与总结是学好化学的重要方法。下列对所学知识的整理,存在错误的是( )
A.物质与其构成粒子的对应关系:
①金——由原子构成
②二氧化碳——由分子构成
B.物质性质与用途的对应关系:
①氧气能助燃——作高能燃料
②氮气化学性质稳定——充入食品包装中以防腐
C.有关“污染源——污染物——解决策略”的对应关系:
①吸烟——尼古丁和一氧化碳——戒烟
②霉变食物——黄曲霉素——不食用
D.物质利用与环境保护的关系:
①使用乙醇汽油——减少汽车尾气污染
②合理使用农药、化肥——减少水污染
8.元素周期表中锌元素的某些信息如图所示,下列有关锌的说法正确的是( )
A.锌离子核外有 30 个电子
B.锌的相对原子质量为65.38g
C.锌原子核内的中子数为30
D.缺锌可能引起发育迟缓,智力低下,得侏儒症
9.化学与人类健康关系密切。下列说法正确的是( )
A.用甲醛溶液保存海鲜
B.人体缺碘易患夜盲症
C.水果、蔬菜能提供多种维生素
D.霉变的大米淘洗后可食用
10.“珍爱生命,远离毒品”。冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为)。有关甲基苯丙胺的说法正确的是( )
A.属于混合物 B.属于有机物
C.一个分子中原子总数为25 D.燃烧只生成二氧化碳和水
11.下列关于人体健康的叙述错误的是( )
A.缺乏维生素C会患夜盲症
B.正常人胃液的pH在0.9-1.5
C.吸烟容易得肺气肿、肺癌
D.老年人缺钙易发生骨质疏松
12.下列做法不利于人体健康的是( )
A.食用用氢氧化钠溶液漂洗的鸡爪 B.食用适量含碘海产品
C.青少年每天饮用奶制品,增加营养 D.焙制糕点时添加适量小苏打
13.下列知识整理的内容完全正确的一组是( )
A.除杂的方法 B.物质与俗名
铜粉中混有铁粉﹣﹣﹣用磁铁充分吸引 FeCl2溶液中混有CuCl2﹣﹣﹣加过量的铁粉 CaCO3中混有NaCl﹣﹣﹣加足量水溶解后过滤 氧化钙﹣﹣﹣生石灰 氢氧化钠﹣﹣﹣纯碱 氢氧化钙﹣﹣﹣消石灰
C.性质与用途 D.食品与安全
取暖防中毒﹣﹣﹣煤炉上放一壶水 防菜刀生锈﹣﹣﹣干燥后悬挂 延长食物保质期﹣﹣﹣放入冰箱中 亚硝酸钠﹣﹣﹣不能当食盐用 霉变食物﹣﹣﹣高温消毒后可食用 甲醛溶液﹣﹣﹣可作食品保鲜剂
A.A B.B C.C D.D
14.羊毛含有蛋白质在灼烧时会有烧焦羽毛的气味,下列物质灼烧时也会产生该气味的是( )
A.鸭毛 B.植物油 C.青菜 D.馒头
15.下列说法正确的是( )
A.铝制品在空气中耐腐蚀是因为其表面生成了一层致密的氧化物薄膜
B.将霉变的食物处理后再食用,不会影响人体健康
C.黄铜片与铜片相互刻画时,黄铜片上会留下明显的划痕
D.配制一定质量分数的氯化钠溶液,量取水时仰视读数会使得溶液的溶质质量分数偏大
16.在催化剂的作用下,淀粉能与水反应生成葡萄糖.下列能证明部分淀粉已与水反应的试剂是 ( )
①碘水 ②CdSO4溶液 ③NaOH溶液 ④新制Cu(OH) 2 ⑤酒精
A.①② B.②③ C.①④ D.全部
二、综合题(共8题)
17.解释下列生活现象:
(1)干冰常用于人工降雨,利用了干冰_____的性质。
(2)高钙牛奶可以为人体补充每天所需的钙元素,预防老年人患_____(填序号)。
A 贫血 B 龋齿 C 骨质疏松
(3)胃酸过多的病人会服用小苏打片缓解,其反应原理用化学方程式表示为_____。
18.在党中央英明领导下,我国率先抗疫成功,赢得了人民群众的高度赞誉。在阻击疫情的过程中,化学起到了很好的作用。请回答下列问题。
(1)起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子______。
(2)上学时,戴口罩。制作口罩用的无纺布面料主要是聚丙烯(C3H6)n,聚丙烯中碳、氢元素的质量比为______。
(3)到校后,勤消毒。过氧乙酸用于教室消毒,其化学性质不稳定,分解的化学方程式为:,则X的化学式为______。推断依据是______。
(4)用餐时,讲营养。如午餐仅食用米饭、红烧肉、鸡蛋汤、牛奶,从均衡营养角度出发还应补充的一种食物是______。
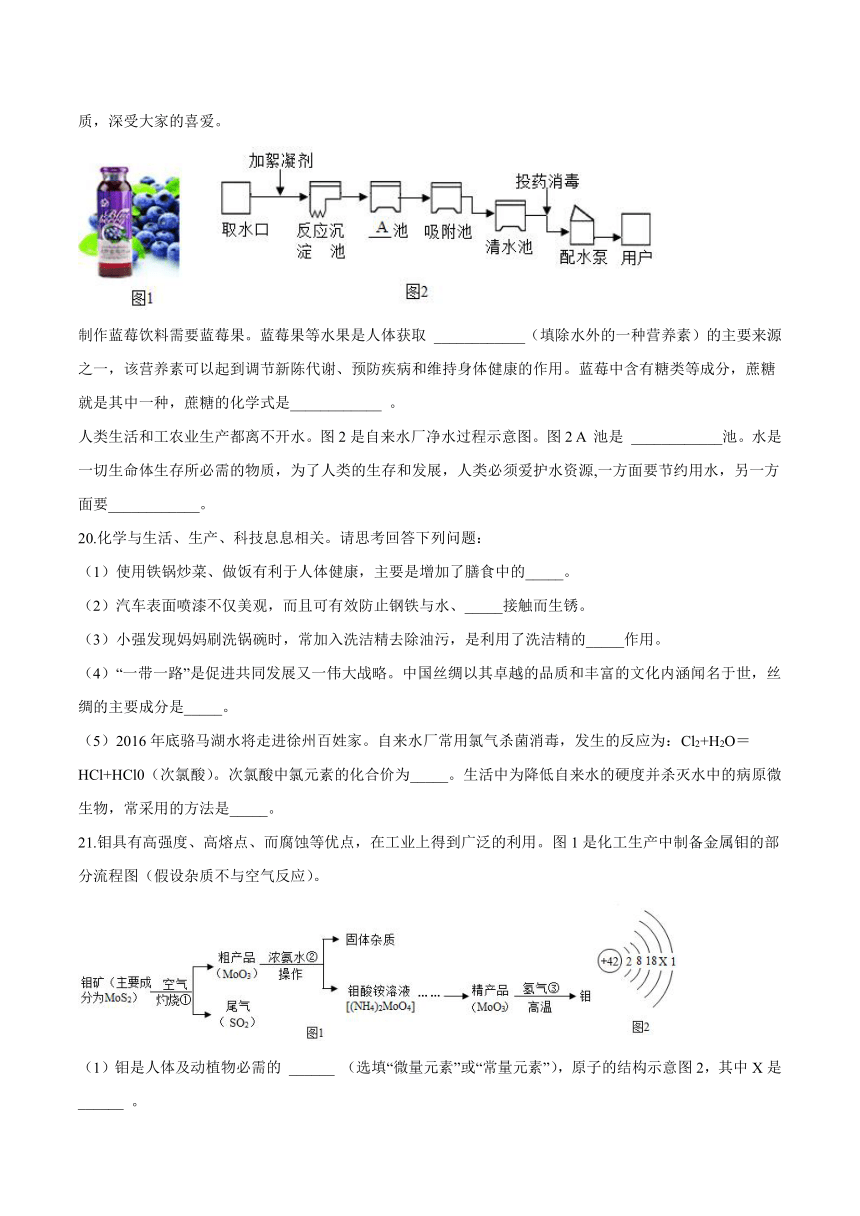
19.黑龙江不仅仅是祖国的大粮仓,绿色食品更是闻名全国。近几年推出的蓝莓系列产品因其天然健康的品质,深受大家的喜爱。
制作蓝莓饮料需要蓝莓果。蓝莓果等水果是人体获取 ____________(填除水外的一种营养素)的主要来源之一,该营养素可以起到调节新陈代谢、预防疾病和维持身体健康的作用。蓝莓中含有糖类等成分,蔗糖就是其中一种,蔗糖的化学式是____________ 。
人类生活和工农业生产都离不开水。图2是自来水厂净水过程示意图。图2 A 池是 ____________池。水是一切生命体生存所必需的物质,为了人类的生存和发展,人类必须爱护水资源,一方面要节约用水,另一方面要____________。
20.化学与生活、生产、科技息息相关。请思考回答下列问题:
(1)使用铁锅炒菜、做饭有利于人体健康,主要是增加了膳食中的_____。
(2)汽车表面喷漆不仅美观,而且可有效防止钢铁与水、_____接触而生锈。
(3)小强发现妈妈刷洗锅碗时,常加入洗洁精去除油污,是利用了洗洁精的_____作用。
(4)“一带一路”是促进共同发展又一伟大战略。中国丝绸以其卓越的品质和丰富的文化内涵闻名于世,丝绸的主要成分是_____。
(5)2016年底骆马湖水将走进徐州百姓家。自来水厂常用氯气杀菌消毒,发生的反应为:Cl2+H2O=HCl+HCl0(次氯酸)。次氯酸中氯元素的化合价为_____。生活中为降低自来水的硬度并杀灭水中的病原微生物,常采用的方法是_____。
21.钼具有高强度、高熔点、而腐蚀等优点,在工业上得到广泛的利用。图1是化工生产中制备金属钼的部分流程图(假设杂质不与空气反应)。
(1)钼是人体及动植物必需的 ______ (选填“微量元素”或“常量元素”),原子的结构示意图2,其中X是 ______ 。
(2)步骤①反应的化学方程式 ______ 。
(3)下列物质可以用来吸收SO2尾气的是 ______ (填字母)。
A 氢氧化钠溶液 B 浓硫酸 C 氨水
(4)(NH4)2MoO4中Mo的化合价是 ______ ,在农业上既是钼肥又是 ______ 肥。
(5)如果在实验室模拟操作Ⅰ,则需要使用的主要玻璃仪器有漏斗、玻璃棒、 ______ 。
(6)利用H2和CO分别还原等质量的精产品(MoO3),所使用的还原剂的质量比为 ______ 。
22.纤维素是一种常见的有机物。
(1)纤维素_____(选填“属于”、“不属于”)糖类物质。
(2)葡萄糖在植物体内会部分转化为纤维素。植物体内的葡萄糖来源于光合作用,请写出反应的化学方程式_____
(3)棉花的主要成分是纤维素,鉴别棉线和羊毛线的方法是_____
(4)科学最新发现,通过简单的化学反应,可以将树木纤维素最终转变为超级储能装置,其中一个反应的微观示意图如下:
①X、Y、Z、W 四种物质中属于单质的是_____
②反应生成的 Z、W 两种物质的质量比为_____
23.如表是100 g某品牌板栗的部分营养成分。
总热量 蛋白质 糖类 油脂 钠 维生素C
1 016 kJ 5.1 g 11.3 g 19 g 4.6 mg 3.3 mg
(1)食物的成分主要有六大类营养素,上表中为人体提供主要能量的是________。
(2)假设该板栗中的钠元素以氯化钠的形式存在,则100 g该板栗中,氯化钠的质量是________?
24.中国有漫长的海岸线,海洋蕴藏着丰富的资源。请按要求填空。
(1)海洋为我们提供了营养丰富的食材。鱼虾富含的 ________ (填一种营养素)是机体生长及修补受损组织的主要原料,海带富含的 _____ (填元素符号)可以预防甲状腺肿大。
(2)我国在海域可燃冰开采技术领域取得重大突破。可燃冰主要含有甲烷水合物,还含少量CO2等气体,可燃冰属于 _______ (选填“纯净物”或“混合物”)。有科学家开采得到一种天然气水合物样品。取50.0克样品放置在一密闭容器内,该样品迅速转化为甲烷气体和水,将甲烷气体分离并完全燃烧,得到17.6克二氧化碳。该天然气水合物样品中甲烷的质量分数为 _____ 。(写出完整的计算过程)
(3)海水淡化可缓解淡水资源匮乏问题。
①水变成水蒸气的过程中,发生变化的是 _______ (填字母序号)。
A分子个数 B分子质量 C分子间隔 D分子种类
②从海水中获得淡水可采取的方法是 ________________ (填“过滤”“吸附”或“蒸馏”)。
(4)海水碳储存,可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减小。
①根据海水pH变化趋势判断:2000年时海水呈 ________ 性。
②“海洋酸化”的原因可用化学方程式表示为 ____ 。
参考答案
1.D
【详解】
A、洗洁精清洗油渍,是乳化原理,不是反应,故A错;
B、称为糖类的有机物不一定有甜味,例如淀粉,故B错;
C、在积雪路面撒盐,目的是降低凝固点,故C错;
D、合金的熔点一般比组成金属低,硬度大,故D正确。
故选D。
2.C
【解析】A、馒头中富含淀粉,淀粉属于糖类,故选项错误;B、苹果中富含维生素,故选项错误;C、鱼肉中富含蛋白质,故选项正确;D、白菜中富含维生素,故选项错误。故选C。
3.D
【详解】
A、钙元素是人体中的常量元素,故A不符合题意;
B、分子间有一定的间隔,1mL水与1mL酒精混合后的总体积小于2mL, 故B不符合题意;
C、实验室用高锰酸钾制取氧气完毕,应该先拿出导管,再熄灭酒精灯,否则容易造成水倒流进热的试管引起试管炸裂,故C不符合题意;
D、二氧化碳不供给呼吸,因此在人群密集的地方二氧化碳的含有高,要注意通风,故D不符合题意;
故选D。
4.D
【详解】
A、原阳大米中富含淀粉,淀粉属于糖类,不符合题意;
B、黄河鲤鱼中富含蛋白质,不符合题意;
C、叶县岩盐中富含无机盐,不符合题意;
D、灵宝苹果中富含维生素,符合题意。故选D。
5.C
【详解】
A、锌影响人的生长和发育,缺乏会食欲不振,生长迟缓,发育不良,缺钙时会患佝偻病、骨质疏松,故A错误;B、钙是构成骨骼和牙齿的主要成分,缺乏时幼儿和青少年患佝偻病,老年人患骨质疏松,缺铁会引起贫血,故B错误;C、氟能防止龋齿,故C正确;D、铁是合成血红蛋白的主要元素,缺铁会患贫血,缺碘会引起甲状腺肿大,故D错误。故选C。
6.C
【详解】
A、高温煮沸,使细菌内蛋白质失去细胞活性,可以杀菌消毒,故A项不符合题意;
B、垃圾回收,资源再生,节能环保,故B项不符合题意;
C、煤气属于可燃性气体,遇明火可能会发生爆炸,故C项符合题意
D、油锅着火,锅盖盖灭,可以隔绝氧气,达到灭火的目的,故D项不符合题意;
答案:C。
7.B
【详解】
A、物质与其构成粒子的对应关系:金属是由原子构成的,二氧化碳由分子构成。故A正确;
B、氧气能助燃,但不能燃烧,故不能作高能燃料,故B错误;
C、吸烟有害健康,应戒烟,黄曲霉素有毒,不能食用,故C正确;
D、物质利用与环境保护的关系:乙醇汽油产生的污染气体少,合理使用化肥能减少污染。故D正确。故选B。
8.D
【详解】
A、根据元素周期表中的信息可知,锌原子的核内质子数是30,锌离子带两个单位的正电荷,即原子失去了2个电子,故核外电子数是30-2=28,此选项表述不正确;
B、元素名称正下方的数值是相对原子质量,但相对原子质量的单位不“g”,此选项表述不正确;
C、已知相对原子质量约等于质子数与中子数之和,故锌原子核内的中子数约等于65-30=35,此选项不正确;
D、人体缺锌可能引起发育迟缓,智力低下,得侏儒症,此选项表述正确。
故选D。
9.C
【详解】
A、甲醛有毒,所以不能用甲醛溶液保存海鲜,故A错误;
B、人体缺碘造成甲状腺肿大,故B错误;
C、水果、蔬菜中富含维生素,所以水果、蔬菜能提供多种维生素,故C正确;
D、霉变的大米含有黄曲霉毒素,所以霉变的大米淘洗后也不可食用,故D错误。
故选:C。
10.B
【详解】
试题分析:A、甲基苯丙胺属于纯净物,错误,B、甲基苯丙胺含有碳元素,属于有机物,正确,C、化学式中元素符号右下角的数字表示的是分子中所含的原子个数,故一个分子中原子总数=10+15+1=26,错误,D、根据质量守恒定律:化学反应前后,元素的种类不变,故燃烧不仅只生成二氧化碳和水,错误,故选B
11.A
【详解】
A、缺乏维生素C,会患坏血病,缺乏维生素A,会患夜盲症,符合题意;
B、正常人胃液的pH在0.9-1.5,显酸性,不符合题意;
C、烟中含一氧化碳、尼古丁等有害物质,吸烟容易得肺气肿、肺癌,不符合题意;
D、幼儿及青少年缺钙易患佝偻病,老年人缺钙易患骨质疏松,不符合题意。
故选A。
12.A
【详解】
A.氢氧化钠具有强烈的腐蚀性,不能用来漂洗食品,故符合题意;
B.适量摄入碘元素可以预防甲状腺肿大,故不合题意;
C.奶制品中富含蛋白质与钙元素,每天饮用奶制品,增加营养,故不合题意;
D.小苏打是一种对人体没有危害的物质,在制造蛋糕的过程中受热会分解生成二氧化碳,蛋糕变得蓬松,故不合题意。
故选:A。
13.A
【详解】
A、铜粉中混有铁粉---用磁铁充分吸引,可以把铁粉除去,方法正确;FeCl2溶液中混有CuCl2---加过量的铁粉,铁粉能把氯化铜转化为氯化亚铁,方法正确;CaCO3中混有NaCl---加足量水溶解后过滤,因为碳酸钙不溶于水,氯化钠溶于水,能够除去杂质,方法正确;
B、氧化钙俗称生石灰,正确;氢氧化钠的俗称应该是火碱或烧碱或苛性钠,错误;氢氧化钙俗称消石灰,正确,故此项错误;
C、煤炉上放一壶水不能防止取暖防中毒,因为一氧化碳不溶于水,错误;防菜刀生锈---干燥后悬挂,正确;延长食物保质期放---入冰箱中,正确;故此项错误;
D、亚硝酸钠有毒,不能当食盐用,正确;食物霉变后已经变质,高温消毒也不能食用了,错误;甲醛有毒,对人体有害,故此项错误。
故选A。
14.A
【解析】
蛋白质是构成细胞的基础物质,鸭毛的细胞中有蛋白质,所以鸭毛在灼烧时会有烧焦羽毛的气味;植物油是油脂,青菜中主要含维生素,馒头中主要是淀粉,灼烧时,都不会有烧焦羽毛的气味。选A
15.A
【详解】
A、铝制品在空气中耐腐蚀是因为其表面生成了一层致密的氧化物薄膜,保护了内部金属不被腐蚀,正确;
B、霉变的食物处理也不能再食用,错误;
C、合金硬度大于成分金属,黄铜片与铜片相互刻画时,纯铜片上会留下明显的划痕,错误;
D、配制一定质量分数的氯化钠溶液,量取水时仰视读数,导致读数偏小,实际所取液体体积偏大,会使得溶液的溶质质量分数偏小,错误。
故选A。
16.C
【详解】
淀粉是高分子化合物,在稀硫酸作催化剂的条件下发生水解反应生成葡萄糖。葡萄糖中含有醛基,可发生银镜反应,也可被新制取的氢氧化铜悬浊液氧化,产生砖红色沉淀。淀粉遇碘变蓝色,淀粉与水反应后只含葡萄糖,故加入淀粉后不会变蓝色。
故选:C。
17.易升华 C NaHCO3+HCl=NaCl+H2O+CO2↑
【详解】
(1)干冰常用于人工降雨,利用了干冰易升华的性质;
(2)缺钙,少年儿童得佝偻病,中老年人得骨质疏松症.故选C;
(3)小苏打与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑。
18.温度越高,分子间隔越大 6:1 质量守恒定律:化学反应前后原子的个数、种类不变 蔬菜或水果
【详解】
(1)温度越高,分子间隔越大,测体温时水银体温计中汞柱会上升的微观原因是汞原子温度越高,分子间隔越大;
(2)聚丙烯(C3H6)n化合物中碳、氢元素的质量比=;
(3),依据质量守恒定律:化学反应前后原子的个数、种类不变,反应前由4个碳原子、8个氢原子、6个氧原子;生成物中有4个碳原子、8个氢原子、4个氧原子,X中含有2个氧原子,则X的化学式为,推断的依据是:质量守恒定律:化学反应前后原子的个数、种类不变;
(4)米饭中富含糖类、红烧肉中富含蛋白质、油脂、牛奶和鸡蛋汤富含蛋白质,从均衡营养角度出发缺少维生素,还应补充一种食物是蔬菜或水果。
19.维生素 C12H22O11 过滤 防止水污染
【详解】
蓝莓果等水果是人体获取维生素的主要来源之一,该营养素可以起到调节新陈代谢、预防疾病和维持身体健康的作用。蓝莓中含有糖类等成分,蔗糖就是其中一种,蔗糖的化学式是 C12H22O11。图2 A 池是除去水中固体杂质,是过滤池。水是一切生命体生存所必需的物质,为了人类的生存和发展,人类必须爱护水资源,一方面要节约用水,另一方面要防止水污染。
20.铁元素 氧气 乳化 蛋白质 +1 煮沸
【详解】
(1)使用铁锅炒菜、做饭有利于人体健康,主要是增加了膳食中的铁元素。
(2)汽车表面喷漆可有效防止钢铁与水和氧气接触而生锈。
(3)常加入洗洁精去除油污,是利用了洗洁精的乳化作用。
(4)丝绸的主要成分是蛋白质。
(5)次氯酸中氢元素的化合价为+1,氧元素的化合价为﹣2,设氯元素的化合价为x,则有,x=+1,生活中为降低自来水的硬度并杀灭水中的病原微生物,常采用的方法是加热煮沸。
21.微量元素 13 2MoS2+7O22MoO3+4SO2 AC +6 氮 烧杯 1:14
【详解】
(1)钼是人体及动植物必需的微量元素;在原子中,核电荷数=核外电子数,原子的结构示意图2,其中X=42-2-8-18-1=13;
(2)根据流程图可知,步骤①反应是MoS2和O2在高温条件下反应生成SO2和MoO3,反应的化学方程式为:2MoS2+7O22MoO3+4SO2;
(3)二氧化硫,能与氢氧化钠、氨水反应,不能与浓硫酸反应,可用来吸收SO2尾气的是氢氧化钠溶液和氨水,故选AC;
(4)在(NH4)2MoO4中,铵根子、氧元素的化合价分别为+1和-2,设:(NH4)2MoO4中钼的化合价为x,根据化合物中元素的化合价的代数和为零,则有:(+1)×2+x+(-2)×4=0
解得x=+6,(NH4)2MoO4中Mo的化合价是+6,(NH4)2MoO4中含有氮元素,在农业上既是钼肥又是氮肥;
(5)操作Ⅰ是将固体与液体分离。如果在实验室模拟操作Ⅰ,则需要使用的主要玻璃仪器有漏斗、玻璃棒、烧杯;
(6)利用H2和CO分别还原等质量的精产品(MoO3),所需的还原剂分别为H2和CO。
设:MoO3的质量为m,所需的还原剂分别为H2和CO质量分别为x、y。
;
;。利用H2和CO分别还原等质量的精产品(MoO3),所需的还原剂的质量比为1:14。
22.属于 6CO2 +6H2OC6H1206+6O2 分别灼烧闻气味 X、Z 7:6
【详解】
(1)纤维素是多糖,属于糖类物质;
(2)光合作用的化学方程式为:6CO2 +6H2OC6H1206+6O2;
(3)羊毛线燃烧会产生烧焦羽毛的气味,棉线没有,故用灼烧闻气味的方法鉴别;
(4)由反应的微观示意图可知,该反应是碳和氨气在一定条件下反应生成了氮气和甲烷,反应的方程式是:3C+4NH32N2+3CH4。
①单质是由一种元素组成的纯净物,故X、Y、Z、W 四种物质中属于单质的是:X、Z,分别是碳、氮气;
②根据方程式,反应生成的 Z、W 两种物质的质量比为:(2×28):(3×16)=7:6。
23.糖类 100 g该板栗中含有4.6 mg钠元素,则氯化钠的质量为4.6 mg÷×100%=11.7 mg
答:氯化钠的质量是11.7 mg。
【详解】
(1)根据人体所需的营养素及其生理功能分析解答;
(2)根据元素的质量=化合物的质量×化合物中该元素的质量分数解答。
(1)糖类、油脂、蛋白质能够为人体提供能量,糖类是人体能量的主要供应者,故填:糖类;
(2)100 g该板栗中含有4.6 mg钠元素,则氯化钠的质量为4.6 mg÷×100%=11.7 mg
答:氯化钠的质量是11.7 mg。
24.蛋白质 碘 混合物 12.8% C 蒸馏 碱
【详解】
(1)鱼虾富含的蛋白质是机体生长及修补受损组织的主要原料,海带富含的 碘可以预防甲状脚肿大。故填:蛋白质;碘;
(2)可燃冰主要含有甲烷水合物,还含少量CO2等气体,属于混合物;
设生成17.6g二氧化碳需要的甲烷的质量为x。
x=6.4g
该天然气水合物样品中甲烷的质量分数为:。
故答案为混合物; 12.8%。
(3)①水变成水蒸气的过程中,发生变化的是水分子间隔,故填:C;
②从海水中获得淡水可采取的方法是蒸馏,故填:蒸馏。
(4)①根据海水pH变化趋势判断:2000年时海水的pH应该是介于8.1和8.2之间,呈碱性;②“海洋酸化”的原因是二氧化碳和水反应生成碳酸,反应的化学方程式表示为:。故填:碱;。
一、选择题(共16题)
1.下列说法正确的是( )
A.用洗洁精清洗油渍,目的是和油渍反应
B.称为糖类的有机物都有甜味
C.在积雪路面撒盐,目的是提高沸点
D.合金的熔点一般比组成金属低,如做保险丝的武德合金
2.下列食物中,富含蛋白质的是( )
A.馒头 B.苹果 C.鱼肉 D.白菜
3.下列说法正确的是
A.铁、钙、锰、碘等为常见微量元素
B.1mL水与1mL酒精混合后的总体积等于2mL
C.实验室用高锰酸钾制取氧气完毕,应该先熄灭酒精灯,再拿出导管
D.二氧化碳不供给呼吸,因此在人群密集的地方注意通风
4.下列河南特产中富含维生素的是( )
A.原阳大米
B.黄河鯉鱼
C.叶县岩盐
D.灵宝苹果
5.对于人体必需元素,我们也要注意合理摄入,摄入不足或过量均不利于人体健康。下列有关几种人体必需元素对人体健康的影响,说法正确的是( )
A.缺锌会引起佝偻病、骨质疏松 B.缺钙会引起贫血
C.缺氟会引起龋齿 D.缺铁会引起甲状腺肿大
6.下列做法不正确的是( )
A.高温煮沸,杀菌消毒 B.垃圾回收,资源再生
C.煤气泄漏,开灯检查 D.油锅着火,锅盖盖灭
7.归纳与总结是学好化学的重要方法。下列对所学知识的整理,存在错误的是( )
A.物质与其构成粒子的对应关系:
①金——由原子构成
②二氧化碳——由分子构成
B.物质性质与用途的对应关系:
①氧气能助燃——作高能燃料
②氮气化学性质稳定——充入食品包装中以防腐
C.有关“污染源——污染物——解决策略”的对应关系:
①吸烟——尼古丁和一氧化碳——戒烟
②霉变食物——黄曲霉素——不食用
D.物质利用与环境保护的关系:
①使用乙醇汽油——减少汽车尾气污染
②合理使用农药、化肥——减少水污染
8.元素周期表中锌元素的某些信息如图所示,下列有关锌的说法正确的是( )
A.锌离子核外有 30 个电子
B.锌的相对原子质量为65.38g
C.锌原子核内的中子数为30
D.缺锌可能引起发育迟缓,智力低下,得侏儒症
9.化学与人类健康关系密切。下列说法正确的是( )
A.用甲醛溶液保存海鲜
B.人体缺碘易患夜盲症
C.水果、蔬菜能提供多种维生素
D.霉变的大米淘洗后可食用
10.“珍爱生命,远离毒品”。冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为)。有关甲基苯丙胺的说法正确的是( )
A.属于混合物 B.属于有机物
C.一个分子中原子总数为25 D.燃烧只生成二氧化碳和水
11.下列关于人体健康的叙述错误的是( )
A.缺乏维生素C会患夜盲症
B.正常人胃液的pH在0.9-1.5
C.吸烟容易得肺气肿、肺癌
D.老年人缺钙易发生骨质疏松
12.下列做法不利于人体健康的是( )
A.食用用氢氧化钠溶液漂洗的鸡爪 B.食用适量含碘海产品
C.青少年每天饮用奶制品,增加营养 D.焙制糕点时添加适量小苏打
13.下列知识整理的内容完全正确的一组是( )
A.除杂的方法 B.物质与俗名
铜粉中混有铁粉﹣﹣﹣用磁铁充分吸引 FeCl2溶液中混有CuCl2﹣﹣﹣加过量的铁粉 CaCO3中混有NaCl﹣﹣﹣加足量水溶解后过滤 氧化钙﹣﹣﹣生石灰 氢氧化钠﹣﹣﹣纯碱 氢氧化钙﹣﹣﹣消石灰
C.性质与用途 D.食品与安全
取暖防中毒﹣﹣﹣煤炉上放一壶水 防菜刀生锈﹣﹣﹣干燥后悬挂 延长食物保质期﹣﹣﹣放入冰箱中 亚硝酸钠﹣﹣﹣不能当食盐用 霉变食物﹣﹣﹣高温消毒后可食用 甲醛溶液﹣﹣﹣可作食品保鲜剂
A.A B.B C.C D.D
14.羊毛含有蛋白质在灼烧时会有烧焦羽毛的气味,下列物质灼烧时也会产生该气味的是( )
A.鸭毛 B.植物油 C.青菜 D.馒头
15.下列说法正确的是( )
A.铝制品在空气中耐腐蚀是因为其表面生成了一层致密的氧化物薄膜
B.将霉变的食物处理后再食用,不会影响人体健康
C.黄铜片与铜片相互刻画时,黄铜片上会留下明显的划痕
D.配制一定质量分数的氯化钠溶液,量取水时仰视读数会使得溶液的溶质质量分数偏大
16.在催化剂的作用下,淀粉能与水反应生成葡萄糖.下列能证明部分淀粉已与水反应的试剂是 ( )
①碘水 ②CdSO4溶液 ③NaOH溶液 ④新制Cu(OH) 2 ⑤酒精
A.①② B.②③ C.①④ D.全部
二、综合题(共8题)
17.解释下列生活现象:
(1)干冰常用于人工降雨,利用了干冰_____的性质。
(2)高钙牛奶可以为人体补充每天所需的钙元素,预防老年人患_____(填序号)。
A 贫血 B 龋齿 C 骨质疏松
(3)胃酸过多的病人会服用小苏打片缓解,其反应原理用化学方程式表示为_____。
18.在党中央英明领导下,我国率先抗疫成功,赢得了人民群众的高度赞誉。在阻击疫情的过程中,化学起到了很好的作用。请回答下列问题。
(1)起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子______。
(2)上学时,戴口罩。制作口罩用的无纺布面料主要是聚丙烯(C3H6)n,聚丙烯中碳、氢元素的质量比为______。
(3)到校后,勤消毒。过氧乙酸用于教室消毒,其化学性质不稳定,分解的化学方程式为:,则X的化学式为______。推断依据是______。
(4)用餐时,讲营养。如午餐仅食用米饭、红烧肉、鸡蛋汤、牛奶,从均衡营养角度出发还应补充的一种食物是______。
19.黑龙江不仅仅是祖国的大粮仓,绿色食品更是闻名全国。近几年推出的蓝莓系列产品因其天然健康的品质,深受大家的喜爱。
制作蓝莓饮料需要蓝莓果。蓝莓果等水果是人体获取 ____________(填除水外的一种营养素)的主要来源之一,该营养素可以起到调节新陈代谢、预防疾病和维持身体健康的作用。蓝莓中含有糖类等成分,蔗糖就是其中一种,蔗糖的化学式是____________ 。
人类生活和工农业生产都离不开水。图2是自来水厂净水过程示意图。图2 A 池是 ____________池。水是一切生命体生存所必需的物质,为了人类的生存和发展,人类必须爱护水资源,一方面要节约用水,另一方面要____________。
20.化学与生活、生产、科技息息相关。请思考回答下列问题:
(1)使用铁锅炒菜、做饭有利于人体健康,主要是增加了膳食中的_____。
(2)汽车表面喷漆不仅美观,而且可有效防止钢铁与水、_____接触而生锈。
(3)小强发现妈妈刷洗锅碗时,常加入洗洁精去除油污,是利用了洗洁精的_____作用。
(4)“一带一路”是促进共同发展又一伟大战略。中国丝绸以其卓越的品质和丰富的文化内涵闻名于世,丝绸的主要成分是_____。
(5)2016年底骆马湖水将走进徐州百姓家。自来水厂常用氯气杀菌消毒,发生的反应为:Cl2+H2O=HCl+HCl0(次氯酸)。次氯酸中氯元素的化合价为_____。生活中为降低自来水的硬度并杀灭水中的病原微生物,常采用的方法是_____。
21.钼具有高强度、高熔点、而腐蚀等优点,在工业上得到广泛的利用。图1是化工生产中制备金属钼的部分流程图(假设杂质不与空气反应)。
(1)钼是人体及动植物必需的 ______ (选填“微量元素”或“常量元素”),原子的结构示意图2,其中X是 ______ 。
(2)步骤①反应的化学方程式 ______ 。
(3)下列物质可以用来吸收SO2尾气的是 ______ (填字母)。
A 氢氧化钠溶液 B 浓硫酸 C 氨水
(4)(NH4)2MoO4中Mo的化合价是 ______ ,在农业上既是钼肥又是 ______ 肥。
(5)如果在实验室模拟操作Ⅰ,则需要使用的主要玻璃仪器有漏斗、玻璃棒、 ______ 。
(6)利用H2和CO分别还原等质量的精产品(MoO3),所使用的还原剂的质量比为 ______ 。
22.纤维素是一种常见的有机物。
(1)纤维素_____(选填“属于”、“不属于”)糖类物质。
(2)葡萄糖在植物体内会部分转化为纤维素。植物体内的葡萄糖来源于光合作用,请写出反应的化学方程式_____
(3)棉花的主要成分是纤维素,鉴别棉线和羊毛线的方法是_____
(4)科学最新发现,通过简单的化学反应,可以将树木纤维素最终转变为超级储能装置,其中一个反应的微观示意图如下:
①X、Y、Z、W 四种物质中属于单质的是_____
②反应生成的 Z、W 两种物质的质量比为_____
23.如表是100 g某品牌板栗的部分营养成分。
总热量 蛋白质 糖类 油脂 钠 维生素C
1 016 kJ 5.1 g 11.3 g 19 g 4.6 mg 3.3 mg
(1)食物的成分主要有六大类营养素,上表中为人体提供主要能量的是________。
(2)假设该板栗中的钠元素以氯化钠的形式存在,则100 g该板栗中,氯化钠的质量是________?
24.中国有漫长的海岸线,海洋蕴藏着丰富的资源。请按要求填空。
(1)海洋为我们提供了营养丰富的食材。鱼虾富含的 ________ (填一种营养素)是机体生长及修补受损组织的主要原料,海带富含的 _____ (填元素符号)可以预防甲状腺肿大。
(2)我国在海域可燃冰开采技术领域取得重大突破。可燃冰主要含有甲烷水合物,还含少量CO2等气体,可燃冰属于 _______ (选填“纯净物”或“混合物”)。有科学家开采得到一种天然气水合物样品。取50.0克样品放置在一密闭容器内,该样品迅速转化为甲烷气体和水,将甲烷气体分离并完全燃烧,得到17.6克二氧化碳。该天然气水合物样品中甲烷的质量分数为 _____ 。(写出完整的计算过程)
(3)海水淡化可缓解淡水资源匮乏问题。
①水变成水蒸气的过程中,发生变化的是 _______ (填字母序号)。
A分子个数 B分子质量 C分子间隔 D分子种类
②从海水中获得淡水可采取的方法是 ________________ (填“过滤”“吸附”或“蒸馏”)。
(4)海水碳储存,可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减小。
①根据海水pH变化趋势判断:2000年时海水呈 ________ 性。
②“海洋酸化”的原因可用化学方程式表示为 ____ 。
参考答案
1.D
【详解】
A、洗洁精清洗油渍,是乳化原理,不是反应,故A错;
B、称为糖类的有机物不一定有甜味,例如淀粉,故B错;
C、在积雪路面撒盐,目的是降低凝固点,故C错;
D、合金的熔点一般比组成金属低,硬度大,故D正确。
故选D。
2.C
【解析】A、馒头中富含淀粉,淀粉属于糖类,故选项错误;B、苹果中富含维生素,故选项错误;C、鱼肉中富含蛋白质,故选项正确;D、白菜中富含维生素,故选项错误。故选C。
3.D
【详解】
A、钙元素是人体中的常量元素,故A不符合题意;
B、分子间有一定的间隔,1mL水与1mL酒精混合后的总体积小于2mL, 故B不符合题意;
C、实验室用高锰酸钾制取氧气完毕,应该先拿出导管,再熄灭酒精灯,否则容易造成水倒流进热的试管引起试管炸裂,故C不符合题意;
D、二氧化碳不供给呼吸,因此在人群密集的地方二氧化碳的含有高,要注意通风,故D不符合题意;
故选D。
4.D
【详解】
A、原阳大米中富含淀粉,淀粉属于糖类,不符合题意;
B、黄河鲤鱼中富含蛋白质,不符合题意;
C、叶县岩盐中富含无机盐,不符合题意;
D、灵宝苹果中富含维生素,符合题意。故选D。
5.C
【详解】
A、锌影响人的生长和发育,缺乏会食欲不振,生长迟缓,发育不良,缺钙时会患佝偻病、骨质疏松,故A错误;B、钙是构成骨骼和牙齿的主要成分,缺乏时幼儿和青少年患佝偻病,老年人患骨质疏松,缺铁会引起贫血,故B错误;C、氟能防止龋齿,故C正确;D、铁是合成血红蛋白的主要元素,缺铁会患贫血,缺碘会引起甲状腺肿大,故D错误。故选C。
6.C
【详解】
A、高温煮沸,使细菌内蛋白质失去细胞活性,可以杀菌消毒,故A项不符合题意;
B、垃圾回收,资源再生,节能环保,故B项不符合题意;
C、煤气属于可燃性气体,遇明火可能会发生爆炸,故C项符合题意
D、油锅着火,锅盖盖灭,可以隔绝氧气,达到灭火的目的,故D项不符合题意;
答案:C。
7.B
【详解】
A、物质与其构成粒子的对应关系:金属是由原子构成的,二氧化碳由分子构成。故A正确;
B、氧气能助燃,但不能燃烧,故不能作高能燃料,故B错误;
C、吸烟有害健康,应戒烟,黄曲霉素有毒,不能食用,故C正确;
D、物质利用与环境保护的关系:乙醇汽油产生的污染气体少,合理使用化肥能减少污染。故D正确。故选B。
8.D
【详解】
A、根据元素周期表中的信息可知,锌原子的核内质子数是30,锌离子带两个单位的正电荷,即原子失去了2个电子,故核外电子数是30-2=28,此选项表述不正确;
B、元素名称正下方的数值是相对原子质量,但相对原子质量的单位不“g”,此选项表述不正确;
C、已知相对原子质量约等于质子数与中子数之和,故锌原子核内的中子数约等于65-30=35,此选项不正确;
D、人体缺锌可能引起发育迟缓,智力低下,得侏儒症,此选项表述正确。
故选D。
9.C
【详解】
A、甲醛有毒,所以不能用甲醛溶液保存海鲜,故A错误;
B、人体缺碘造成甲状腺肿大,故B错误;
C、水果、蔬菜中富含维生素,所以水果、蔬菜能提供多种维生素,故C正确;
D、霉变的大米含有黄曲霉毒素,所以霉变的大米淘洗后也不可食用,故D错误。
故选:C。
10.B
【详解】
试题分析:A、甲基苯丙胺属于纯净物,错误,B、甲基苯丙胺含有碳元素,属于有机物,正确,C、化学式中元素符号右下角的数字表示的是分子中所含的原子个数,故一个分子中原子总数=10+15+1=26,错误,D、根据质量守恒定律:化学反应前后,元素的种类不变,故燃烧不仅只生成二氧化碳和水,错误,故选B
11.A
【详解】
A、缺乏维生素C,会患坏血病,缺乏维生素A,会患夜盲症,符合题意;
B、正常人胃液的pH在0.9-1.5,显酸性,不符合题意;
C、烟中含一氧化碳、尼古丁等有害物质,吸烟容易得肺气肿、肺癌,不符合题意;
D、幼儿及青少年缺钙易患佝偻病,老年人缺钙易患骨质疏松,不符合题意。
故选A。
12.A
【详解】
A.氢氧化钠具有强烈的腐蚀性,不能用来漂洗食品,故符合题意;
B.适量摄入碘元素可以预防甲状腺肿大,故不合题意;
C.奶制品中富含蛋白质与钙元素,每天饮用奶制品,增加营养,故不合题意;
D.小苏打是一种对人体没有危害的物质,在制造蛋糕的过程中受热会分解生成二氧化碳,蛋糕变得蓬松,故不合题意。
故选:A。
13.A
【详解】
A、铜粉中混有铁粉---用磁铁充分吸引,可以把铁粉除去,方法正确;FeCl2溶液中混有CuCl2---加过量的铁粉,铁粉能把氯化铜转化为氯化亚铁,方法正确;CaCO3中混有NaCl---加足量水溶解后过滤,因为碳酸钙不溶于水,氯化钠溶于水,能够除去杂质,方法正确;
B、氧化钙俗称生石灰,正确;氢氧化钠的俗称应该是火碱或烧碱或苛性钠,错误;氢氧化钙俗称消石灰,正确,故此项错误;
C、煤炉上放一壶水不能防止取暖防中毒,因为一氧化碳不溶于水,错误;防菜刀生锈---干燥后悬挂,正确;延长食物保质期放---入冰箱中,正确;故此项错误;
D、亚硝酸钠有毒,不能当食盐用,正确;食物霉变后已经变质,高温消毒也不能食用了,错误;甲醛有毒,对人体有害,故此项错误。
故选A。
14.A
【解析】
蛋白质是构成细胞的基础物质,鸭毛的细胞中有蛋白质,所以鸭毛在灼烧时会有烧焦羽毛的气味;植物油是油脂,青菜中主要含维生素,馒头中主要是淀粉,灼烧时,都不会有烧焦羽毛的气味。选A
15.A
【详解】
A、铝制品在空气中耐腐蚀是因为其表面生成了一层致密的氧化物薄膜,保护了内部金属不被腐蚀,正确;
B、霉变的食物处理也不能再食用,错误;
C、合金硬度大于成分金属,黄铜片与铜片相互刻画时,纯铜片上会留下明显的划痕,错误;
D、配制一定质量分数的氯化钠溶液,量取水时仰视读数,导致读数偏小,实际所取液体体积偏大,会使得溶液的溶质质量分数偏小,错误。
故选A。
16.C
【详解】
淀粉是高分子化合物,在稀硫酸作催化剂的条件下发生水解反应生成葡萄糖。葡萄糖中含有醛基,可发生银镜反应,也可被新制取的氢氧化铜悬浊液氧化,产生砖红色沉淀。淀粉遇碘变蓝色,淀粉与水反应后只含葡萄糖,故加入淀粉后不会变蓝色。
故选:C。
17.易升华 C NaHCO3+HCl=NaCl+H2O+CO2↑
【详解】
(1)干冰常用于人工降雨,利用了干冰易升华的性质;
(2)缺钙,少年儿童得佝偻病,中老年人得骨质疏松症.故选C;
(3)小苏打与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑。
18.温度越高,分子间隔越大 6:1 质量守恒定律:化学反应前后原子的个数、种类不变 蔬菜或水果
【详解】
(1)温度越高,分子间隔越大,测体温时水银体温计中汞柱会上升的微观原因是汞原子温度越高,分子间隔越大;
(2)聚丙烯(C3H6)n化合物中碳、氢元素的质量比=;
(3),依据质量守恒定律:化学反应前后原子的个数、种类不变,反应前由4个碳原子、8个氢原子、6个氧原子;生成物中有4个碳原子、8个氢原子、4个氧原子,X中含有2个氧原子,则X的化学式为,推断的依据是:质量守恒定律:化学反应前后原子的个数、种类不变;
(4)米饭中富含糖类、红烧肉中富含蛋白质、油脂、牛奶和鸡蛋汤富含蛋白质,从均衡营养角度出发缺少维生素,还应补充一种食物是蔬菜或水果。
19.维生素 C12H22O11 过滤 防止水污染
【详解】
蓝莓果等水果是人体获取维生素的主要来源之一,该营养素可以起到调节新陈代谢、预防疾病和维持身体健康的作用。蓝莓中含有糖类等成分,蔗糖就是其中一种,蔗糖的化学式是 C12H22O11。图2 A 池是除去水中固体杂质,是过滤池。水是一切生命体生存所必需的物质,为了人类的生存和发展,人类必须爱护水资源,一方面要节约用水,另一方面要防止水污染。
20.铁元素 氧气 乳化 蛋白质 +1 煮沸
【详解】
(1)使用铁锅炒菜、做饭有利于人体健康,主要是增加了膳食中的铁元素。
(2)汽车表面喷漆可有效防止钢铁与水和氧气接触而生锈。
(3)常加入洗洁精去除油污,是利用了洗洁精的乳化作用。
(4)丝绸的主要成分是蛋白质。
(5)次氯酸中氢元素的化合价为+1,氧元素的化合价为﹣2,设氯元素的化合价为x,则有,x=+1,生活中为降低自来水的硬度并杀灭水中的病原微生物,常采用的方法是加热煮沸。
21.微量元素 13 2MoS2+7O22MoO3+4SO2 AC +6 氮 烧杯 1:14
【详解】
(1)钼是人体及动植物必需的微量元素;在原子中,核电荷数=核外电子数,原子的结构示意图2,其中X=42-2-8-18-1=13;
(2)根据流程图可知,步骤①反应是MoS2和O2在高温条件下反应生成SO2和MoO3,反应的化学方程式为:2MoS2+7O22MoO3+4SO2;
(3)二氧化硫,能与氢氧化钠、氨水反应,不能与浓硫酸反应,可用来吸收SO2尾气的是氢氧化钠溶液和氨水,故选AC;
(4)在(NH4)2MoO4中,铵根子、氧元素的化合价分别为+1和-2,设:(NH4)2MoO4中钼的化合价为x,根据化合物中元素的化合价的代数和为零,则有:(+1)×2+x+(-2)×4=0
解得x=+6,(NH4)2MoO4中Mo的化合价是+6,(NH4)2MoO4中含有氮元素,在农业上既是钼肥又是氮肥;
(5)操作Ⅰ是将固体与液体分离。如果在实验室模拟操作Ⅰ,则需要使用的主要玻璃仪器有漏斗、玻璃棒、烧杯;
(6)利用H2和CO分别还原等质量的精产品(MoO3),所需的还原剂分别为H2和CO。
设:MoO3的质量为m,所需的还原剂分别为H2和CO质量分别为x、y。
;
;。利用H2和CO分别还原等质量的精产品(MoO3),所需的还原剂的质量比为1:14。
22.属于 6CO2 +6H2OC6H1206+6O2 分别灼烧闻气味 X、Z 7:6
【详解】
(1)纤维素是多糖,属于糖类物质;
(2)光合作用的化学方程式为:6CO2 +6H2OC6H1206+6O2;
(3)羊毛线燃烧会产生烧焦羽毛的气味,棉线没有,故用灼烧闻气味的方法鉴别;
(4)由反应的微观示意图可知,该反应是碳和氨气在一定条件下反应生成了氮气和甲烷,反应的方程式是:3C+4NH32N2+3CH4。
①单质是由一种元素组成的纯净物,故X、Y、Z、W 四种物质中属于单质的是:X、Z,分别是碳、氮气;
②根据方程式,反应生成的 Z、W 两种物质的质量比为:(2×28):(3×16)=7:6。
23.糖类 100 g该板栗中含有4.6 mg钠元素,则氯化钠的质量为4.6 mg÷×100%=11.7 mg
答:氯化钠的质量是11.7 mg。
【详解】
(1)根据人体所需的营养素及其生理功能分析解答;
(2)根据元素的质量=化合物的质量×化合物中该元素的质量分数解答。
(1)糖类、油脂、蛋白质能够为人体提供能量,糖类是人体能量的主要供应者,故填:糖类;
(2)100 g该板栗中含有4.6 mg钠元素,则氯化钠的质量为4.6 mg÷×100%=11.7 mg
答:氯化钠的质量是11.7 mg。
24.蛋白质 碘 混合物 12.8% C 蒸馏 碱
【详解】
(1)鱼虾富含的蛋白质是机体生长及修补受损组织的主要原料,海带富含的 碘可以预防甲状脚肿大。故填:蛋白质;碘;
(2)可燃冰主要含有甲烷水合物,还含少量CO2等气体,属于混合物;
设生成17.6g二氧化碳需要的甲烷的质量为x。
x=6.4g
该天然气水合物样品中甲烷的质量分数为:。
故答案为混合物; 12.8%。
(3)①水变成水蒸气的过程中,发生变化的是水分子间隔,故填:C;
②从海水中获得淡水可采取的方法是蒸馏,故填:蒸馏。
(4)①根据海水pH变化趋势判断:2000年时海水的pH应该是介于8.1和8.2之间,呈碱性;②“海洋酸化”的原因是二氧化碳和水反应生成碳酸,反应的化学方程式表示为:。故填:碱;。
